复配醇胺溶液对CO2的吸收解吸性能及其降解性能
李红,吉轲,齐天勤机,李晓静,万慧慧,张永春,陈绍云,2
(1 大连理工大学化工学院精细化工国家重点实验室,辽宁 大连 116024;2 大连理工大学洛阳研究院,河南 洛阳 471000)
随着全球工业不断发展,化石能源大量消耗,大量二氧化碳(CO)排入大气,全球变暖程度不断加剧。2015 年,针对气候变化的《巴黎协定》在世界各国正式达成一致,随即碳减排技术成为首要攻克的难题,而碳捕集与封存是公认的减少CO排放的重要手段。CO捕集具体的主要方法包括吸收法、吸附法、膜分离法、低温分离法。
目前,化学吸收法由于其具有吸收效率高、处理能力大的特点,成为最适合各行业大规模碳捕集的技术。此方法一般采用的是胺类化学溶剂,可广泛用于水泥制造、钢铁生产以及化石燃料发电厂等工业过程的碳捕集。海螺集团建成的世界首个海螺水泥窑烟气碳捕集项目就采用了我国自主研发的胺法化学吸收。然而,胺类很容易发生降解,特别是醇胺类吸收剂。烟气中与CO共存的氧气(O)、硫氧化物(SO)、氮氧化物(NO)都会导致醇胺发生不同机制的降解,导致溶剂的CO捕集效率下降,同时产生的副产物会腐蚀捕集装置,造成胺的损失和运行成本的增加。例如,醇胺类物质在氧化降解和硫降解产生的腐蚀性耐热盐(HSS),不仅会引起胺溶液的起泡现象而且会对工厂建筑材料造成损坏,其他的中性产物(非HSS)会改变胺的化学性质(如碱度和黏度)。除此之外,由于吸收剂的解吸在高温条件下进行,因此会造成胺溶液的热降解。目前研究最广泛的胺主要有:以单乙醇胺(MEA)为代表的伯胺,以二乙醇胺(DEA)、-乙基乙醇(EMEA)为代表的仲胺,以2-氨基-2-甲基-1,3丙二醇(AMPD)、2-氨基-2-甲基-1-丙醇(AMP)为代表的空间位阻胺,以及以二甲基乙醇胺(MDEA)、二乙氨基乙醇(DEEA)为代表的叔胺。捕集能力和解吸能耗按照以上顺序呈现下降的趋势,其中空间位阻胺兼顾了捕集能力与解吸能耗的优点。
工业应用时,利用各类胺的特性,人们将不同种类的胺进行复配,获得性能优越的吸收剂,也是目前研究的热点之一。但目前的研究多数集中于强化复配溶液的吸收解吸性能方面,对于复配溶液的降解性能的研究较少。本文使用的混合胺组成参照了文献报道中性能优异的混合醇胺溶液,并进行了调整,测试了复配胺溶液的吸收解吸性能,重点考察了复配溶液的热降解和氧化降解特性,为今后碳捕集工业化应用提供基本参考依据。
1 材料与装置
1.1 试剂
高纯二氧化碳气体(CO)、高纯氮(N),大连化学物理研究所,纯度为99.99%。氧气与氮气混合气体(13.00%O+87.00%N,体积分数),大连化学物理研究所。实验用水均为去离子水。-乙基乙醇胺(EMEA),东京化成工业株式会社,纯度为99.00%。二乙氨基乙醇(DEEA)、哌嗪(PZ)、2-氨基-2-甲基-1,3丙二醇(AMPD)、羟乙基乙二胺(AEEA)、二乙醇胺(DEA)、环丁砜(SUL)、甘油(GI),上海阿拉丁生化科技股份有限公司,纯度为99.00%。2-氨基-2-甲基-1-丙醇(AMP),上海阿拉丁生化科技股份有限公司,纯度为97.00%。-甲基二乙醇胺(MDEA),上海阿拉丁生化科技股份有限公司,纯度为98.00%。乙醇胺(MEA),上海麦克林生化科技有限公司,纯度为99.00%。二甲基亚砜(DMSO),天津市富宇精细化工有限公司,分析纯。
1.2 不同配方的醇胺溶液
实验所使用的复配醇胺溶液的具体配比如表3所示。目前在工业上AEEA 水溶液是除了MEA 水溶液之外应用最广泛的醇胺吸收剂。EMEA+DEEA+PZ 溶液是实验室所研究的醇胺配方,其余的复配醇胺溶液是根据文献[19-26]报道中吸收解吸性能较好的醇胺配方,将具体的醇胺配比进行调整,由于在工业应用中,醇胺吸收剂不可避免地会受到水的影响,故将文献中的非水溶液配方调整为含有水的复配醇胺溶液之后,再进行吸收解吸性能的实验。
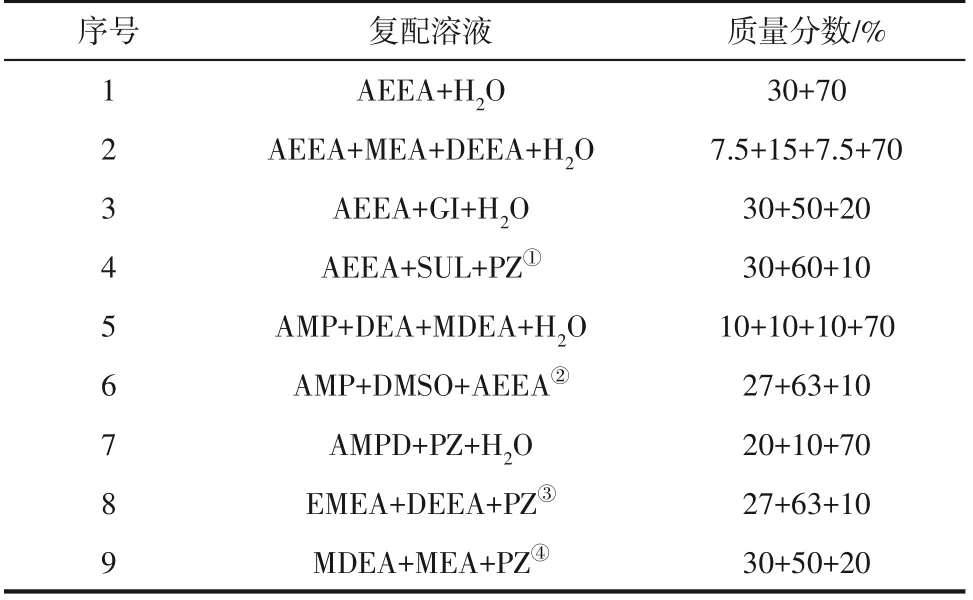
表3 复配溶液的配方
1.3 实验装置图
图1~图3分别是CO吸收解吸实验装置、氧化降解实验装置和热降解实验装置示意图。
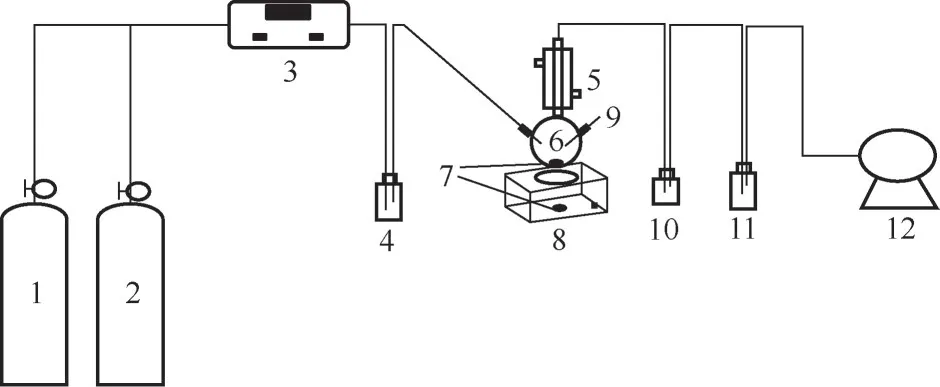
图1 CO2吸收解吸装置示意图
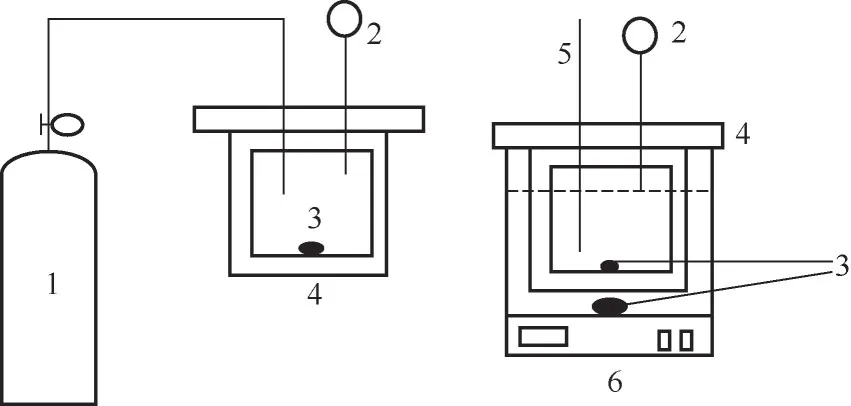
图2 氧化降解装置示意图

图3 热降解装置示意图
1.4 分析测试仪器
采用三重四级杆液相色谱质谱联用仪(TSQ Quantum Ultra 型,美国Thermo Scientific 公司)检测样品中的主吸收胺含量;线性离子阱-高分辨液质联用仪(电喷雾质谱ESI-MS,LTQ Orbitrap XL型,Thermo Scientific 科技有限公司)检测样品中分子量在50~300 之间的物质;气体进入装置的流量由质量流量计(D08-1F 型,北京七星华创)控制;吸收解吸装置出口的气体累积流量通过湿式防腐气体流量计(LMF-1 型,长春阿尔法仪表有限公司)来计量。
1.5 实验过程
在进行吸收解吸实验时,首先称量100g 复配醇胺溶液,放入三口烧瓶中后,使用油浴将其加热到40℃,通入高纯CO气体进行吸收,CO气体的流速为173mL/min,在溶液吸收至饱和后,设置油浴温度为110℃,在升温过程中进行解吸实验,实验全程在常压状态下进行。实验后得到的吸收量、解吸量误差在±0.02L CO/kg之间。
在进行热降解实验时,将100g 负载量为(1.5±0.01)L CO/kg的复配醇胺溶液放入高压釜内,将高压釜放入烘箱后(釜内约3h 达到140℃),向其中充入0.2MPa 氮气,实验过程中烘箱温度为140℃,实验进行144h,每隔36h进行取样。
在进行氧化降解实验时,将100g 负载量为(1.5±0.01)L CO/kg 的复配醇胺溶液放入高压釜内,向其中充入1MPa 混合气(13%O+87%N,体积分数),将其放入油浴中加热(釜内约2h达到70℃),使釜内溶液温度为70℃,实验进行96h,每隔24h进行取样。
在降解实验结束后,使用液质联用测定溶液中剩余的胺含量(±0.0045g/mL),并将降解前与降解后的溶液进行质谱分析,根据ESI-MS 结果推测降解机理。
2 结果与讨论
由于-乙基乙醇胺(EMEA)、二乙氨基乙醇(DEEA)、哌嗪(PZ)、2-氨基-2-甲基-1,3丙二醇(AMPD)、2-氨基-2-甲基-1-丙醇(AMP)、羟乙基乙二胺(AEEA)、二乙醇胺(DEA)、-甲基二乙醇胺(MDEA)、乙醇胺(MEA)等醇胺被广泛应用在工业上,所以针对以上醇胺溶液按照不同比例进行混合形成的复配醇胺溶液的研究是十分有价值的。
2.1 醇胺溶液的吸收解吸性能对比
醇胺溶液吸收CO后,都会形成一定量稳定中间体无法通过加热完全解吸,因此测试胺溶液性能时,都进行两次实验进行对比。图4~图6分别是9种醇胺溶液的两次吸收量、解吸量以及解吸率的数据比较,柱状图中的红色柱图与黑色柱图分别代表 AMPD+PZ+HO、 EMEA+DEEA+PZ 两 种 溶液的两次吸收量、解吸量以及解吸率数据。从图4~图6可以看出,将9种溶液进行两次吸收解吸实验之后发现,其中AEEA+HO、AEEA+SUL+PZ、AEEA+MEA+DEEA 三种溶液的两次吸收量相差较大,分别相差24.60L CO/kg、15.40L CO/kg 和18.05L CO/kg; AEEA+GI+HO、 MDEA+MEA+PZ两种溶液在进行两次吸收解吸实验后,不仅两次吸收量相差较大,相差量分别为23.80L CO/kg、50.45L CO/kg,而且解吸量和解吸效率明显低于其他7 种溶液;AMP+DEA+MDEA、AMP +DMSO+AEEA两种溶液虽然两次吸收量、解吸量和解吸效率相差不大,但是两种溶液的吸收量小于AMPD+PZ+HO、EMEA+DEEA+PZ 分别为50.15L CO/kg、46.35L CO/kg、41.55L CO/kg、40.40L CO/kg;而AMPD+PZ+HO、EMEA+DEEA+PZ 两种溶液两次吸收量分别为61.50L CO/kg、 57.10L CO/kg、57.15L CO/kg、55.75L CO/kg,平均解吸率都达到了94.00%以上,每种溶液的两次解吸率之差均为4.00%。
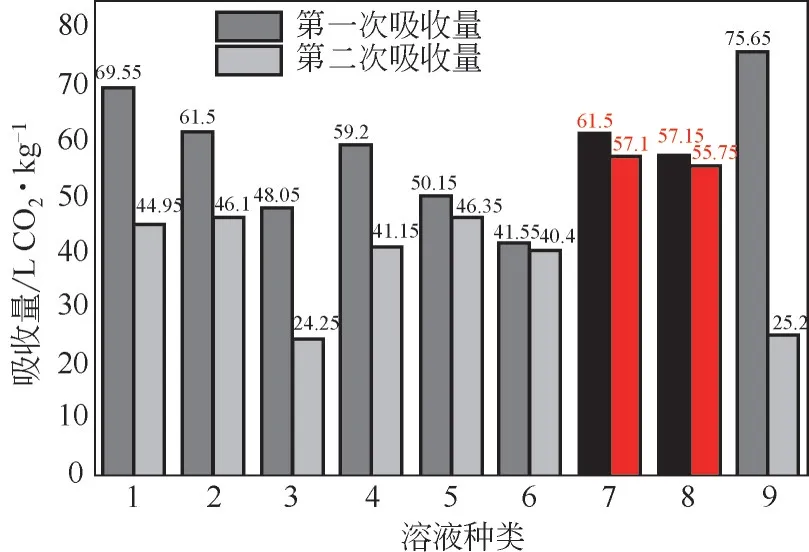
图4 复配醇胺溶液的吸收稳定性比较
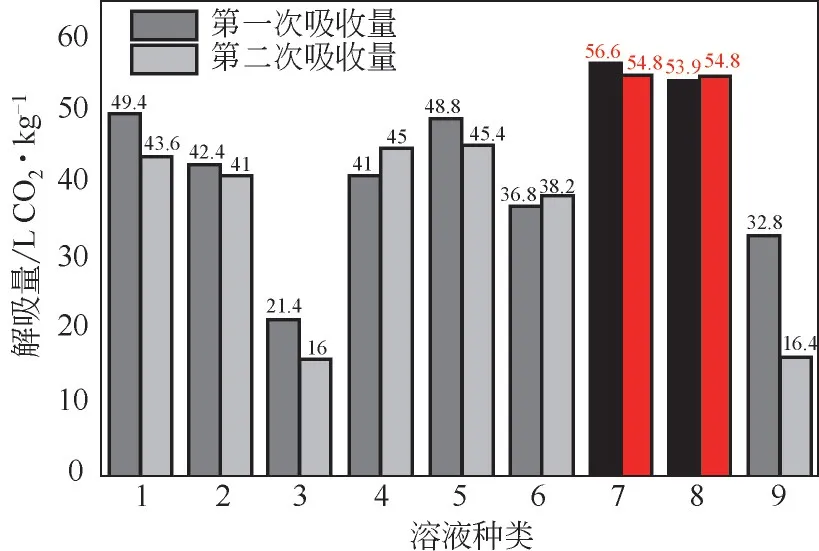
图5 复配醇胺溶液的解吸稳定性对比
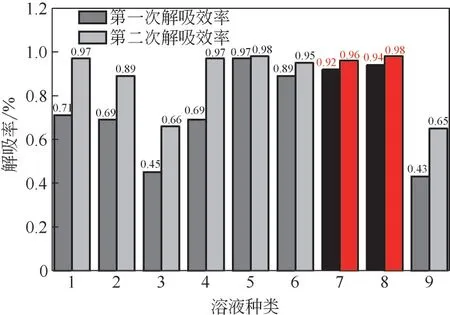
图6 复配醇胺溶剂的二次解吸率对比
综上,在对以上9种醇胺溶液进行两次吸收解吸实验之后,AMPD+PZ+HO、EMEA+DEEA+PZ两种溶液的吸收解吸性能优于其他7种溶液,对于工业应用来说具有较好的研究价值。为此,有必要进一步探究其在实际应用时可能发生的降解情况。
2.2 醇胺溶液降解后性能测试
2.2.1 EMEA+DEEA+PZ溶液性能变化
图7~图9 分别是EMEA+DEEA+PZ 溶液降解前后的吸收解吸性能对比图,从吸收量、解吸量以及解吸率三个方面来评价降解的影响。从图7~图9可以看出,EMEA+DEEA+PZ 热降解后的溶液两次吸收量分别为58.00L CO/kg、58.05L CO/kg,两次解吸量分别为53.90L CO/kg、54.80L CO/kg。氧化降解后的溶液两次吸收量分别为58.00L CO/kg、54.00L CO/kg,两次解吸量分别为52.40L CO/kg、52.80L CO/kg。溶液的两次吸收解吸性能较稳定。从图7 可以看出,在经过热降解之后,EMEA+DEEA+PZ 溶液的吸收解吸性能稳定性较高,溶液平均吸收量、平均解吸量略有升高,分别升高了1.58L CO/kg、0.35L CO/kg,平均解吸率下降2.04%;而氧化降解造成平均吸收量、平均解吸量分别下降0.45L CO/kg、1.75L CO/kg,平均解吸率下降2.25%,对于EMEA+DEEA+PZ 的吸收解吸性能来说,氧化降解的影响大于热降解。
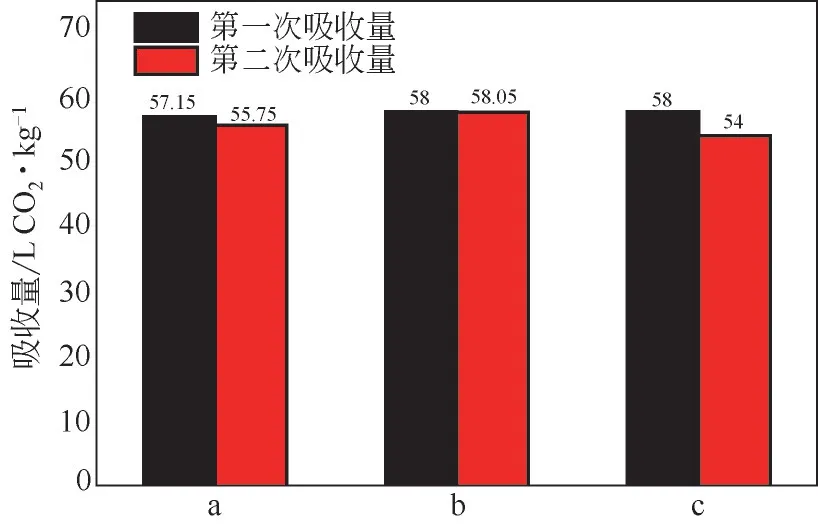
图7 EMEA+DEEA+PZ溶液降解前后吸收量对比
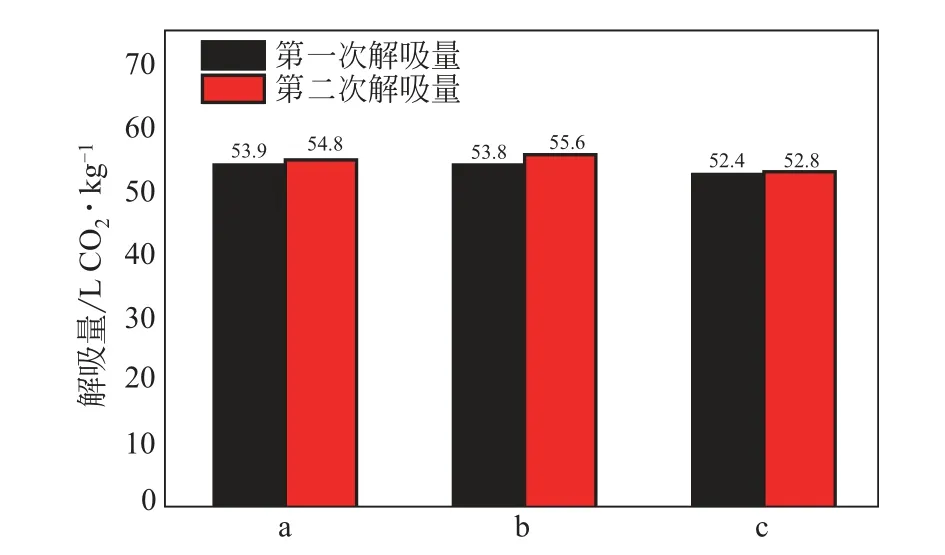
图8 EMEA+DEEA+PZ溶液降解前后解吸量对比
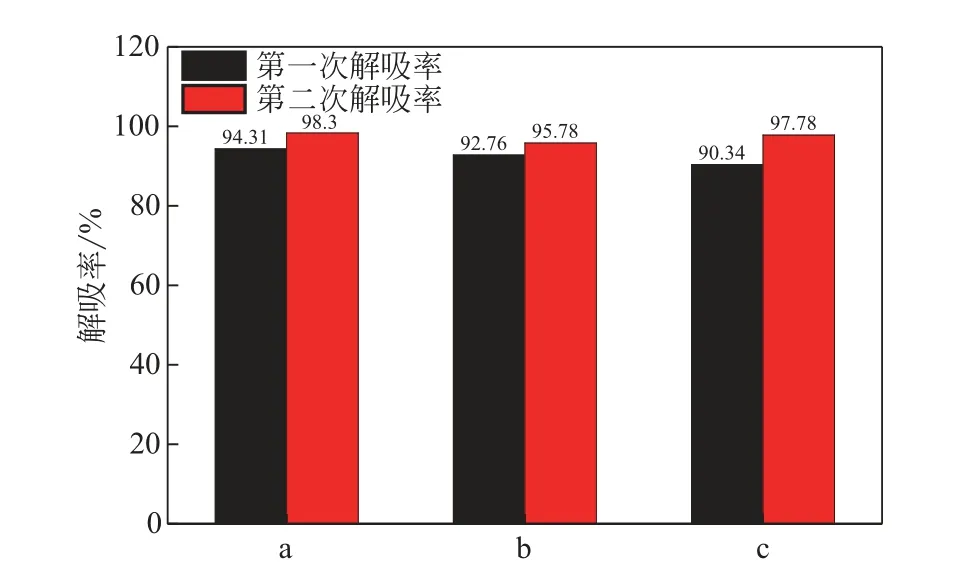
图9 EMEA+DEEA+PZ溶液降解前后解吸率对比
2.2.2 AMPD+PZ+HO溶液性能变化
图10~图12 分别是AMPD+PZ+HO 溶液降解前后的吸收解吸性能对比图,从吸收量、解吸量以及解吸率三个方面来评价降解的影响。从图10~图12可以看出,在经过热降解和氧化降解之后,进行了两次吸收解吸实验,溶液的两次吸收量分别为55.56L CO/kg、51.78L CO/kg,两次解吸量分别为52.78L CO/kg、50.56L CO/kg。氧化降解后的溶液两次吸收量分别为57.19L CO/kg、59.31L CO/kg,两次解吸量分别为55.00L CO/kg、55.00L CO/kg。在经过两次吸收解吸实验后,溶液的两次吸收解吸性能较稳定。热降解对于AMPD+PZ+HO溶液吸收解吸性能影响较大,造成溶液平均吸收量、平均解吸量分别下降5.63L CO/kg、4.03L CO/kg,平均解吸率升高2.32%,在经过氧化降解之后,溶液的平均吸收量、平均解吸量分别下降1.05L CO/kg、0.70L CO/kg,平均解吸率升高0.59%。对于AMPD+PZ+HO的吸收解吸性能来说,热降解的影响大于氧化降解。

图10 AMPD+PZ+H2O溶液降解前后吸收量对比

图11 AMPD+PZ+H2O溶液降解前后解吸量对比
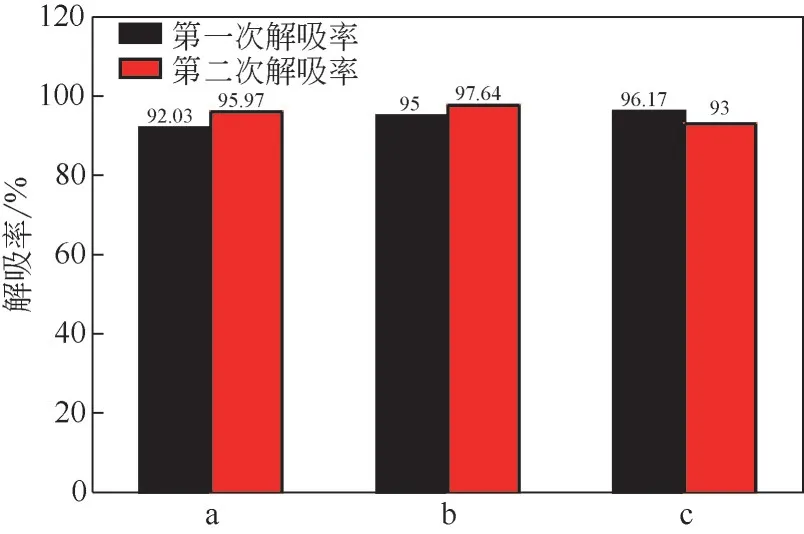
图12 AMPD+PZ+H2O溶液降解前后解吸率对比
2.3 胺溶液降解过程中胺浓度的变化
图13、图14 描述了在热降解和氧化降解过程中EMEA+DEEA+PZ、AMPD+PZ+HO 内主吸收胺浓度的变化。由图13、图14 可以看出,随着降解时间增加,样品中的胺含量逐渐减少。在热降解过程中,EMEA浓度降低了19.67%,AMPD浓度降低了71.89%;在氧化降解过程中,EMEA浓度降低了18.18%,AMPD 浓度降低了74.53%。选定的组成条件下,EMEA在热降解和氧化降解过程中的损失量远远小于AMPD。
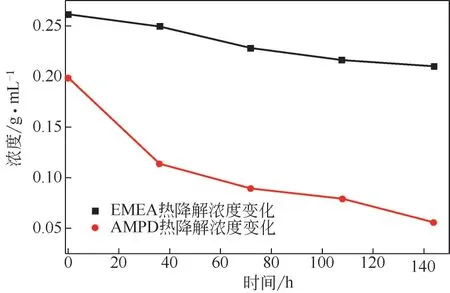
图13 EMEA与AMPD在热降解过程中的浓度变化
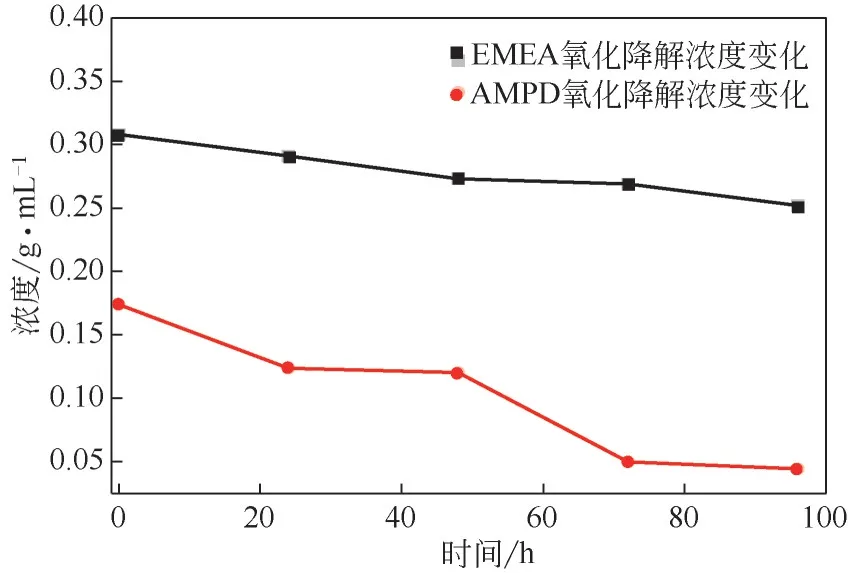
图14 EMEA与AMPD在氧化降解过程中的浓度变化
综上,在对EMEA+DEEA+PZ、AMPD+PZ+HO 两种溶液分别进行热降解和氧化降解之后发现,EMEA+DEEA+PZ 溶液在抗热降解、抗氧化降解性能方面优于AMPD+PZ+HO溶液。
2.4 醇胺溶液降解机理分析
2.4.1 EMEA+DEEA+PZ热降解机理分析

图15 EMEA+DEEA+PZ溶液在热降解前ESI-MS图
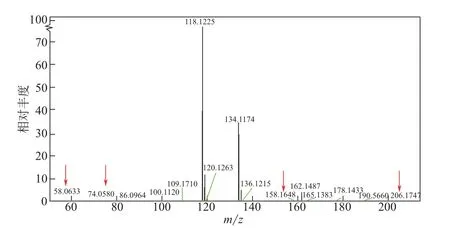
图16 EMEA+DEEA+PZ溶液在热降解后ESI-MS图
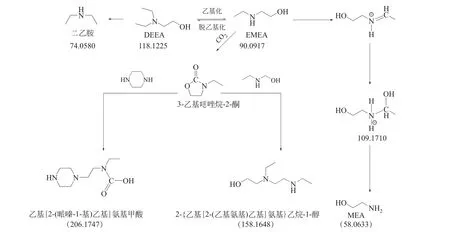
图17 EMEA+DEEA+PZ热降解的机理分析
2.4.2 AMPD+PZ+HO热降解机理分析

图18 AMPD+PZ+H2O溶液在热降解前ESI-MS图

图19 AMPD+PZ+H2O热降解后ESI-MS图
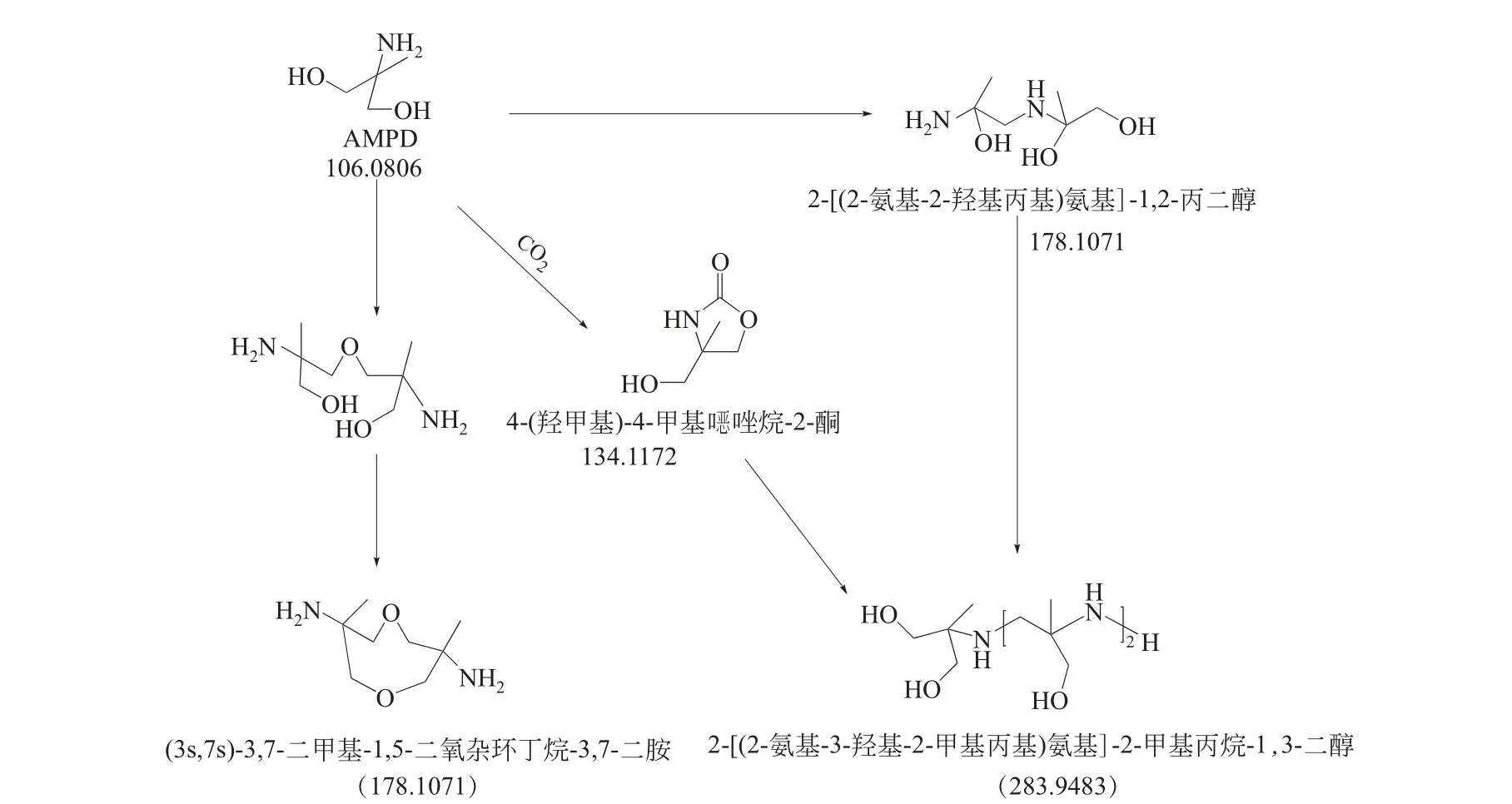
图20 AMPD+PZ+H2O热降解机理分析
2.4.3 EMEA+DEEA+PZ氧化降解机理分析
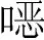

图21 EMEA+DEEA+PZ氧化降解前ESI-MS图

图22 EMEA+DEEA+PZ氧化降解后ESI-MS图
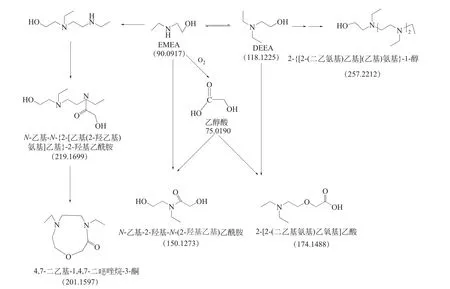
图23 EMEA+DEEA+PZ氧化降解机理分析
2.4.4 AMPD+PZ+HO氧化降解机理分析
图24、图25 分别是AMPD+PZ+HO 在氧化降解前后的电喷雾质谱图,将两张图进行对比可以看出氧化降解的产物峰,并将图26 中物质的峰在图25 中用箭头标出。由图24、图25 质谱图的结果可以推测出AMPD+PZ+HO 氧化降解机理(图26),AMPD分为两种路径被氧化:第一种是经过三次氧化后生成乙烷-1,1,1-三羧酸(164.0915);第二种路径中,首先AMPD被氧化生成2-亚氨基丙烷-1-醇和甲酸,生成的甲酸与AMPD 继续反应生成-(1, 3- 二 羟 基-2- 甲 基 丙 烷-2- 基) 甲 酰 胺(134.1171),而2-亚氨基丙烷-1-醇与水反应生成氨气与1-羟基丙-2-酮,氨气与碱性物质反应后和1-羟基丙-2-酮反应生成(Z)-1-羟基丙-2-酮肟(90.0917),1-羟基丙-2-酮与碱性物质反应生成甲醛和乙酸,甲醛与1-羟基丙-2-酮反应生成1,4-二羟基丁-2-酮(106.0860)。哌嗪被氧化成哌嗪-2-酮(101.0710)。
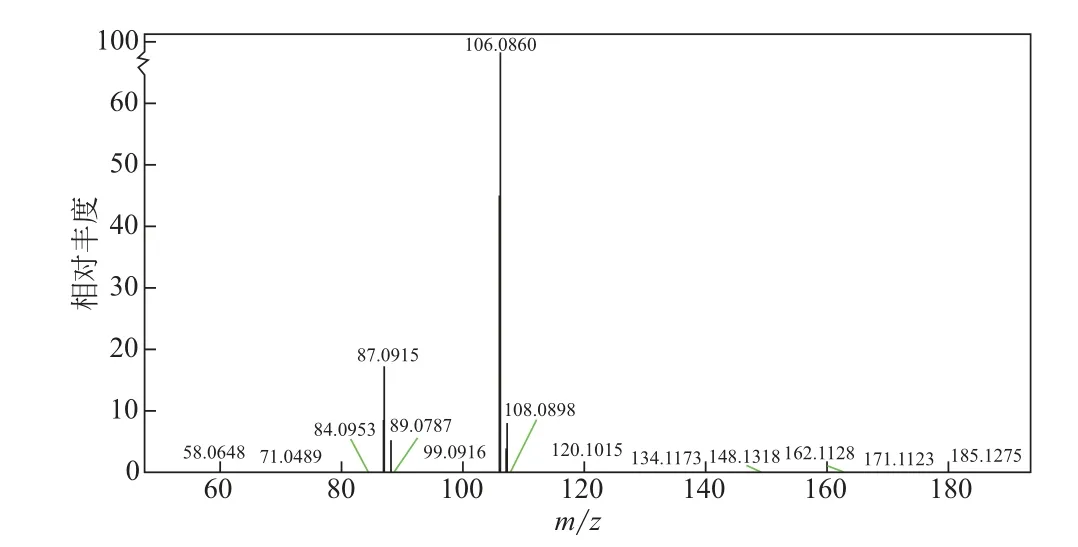
图24 AMPD+PZ+H2O氧化降解前ESI-MS图
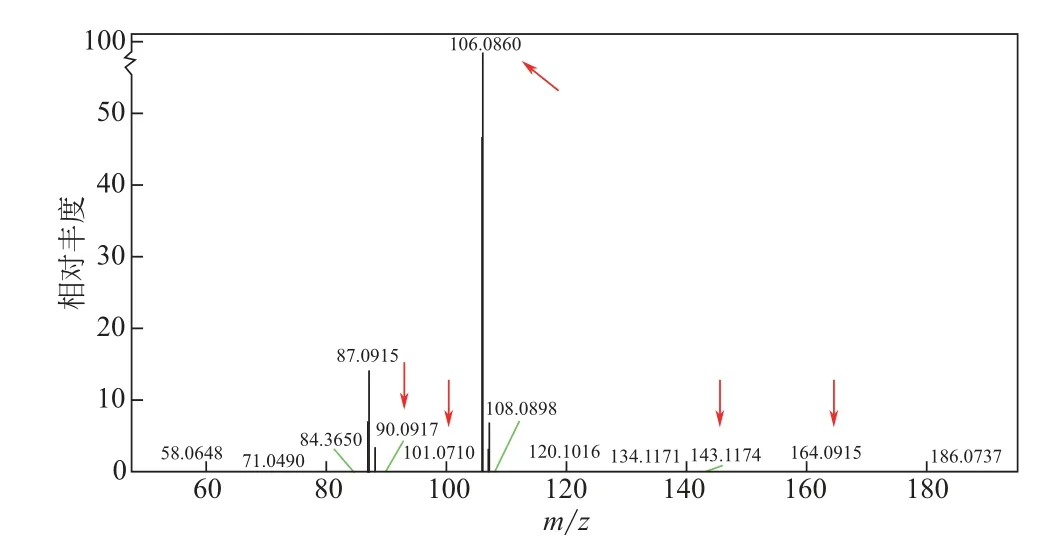
图25 AMPD+PZ+H2O氧化降解后ESI-MS图
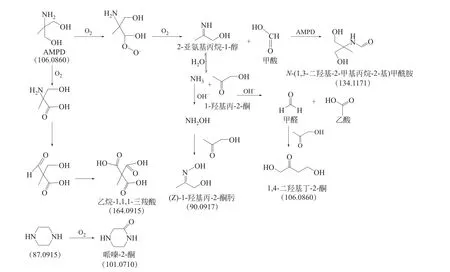
图26 AMPD+PZ+H2O氧化降解机理分析
3 结论
(1) AMPD+PZ+HO、EMEA+DEEA+PZ 两 种溶液在9 种不同复配溶液中,吸收和解吸性能最佳。
(2)EMEA+DEEA+PZ 溶液在抗热降解和抗氧化降解方面优于AMPD+PZ+HO溶液,在进行液质联用的表征之后也发现EMEA 的损失量远远小于AMPD。

(4) 对 于 本 文 中 研 究 的AMPD+PZ+HO、EMEA+DEEA+PZ 两种溶液体系,热降解显示了不同的影响,造成EMEA+DEEA+PZ 的吸收量、解吸量升高,AMPD+PZ+HO 的吸收量、解吸量降低,而氧化降解对于两种溶液体系的吸收解吸性能均具有负作用。

