莲藕可溶性膳食纤维与多酚复合物的稳定性及脂肪吸附活性研究
雷 丹, 李军胜, 李书艺,3*, 祝振洲,3, 何静仁,3
(1 武汉轻工大学食品科学与工程学院 武汉430023 2 湖北省农产品加工与转化重点实验室 武汉430023 3 武汉轻工大学硒科学与工程现代产业学院 武汉430023)
我国传统膳食主要是植物性食物,然而,随着经济和工业的高速发展, 人民的生活水平不断提高,饮食结构和膳食水平发生改变,过量糖类、脂肪及蛋白质的摄入及饮食的精细化导致高血糖、高血压、肥胖等代谢疾病患病率显著增高[1]。 随着食品营养学的发展,人们认识到谷物、蔬菜和水果等食物中富含的膳食纤维虽不能被人体消化吸收, 但对人体有很好的保健作用并起到多种疾病的预防作用[2]。 膳食纤维被称为“第七类营养素”,具有很强的持水性、 膨胀性以及吸附有机分子和交换阳离子等能力, 在人体健康中发挥着重要作用,如降低血浆胆固醇,改善血糖生成,控制体重,降血压和预防心脑血管等疾病[3-5]。 莲藕中含有丰富的膳食纤维(Dietary fiber, DF),藕皮、藕节中的DF 含量分别为21.14%和29.35%, 根据DF 的溶解性不同可将其分为水不溶性膳食纤维(Insoluble dietary fiber, IDF) 和水溶性纤维(Soluble dietary fiber, SDF)[6-8]。 食物中的IDF 具有显著增加粪便体积和质量, 促进排便, 预防结肠癌的功能,而SDF 的持水力高,黏性大,能够作为肠道微生物的基质,调节肠道菌群,降低餐后血糖和吸附脂肪、胆固醇等,增加粪便中脂肪及胆固醇的排出量,促进胆固醇转化为胆酸,降低脂肪及胆固醇的吸收[9]。
Macagnan 等[10]发现摄入高含量的多酚会为机体带来健康益处,这与多酚的降糖、改变肠道微生物、降血脂、抗肿瘤特性有关。 食物基质中的部分酚类化合物可从胃肠道上部释放出来, 直接被消化吸收,部分酚类化合物与SDF 结合通过胃肠道上部, 而这些未被小肠吸收的酚类化合物会在结肠中释放[11-12]。酚类化合物可在一定程度上抑制脂质的消化, 并在肠道内吸附胆酸盐和减少脂肪的吸收,使机体保持健康[13]。 研究表明莲藕中主要的酚类化合物包括儿茶酚、没食子酸、儿茶素、咖啡酸、香豆酸、白藜芦醇、芦丁、表儿茶素、绿原酸等,莲藕膳食纤维与这些酚类化合物质常以结合态存在, 可选择含量较大且不同构型的没食子酸与儿茶素作为研究对象, 探究可溶性膳食纤维与多酚之间的相互作用及复合物的功能特性[14]。
多糖与多酚等分子在食品加工过程中容易发生物理、化学反应,其非共价相互作用由氢键、静电吸引力、范德华力、疏水相互作用的组合共同驱动,改变多酚的功能特性,影响食品的感官品质和营养价值[15]。 在体内代谢中,多糖与多酚形成的复合物能够改善多酚的性质,如谢吉敏[16]利用环糊精衍生物包合多酚类物质,提高了多酚的溶解度、稳定性以及生物利用度。 Costa 等[17]评估了多酚物质儿茶素、阿魏酸、咖啡酸分别与多糖类物质纤维素、木聚糖间的相互作用,发现这两种膳食纤维不会降低酚类化合物的生物适应性, 且摄入适当的膳食纤维与多酚能够显著改善小鼠体内高脂高血糖等症状。 尽管多糖与多酚相互作用会影响多酚的功能特性,然而关于SDF 与多酚相互作用对油脂吸附特性的影响鲜见报道。 本试验基于多酚与多糖的非共价相互作用,制备莲藕SDF 与多酚的复合物,研究复合物对油脂、胆固醇吸附特性和阳离子交换能力的影响, 以促进莲藕中活性资源的综合利用,为SDF-多酚复合物在功能性食品中的应用提供参考。
1 材料与方法
1.1 材料与仪器
莲藕(品种为“鄂莲五号”3735),武汉菱湖净菜中心;没食子酸(Gallic acid, GA)(纯度95%)、儿茶素(Catechin, CC)(纯度95%),上海源叶生物有限公司;花生油、猪油,购买于武汉常青花园武商量贩超市;胆酸钠(分析纯级),天津化工试剂集团;所有的酸均为分析纯级。
ME104E 万分之一电子分析天平,梅特勒-托利多仪器有限公司;SHZ-82 恒温摇床, 国华仪器公司;T6 紫外分光光度计, 北京普析通用仪器公司。
1.2 试验方法
1.2.1 莲藕中可溶性膳食纤维的提取 根据GB/T 5009.88-2014《食品安全国家标准 食品中膳食纤维的测定》中的方法提取莲藕中的SDF。
1.2.2 可溶性膳食纤维与多酚复合物、 混合物的制备 取可溶性膳食纤维120 mg, 溶解于60 mL蒸馏水中,在80 ℃下磁力搅拌2 h 至完全溶解。冷却至室温后分别加入30 mL 1 mg/mL GA 和CC溶液, 混合均匀后将混合液转入预先处理好的透析袋(截留尺寸为1 000 u)中,再将透析袋放入装有500 mL 蒸馏水的烧杯中,控制反应温度,透析至吸附平衡,以透析袋外游离的GA 或CC 在波长280 nm 处的吸光值恒定不变为平衡终点[18]。 取出透析袋中溶液,经醇沉、冷冻干燥得到SDF-GA 复合物/SDF-CC 复合物, 并用福林酚法测得复合物中的总酚含量。
物理混合物的制备方法如下: 按照醇沉干燥后得到的复合物中SDF 与GA 质量比为69.4∶1。称取SDF 与GA 粉末, 将二者的固体粉末混合均匀得到SDF 和GA 的物理混合物; 同样方法制备SDF 与CC 质量比为56.2∶1 的物理混合物。
1.2.3 复合物中酚类物质稳定性测定
1.2.3.1 热稳定试验 参考羊芹[19]的方法,改用蒸馏水配置一定质量浓度的复合物样品溶液(1 mg/mL),分别取0.5 mL 样品溶液加入试管中避光,于20,30,40,50,60 ℃中水浴加热处理,1 h 后测定其总酚含量。
1.2.3.2 pH 值稳定性试验 分别配置pH 值为:2.0,3.0,4.0,5.0,6.0,7.0 的磷酸缓冲液,再用不同pH 值的缓冲液溶解样品, 制成质量浓度为1 mg/mL 不同pH 值的样品溶液, 装入试管中避光,水浴恒温(30 ℃)下,1 h 后测定其总酚含量。
1.2.4 复合物及混合物对油脂的吸附试验
1.2.4.1 饱和脂肪的吸附 采用王崇队等[20]和陈亚非等[21]的试验方法,测定复合体对含油脂物质的吸附量。准确称取5.000 g 样品,置于烧杯中,加入饱和脂肪100 mL,搅拌均匀,加入pH 2.0 的盐酸水溶液50 mL,于恒温振荡摇床37 ℃振荡1 h,4 000 r/min 离心20 min,去上层油,滤纸吸干残渣游离的脂肪,称重。 油脂的吸附量按下式计算:

式中,Q——油脂的吸附量,g/g;m1——所用油的质量,g;m2——游离油的质量,g;m3——样品的质量,g。
1.2.4.2 不饱和脂肪的吸附试验 准确称取5.000 g 样品, 置于烧杯中, 加入不饱和脂肪100 mL,搅拌均匀,加入pH 2 的盐酸水溶液50 mL,于恒温振荡摇床37 ℃振荡1 h,4 000 r/min 离心20 min,去上层油,滤纸吸干残渣游离的脂肪,称重。 计算公式如(1)式所示。
1.2.5 复合物及混合物对胆固醇的吸附试验 采用邻苯二甲醛法比色法测定胆固醇含量。 取新鲜鸡蛋蛋黄,用9 倍量蒸馏水充分搅打成乳液,准确称取0.500 g 样品于50 mL 锥形瓶中,加入50 g 稀释蛋黄,搅拌均匀,调pH 值至2.0(胃环境)或7.0(小肠环境),放置在37 ℃恒温摇床中震荡2 h,4 000 r/min 离心20 min,取上清液0.04 mL,用蒸馏水补齐至0.4 mL, 加入1 mg/mL 邻苯二甲醛溶液0.2 mL,混合酸(90%醋酸加等体积浓硫酸)4.0 mL,混匀后静置10 min,在波长550 nm 处比色测量吸光值[22-23]。 以胆固醇为标准品,按照相同方法测定吸光值,并绘制标准曲线y=21.837x+0.0241,R2=0.9958。
1.2.6 复合物及混合物胆酸盐的吸附试验 分别精确称取各样品0.2000 g 置于具塞试管中,加入1 mL 60%冰醋酸制备的1 mg/mL 胆酸钠溶液,再分别加入新制的糠醛溶液1.0 mL, 冰水浴5 min,再加入13 mL 硫酸溶液 (硫酸50 mL+蒸馏水65 mL),混匀,在70 ℃水浴10 min,然后迅速冰水浴2 min 后于波长605 nm 处测吸光值[21,24]。以胆酸钠为标准品, 按照相同方法制备标准曲线为y=0.308x+0.0668,R2=0.9956。
1.2.7 复合物及混合物的阳离子交换试验 准确称取SDF 与多酚复合物样品300 mg, 溶解于30 mL 0.01 mol/L HCl 溶液中,在4 ℃下过夜,用0.1 mol/L NaOH 滴定, 记录NaOH 消耗体积和溶液pH 值变化,作VNaOH-pH 关系图[24-25]。 以不加样品的30 mL 0.01 mol/L HC1 溶液做空白。
1.3 数据分析
每组试验设置3 个平行,结果取平均值,采用Excel,Origin 9.0 作图和SPSS 19.0 进行统计学分析,差异显著水平P <0.05 与非常显著P <0.01。
2 结果与分析
2.1 复合物中酚类物质的稳定性
2.1.1 温度对热稳定性影响 如图1 所示, 随着温度升高,复合物中的总酚含量逐渐降低。 在20~40 ℃范围内多酚含量变化不大, 温度升高到40℃以上SDF-CC 复合物中酚类化合物含量迅速降低4.80%, 而SDF-GA 复合物中的酚类含量降低4.47%,这种酚类含量随温度变化的结果与李利华等[26]及矫馨瑶等[27]的结论一致。 SDF-CC 复合物中酚类化合物的含量比SDF-GA 复合物降低快,这是由于具有更多羟基数目的CC 比GA 在加热情况下更容易氧化。郑燕菲等[28]和赵玉等[29]发现多酚置于较高温度环境下会发生裂解等反应, 这是因为具有不饱和键的多酚类化合物会发生氧化聚合被降解,且羟基的数目与其还原性的强弱有关,酚羟基数目越多越易受热氧化, 且温度越高氧化发生越快,酚类含量损失越大。
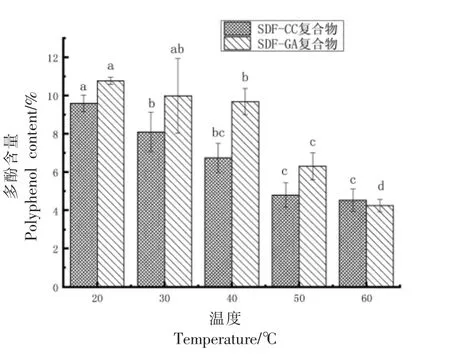
图1 不同温度对复合物中酚类物质的稳定性影响Fig.1 Effect of different temperatures on the stability of phenolic compounds in complex
2.1.2 pH 值对复合物稳定性的影响 如图2 所示,在不同pH 值条件下,两种复合物酚类化合物含量的变化表现出相同的趋势, 复合物中的酚类在较强的酸性环境下较为稳定, 体系pH 值大于5.0 后复合物中的酚类含量降低较明显,SDF-GA复合物总酚含量减少1.76%,SDF-CC 复合物中酚类含量降低1.17%。 这与高凝轩等[30]发现多酚在pH 2.0~3.0 范围最为稳定,pH 值大于5.0 以后多酚的保留率显著降低结果一致。 两种酚类化合物对于不同的pH 值溶液的稳定性差异, 可能是负载的酚类CC 与GA 结构中酚羟基数目多少与结构的差异,另外由于多酚中含有大量的羟基,呈弱酸性,所以在酸性环境下较为稳定。 席利莎等[31]在不同pH 值条件下对甘薯茎叶进行加工, 发现甘薯茎叶中多酚的稳定性在中性和弱酸性体系中较好。
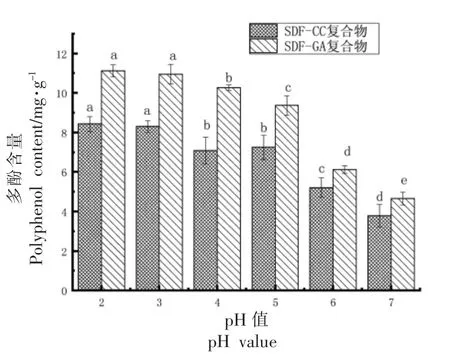
图2 不同pH 值对复合物中酚类物质稳定性的影响Fig.2 Effect of different pH value on the stability of phenolic compounds in complex
2.2 复合物对油脂的吸附作用
改性可溶性膳食纤维在胃肠道内黏性增大,膨胀后产生饱腹感可减少总能量的摄入, 吸附脂肪后延缓脂肪的消化吸收,抑制脂肪的摄入,从而达到降脂作用[32]。 复合物对油脂的吸附作用如图3a 所示,SDF、SDF-GA 复合物、SDF-GA 物理混合物、SDF-CC 复合物及SDF-CC 物理混合物对饱和脂肪的吸附量分别为(1.20±0.15),(3.06±0.28),(1.61±0.23),(3.12±0.42)g/g 和(1.57±0.21)g/g;对不饱和脂肪的吸附量分别为(1.60±0.10),(5.92±0.19),(1.87±0.16),(7.52±0.46)g/g 和(1.96±0.16)g/g。 由结果可知, 两复合物对油脂的吸附量明显(P<0.01)比SDF 大,而两物理混合物对油脂的吸附效果与SDF 相比无明显区别。 SDF-CC 复合物与SDF-GA 复合物对不饱和脂肪的吸附显著强于饱和脂肪, 原因可能是复合物易与不饱和键中的氢原子相互吸引和结合。 在前期试验中发现复合物的粒径小于混合物的粒径, 且其对油脂的吸附量大小与粒径大小有相关性, 这种由于复合物粒径较小对脂肪的吸附量大的结果与Raghavendra等[33]的结论一致。 Raghavendra 等[33]发现椰子渣膳食纤维的粒度减小, 其水合性能及脂肪吸收能力反而增大,这是由于随着粒度减小其表面积、总孔体积变大,导致其对脂肪的吸附容量变大。

图3 复合物及混合物对不同脂肪酸的吸附能力Fig.3 Adsorption capacity of complex and mixture for different fatty acids
2.3 复合物对胆固醇的吸附作用
膳食纤维通过刺激血浆和肝脏中的胆固醇使其转变成胆酸,并与胆酸结合防止其重吸收,进而抑制胆固醇的合成,增加粪便中胆固醇的含量,从而降低体内胆固醇[34-35]。 如图4 所示,模拟环境溶液在pH 7.0 条件下,SDF、SDF-GA 复合物、SDFGA 混合物、SDF-CC 复合物及SDF-CC 混合物对胆固醇的吸附量分别为(7.05±0.19),(8.17±1.12),(8.73±0.02),(8.09±0.02)mg/g 和(6.23±0.05)mg/g,复合物对胆固醇的吸附效果极显著高于SDF(P<0.01)。 在pH 2.0 时对胆固醇的吸附量分别为(5.43±0.01),(6.25±0.02),(6.12±0.01),(5.03±0.01)mg/g 和(2.83±0.04)mg/g,这说明不同多酚与SDF 之间相互作用会改变SDF 对胆固醇的吸附能力, 且复合物在中性条件下对胆固醇的吸附量比酸性条件下的高。周笑犁等[36]和杨振寰[37]发现可溶性膳食纤维对胆固醇的吸附能力与体系的酸碱性有较大的关系, 且在中性条件下膳食纤维对胆固醇的吸附量比在酸性条件大。
2.4 复合物对胆酸盐吸附作用
胆酸盐是指人体和动物胆汁中由胆固醇衍生的具有甾核结构的一类两性大分子, 胆酸盐被膳食纤维吸附排出体外, 从而对脂肪和胆固醇的消化吸收起重要作用[35,38]。 如图5 所示,SDF 对胆酸钠的吸附量最小,SDF-GA 复合物对胆酸钠的吸附量高于SDF-GA 物理混合物(P<0.05),而SDFCC 复合物对胆酸钠的吸附作用与SDF-CC 物理混合物无明显区别。结果表明,酚类的存在能显著性提高SDF 对胆酸钠的吸附作用,且吸附量大小与酚类化合物种类有关。 胡凯等[38]通过体外模拟不同茶叶结合胆酸钠的试验, 发现茶多酚结合胆酸盐的能力与茶多酚含量成正相关。 刘淑敏等[39]在模拟pH 值与尿素对胆酸盐吸附试验中,同样发现绿茶多酚是绿茶浸提液中结合胆酸盐的功能成分,且主要相互作用力是静电引力与氢键作用。
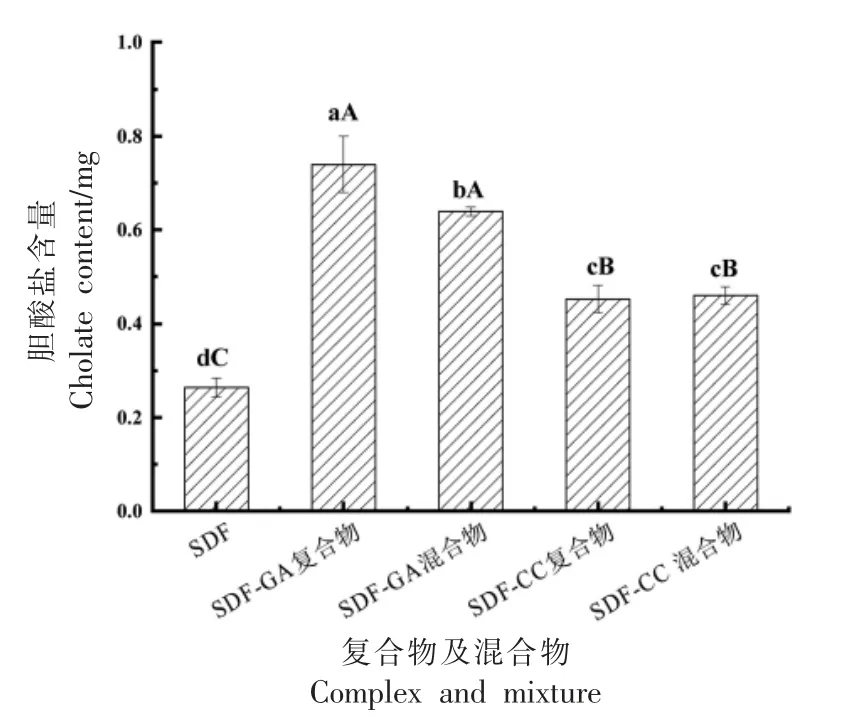
图5 复合物及混合物对胆酸盐的吸附能力Fig.5 Adsorption capacity of complex and mixture for cholate
2.5 复合物对阳离子交换能力
阳离子交换能力是膳食纤维维持肠道pH 值稳定和保持离子浓度平衡的一种能力, 膳食纤维与酚类化合物的分子结构带有一些含有羧基和羟基的侧链基团, 侧链基团中的羧基和羟基可以与弱酸性阳离子实现可逆交换[24,40]。 曲鹏宇等[3]试验发现曲线斜率越小表示SDF 的阳离子交换能力越强。 如图6a 所示,各组物质对阳离子的交换能力依次为SDF-GA 物理混合物>SDF-GA 复合物>SDF,图6b 所示各组物质对阳离子的交换能力依次为SDF-CC 复合物>SDF-CC 物理混合物>SDF,表明酚类加入可以显著提高SDF 的阳离子交换能力。 这是因为SDF 与酚类化合物之间相互作用以一定的方式连接改变了复合物的部分性质,复合物比SDF 中维持溶液的pH 值的基团多, 使得复合物维持溶液pH 值能力显著高于SDF。
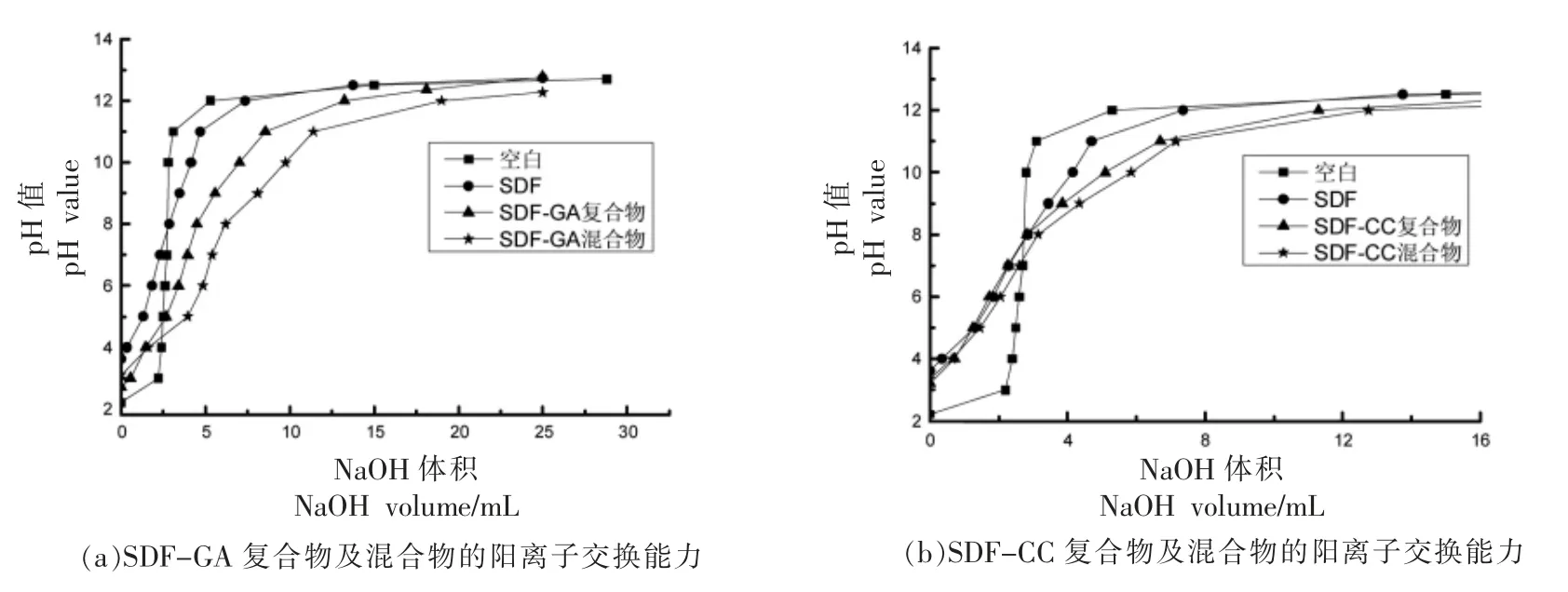
图6 复合物及混合物的阳离子交换能力Fig.6 Cation exchange capacity of complex and mixture
3 结论
通过体外模拟试验可知温度、pH 值对莲藕可溶性膳食纤维与多酚复合物的稳定性有显著影响,随着温度的不断升高,复合物中多酚含量逐渐下降。 在极酸的环境条件下复合物中的多酚类物质较稳定, 随着pH 值升高酚类物质显著性降低。另外,SDF 与酚类化合物之间的相互作用显著增强了SDF 对油脂、胆固醇、胆酸盐的吸附能力和阳离子交换能力, 且复合物对不饱和油脂的吸附量强于饱和油脂。综上可见,莲藕可溶性膳食纤维与多酚间的相互作用在降脂、 降胆固醇等方面有积极的保健作用。

