喹啉酮-香豆素类Hg2+比色荧光探针的合成及应用
唐 倩,但飞君,郭 涛,兰海闯
(三峡大学生物与制药学院,宜昌 443002)
Hg2+被认为是毒性最强的离子之一,它能够通过食物链转移,在生物体内累积[1~4].对于人类来说,即使很低浓度的Hg2+也可能会永久破坏肾脏、心脏及神经系统[5~8].鉴于Hg2+的高毒性,中华人民共和国国家标准规定生活饮用水中Hg2+含量不得高于0.001 mg/L(0.5×10−8mol/L),地表水中Hg2+含量不得高于0.05 mg/L(2.5×10−7mol/L)[9].因此,探索具有高灵敏度、高选择性、原位实时以及低成本的Hg2+检测方法具有重要意义.目前,将原子荧光光谱分析法[10]、电感耦合等离子体质谱法[11]和高效液相色谱法[12,13]等方法用于检测Hg2+已有研究报道.与这些方法相比,比色法和荧光法具有操作简便[14]、原位实时监测[15]及成本低[16,17]等优点,在离子检测、环境和生命等领域应用广泛[18,19].比色法和荧光法的核心之一是识别离子的探针,已报道的Hg2+探针多是基于单一信号的探针[20,21],相比之下,利用2个或多个不同波长的信号比值变化的比率型探针自带内标效应,可以在一定程度上抵消外界干扰因素,提高分析结果的准确度[22,23].
喹啉酮和香豆素结构类似,其分子结构刚性,具有较大的共轭平面[24]和较好的光学性能[25~27],其结构中的杂原子与金属离子作用后[28],可引起其溶液颜色、吸收和发射光谱的改变.本文通过缩合反应得到含有喹啉酮和香豆素结构的探针7-二乙氨基-3-[3-(7-二乙氨基)香豆素基-3-氧代丙烯基]喹啉-2-酮(QCO).该探针分子中的杂原子选择性地与Hg2+作用后,其最大吸收峰明显蓝移(约120 nm),溶液颜色由红色变为黄色;同时,位于650 nm最大发射峰的荧光强度显著降低,溶液由红色荧光变为蓝色荧光.通过测定吸收值比(A500/A380)和650 nm发射强度,探针QCO可以实现对Hg2+快速、准确的比色及荧光双通道检测.该方法可用于实际水样中Hg2+的测定.
1 实验部分
1.1 试剂与仪器
3-二乙氨基乙酰苯胺、4-二乙氨基水杨醛和乙酰乙酸乙酯购于上海安耐吉化学有限公司;固体光气(BTC)、乙醇(EtOH)、乙酸(AcOH)、1,2-二氯乙烷、N,N-二甲基甲酰胺(DMF)、哌啶(Pip)、甲醇和乙酸乙酯购于国药集团化学试剂有限公司;所用试剂及溶剂均为分析纯;实验用水为二次蒸馏水.
Bruker AV 400 MHz型核磁共振波谱仪(NMR,瑞士Bruker公司);Amazon SL-ESI-trap-MS型质谱仪(MS,德国Bruker公司);WRS-1A型熔点仪(上海索光光电技术有限公司);F-4600型荧光光谱仪(日本Hitachi公司);UV-2600型紫外-可见分光光度仪(UV-Vis,日本Shimadzu公司);Nicolet NEXUS 470型红外光谱仪(IR,美国Perkin-Elmer公司).
1.2 实验过程
探针QCO的合成路线如Scheme 1所示.

Scheme 1 Synthesis of probe QCO
1.2.1 2-氯-7-二乙氨基喹啉-3-甲醛(1)的合成 参照文献[29]方法合成化合物1,产率74.77%,m.p.98.6~99.1℃(文献值[29]:98.6~99.1℃),核磁共振谱图见本文支持信息图S1和图S2.
1.2.2 3-甲酰基-7-二乙氨基喹啉-2(1H)-酮(2)的合成 向50 mL两口瓶中加入1.00 g(3.8 mmol)化合物1和10 mL 70%(体积分数)乙酸水溶液,升温至80℃搅拌4 h.反应完成后(薄层色谱法监测),冷却至室温,抽滤,滤饼用甲醇和水重结晶,干燥,得到0.84 g褐色固体2,产率90%,m.p.245.2~246.5℃.1H NMR(400 MHz,CDCl3),δ:12.06(s,1H),10.40(s,1H),8.33(s,1H),7.50(d,J=9.1 Hz,1H),6.69(dd,J=9.1,2.3 Hz,1H),6.51(s,1H),3.53(q,J=7.1 Hz,4H),1.31(t,J=7.1 Hz,6H);13C NMR(100 MHz,CDCl3),δ:189.19,165.05,152.08,144.08,142.15,132.32,119.05,110.49,94.75,45.14,12.57(核磁共振谱图见本文支持信息图S3和图S4).
1.2.3 3-乙酰基-7-二乙胺基香豆素(3)的合成 参照文献[30]方法合成化合物3,产率为90.0%,m.p.156~158℃(文献值[31]:148~149℃),核磁共振谱图见本文支持信息图S5和图S6).
1.2.4 探针QCO的合成 向100 mL两口瓶中依次加入2.60 g(10.0 mmol)化合物2,2.44 g(10.0 mmol)化合物3和50 mL乙醇,再加入1.0 mL乙酸和1.0 mL哌啶,搅拌溶解,回流反应12 h.将反应液冷却至室温,抽滤,用甲醇重结晶,干燥,得到QCO红色固体4.22 g,产率87.0%,m.p.248.1~249.3℃.IR(KBr),ν͂/cm−1:3300,1690,1630,1570;1H NMR(400 MHz,DMSO-d6),δ:11.43(s,1H),8.54(s,1H),8.22(s,1H),8.17(d,J=9.6 Hz,1H),7.71(dd,J=15.6,10.8 Hz,2H),7.51(d,J=9.2 Hz,1H),6.80(d,J=10.0 Hz,1H),6.69(d,J=9.2 Hz,1H),6.61(s,1H),6.48(s,1H),3.50(q,J=6.4 Hz,4H),3.42(q,J=13.2 Hz,4H),1.15(t,J=6.4 Hz,12H);13C NMR(100 MHz,DMSOd6),δ:186.40,161.88,160.21,158.52,153.17,150.71,148.35,142.28,141.44,139.42,132.58,130.75,123.76,119.66,116.74,110.44,109.42,108.34,96.35,94.20,44.88,44.63,12.95,12.84;ESI-MS(C29H31N3O4理论值),m/z:486.23(486.03);核磁共振谱图及质谱图见本文支持信息图S7~图S9.
1.2.5 光谱测量方法 将探针QCO溶于N,N-二甲基甲酰胺中配制成1.0×10−3mol/L的储备液.将储备液用甲醇/水(体积比7∶3)稀释至1.0×10−5mol/L用于光谱测试.实验中光谱测试均在甲醇/水(体积比7∶3)体系中进行,金属离子的浓度为1.0×10−4mol/L.不加入待测样品的溶液即为空白试液.将待测液放置1.0 h后,测定紫外-可见光谱和荧光光谱(激发波长为500 nm).
1.2.6 实际样品的检测 分别以自来水和江水(取自长江宜昌段,测试前先过滤掉其中的泥沙)作为待测水样,所取水样经过滤和除杂后,与甲醇以体积比7∶3混合,测定并调整pH后,加入探针QCO及不同量的Hg2+,测定650 nm处的荧光强度.
2 结果与讨论
2.1 探针QCO对Hg2+的选择性识别

Fig.1 UV⁃Vis spectra and photos(A),fluorescence spectra and photos(B)of probe QCO(1.0×10−5 mol/L)with different metal ions(Na+,K+,Ag+,Ca2+,Ba2+,Mn2+,Co2+,Cu2+,Ni2+,Zn2+,Cd 2+,Hg2+,Pb2+,Fe3+,Al3+and Cr3+,1.0×10−4 mol/L)in MeOH/H2O solution
为了考察探针QCO对金属离子的识别能力,分别测定空白试液和添加各种金属离子(Na+,K+,Ag+,Ca2+,Ba2+,Mn2+,Co2+,Cu2+,Ni2+,Zn2+,Cd2+,Hg2+,Pb2+,Fe3+,Al3+及Cr3+)后探针QCO溶液的紫外-可见光谱和荧光光谱(图1).结果表明,探针QCO的吸收峰位于500 nm处,当加入不同金属离子后,仅Hg2+使探针QCO在500 nm处的吸收峰消失,在380和450 nm处产生新的吸收峰,且探针QCO溶液由浅粉红色变为黄色[图1(A)].同时,探针QCO溶液呈现深粉红色荧光,最大发射峰位于650 nm,当加入不同金属离子后,也只有Hg2+能引起探针QCO溶液发射光变为青色,650 nm处的荧光强度明显减弱[图1(B)].可见,探针QCO对Hg2+的检测具有高选择性,可裸眼识别.
为了进一步考察在其它金属离子存在下,探针QCO检测Hg2+的选择性识别,尝试了在相同检测条件下,其它金属离子与Hg2+共存时对探针QCO的紫外-可见光谱和荧光光谱的影响.由图2可见,其它金属离子与Hg2+共存时,探针QCO的吸收值和荧光强度几乎不变.表明探针QCO对Hg2+的检测几乎不受其它金属离子的干扰.

Fig.2 Absorbance(A)and fluorescence intensity(B)changes of probe QCO(1.0×10−5 mol/L)upon addition of various metal ions(1.0×10−4 mol/L)in the presence of Hg2+
2.2 探针QCO对Hg2+的定量识别
为了考察Hg2+对探针QCO的紫外-可见吸收光谱和荧光光谱的影响,测定了甲醇/水(体积比7∶3)溶液中含不同浓度的Hg2+时探针QCO的光谱.由紫外-可见吸收光谱[图3(A)]可见,随着Hg2+的浓度逐渐增加,探针QCO在500 nm的吸收峰不断降低,在380和450 nm处的吸收峰不断增强,且在465 nm处出现1个等吸收点.Hg2+浓度在0~32.5 μmol/L范围内,探针QCO在500和380 nm处吸收值的比值(y)与Hg2+浓度(x)呈现良好的线性关系(y=−0.2524x+9.1169,R2=0.9904),检出限(LOD)为2.62×10−8mol/L[图3(B)].同时,随着Hg2+浓度的增加,QCO在650 nm处的荧光强度不断降低[图4(A)],荧光强度与Hg2+浓度(0~40 μmol/L)呈现出良好的线性相关[图4(B)],其方程为y=−17.2785x+844.018,R2=0.9914,检出限为5.42×10−8mol/L.上述结果可知,在一定范围内,探针QCO可用于Hg2+的比色、荧光定量检测,且具有高灵敏性,检出限均低于工业废水中Hg2+的最大允许浓度,可用于工业废水中Hg2+的检测.

Fig.3 UV⁃Vis spectra of probe QCO(1.0×10−5 mol/L)with different concentrations of Hg2+in MeOH/H2O solution(pH=6.5)(A)and the linearity of the absorbance ratio A500/A380 at 500 and 380 nm as a function of Hg2+concentration(B)
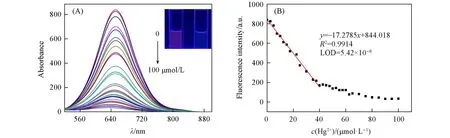
Fig.4 Fluorescence spectra of probe QCO(1.0×10−5 mol/L)with different concentrations of Hg2+in MeOH/H2O solution(pH=6.5)(A)and the linearity of the fluorescence intensity vs.concentration of Hg2+(B)
2.3 时间和pH值对探针QCO识别Hg2+的影响
通过随时间变化的荧光光谱研究了探针QCO和Hg2+之间的反应动力学行为.由图5可见,向探针QCO溶液中添加Hg2+后,5 min内探针QCO在650 nm处的荧光强度迅速降低,延长至60 min,荧光强度基本保持不变.此现象表明,QCO和Hg2+结合反应迅速且稳定,探针QCO可以实时检测水溶液中Hg2+.进一步考察了pH对探针QCO识别Hg2+的影响(图6).在pH=4.5~13.5范围内,探针QCO的吸收值和荧光强度基本保持稳定,表明探针QCO可在较宽的pH范围内应用.添加Hg2+后,探针QCO的吸收值与荧光强度在pH=6.5~9.5范围内变化不大.产生这种现象的原因可能是探针QCO有多个质子化位点,在酸性条件下探针质子化,影响了对Hg2+的识别;另外,强碱性条件下Hg2+会产生氧化物沉淀.基于此,推断探针QCO适合在中性或弱碱性条件下识别Hg2+.
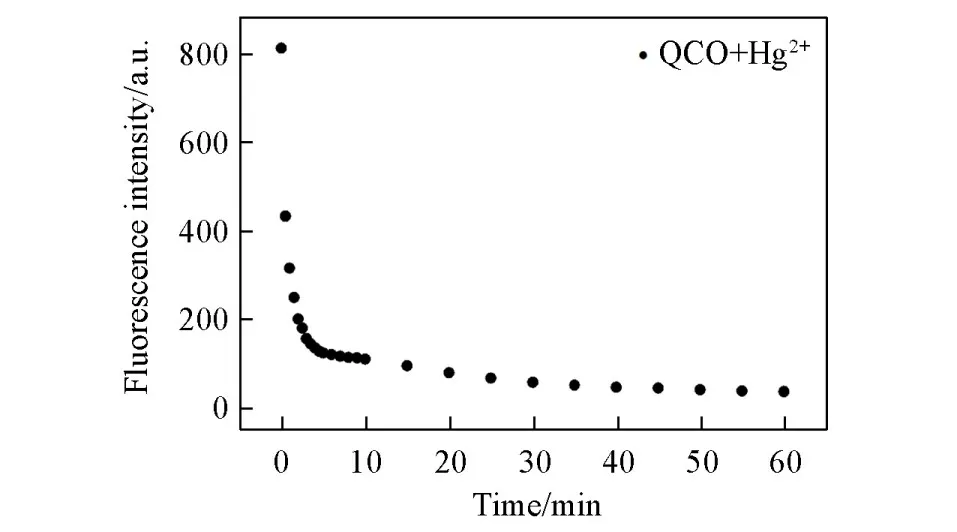
Fig.5 Effect of time on the fluorescence intensity of probe QCO(1.0×10−5 mol/L)to Hg2+(1.0×10−4 mol/L)

Fig.6 Effect of pH on absorbance(A)and fluorescence intensity(B)of probe QCO(1.0×10−5 mol/L)to Hg2+(1.0×10−4 mol/L)
2.4 探针QCO对Hg2+的识别机理
采用Job’s Plot法、质谱和红外光谱探究了探针QCO对Hg2+的识别机理.为了确定探针QCO与Hg2+络合的化学计量比,运用Job’s Plot法进行分析测定.由图7(A)可知,当[Hg2+]/([Hg2+]+[QCO])=0.5时,探针QCO在650 nm处的荧光强度达到最大值,表明探针QCO与Hg2+络合的摩尔比为1∶1.
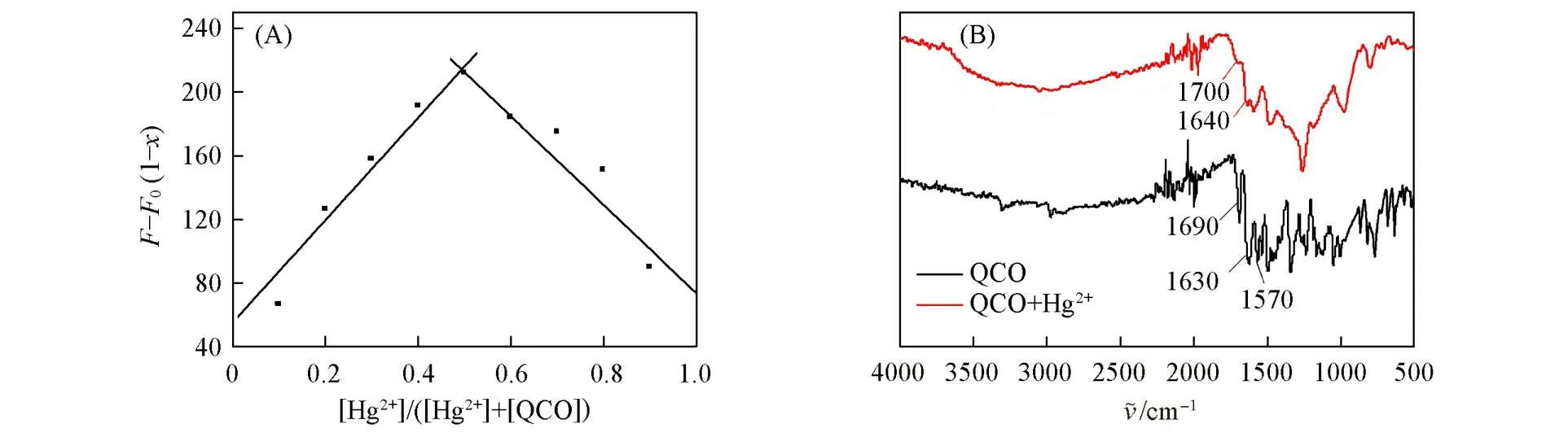
Fig.7 Job’s plot of the binding between probe QCO and Hg2+(A)and IR spectra of probe QCO,QCO and Hg2+complex in KBr disks(B)
为了进一步确定探针QCO对Hg2+的识别机理,测定了探针了QCO与Hg2+络合物的质谱,结果见图8.在探针QCO与Hg2+络合物的质谱图中,碎片峰m/z486.73和683.78分别归属于[QCO+H]+和[QCO+Hg]+.这表明探针QCO与Hg2+通过络合作用形成了摩尔比为1∶1的络合物.

Fig.8 Mass spectra of probe QCO and Hg2+complex
通过探针QCO,QCO与Hg2+络合物的红外光谱进一步推测了QCO对Hg2+的识别机理[图7(B)].在QCO的红外光谱中,1690 cm−1处的峰归属为香豆素C=O的拉伸振动[32],1630和1570 cm−1处的峰为喹啉酮中酰胺的吸收峰[33].QCO与Hg2+络合物的红外光谱中进行实验,香豆素和喹啉酮的C=O吸收峰分别红移至1700和1640 cm−1处.根据以上实验结果,推测了QCO对Hg2+的可能识别机理(见Scheme 2),探针QCO与Hg2+的络合位点可能是香豆素C=O的O和喹啉酮C=O的O.

Scheme 2 Possible recognition mechanism of probe QCO to Hg2+
2.5 探针QCO对Hg2+的实际检测
为了研究探针在Hg2+检测中的实际应用,将含QCO的硅胶板浸入到不同浓度(0,1.0×10−6,1.0×10−5,1.0×10−4,1.0×10−3和1.0×10−2mol/L)的Hg2+溶液中进行实验.由图9可见,随着Hg2+浓度的增加,在自然光下,TLC板的颜色从浅粉红色变为黄色;在365 nm的紫外灯照射下,其颜色从深粉红色变为青色.即使当Hg2+浓度为1.0×10−6mol/L时,仍然可以区分出差异.此结果表明,采用探针QCO可通过裸眼识别痕量的Hg2+.

Fig.9 Photos of the TLC plates coated QCO with various concentrations of Hg2+under the natural light(A)and a 365 nm UV lamp(B)
为了评估探针QCO对Hg2+识别的实际应用价值,采用自来水和江水2种水样,加入不同浓度的Hg2+,用探针QCO检测其Hg2+浓度.测试结果如表1所示,不同水样中Hg2+的回收率在87%~105%之间,RSD小于2%.此结果表明,探针QCO可应用于实际水样中的Hg2+的检测.

Table 1 Detection of Hg2+in actual water samples
3 结 论
通过醛酮缩合反应得到新型喹啉酮-香豆素类探针QCO,其合成方法简单、产率高.探针QCO能以比色法和荧光法识别Hg2+,选择性好、灵敏度高.尤其是探针QCO在330~600 nm范围内的吸收光谱显著蓝移(120 nm),其可作为比率型探针裸眼识别Hg2+;探针QCO的发射波长在520~850 nm范围内,其可作为近红外探针应用于实际水样中Hg2+的检测.因此,这些优异的性能为探针QCO用于环境中Hg2+的监测和生物样品中Hg2+的检测提供了重要依据.
支持信息见http://www.cjcu.jlu.edu.cn/CN/10.7503/20210660.

