玻璃纤维负载Fe3O4催化膜的制备及其降解染料性能
赵永男,黄国辉,高海燕,安仁德,吕铭含
(1.天津工业大学 天津市先进纤维与储能技术重点实验室,天津 300387;2.天津工业大学 材料科学与工程学院,天津 300387)
合成染料广泛应用于纺织、涂料和塑料工业。由于染料的化学稳定性,染料废水一直是一个严重的环境问题[1-2]。高级氧化法(AOPs)具有氧化能力强、反应速度快、效率高、选择性低等优点,已成为一种颇具前景的水处理替代策略[3-4]。作为一种经典的AOPs,芬顿反应对大多数有机污染物具有快速高效降解的技术优势[5-6]。然而,经典的芬顿反应面临以下问题:在中性或碱性条件下降解活性较低、H2O2浓度要求高、催化剂回收困难以及与铁氧化物沉积相关的二次污染[7-8]。近年来,非均相芬顿反应得到了广泛的研究,已成为克服铁浸出和强酸反应条件挑战的一种有吸引力的方法[9-10]。Fe3O4由于Fe2+含量高、成本低、生态友好、独特的磁性和可见光驱动活性等优点,被证明是一种有效的非均相光芬顿催化材料[11-13]。尽管如此,Fe3O4仍存在光生电子空穴对复合率高、易团聚、所需H2O2浓度高等缺点[11]。而玻璃纤维具有高比表面积、化学稳定性、柔韧性和透光性[14],可以很好地作为Fe3O4的载体以克服其在催化过程中的问题。本文以玻璃纤维为载体,通过简单的溶剂热法,制备玻璃纤维负载Fe3O4薄膜的非均相芬顿催化剂并研究其降解染料性能。
1 实验部分
1.1 试剂与仪器
试剂:乙二醇,分析纯,天津市科密欧化学试剂有限公司产品;六水合氯化铁(FeCl3·6H2O)、氢氧化钠,分析纯,上海阿拉丁试剂有限公司产品;活性红、玻璃纤维,市售。
仪器:D8 ADVANCE型X射线衍射仪(XRD,Cu-Kα射线,λ=0.154 06 nm),德国Bruker公司产品;Hitachi S-4800型扫描电子显微镜,日本Hitachi公司产品;JEM-2100型高分辨率透射电子显微镜,日本电子株式会社公司产品;Lambda-750紫外可见分光光度计,美国Thermofisher科技公司产品。
1.2 样品的合成
采用溶剂热法制备玻璃纤维负载Fe3O4催化膜。首先用异丙醇清洗,再依次用4 mol/L盐酸、去离子水和无水乙醇超声清洗玻璃纤维,室温下干燥。然后称取5 mmol的FeCl3·6H2O溶于40mL的乙二醇中,室温下搅拌至溶液透明,再加入15mmol的NaOH,继续快速搅拌30min。然后将清洁的玻璃纤维与混合液置于100 mL的反应釜中,密封后在180℃温度条件下反应8 h,自然冷却至室温,取出玻璃纤维并用去离子水和无水乙醇清洗多次,在60℃温度条件下干燥12 h得到催化剂,命名为FOGF。催化剂中Fe3O4的含量采用质量法测量。
1.3 光催化测试
将催化剂FOGF(用量为包覆的Fe3O4质量)加入到50 mL质量浓度为40 mg/L的活性红溶液中,用0.1 mol/LHCl或0.1mol/LNaOH溶液调节初始pH值。然后加入0.3 mL 30%的H2O2溶液至反应器中,在300 W氙灯的照射下开始反应。在光照过程中,每10 min取5 mL反应液,测量吸光度。降解率D的计算公式为:

式中:D为t时刻的降解率;C0表示初始浓度;Ct表示t时刻的浓度。
为了探究光芬顿催化膜的催化寿命,以60 min为1个光催化降解周期,用同一组纤维催化剂进行多次反应,每次反应后将催化膜洗净晾干,然后在相同条件下对新配置的染料溶液进行降解,通过每次反应的降解率评价催化剂的催化寿命。
2 结果与讨论
2.1 材料的表征
样品的XRD图如图1所示。

图1 FOGF的XRD图谱Fig.1 XRD patternsof FOGF
由图1可见,样品在18.1°、30.10°、35.50°、43.16°、53.62°、57.05°、62.61°和74.08°处出现衍射,对应于立方相反尖晶石Fe3O4(JCPDSNo.89-2355)的(111)、(220)、(311)、(400)、(422)、(511)、(440)和(533)晶面。无杂质峰出现,表明颗粒膜为纯相。图2为裸纤维维和FOGF的SEM图像。

图2 裸纤维和FOGF的SEM图像Fig.2 SEM imagesof nude glass fiber and FOGF with different magnification
由图2可见,裸纤维的表面非常光滑,而溶剂热反应后,纤维表面覆盖了较均匀的Fe3O4薄膜,放大图像表明,Fe3O4薄膜由大量纳米颗粒堆积而成,颗粒之间存在大量缝隙,球形纳米粒子的平均粒径为14 nm。
采用透射电子显微镜进一步表征FOGF的微观形貌,结果如图3所示。

图3 FOGF的TEM图、SAED图谱和HRTEM图谱Fig.3 TEM images,SAEDpattern and HRTEM imageof FOGF
由图3(a)可见,Fe3O4纳米颗粒为表面粗糙的球形颗粒,分散比较均匀。从图3(b)中可以清楚地看到纳米晶的平均粒径为3~4 nm。制备的纳米球形晶粒尺寸较小,比表面积较大,在催化过程中可以暴露更多的活性位点。选定区域电子衍射(图3(c))显示了多晶衍射环,说明纳米颗粒为多晶,由多个微晶颗粒聚集而成。多晶衍射环可归属为Fe3O4的(220)、(311)、(440)、(430)和(531)晶面,进一步说明了了纳米颗粒由Fe3O4纳米晶聚集而成。HRTEM图(图3(d))中显示出清晰的晶格条纹,晶面间距值为0.253 nm,对应于立方晶系Fe3O4粒子的(331)晶面。
2.2 FOGF对活性红的光催化氧化性能
图4显示了不同反应条件下活性红的降解效率。
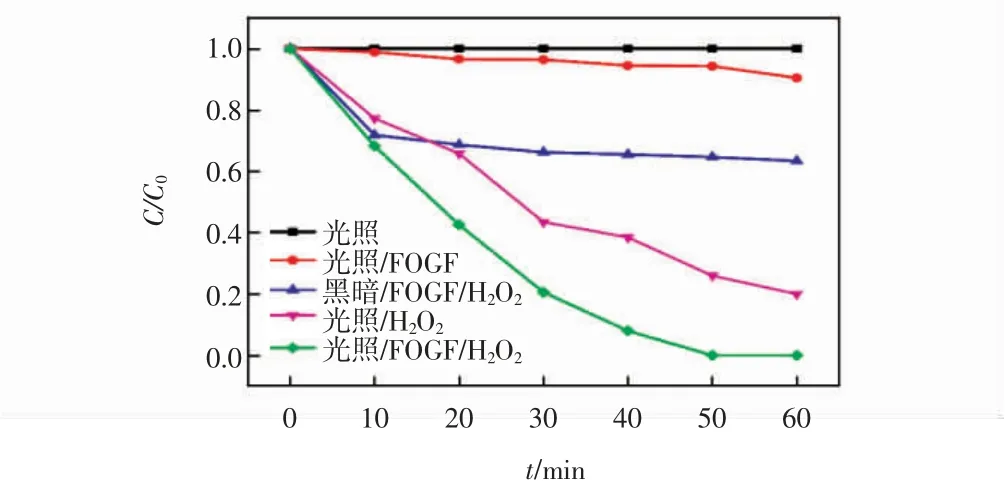
图4 不同条件下活性红降解效率Fig.4 Degradation efficiency of reactivered with different process
由图4可见,只有光照的条件下反应1 h后,活性红几乎没有降解,说明光照难以快速降解活性红。在光照的条件下加入0.08 g催化剂FOGF反应60 min,活性红的脱色率只有9.5%,可能是光照导致FOGF光生电子和空穴对分离,空穴氧化降解了少量活性红,以及FOGF的弱吸附作用。暗环境下加入催化剂FOGF和H2O2反应60 min后,活性红的催化降解效率为35.3%。在光照的条件下用H2O2氧化处理60 min,活性红的降解率达到80%,说明单纯的光照也有助于增强H2O2分解产生·OH。当光照条件下同时加入H2O2和催化剂FOGF反应50 min后,活性红溶液就达到了100%脱色,说明FOGF和光照在催化反应过程中具有协同作用,光照加速了Fe2+和Fe3+的转化,加速了H2O2分解产生·OH,提高了反应效率。
2.3 p H值对FOGF催化降解性能的影响
传统芬顿法降解有机污染物需要在pH=2~4的酸性条件下进行,pH值过低,H+对·OH的清除作用会变强,导致芬顿法的氧化能力降低[15-16]。而且由于Fe2+的稳定性与pH值密切相关,当pH>4时,Fe2+会快速被氧化为Fe3+,并发生水解形成沉淀,导致Fe2+的催化能力降低。因此,在低pH值和高pH值下,传统芬顿工艺都不能有效处理废水中的有机污染物[17-18]。虽然受催化剂的组成和结构、有机污染物的种类和浓度等因素的影响,反应体系的pH值有所差异,但是各种改进型芬顿反应处理废水中有机污染物工艺均要求较苛刻的pH值范围[19-20]。而FOGF催化降解活性红的反应却表现宽泛的pH值相容性。pH值对FOGF催化降解甲基橙活性的影响如图5所示。
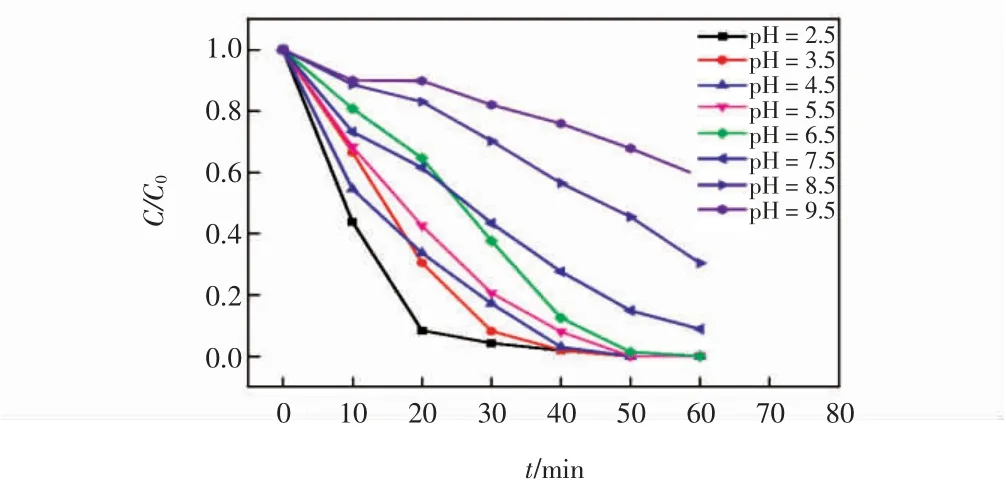
图5 pH值对FOGF催化降解甲基橙活性的影响Fig.5 Effect of pH values on catalytic activity of FOGF for degradation of Reactivered
由图5可见,pH=2.5时,活性红的降解率在反应10 min后即达到56.2%,反应20 min时达到91.6%,反应50 min后,降解率达到100%。当pH值提高到3.5时,活性红的降解速率有所减缓,反应10 min后降解率为33.5%,反应50 min时也达到了100%。随着pH值不断升高,活性红的降解速率不断减缓,但是在pH值为4.5和5.5时,活性红溶液均能在50 min内完全脱色。进一步提升pH值至6.5,反应50 min后,活性红的降解率也高达98.6%,至反应60 min时,降解率达到100%。继续升高pH至7.5、8.5和9.5,反应60 min后,活性红降解率分别为91.1%、69.6%、41.3%。而且,在所有pH值条件下,溶液中均未发现颗粒或絮状沉淀物,说明Fe3O4纳米颗粒牢固附着于玻璃纤维的表面,而且在反应过程中,未发生Fe3+水解形成碱式铁氧化物沉淀,避免了传统芬顿反应的铁氧化物污泥的问题。随着pH值的升高,H2O2自身分解为水和氧气速率会加剧,导致形成的强氧化性的羟基自由基的数量减少,致使活性红的降解速率和降解率均呈下降趋势。此外,由于空气中氧分子的氧化作用,pH值升高会加速Fe2+转化为Fe3+反应过程,使起到催化作用的Fe2+的含量降低,也导致强氧化性的羟基自由基的数量减少,进而引起活性红染料降解速率和降解率的降低。但是,pH=6.5时,FOGF也能在60 min内完全催化降解活性红,避免了传统芬顿反应调节pH值的过程,不但简化了工艺过程,而且避免了二次酸污染的问题。
2.4 FOGF的稳定性
催化寿命和稳定性是评价非均相催化剂的重要参数,且直接影响工艺过程和成本。为了考查FOGF的催化稳定性,在pH=5.5、3 mmol/LH2O2的条件下,对降解40 mg/L活性红染料废水进行了多次循环反应,结果如图6所示。

图6 FOGF长周期催化活性Fig.6 Long-term catalytic stability of FOGF
由图6可见,经过6次循环反应,FOGF的催化性能无明显衰减,均能在60 min内实现活性红溶液的100%脱色,表现出良好的催化稳定性。而且,每次反应后,溶液中均未见明显的颗粒物或絮状沉淀,进一步证明了FOGF可有效避免传统芬顿反应形成铁氧化物污泥的问题。
2.5 FOGF对不同染料的催化降解
为了探究催化剂FOGF催化降解染料废水的普适性,配置了浓度为40 mg/L的活性黄和活性蓝溶液,在pH=5.5、3 mmol/L H2O2的条件下考查了光辅助芬顿反应在FOGF催化下对活性黄、活性蓝染料溶液的降解脱色性能,如图7所示。

图7 FOGF对活性黄、活性蓝的降解性能Fig.7 Degradation performance of FOGF for Reactive yellow,Reactive blue
由图7可知,反应60 min后,活性黄的脱色率是82%,而活性蓝的脱色率是97.3%。不同染料溶液降解速率的差异可能源于染料分子结构的不同,但是FOGF催化下的光辅助芬顿反应对活性染料均具有较好的降解脱色效果。
3 结论
采用溶剂热法制备了玻璃纤维负载的Fe3O4薄膜,并对其进行了XRD、SEM、TEM表征,对活性红溶液进行了光芬顿降解,结果表明:
(1)Fe3O4薄膜由多晶Fe3O4球形纳米颗粒堆积而成,纳米晶的平均粒径为3~4 nm,分布较均匀。
(2)在0.16 g/L的催化剂和3 mmol/L的H2O2的条件下,40 mg/L的活性红溶液在50 min后降解率能够达到100%。该催化膜在高pH下也表现出较高的活性,pH=8.5时,活性红的降解效率仍然达到69.6%。
(3)该催化膜具有良好的催化稳定性,对活性红溶液进行6次循环降解后,活性红溶液仍然能够实现100%脱色。该催化剂对活性染料降解脱色具有一定的普适性。
(4)FOGF催化剂不但可避免传统芬顿氧化的强酸性环境导致的酸污染问题,而且解决了形成铁氧化物污泥固废的问题。

