数形有机融合 渗透素养考查
——以2021年典型高考题为例
尉言勋
(安徽省砀山第四中学 235300)
2021年高考试题彰显化学核心素养,注重学科之间相互融合,拓展了学生思维空间.题目创新信息呈现形式,加大数形结合,注重能力考查;著名数学家华罗庚先生指出:“数缺形时少直观,形少数时难入微.数形结合百般好,隔离分家万事休.”可见数、形之间相辅相成,有机结合,可以使数字信息更加直观化,充分发挥学生的想象力和逻辑思维能力解决实际的化学问题.
1 以负对数做横、纵坐标,考查沉淀溶解平衡
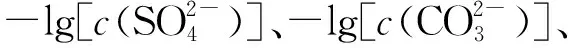
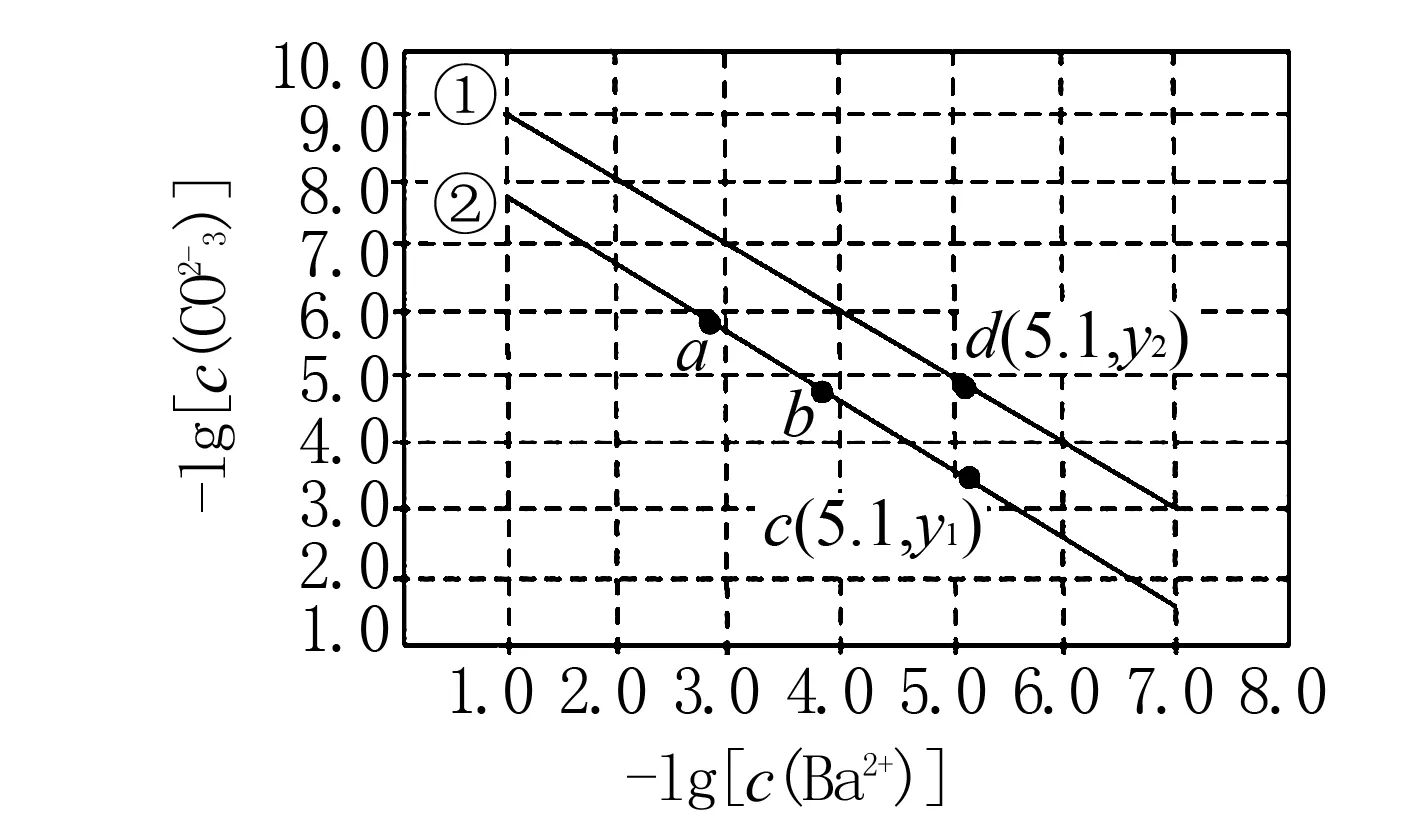
图1
下列说法正确的是( ).
A.曲线①代表BaCO3的沉淀溶解曲线
B.该温度下BaSO4的Ksp(BaSO4)值为1.0×10-10
C.加适量BaCl2固体可使溶液由a点变到b点
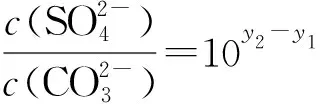
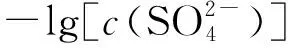
点评本题图形信息新颖、陌生度大,拓展了学生思维空间,需要学生具有一定的数学素养;学生有效读取图中数据信息,推测两种沉淀的沉淀溶解曲线、计算Ksp、分析沉淀溶解平衡的移动.利用浓度的负对数作为纵坐标在2018全国Ⅲ卷12题、2017全国Ⅲ卷13题均考查过.试题在往年的基础上,继续探索通过图像的形式,向学生提供信息,融合数学知识,考查学生的信息获取加工能力.
2 以c2(M+)-c(H+)的线性关系为载体,考查离子浓度比较、Ka的计算
例2(2021·全国乙卷·13) HA是一元弱酸,难溶盐MA的饱和溶液中c(M+)随c(H+)而变化,M+不发生水解.实验发现,298K时c2(M+)~c(H+)为线性关系,如图2中实线所示.
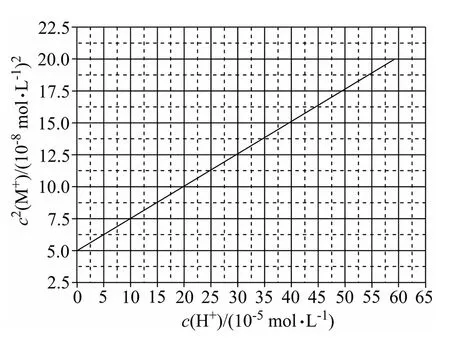
图2
下列叙述错误的是( ).
A.溶液pH=4时,c(M+)<3.0×10-4mol/L
B.MA的溶度积Ksp(MA)=5.0×10-8
C.溶液pH=7时,c(M+)+c(H+)=c(A-)+c(OH-)
D.HA的电离常数Ka(HA)= 2.0×10-4
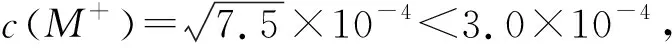
HAH++A-
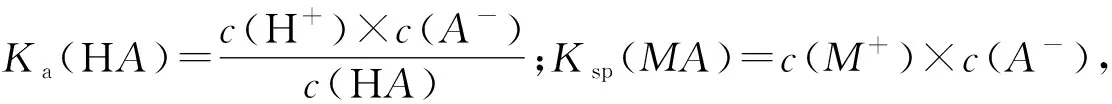
3 以lgc为纵坐标,pH为横坐标,考查图像的分析
例3(2021山东卷·17节选)工业上以铬铁矿(FeCr2O4,含Al、Si氧化物等杂质)为主要原料制备红矾钠(Na2Cr2O7·2H2O)的工艺流程如图3所示.回答下列问题:
矿物中相关元素可溶性组分物质的量浓度c与pH的关系如图4所示.当溶液中可溶组分浓度c≤1.0×10-5mol·L-1时,可认为已除尽.
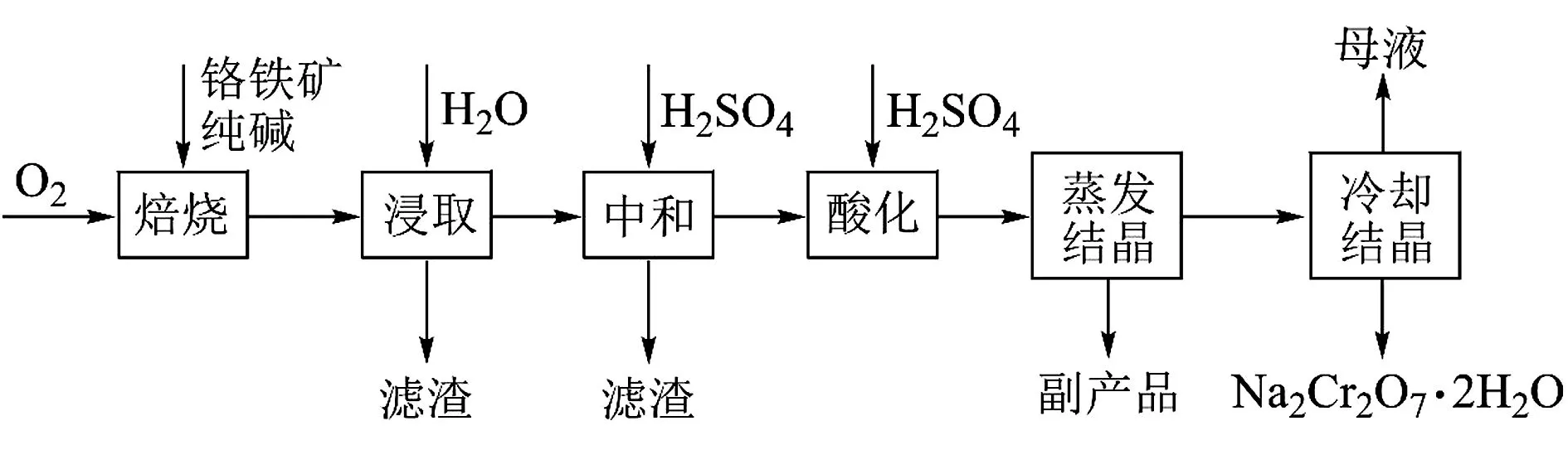
图3
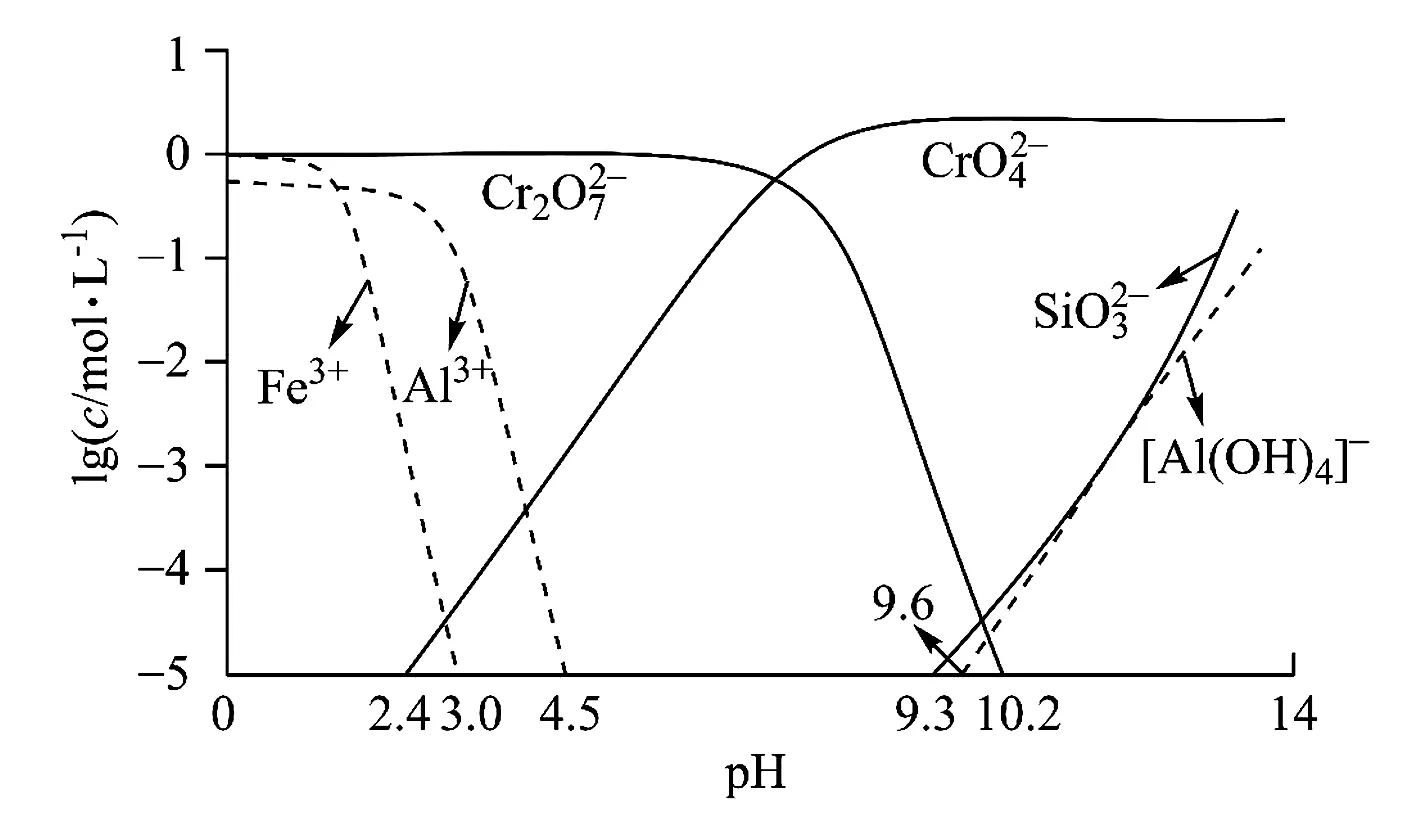
图4
中和时pH的理论范围为____;酸化的目的是____;铁元素在____(填操作单元的名称)过程中除去.
降低溶液pH,可提高Na2Cr2O7的产率;由上述分析可知,铁元素在“浸取”操作中除去.
点评本题通过随着pH的变化,溶液中离子的变化情况,考查pH的理论范围、酸化目的等相关知识,侧重考查图像的分析能力,证据推理与模型认知的化学核心素养.题目的创新之处是改变了信息的呈现形式,把以往的离子沉淀pH变化表格图,转化成了坐标系图.
4 在原理综合题中,给予或的线性关系
例4(2021全国乙卷·28节选)一氯化碘(ICl)是一种卤素互化物,具有强氧化性,可与金属直接反应,也可用作有机合成中的碘化剂.回答下列问题:
McMorris测定和计算了在136~180℃范围内下列反应的平衡常数Kp.
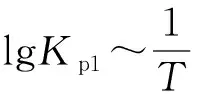
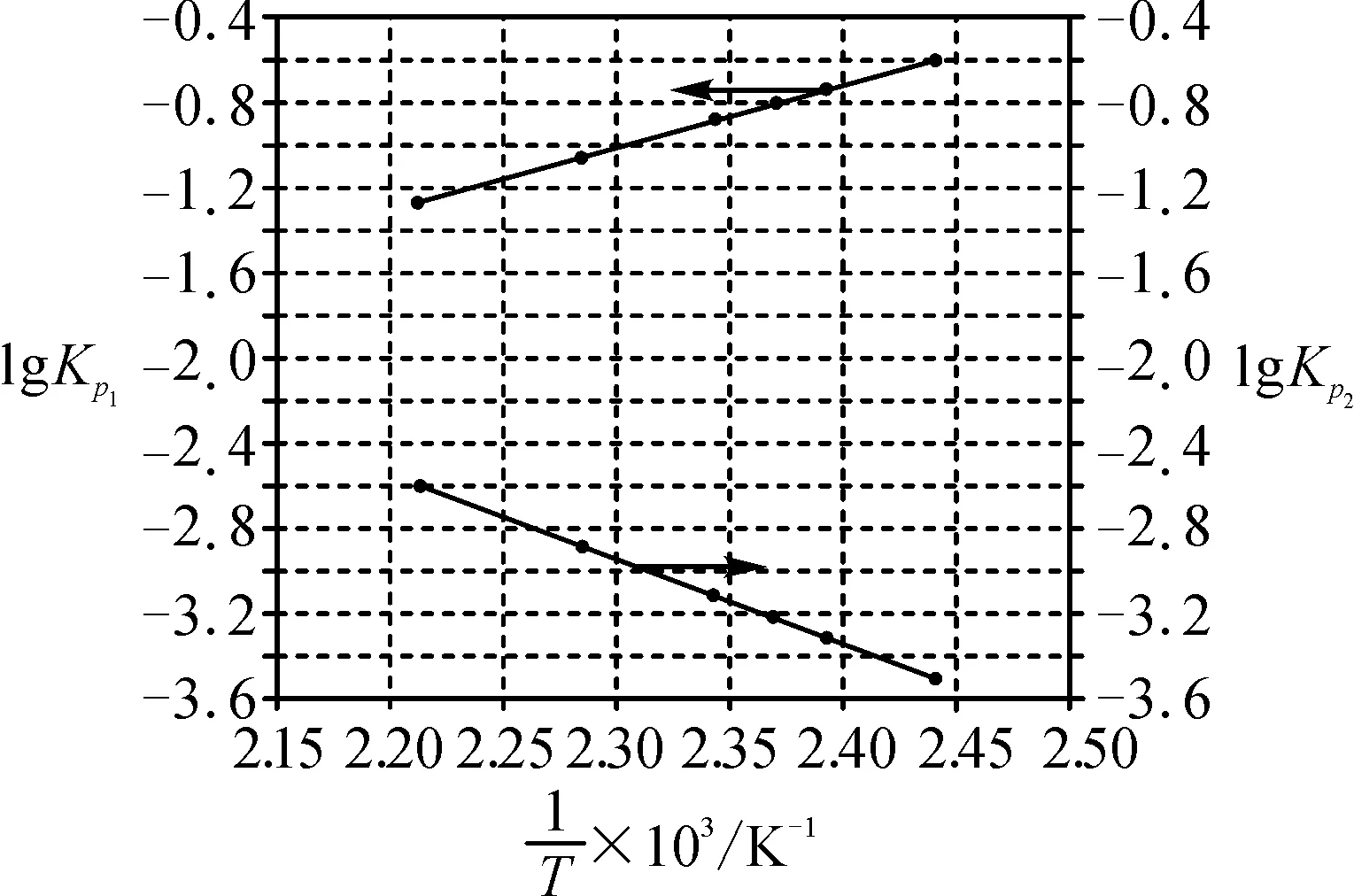
图5
(1)由图可知,NOCl分解为NO和Cl2反应的ΔH____0(填“大于”或“小于”)
(2)反应
的K=____(用Kp1、Kp2表示):该反应的ΔH____0(填“大于”或“小于”),写出推理过程____.
解析(1)由图中信息可知,温度越高,1/T越小,lgKp2越大,则Kp2越大,说明升高温度平衡
正向移动,则NOCl分解为NO和Cl2反应的ΔH大于0;
Kp1
(2)+(3)得
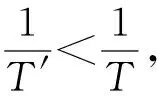
点评题目巧妙地将两个反应平衡常数的对数与温度的倒数绘制成线性关系图,要求学生利用图中数据信息归纳平衡常数与温度内在关系,并在此基础上论证第三个反应的平衡常数与温度的关系.注意题目中箭头的方向,上面的斜线代表对于左侧的纵坐标,下面的斜线对应右侧的纵坐标
例5(2021广东卷·19)我国力争于2030年前做到碳达峰,2060年前实现碳中和.CH4与CO2重整是CO2利用的研究热点之一.该重整反应体系主要涉及以下反应:




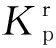
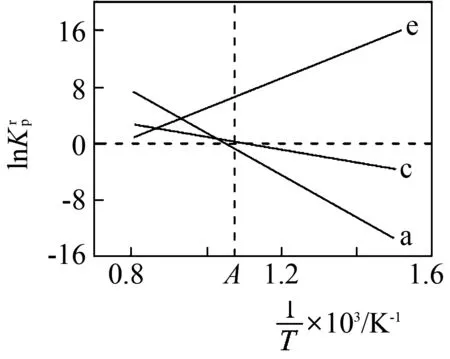
图6
①反应a、c、e中,属于吸热反应的有____(填字母).
③在图中A点对应温度下、原料组成为n(CO2)∶n(CH4)=1∶1、初始总压为100 kPa的恒容密闭容器中进行反应,体系达到平衡时H2的分压为40kPa.计算CH4的平衡转化率,写出计算过程____.
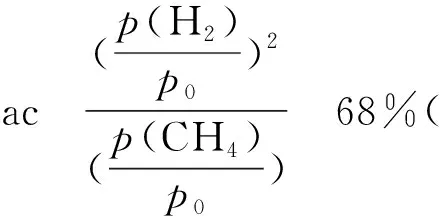
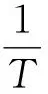
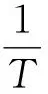
5 一图多用,等温线、等压线以及物质的量在一个图形中呈现
例6(2021年·全国甲卷·28节选)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳.二氧化碳加氢制甲醇的总反应可表示为:

合成总反应在起始物n(H2)/n(CO2)=3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下的x(CH3OH)~p、在p=5×105Pa下的x(CH3OH)~t如图7所示.
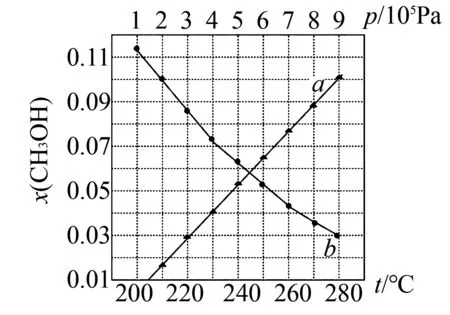
图7
(1)用各物质的平衡分压表示总反应的平衡常数,表达式Kp=____;
(2)图中对应等压过程的曲线是____,判断的理由是____;
(3)当x(CH3OH)=0.10时,CO2的平衡转化率α=____,反应条件可能为____或____.
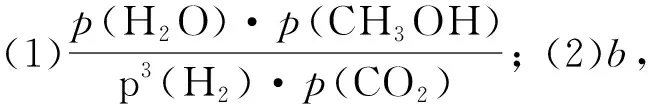
解析(1)二氧化碳加氢制甲醇的总反应为

因此利用各物质的平衡分压表示总反应的平衡常数,表达式
(2)总反应ΔH<0,升高温度时平衡逆向移动,体系中x(CH3OH)将减小,因此图中对应等压过程的曲线是b.
(3)设起始n(CO2)=1mol,n(H2)=3mol,则

起始/mol 3 1 0 0
转化/mol 3xxxx
平衡/mol 3-3x1-xxx
当x(CH3OH)=0.10时,
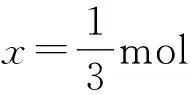
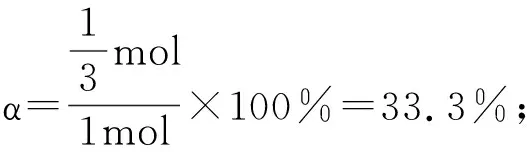
点评本题考查学生利用数据进行归纳论证的能力.题目给予真实的情景,H2与CO2反应制备燃料甲醇的技术,有利于减少温室气体;通过创设数据的呈现形式,巧妙设置问题情境,加强对学生逻辑推理能力的考查.在计算能力要求上难度降低,Kp的计算只需要列出表达式,平衡时CO2的转化率通过简单的三段式即可求得.注意准确判断等压线、等温线的是解题的关键.
总之,数形结合不仅可使信息呈现更加简单易懂、直观形象,而且有利于培养学生的抽象思维能力和形象思维能力.在复习备考时要针对性的培养学生识图能力,关注横纵坐标的数学表达形式的创新,加强学生分析推理能力的训练.

