TACE联合低剂量阿帕替尼治疗中晚期肝癌的疗效及生存预后分析
顾 杰, 许 晨, 周卫忠, 刘 圣, 施海彬
肝细胞癌(HCC)发病率及病死率均较高,且一般患者无明显前驱症状,当疾病诊断时,大多数患者已进入中晚期[1]。根据经典的巴塞罗那分期,TACE是中期(B期)患者的首选治疗方案,而晚期(C期)建议选择口服索拉菲尼或仑伐替尼作为一线治疗方案[2]。然而,TACE治疗后,肿瘤因血供阻断,造成缺血、缺氧状态,可导致病灶缩小,短期疗效尚可,远期疗效欠佳,因为缺血缺氧诱导血管内皮生长因子(VEGF)的过度表达,最终导致肿瘤新生血管生成,导致肿瘤复发或转移[3-4]。因此,TACE联合抗血管生成药物是中晚期HCC更好的治疗方案[5-6]。阿帕替尼是一种新型小分子靶向抗血管生成药物,秦叔逵等[7]的Ⅱ期临床研究也明确了单用阿帕替尼在中晚期HCC的临床价值。如今,有研究采用TACE联合阿帕替尼治疗中晚期HCC,且取得了不错的疗效,但大多数研究注重临床疗效和安全性,关于TACE联合低剂量阿帕替尼治疗中晚期HCC的预后分析的研究尚缺乏[8-10]。本研究回顾性分析TACE联合低剂量阿帕替尼治疗中晚期HCC患者的临床疗效和影响预后的相关因素,为日后的临床治疗决策和预后提供参考。'
1 材料与方法
1.1 资料来源
收集2016年6月至2019年6月我科接受TACE联合阿帕替尼治疗的61例中晚期肝癌患者临床资料。患者入组标准为:①影像或病理证实为肝细胞癌;②失去或拒绝外科切除;③巴塞罗那B或C期,ECOG≤2分;④术前肝功能评分A或B级;⑤仅接受TACE联合阿帕替尼;⑥服用阿帕替尼≥4周。排除标准:①合并其他恶性肿瘤;②联合其他局部治疗,如消融、碘粒子和放疗等和其他系统治疗,如索拉菲尼、仑伐替尼等;③失访或缺乏影像学及血液指标;④停用阿帕替尼>4周。
1.2 方法
1.2.1 TACE 常规消毒铺巾,局部麻醉后,采用改良的Seldinger法经股动脉穿刺插管,经股动脉穿刺置入5 F鞘(泰尔茂,日本),置入5 F的RH导管(泰尔茂,日本),进入肠系膜上动脉及腹腔行DSA造影。明确肿瘤供血动脉后,用2.7 F微导管(泰尔茂,日本)超选进入肿瘤供血动脉,并经造影证实。然后根据术前评估的肝功能状态和术中肿瘤情况,先于肝固有动脉缓慢灌注适量雷替曲塞和洛铂(剂量根据体表面积计算),再注入适量碘化油与上述化疗药混悬乳液进行栓塞,最后明胶海绵或颗粒加强栓塞至造影明确肿瘤供血基本阻断,最后拔除导管及鞘管,加压包扎止血,下肢伸直制动。
1.2.2 阿帕替尼 在行TACE治疗后1周内患者口服低剂量阿帕替尼,首次剂量250 mg/d,4周为一个疗程,如不能耐受药物不良反应,根据患者自身状况决定是否减量为125 mg/d,恢复后继续原剂量给药,直至肿瘤进展或死亡。
1.2.3 随访或观察指标 治疗后每6~12周复查上腹部CT或MR平扫加增强、血常规、尿常规及肿瘤指标等,当复查发现肿瘤仍有活性时,需再次TACE巩固;当证实肿瘤无活性时,继续随访观察,间隔8~12周。利用改良的实体瘤评判标准[11](mRECIST)评估治疗后的肿瘤反应,同时,阿帕替尼相关不良反应按美国癌症研究所事件通用术语标准4.03进行判定。总生存期(OS)定义为从患者入组开始,直至死亡或随访截止日期;无疾病进展生存期(PFS)定义为患者入组到疾病进展,直至死亡或随访截至2020年9月1日。
1.3 统计学分析
计量资料用均数±标准差描述,计数资料以例数描述。使用SPSS25.0分析软件,Kaplan-Meier法进行全组生存分析。使用Kaplan-Meier中的log-rank检验或Cox进行单因素分析,将单因素分析中差异有统计学意义的因素纳入Cox比例风险回归模型进行多因素分析。P<0.05为差异有统计学意义。
2 结果
2.1 患者基线资料
61例中晚期肝癌患者中,男48例,女13例,年龄为(56.7±11.6)岁。BCLC B期22例,C期39例。病灶最大直径为(9.2±4.0)cm,直径>10 cm者28例(46%)。患者接受TACE的次数为(4.6±3.3)次(1~15次)。患者服用阿帕替尼的平均时间为5.9个月,基线资料见表1。
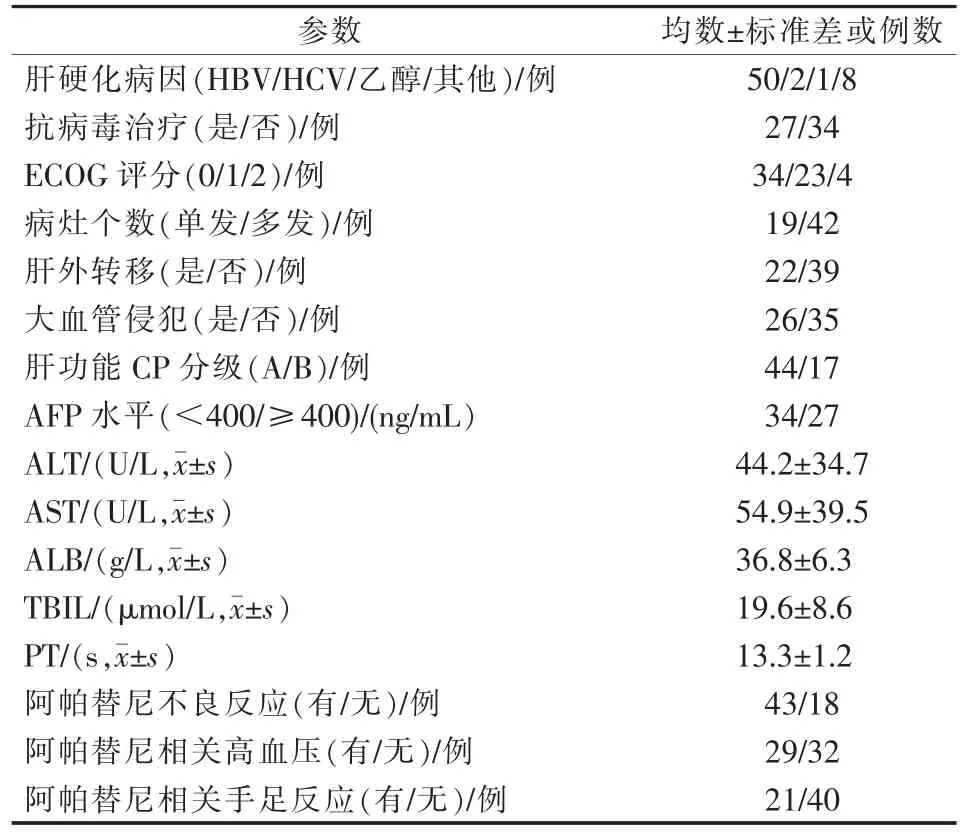
表1 基线资料
2.2 患者生存分析
随访截止时间为2020年9月1日,61例中死亡49例,其余12例仍生存。全组患者OS为3.0~53.8个月,中位OS为17.3个月,PFS为1.1~42.3个月,中位PFS为10.3个月。患者1、2和3年累积生存率分别为64%、33%和16%。
2.3 影响OS的单因素分析
结果显示共有15个因素与OS相关,分别为:抗病毒治疗、ECOG评分、病灶个数、病灶大小、肝外转移、大血管侵犯、BCLC分期、CP分级、AFP水平、阿帕替尼疗程、阿帕替尼相关不良反应、阿帕替尼相关高血压、阿帕替尼相关手足综合征、TACE次数、AST。见表2。

表2 单因素K-M生存或COX风险回归模型分析
2.4 影响OS的多因素分析
将上述P<0.05的15个因素纳入多因素Cox生存风险回归模型分析,结果显示OS的独立影响因素分别为ECOG评分、肝外转移、TACE次数、阿帕替尼相关高血压、阿帕替尼相关手足综合征及阿帕替尼疗程等,见表3。根据Kaplan-Meier生存分析结果显示,ECOG评分0分患者明显优于1~2分的患者的中位OS(25.7个月比8.8个月,P<0.01);病灶<10 cm的患者优于病灶≥10 cm患者的OS(25.6个月比9.9个月);无肝外转移的患者优于存在肝外转移的mOS(22.9个月比12.4个月,P=0.016);存在阿帕替尼相关性高血压患者明显优于无高血压的mOS(25.7个月比9.9个月,P=0.01);发生阿帕替尼相关性手足综合征的患者明显优于没有该反应的中位OS(25.7个月比9.9个月,P=0.001);BCLC B期患者优于C期患者的OS(42.7个月比11.9个月);另外联合服用阿帕替尼不同疗程患者中位OS随时间长短成正相关(9.8个月比19.1个月比36.9个月,P<0.01)。
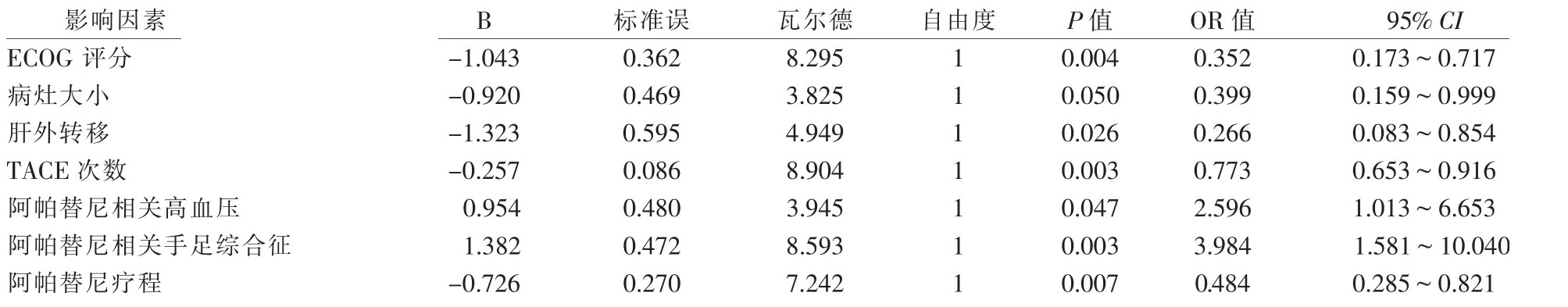
表3 多因素Cox比例风险回归模型
3 讨论
依据HCC BCLC临床分期,B期或C期患者的治疗方式有限,TACE联合分子靶向药已成为主要的治疗模式[12]。本研究中所有患者采用TACE联合低剂量阿帕替尼作为初始治疗方案,总体mOS为17.3个月,mPFS为10.3个月,所有患者1、2和3年累积生存率分别为64%、33%及16%。近年来,阿帕替尼在HCC中的抗肿瘤活性得到证实,单药或TACE联合阿帕替尼均可改善患者的预后[7-9]。Chen等[13]认为,TACE联合阿帕替尼治疗相比较于TACE,能够显著延长BCLC C期患者的mOS:(13.0个月比9.9个月,P=0.041)。与本研究中BCLCC期的中位OS(11.9个月)基本一致,少许差异可能是本研究中阿帕替尼的剂量低于上述的研究。Lu等[14]评估了TACE联合阿帕替尼治疗不可切除的肝癌的疗效,认为联合治疗可显著延长中晚期肝癌患者的中位PFS(12.5个月比6个月),联合组的mPFS与本研究的10.3个月类似。既往研究提示,大剂量(850 mg或750 mg)阿帕替尼患者出现3级以上不良反应概率较大,分别为67.1%和72.1%[7]。为了降低患者的不良反应,本研究中患者采用低剂量阿帕替尼(250 mg),结果显示联合治疗仍明显改善患者的预后。
本研究多因素分析结果显示ECOG评分、肝外转移、TACE次数、阿帕替尼相关高血压、阿帕替尼相关手足综合征及阿帕替尼疗程是患者OS的影响因素。ECOG评分0分的患者明显优于1~2分的患者的mOS,评分越高说明患者的体能状况越差,一般ECOG评分>2分患者不建议服用分子靶向药,这些患者不能耐受药物引起不良反应,所以评分越低的患者越能从TACE联合阿帕替尼治疗中获益,本研究结果与王卫东等研究一致[15]。Liu等[16]研究认为影响肝癌OS的独立因素有病灶大小和有无大血管侵犯,TACE联合阿帕替尼组的mOS长于单独TACE的mOS(210 d比167 d),虽然本研究病灶大小不是独立因素,但P值趋近小于0.05。本研究中病灶直径>10 cm的患者占了近半数,以往研究认为病灶越大,发生大血管侵犯和远处转移的概率增加,而反复TACE使患者发生肝衰竭等风险增加,所以大肝癌患者预后不佳。TACE次数是肝癌患者预后的保护性因素,病灶越大,接受TACE的次数相对减少。本研究中大血管侵犯并不是影响OS的独立危险因素,潜在原因可能是样本量较小。
Sohn等[17]研究认为索拉菲尼可使肝外转移的HCC获益,mOS延长至9.6个月,本研究中,存在肝外转移患者的mOS为12.4个月,而无肝外转移患者的mOS为22.9个月,说明TACE联合阿帕替尼治疗不仅能使远处转移HCC患者获益,而且疗效优于单药治疗。Zheng等[18]研究认为BCLC分期是影响OS的独立因素,TACE和索拉非尼使BCLC B期HCC患者的mOS显著高于C期患者(26.1个月比9.7个月),本研究结果显示BCLC分期并不是独立影响因素,即使BCLC B期患者的mOS同样长于C期(42.7个月比11.9个月),可能原因是病例数、分期占比或者研究方法不同。与以往研究不同的是,本研究把靶向药相关的不良反应作为判断预后的因素,发现阿帕替尼相关性高血压和手足综合征均可预测患者的生存情况,与近期研究的结果类似[19-20]。以往研究认为,因严重药物性反应停药或减量的发生率很高,使患者长期疗效欠佳,所以本研究采用低剂量阿帕替尼联合TACE,结果发现持续联合服用阿帕替尼可明显改善中晚期HCC患者预后,与王卫东等[15]结果相似。
本研究亦有不足之处。首先,是单中心回顾性研究,其次,样本量偏少,本量,再者,只纳入TACE和阿帕替尼治疗,未纳入其他局部治疗和免疫治疗的患者。
综上所述,TACE联合低剂量阿帕替尼的治疗效果良好。独立影响OS的危险因素包括肝外转移和ECOG评分1~2分。TACE次数和阿帕替尼疗程对患者的预后起到保护性作用。阿帕替尼相关性高血压和手足综合征可独立预测预后。

