与良性阵发性位置性眩晕相关的影响因素分析*
王宝爱,韩秀琴,陈 伟,陈 荣,徐玉婷,陈 刚,符文雄,韦辉燕,王 瑜
海南省海口市中医医院:1.脑病科;2.老年病科,海南海口 570216
良性阵发性位置性眩晕(BPPV)是临床比较高发的一种眩晕性疾病,主要临床症状表现为短暂性眩晕反复发作和特征性眼球震颤,具有自限性和易复发的特点[1-2]。BPPV的发病机制较为复杂,目前尚没有明确统一的定论,但大多数研究者对耳石脱落学说持认可的态度。耳石位于球囊斑和椭圆囊斑的顶部耳石膜中,是一种碳酸钙结晶,一般情况下,囊斑周围的暗细胞可以吸收少量脱落的耳石碎屑[3-4],使得耳石处于一种动态平衡的状态;但若是出现暗细胞吸收障碍或是耳石脱落量加大等异常情况时,过量的耳石碎片便会进入半规管内或是黏附于半规管壶腹嵴终顶上,造成壶腹嵴顶的密度增加,且高于内淋巴液。此时,若患者头部发生重力位的改变,导致淋巴液流动,致使壶腹嵴顶偏斜,患者就会出现发作性眩晕、特征性眼震等症状[5-6]。本研究旨在探讨BPPV发生的危险因素,为BPPV的临床诊断与治疗提供依据。
1 资料与方法
1.1一般资料 选取2018年9月至2020年9月本院神经内科就诊的BPPV患者,参照BPPV相关诊断标准[7],共纳入126例患者作为BPPV组,选择同期年龄、性别相匹配的70例体检健康者作为对照组。本研究经本院医学伦理委员会批准,所有受试者均签署知情同意书。BPPV组中女 57 例,男 69 例;平均年龄(48.35 ± 10.81)岁。对照组中男31例,女39例;平均年龄(47.36±9.88)岁。BPPV患者纳入标准:(1)符合BPPV相关诊断标准[7];(2)年龄35~75 岁。排除标准:(1)急性期接受过其他物理治疗者;(2)管石复位术禁忌证者;(3)伴有重大器质性病变及血液系统病变者;(4)不能配合完成相关病史采集者。
1.2方法 ( 1)详细记录两组受试者病史:包括饮酒史、吸烟史、高血压、糖尿病、家族冠心病、偏头痛病史。所有受试者入组后,于次日清晨抽取肘静脉血3 mL,室温静置0.5 h,4 ℃下以5 000 r/min离心10 min,收集血清,检测白细胞计数(WBC)、血小板(Plt)、血红蛋白(Hb)、总胆固醇(TC)、三酰甘油(TG)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、尿酸(UA)、肌酐(Cr)、钙离子(Ca2+)、无机磷、去甲肾上腺素(NE)、多巴胺(DA),以及单胺类神经递质及其代谢物包括5-羟色胺(5-HT)、3-甲氧基-4-羟基苯乙醇(MHPG)、3,4-双羟苯乙酸(DOPAC)、高香草酸(HVA)、5-羟吲哚醋酸(5-HIAA)水平,女性月经期暂不采血。

2 结 果
2.1两组一般情况比较 与对照组比较,BPPV组患者在性别、年龄、饮酒史、吸烟史、高血压、偏头痛病史、家族冠心病史等方面差异均无统计学意义(P>0.05);BPPV组糖尿病发生率较高,差异有统计学意义(P<0.05)。见表1。

表1 两组一般情况比较
2.2两组血液生化指标水平比较 与对照组比较,BPPV组患者Ca2+、无机磷水平降低,差异有统计学意义(P<0.05),见表2。

表2 两组血液生化指标比较

组别nTG(μmol/L)LDL-C(μmol/L)HDL-C(μmol/L)Ca2+(mmol/L)无机磷(mmol/L)对照组701.95±0.152.12±0.271.15±0.122.22±0.211.42±0.12BPPV组1262.13±0.192.71±0.161.23±0.131.57±0.151.04±0.08t1.6811.8242.1575.5827.647P>0.05>0.05>0.05<0.05<0.05
2.3两组血清中单胺类神经递质及其代谢物水平比较 与对照组比较,BPPV组血清NE、5-HT、DA、DOPAC、MHPG、5-HIAA 水平明显降低,HVA水平明显升高,差异有统计学意义(P<0.05),见表3。

表3 两组血清单胺类神经递质及其代谢物水平比较
2.4多因素Logistic回归分析 以BPPV发生与否为因变量,糖尿病、Ca2+、无机磷、NE、5-HT、DA、DOPAC、MHPG、5-HIAA、HVA为自变量,进行多因素Logistic回归分析,结果显示,糖尿病、Ca2+、无机磷、NE、DA、5-HT是BPPV发生的影响因素,见表4。
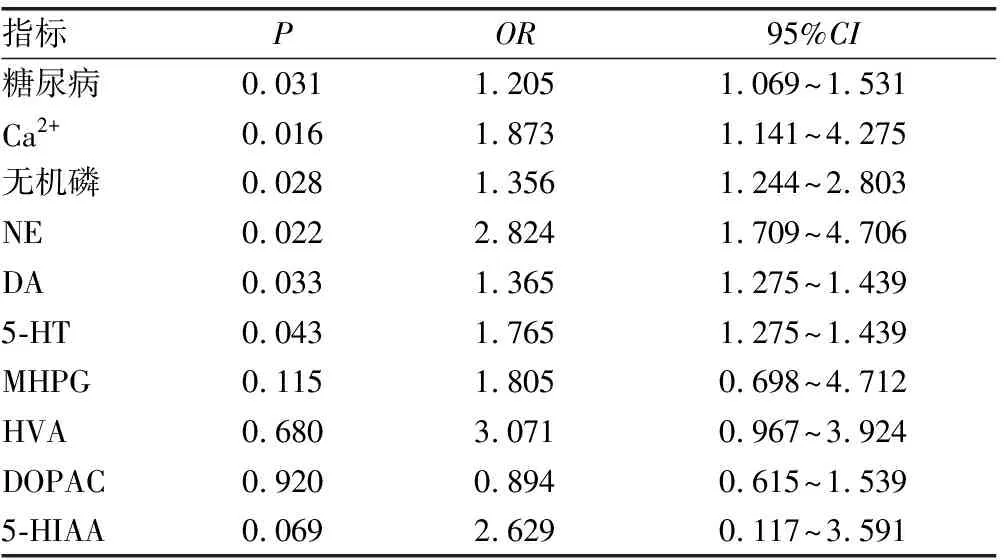
表4 多因素Logistic 回归分析
2.5BPPV各影响因素的预测价值比较 对BPPV发生的影响因素进行ROC曲线分析,结果显示Ca2+<1.89 mmol/L,DA<29.35 mg/L,5-HT<119.4 mg/L对BPPV预测的灵敏度、特异度、准确度较高。见表5。
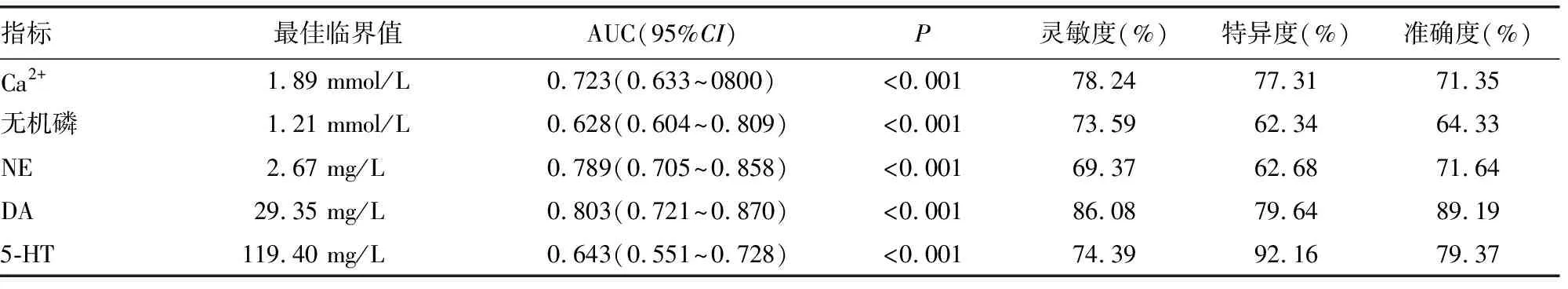
表5 BPPV各影响因素的预测价值比较
3 讨 论
有研究显示,部分神经退行性疾病可能是引发耳石脱落的重要原因[8],而相关研究发现单胺神经递质在退行性疾病中发挥关键作用[9-10]。单胺神经递质主要包含NE、DA、5-HT。5-羟色胺能神经元是构成大脑皮层神经末端的主要神经元,退行性疾病患者均显示出一定程度的5-HT神经功能损伤[11-12]。5-HT几乎分布在整个中枢神经系统,是大脑中非常重要的抑制性神经递质,被认为是引起抑郁情绪最主要的因素[13],减少大脑内5-HT的合成,会引起明显的恶心、眩晕、畏光等症状[14-15]。在BPPV患者中,5-HT合成减少导致患者平衡障碍,给予5-HT激动剂干预后,前庭功能障碍引起的眩晕有明显改善,由此证实5-HT的合成对预防BPPV是有效的[16]。DA也是大脑内非常重要的一个神经递质,对于机体的各种精神活动均发挥调节作用。DA与多种精神疾病的发生具有相关性。有研究报道,给狗脑室或静脉注射多巴胺会引起眩晕、呕吐等症状,当通过使用药物抑制DA的合成时,狗眩晕、呕吐的症状得到了明显缓解[17]。本研究通过比较BPPV患者与体检健康者血清中的单胺类神经递质及代谢物水平,结果显示与体检健康者比较,BPPV患者NE、DA、5-HT 及其相应代谢物MHPG、DOPAC、5-HIAA水平降低(P<0.05),而HVA水平升高(P<0.05)。采用多因素Logistic回归模型对各指标进行分析,结果显示DA、5-HT是 BPPV发生的影响因素(P<0.05)。DA<29.35 mg/L,5-HT<119.40 mg/L对BPPV预测的特异度、准确度、灵敏度较高。
由于耳石外围的主要成分为碳酸钙[18],有部分学者提出血钙水平降低可能与BPPV的发病相关,其原因是血钙水平降低后可能导致椭圆囊斑功能发生退化,导致耳石易松动脱落,打破其动态平衡状态[19]。VIBERT等[20]采用双侧卵巢切除的大鼠建立骨质疏松的模型,与对照组比较,模型组大鼠耳石密度明显偏低,作者认为Ca2+水平降低导致BPPV的机制可能有以下几个方面:(1)血清钙代谢紊乱,可能使耳石自身结构重塑,导致耳石在耳膜上的黏附力变差[21];(2)钙重吸收增加,内淋巴液中Ca2+水平的升高,由此可能导致其溶解脱落耳石的能力降低[22]。故推测Ca2+水平可能与BPPV的发生有关,而在机体中,钙磷调节本为一体,所以无机磷也可能参与BPPV的发生。本研究探讨了BPPV发病对Ca2+、磷水平的影响,发现BPPV组的Ca2+、无机磷水平明显低于对照组(P<0.05)。多因素Logistic回归分析结果显示,Ca2+是BPPV发生的影响因素(P<0.05),Ca2+<1.89 mmol/L对BPPV预测的准确度、特异度、灵敏度较高。
糖尿病与BPPV的关系尚不清楚。一项对3 933例BPPV患者进行的回顾性研究显示,有46%的BPPV患者伴有2型糖尿病的发生,37%的患者未发现糖尿病(P<0.05),在46%的2型糖尿病患者中,有42%的患者是由高血压介导的BPPV[23],因此怀疑高血压是导致2型糖尿病患者BPPV 患病率增加的中介因素。此外,高血压还可损伤胞囊和球囊的黄斑,导致耳石移位,这就更加大了高血压对BPPV发生的影响程度。WEBSTER等[24]研究发现,糖尿病在BPPV患者中普遍存在,且会增加BPPV的复发率。本研究中也发现BPPV组糖尿病发生率明显高于对照组,与上述研究一致。
综上所述,BPPV患者血清单胺类神经递质水平及钙磷代谢水平低于健康群体,Ca2+、DA、5-HT水平与BPPV的发病情况有关。

