P波指数对缺血性卒中后心房颤动的预测价值研究
杨晓萌,吴越阳,,尤佳,姜勇,黄馨莹,王拥军,,4
卒中是我国首位致死及致残原因,其中缺血性卒中在脑血管病中所占的比例高达77.8%,是最常见的卒中类型[1]。心房颤动是缺血性卒中的重要危险因素,中国心房颤动相关的缺血性卒中及TIA比例高达20.2%[2]。随着长程心电监测技术的普及应用,缺血性卒中后心房颤动(atrial fibrillation detected after stroke,AFDAS)的检出率得到了显著的提升[3]。有研究发现,AFDAS患者的1年缺血性卒中复发率为10.9%,死亡率高达22.0%,与卒中前有心房颤动史的患者类似,且显著高于窦性心律的卒中患者,其危害性需要引起重视[4]。由于目前缺乏有效的针对性量表和标志物,快速、高效地识别AFDAS高危人群是临床工作及相关研究的难点。
目前研究认为纤维化可能是与心房颤动有关的基础结构病理改变[5]。P波指数包括P波时限、P波离散度、V1导联P波终末电势(P wave terminal force in lead V1,PTFV1)、PR间期等不同项目,是心电图中反映心房电活动的主要指标,被认为可预测心房颤动的发生[6-9]。目前应用心电图P波指数预测AFDAS的研究较少,更缺乏大型的前瞻性队列研究。本研究利用大样本临床研究数据库探讨P波指数对AFDAS的预测价值,以期尽早识别此类患者,优化其二级预防策略,从而改善患者预后。
1 对象与方法
1.1 研究设计与人群 中国国家卒中登记Ⅲ研究是一项全国性、前瞻性、基于医院人群的登记研究,2015年8月-2018年3月共纳入来自全国26个省、直辖市和自治区201家医院的15 166例缺血性卒中和TIA患者[10]。入组标准:①年龄>18岁;②诊断为缺血性卒中或TIA;③发病距住院时间≤7 d。中国国家卒中登记Ⅲ研究由首都医科大学附属北京天坛医院及参与医院的伦理委员会批准,所有受试者均签署知情同意书。
本研究入组标准:①中国国家卒中登记Ⅲ研究录入的患者;②既往无心房颤动病史;③入院心电图显示无心房颤动;④心电图图像清晰,可完成P波指数判读。
依据患者既往史、住院期间的心电图及24 h心电监测结果将患者分为两组:①AFDAS组:既往无心房颤动病史但此次缺血性卒中后发现了心房颤动;②窦性心律组:既往无心房颤动病史且住院期间未发现心房颤动。
1.2 基线资料收集 收集患者的基本信息,包括年龄、性别等人口学信息,入院时神经功能缺损程度(用NIHSS评价)、BMI,既往高血压、糖尿病、脂代谢紊乱、冠心病、心力衰竭、心肌梗死、卒中及TIA等病史,吸烟、饮酒等生活习惯信息。所有患者在住院期间均接受以下辅助检查:头颅CT或MRI(1.5T或3.0T),颅内外血管评价(超声、CTA或MRA或DSA),心脏节律评价(12导联心电图或24 h心电监测)及左心房直径、左心室射血分数等心脏结构评价(经胸或经食道超声心动图)。
所有影像学和心电图检查结果均收集至首都医科大学附属北京天坛医院神经影像中心进行中心化判读。根据影像检查判读梗死灶特征,包括是否存在皮层梗死和陈旧梗死灶;根据超声心动图判读左心房直径和左心室射血分数;根据入院心电图判读PR间期、PTFV1、P波离散度、P波时限等指标。
1.3 心电图的判读 12导联心电图检查和判读标准:走纸速度设为25 mm/s,电压设定为10 mm/mV,取基线平稳、图形清晰的心动周期进行采样,测量工具为心电卡尺[Cardio Calipers,version 3.3(http://www.iconico.com)]。P波时限(ms)定义为P波起始至终止(回落至基线)的时间;当V1导联P波呈正负双向时,测量终末P波(负向部分)的振幅(μV)和时间(ms),取其乘积的绝对值作为PTFV1(μV·ms)。测量任一导联最大P波时限及最小P波时限,两者的差值为P波离散度(ms)。PR间期(ms)是测量Ⅱ导联P波起始至QRS波起始的时间。上述指标均由一位有经验的心内科医师盲法测量。
依据既往研究的定义,P波时限延长定义为最长P波时限>120 ms;P波离散度增加定义为>40 ms;PR间期延长定义为PR间期>200 ms。PTFV1异常界值为>4000 μV·ms[11-12]。
1.4 统计方法 统计分析应用SAS 9.4(SAS Institute,Cary,North Carolina,USA)软件包。非正态分布的计量资料用M(P25~P75)表示,组间比较采用Kruskal-Wallis秩和检验;正态分布的计量资料用表示,组间比较采用ANOVA检验;计数资料用率表示,组间比较采用χ2检验。根据既往研究和临床判断,将可能对AFDAS产生影响的因素作为协变量纳入多因素logistic回归分析,探讨各项P波指数对AFDAS的预测作用,并采用ROC曲线来分析其预测价值。所有统计检验均为双侧检验,P<0.05为差异有统计学意义。
2 结果
2.1 基线数据 研究共纳入12 248例符合纳入标准的患者,平均年龄为61.7±11.1岁,其中男性8464例(69.1%)。缺血性卒中后新发心房颤动54例(0.4%),窦性心律患者12 194例(99.6%)。
AFDAS组年龄、入院NIHSS评分、皮层梗死及有陈旧梗死灶的比例高于窦性心律组,左心房直径大于窦性心律组;BMI、脂蛋白代谢紊乱比例及左心室射血分数低于窦性心律组(表1);P波指数中,PTFV1、P波时限大于窦性心律组,PTFV1>4000 μV·ms的比例和P波时限>120 ms的比例高于窦性心律组(表2)。

表1 缺血性卒中后心房颤动组和窦性心律组的基线特征比较
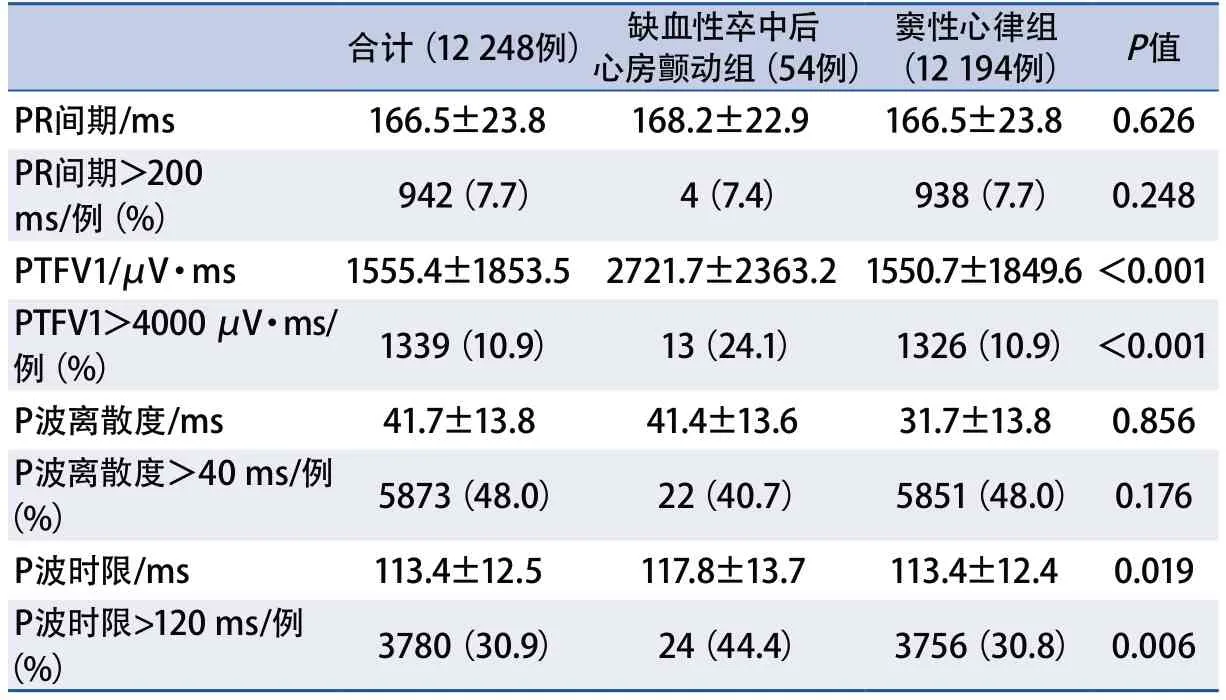
表2 缺血性卒中后心房颤动组和窦性心律组的P波指数比较
2.2 多因素分析及ROC结果 多因素分析结果显示,P波离散度增加、PR间期延长、P波时限延长不是AFDAS的预测因素,而PTFV1增加或PTFV1>4000 μV·ms与AFDAS的发生独立相关。在分别校正了年龄、性别、NIHSS、高血压、糖尿病、心力衰竭、冠心病、心肌梗死、卒中、TIA病史后,上述差异仍达到了统计学意义(表3)。PTFV1增加1000 μV·ms预测AFDAS的AUC为0.604(95%CI0.528~0.679)(图1)。
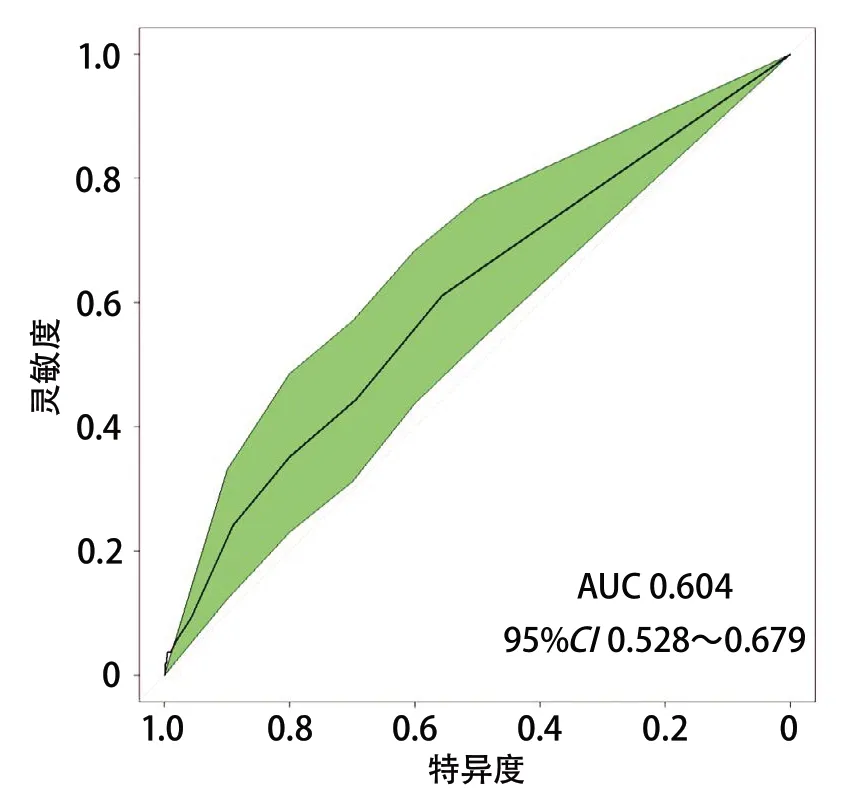
图1 PTFV1增加1000 μV·ms预测缺血性卒中后心房颤动的曲线下面积
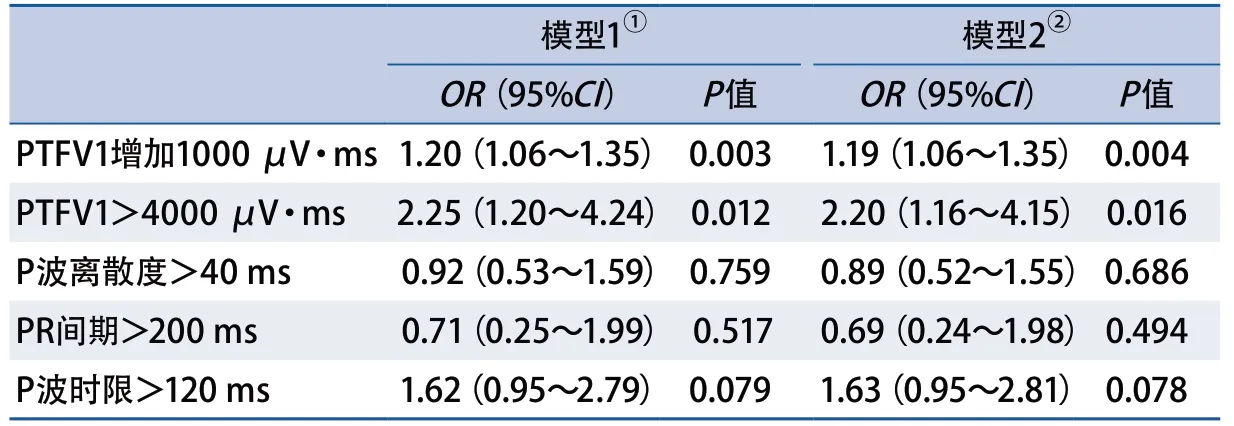
表3 P波指数与缺血性卒中后心房颤动关系的多因素分析结果
3 讨论
本研究基于大型前瞻性队列研究的数据,发现入院心电图的PTFV1是AFDAS的有效预测指标,而其他几项P波指数未显示出明确的预测意义。心房的纤维化重构及扩大是心房基质异常进而导致心房颤动发生的主要病理基础,也是血栓前状态形成的关键环节[13],PTFV1被认为是判断左心房压力增加、左心房肥大及房间传导异常的指标[14],有研究显示心房颤动的发生与心脏的这些结构改变和左心房电重塑具有显著的相关性[15]。既往多项研究证实PTFV1可预测一般人群发生心房颤动的风险[6,9,16],有研究还提示PTFV1可预测缺血性卒中的发生风险[17]。有研究探索了PTFV1与AFDAS的关系,发现PTFV1每增加1000 μV·ms与AFDAS独立相关(OR1.61,95%CI1.24~2.09),与本研究结果一致[7]。
既往研究者还发现,除PTFV1以外,其他P波指数,如P波时限延长,P波离散度增加,PR间期延长也可能与心房颤动风险增高相关[7,17-22]。本研究并未发现以上几个指标对AFDAS的显著预测价值,可能与本研究对象为缺血性卒中人群,卒中后一些与AFDAS发生可能相关的因素如梗死部位、梗死后炎症反应等影响了P波指数对AFDAS的预测性能[4]。此外,本研究中AFDAS例数较少,排除了既往持续性心房颤动患者等因素也可能对研究结果产生一定影响。
本研究证实了方便易获取的心电图指标可预测AFDAS的发生,这一发现对于早期识别卒中后心房颤动的高危人群具有一定的临床应用价值。本研究尚存在着一定的局限性。首先,本研究患者来源于全国多中心,患者入院心电图距发病时间的差异可能会对结果产生一定的影响;其次,本研究AFDAS的定义主要依据入院后24 h心电监测,因此可能会遗漏一些阵发性心房颤动患者,造成一定的偏倚。未来本团队将继续开展基于长程心电监测的AFDAS预测和干预研究,进一步评价心电异常指标对AFDAS的预测价值和临床意义。

