卒中:回眸2021
王拥军,熊云云,李子孝,张玉梅,杨晓萌,王上,霍晓川,杨明,谢雪微,罗岗,陈晓霖,李光硕,王利圆,王传颖,闫然,王文洁,段春苗,路正钊
2021年,距离首项脑血管病循证医学研究——NASCET已经过去了30年[1]。与脑血管病的循证医学发展同步,2021年,Cerebrovascular Diseases杂志也已创刊30周年。杂志约请Hankey教授[2]回顾了30年间脑血管病循证医学的进程及最重要的研究进展:卒中单元的建立[3],加压弹力袜用于下肢静脉血栓的预防[4],1995年NINDS研究开启了缺血性卒中溶栓治疗的历程[5],1997年CAST和IST试验奠定了阿司匹林治疗的基石[6-7],2013年CHANCE研究证实短程、双联抗血小板治疗轻型缺血性卒中的有效性和安全性[8],2015年五大临床研究证明机械取栓(endovascular thrombectomy,EVT)的有效性[9-13],DEFUSE 3、DAWN及EXTEND试验扩展了EVT和静脉溶栓的时间窗[14-16],THALES试验进一步为非致残性缺血性脑血管病提供了新的药物选择等[17]。循证医学的引入与进步使脑血管病研究的面貌焕然一新,也赋予了脑血管病治疗更有效的评估工具。
2021年,受新型冠状病毒肺炎疫情的影响,全球的临床研究入组延缓、部分试验提前终止,但是脑血管病的院前管理、急性期治疗、二级预防及神经康复等领域仍然取得了重大进展,尤其是急性期再灌注治疗和二级预防领域,是本年度备受关注的焦点。美国心脏学会(American Heart Association,AHA)/美国卒中学会(American Stroke Association,ASA)将针对移动卒中单元(mobile stroke units,MSU)的BEST-MSU研究[18]、心房颤动监测相关的STROKE-AF研究[19]等作为2021年卒中领域最具突破性的进展,强调速度和需求的重要性。在2022年初,让我们回眸2021,共同梳理过去一年卒中领域重要的临床研究,把握未来卒中研究发展的方向。
1 争分夺秒——移动卒中单元提高挽救生命的机会
急性缺血性卒中患者应紧急接受再灌注治疗。早在2010年,对ECASS、ATLANTIS、NINDS和EPITHET 4项大型溶栓临床研究的荟萃分析就显示从急性缺血性卒中发病到开始溶栓的时间越短,患者获得3个月预后良好的可能就越大[20]。2016年,另一项关于血管内治疗的荟萃分析同样说明,更早进行EVT治疗能降低缺血性卒中患者发病3个月的残疾率[21]。因此,如何早期筛选出适合再灌注治疗的急性缺血性卒中患者,并尽快对其进行溶栓或EVT治疗,成为改善患者预后的重要研究方向之一。
目前急性缺血性卒中的常规急诊医疗服务(emergency medical services,EMS)包括救护车转运患者到达急诊室,然后对有溶栓指征的患者进行阿替普酶溶栓,对经过筛选的大血管闭塞患者进行EVT治疗[18]。患者就医延迟,院前和院内处置时间较长,是导致时间窗内接受再灌注治疗比例低、再灌注治疗启动时间延迟的原因之一。
2003年,Fassbender教授团队[22]提出了MSU这一新的缺血性卒中急诊救治模式。MSU指配备专业工作人员、小型CT设备和床旁实验室检查的救护车[23]。MSU较常规EMS可更快地进行阿替普酶溶栓治疗,但其能否改善患者的功能结局尚未得到大型临床研究的证实。
2021年2月,德国柏林的Audebert教授团队[24]进行了前瞻性、非随机对照、盲法判定终点的B_PROUD研究,在1543例符合溶栓或EVT标准的急性缺血性卒中患者中比较MSU 模式和一般救护车转运患者至医院急诊治疗的EMS 模式对患者预后的影响。该研究发现,在所有接受阿替普酶溶栓的患者中,使用MSU模式的患者(749例)发病后60 min内的溶栓率是使用EMS模式患者(794例)的3倍左右(12.8%vs. 4.0%,未校正OR2.96,95%CI1.93~4.53)。3个月随访时,MSU组mRS中位数为1(0~3)分,较EMS组的mRS[2(0~3)分]显著降低(OR0.71,95%CI0.58~0.86,P<0.001)(图1)。这项干预研究的结果显示,与仅使用传统救护车相比,使用MSU能更有效地降低急性缺血性卒中患者3个月的整体残疾率。该研究是在全球MSU布局最好的城市——德国柏林展开的,亟待开展其他地区相关的MSU研究以明确该模式在不同的环境下是否同样有效。

图1 B_PROUD研究中患者3个月mRS分布情况(未校正)[24]
2021年9月,美国的Grotta教授团队[18]在N Engl J Med上公布了BEST-MSU研究的结果。这项观察性、前瞻性、多中心、群组对照(每周EMS和MSU交替)研究的主要结局分析共纳入了发病4.5 h内、阿替普酶溶栓治疗的急性缺血性卒中患者1047例,其中617例使用MSU,430例使用传统的EMS。研究结果显示,与EMS相比,使用MSU可提高患者的静脉溶栓率(97.1%vs. 79.5%),缩短卒中发病至溶栓时间(72 minvs. 108 min);在3个月结局方面,MSU组的效用加权mRS平均值(0.72±0.35分vs. 0.66±0.36分,合并差异0.07,95%CI0.03~0.11)和达到良好功能结局患者的比例(53.4%vs. 43.0%,合并OR2.43,95%CI1.75~3.36,P<0.001)均显著高于EMS组(图2)。

图2 BEST-MSU研究中患者90 d mRS分布[18]
B_PROUD和BEST-MSU是2021年发表的针对MSU最重要的研究,均证明MSU可缩短急性缺血性卒中患者从发病到溶栓的治疗时间,提高溶栓率,优化院前分诊,并可改善患者3个月的临床预后。然而,目前针对MSU的研究多在大城市展开,其效果是否受地域或文化的影响尚未可知。此外,这两项大型研究均未证明目前的MSU模式能增加急性缺血性卒中患者EVT的治疗率或缩短发病到开始EVT治疗的时间。对于可能有急诊EVT适应证的患者,通常需要进行CTA和(或)CTP检查以进一步筛选,但MSU上所配备的CT设备不足以完成高级影像学检查,可能会影响MSU在此类患者中的应用。此外,MSU的实施和维护成本高、劳动强度大,也可能限制其应用。不过,根据澳大利亚一项研究的结果,MSU具有成本效益[23]。未来MSU还可能用于其他脑血管病的急诊救治,研究者也可利用MSU进一步探索脑出血等其他脑血管病的超早期治疗方案。澳大利亚正在进行的STOP-MSU试验(NCT03385928),就是使用MSU探索氨甲环酸治疗超急性期自发性脑出血患者的效果,该研究预计在2024年结束。
2 黎明之神——晚时间窗再灌注治疗再现证据力量
2015年发表的五大取栓研究奠定了发病6 h内静脉溶栓桥接EVT相对于药物治疗(包括单纯静脉溶栓)在前循环大血管闭塞性缺血性卒中超早期治疗中的优势地位[9-13]。随着影像学的发展,2018年发表的DEFUSE 3研究利用MRI或CTP影像筛选发病6~16 h之间,存在可挽救半暗带的前循环大血管闭塞性缺血性卒中患者,证明了这部分患者可以从EVT治疗中获益[14]。同年的DAWN研究利用临床-影像错配筛选能从EV T治疗中获益的发病6~24 h的前循环大血管闭塞患者[15]。对缺血性卒中再灌注时间窗的拓展一直是研究者所关注和致力的方向,目前,AHA/ASA指南对发病16 h内的筛选患者进行再灌注治疗的推荐等级均为Ⅰ级,但针对发病16~24 h的再灌注治疗,尚缺乏对研究的汇总分析,指南目前的推荐级别为Ⅱ级[25]。
2021年,Jovin和Nogueira[26]带领团队建立了发病6 h后取栓治疗的随机试验数据汇总分析(analysis of pooled data from randomized studies of thrombectomy more than 6 hours after last known well,AURORA)数据库,纳入了DAWN、DEFUSE、ESCAPE、REVASCAT、POSITIVE、RESILIENT 6项前循环晚时间窗再灌注治疗的研究数据,以期更全面地了解EVT在发病6 h后的前循环大血管闭塞患者中的安全性及有效性。研究者用黎明女神的名字“AURORA”命名该数据库,体现了他们对晚时间窗再灌注治疗再现黎明的信心。AURORA数据库在2021年产出了两篇重要的数据分析文章,被认为是卒中领域2021年的重大进展。
第一项研究对晚时间窗溶栓进行了患者个体水平的meta分析,结果发表在Lancet杂志上。该研究共纳入了505例患者,结果显示,EVT组在90 d功能结局方面显著优于最佳内科治疗组(校正OR2.54,95%CI1.83~3.54)[26]。同时,EVT组90 d mRS 0~2分患者的比例也显著高于最佳内科治疗组(45.9%vs. 19.3%,校正OR3.88,95%CI1.94~7.78)。两组的安全性事件,包括症状性颅内出血(symptomatic intracerebral hemorrhage,sICH)的发生率(EVT组5.3%vs. 对照组3.3%,校正OR1.74,95%CI0.70~4.31,P=0.23)和90 d死亡率(EVT组16.5%vs. 对照组19.3%,校正OR0.96,95%CI0.58~1.60,P=0.88)未见显著差异(表1)。

表1 AURORA数据库中EVT组与对照组的90 d终点事件比较[26]
此项研究结果加强了EVT治疗对发病6~24 h,存在可挽救脑组织的急性缺血性卒中患者有利的证据,证明了在影像学检查提示存在缺血半暗带的前循环大血管闭塞性缺血性卒中患者中进行晚时间窗EVT治疗安全有效,且这部分患者与发病6 h时间窗内进行EVT治疗的患者相比,90 d mRS 0~2分的比例相似。
目前临床研究中筛选适合EVT治疗的发病晚时间窗的缺血性卒中患者一般采用影像错配或临床错配两种标准。DEFUSE 3研究采用的是影像错配标准(核心梗死体积<70 mL,缺血组织/核心梗死体积≥1.8,缺血半暗带体积≥15 mL)。DAWN研究采用的是临床错配标准(年龄>80岁的标准:NIHSS>10分,核心梗死体积<21 mL;年龄<80岁的标准:NIHSS>10分,核心梗死体积<31 mL或NIHSS>20分,核心梗死体积<51 mL)。AURORA数据库产出的第二项重要研究对这两种错配标准筛选患者的效果进行了评价。在这项研究中,Albers教授等[27]分析了295例临床错配亚组和359例影像错配亚组的患者数据,结果显示,在发病6~24 h的晚时间窗内,两种错配标准筛选患者的获益相似(图3),与最佳药物治疗相比,临床错配亚组中EVT治疗可降低2.57倍(OR3.57,95%CI2.29~5.57,P<0.001)的90 d残疾,影像错配亚组中,该指标为2.13倍(OR3.13,95%CI2.10~4.66,P=0.001)。研究结果支持不论是临床错配还是影像错配都可用于筛选适合EVT治疗的缺血性卒中患者。
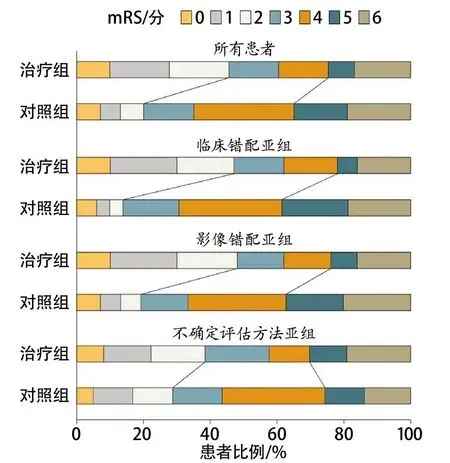
图3 不同错配标准亚组患者的90 d mRS分布情况[27]
尽管不同研究的筛选方式存在差异,但总体来说,这些方法都有利于筛选出存在缺血半暗带,进而能从EVT治疗中获益的患者。除了EVT,通过灌注影像等方式筛选具有缺血半暗带、适合阿替普酶静脉溶栓治疗的患者以拓宽静脉溶栓时间窗也已被证明切实可行。未来基于影像学的“组织窗”可以替代传统的“时间窗”来更精准地筛选出能从再灌注治疗中获益的缺血性卒中患者,从而使更多的患者能进行再灌注治疗。
3 孜孜求索——基底动脉取栓治疗循证基础未牢
基底动脉闭塞(basilar artery occlusion,BAO)所致卒中具有高致死率和高致残率,在临床中不容忽视。目前对BAO进行EVT治疗尚缺乏循证医学证据。尽管有一些Ⅱ期或样本量较小的Ⅲ期临床研究也为后循环EVT治疗提供了部分证据,但因研究质量和样本量的问题,无法为指南推荐提供有效的依据。之前,中国开展的BEST研究因入组缓慢,跨组率高而被提前终止,对其前期数据的意向性分析并没有显示出EVT治疗明显的优势[28]。
2021年5月,N Engl J Med发表了由荷兰发起的,7个国家23家中心共同参与的随机对照试验——BASICS研究的结果[29]。BASICS研究的设计和质量控制相对优良,共纳入300例发病6 h内的BAO患者,随机分为EVT组和药物治疗组。EVT组154例患者中有68例(44.2%)在发病90 d获得良好的功能结局(mRS≤3分),药物治疗组146例患者中有55例(37.7%)获得良好的功能结局,两组的预后良好率差异无统计学意义(RR1.18,95%CI0.92~1.50)(图4)。不良事件方面,两组的sICH与死亡率差异也无统计学意义。

图4 BASICS研究90 d mRS分布情况[29]
BASICS研究耗时8年(2011-2019年),体现了后循环研究入组慢的问题。另外,由于研究时间太长,即使在同一分组,患者的治疗方式也存在一些差异。如EVT组采用二代或三代取栓器械的比例为94%;药物治疗组中进行静脉溶栓的患者比例为79.5%。值得注意的是,BASICS研究在后期放宽了入组标准,部分高龄和低NIHSS患者也被纳入其中。亚组分析中,不同NIHSS评分组中EVT治疗的效果也有不同,其中NIHSS 10~19分亚组和NIHSS≥10分亚组中,EVT治疗可以改善患者的90 d预后。
总之,目前针对BAO进行EVT治疗的循证证据仍然不足,未来需要全球共同努力,为后循环闭塞患者的血管内治疗提供更丰富、更坚实的循证医学证据。
4 左右不定——直接取栓取代桥接治疗结论不明
对于发病4.5 h内的急性前循环大动脉闭塞性卒中,目前标准的治疗方式为阿替普酶静脉溶栓桥接EVT[25]。近年来研究者也在不断探索针对这部分患者新的治疗模式,除了尝试用再通率更高的替奈普酶替代阿替普酶静脉溶栓外,舍弃静脉溶栓步骤直接进行EVT的模式也一直是研究的热点。《卒中:回眸2020》中,我们回顾了海军军医大学第一附属医院(上海长海医院)刘建民教授主持的非劣效性试验
DIRECT-MT[30]。该研究证实,对于发病4.5 h内的前循环大血管闭塞性缺血性卒中患者,在90 d临床结局方面,直接进行EVT不劣于桥接治疗[31]。2021年又有3项相关的随机对照试验陆续发表。
DEVT研究是由陆军军医大学第二附属医院(新桥医院)杨清武教授主导开展的直接取栓对比桥接取栓非劣效性的多中心随机对照试验[32]。该研究在中期分析时由于达到了非劣效性界值(10%率差)而提前终止,最终入组234例发病4.5 h内的前循环颅内大血管闭塞患者,结果发表在2021年3月份的JAMA上。数据分析结果显示,直接取栓组90 d预后良好(mRS 0~2分)的比例甚至高于桥接取栓组(54.3%vs. 46.6%,P=0.003)(图5)。同时,两组的死亡率、sICH发生率等安全性结局无显著差异。DEVT研究的统计数据虽然达到了设计的非劣效性界值,结果也支持直接进行取栓治疗,但因为非劣效性界值设定过于宽泛,可能会影响研究的价值,研究结论很难成功改写指南。
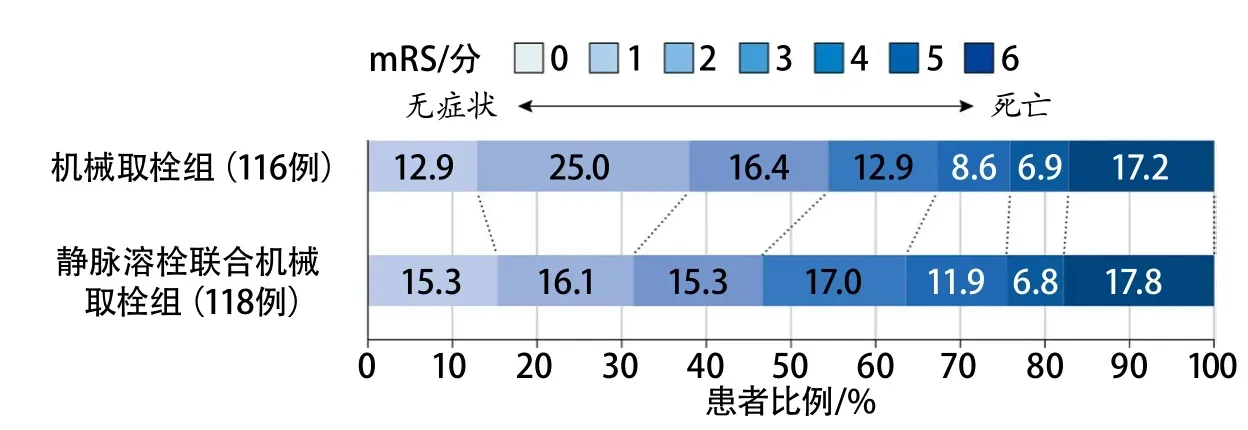
图5 DEVT研究90 d mRS分布情况[32]
与DEVT研究同期发表在JAMA上的SKIP研究是一项2017-2019年在日本进行的对比直接取栓与桥接取栓的非劣效性多中心随机对照试验[33]。入组了204例发病4.5 h内颈内动脉或大脑中动脉M1段闭塞所致的急性缺血性卒中患者,其中101例进行直接取栓治疗,103例接受0.6 mg/kg阿替普酶静脉溶栓后桥接取栓治疗。在90 d功能结局方面,直接取栓组有59.4%的患者达到了mRS 0~2分,桥接取栓组有57.3%达到mRS 0~2分(OR1.09,97.5%CI0.63~∞,P=0.18)(图6),因未达到预先设定的非劣效性界值(OR0.74),故研究的结果是不支持进行直接取栓治疗的。不过,该试验结局评估的95%CI较为宽泛,也不能证实结果的劣效性。
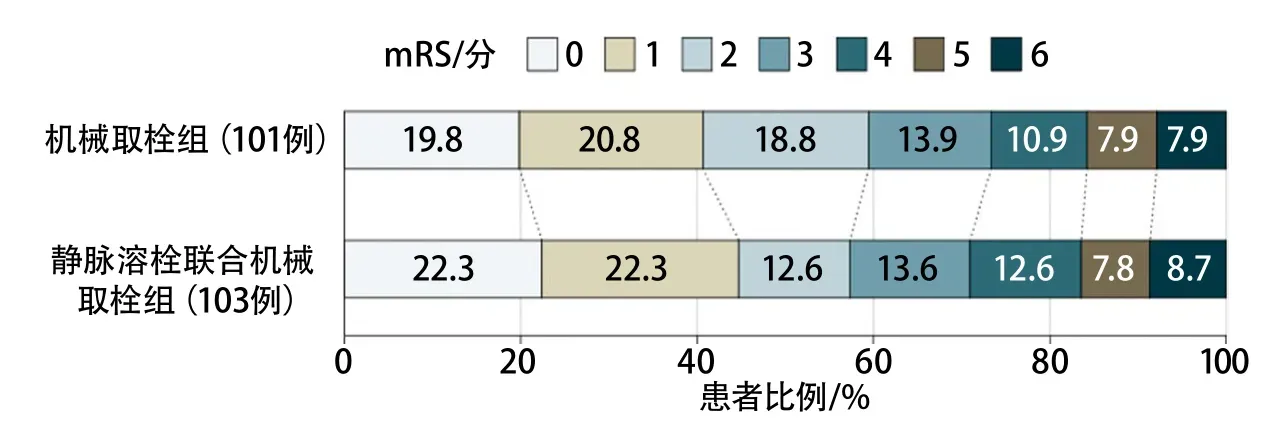
图6 SKIP研究90 d mRS分布情况[33]
DEVT和SKIP研究都来自亚洲人群,来自荷兰的MR CLEAN NO-Ⅳ研究发现在欧洲人群中直接取栓并不优于桥接治疗,且未达到非劣效的标准[34]。MR CLEAN NO-Ⅳ研究共入组539例发病4.5 h内颈内动脉或大脑中动脉M1/M2段闭塞的缺血性卒中患者,比较直接取栓治疗是否优于/不劣于桥接取栓治疗,结果显示,直接取栓组(273例)的90 d mRS中位数为3(2~5)分,桥接取栓组(266例)为2(2~5)分,差异无统计学意义(OR0.84,95%CI0.62~1.15,P=0.28)(图7),未达到非劣效性界值,两组的sICH发生率和死亡率也无显著差异。该研究的结论不支持舍弃桥接治疗。MR CLEAN NO-Ⅳ研究的结果发表于N Engl J Med,在发表同期,意大利的Ciccone教授应邀对该研究进行了述评,他认为部分基于MR CLEAN NO-Ⅳ研究的结果,目前对大血管闭塞性急性缺血性卒中患者进行取栓治疗前,尚不能放弃静脉溶栓治疗[35]。
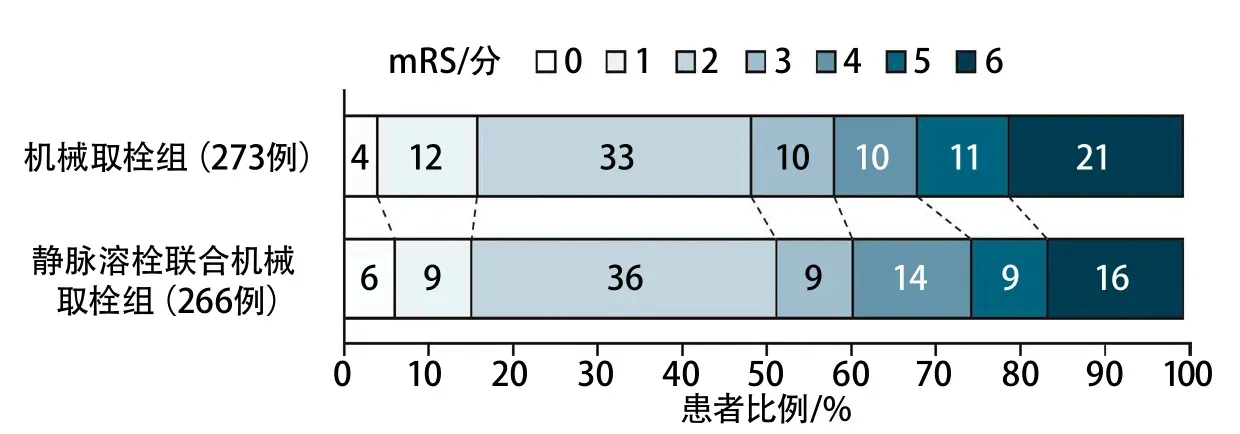
图7 MR CLEAN NO-Ⅳ研究90 d mRS分布情况[34]
近期Podlasek教授团队[36]公布了对上述4项研究进行荟萃分析的结果。该荟萃分析共纳入1633例患者,数据分析显示,直接取栓治疗与桥接取栓相比,对患者90 d功能结局的影响无显著差异(OR1.02,95%CI0.84~1.25,P=0.64),对sICH发生率和90 d死亡率的影响也无显著差异,但直接取栓治疗可以显著降低所有颅内出血风险(27.8%vs. 36.3%,OR0.65,95%CI0.49~0.86,P=0.003),不过同时也降低了成功再灌注(T I C I≥2 b级)的比例(76.5%vs. 80.9%,OR0.76,95%CI0.60~0.97,P=0.03)。值得注意的是,在这4项研究中,直接取栓组和桥接治疗组入院到腹股沟穿刺时间相似,这或许并不能完全体现真实世界中桥接取栓和直接取栓的治疗流程。
总体来说,这4项研究由于人种、病因组成、医疗流程等不同,结论并不一致。另外,宽泛的非劣效性界值,除SKIP外其他研究排除了溶栓后转诊进行取栓的患者,均未使用比阿替普酶再通率更高的替奈普酶进行桥接治疗等局限性也影响了研究结论的可靠性,直接取栓与桥接取栓孰优孰劣仍是未知数,值得临床研究继续探索。随着取栓装置和溶栓药物的更新,将会有越来越多的临床研究涌现,带来更多的证据。而在单一比较两者干预方式孰优孰劣之外,寻找两种干预方式各自最适合的人群或许是另一个值得探索的研究方向。基于现有证据,静脉溶栓桥接取栓治疗仍然是发病4.5 h内急性前循环大动脉闭塞性缺血性卒中患者的首选治疗方式。
5 紫苑花开——急性卒中血管内取栓模式确定
EVT已被证实可以显著改善前循环大血管闭塞患者的功能结局,其关键在于可短时间内实现血管再通。因此,无论使用可回收支架进行取栓还是其他取栓方式,快速开通闭塞的血管是第一目标。自2016年开始,包括THERAPY[37],ASTER[38],COMPASS[39]试验在内的多项大型研究陆续开展,目的在于探究抽吸取栓在改善缺血性卒中患者临床预后及血管再通中的价值。其中最具有代表性的就是ASTER试验,这项被命名为“紫苑花”的研究纳入了来自法国8家综合性卒中中心的381例急性缺血性卒中患者,结果显示,对于发病6 h内的前循环大血管闭塞性缺血性卒中患者,在血管再通和改善临床预后方面,血管再通过程中使用直接血栓抽吸相比支架取栓并无优势。
2021年,紫苑花花开二度,法国Lapergue教授团队[40]发表了AS TER 2的研究结果。ASTER 2研究旨在探索对发病8 h内的前循环大血管(颈内动脉或大脑中动脉M1/M2段)闭塞患者,可回收支架联合接触式抽吸导管取栓较单纯可回收支架取栓能否提高血管成功再通率。该研究是多中心、随机对照、开放标签、终点盲法设计,在法国11家卒中中心纳入了405例患者,其中支架联合抽吸取栓组203例,可回收支架组202例。研究的主要终点为手术完成后闭塞血管达到近全或完全再通,即扩展脑梗死溶栓(expanded thrombolysis in cerebral infarction,eTICI)分级为2c或3级。研究结果显示,两组患者的主要终点事件发生率无显著差异(支架联合抽吸取栓组64.5%vs. 可回收支架组57.9%,校正OR1.33,95%CI0.88~1.99,P=0.17)。两组患者90 d及1年的良好功能预后(mRS≤2分)率差异无统计学意义。在不良事件方面,两组的sICH发生率和死亡率无显著差异(表2)。这项研究提示,对于急性前循环大动脉闭塞性缺血性卒中患者,相较于单纯支架取栓,支架联合抽吸取栓在提高血管完全再通率上无显著优势。但是该研究也显示,仅使用随机后的取栓方式,无补救治疗操作前,支架联合抽吸取栓组的血管成功再通(eTICI 2c/3级)率(59.6%vs. 49.5%,P=0.04)和良好再通(eTICI 2b50/2c/3级)率(86.2%vs. 72.3%,P<0.001)均显著高于可回收支架组,该结果提示可以首选支架联合抽吸取栓作为急性大动脉闭塞性缺血性卒中患者的首选介入治疗方案,但未来仍然需要更多大型研究验证其有效性。

表2 ASTER 2研究的主要临床结局[40]
ASTER 2研究的设计与前期相关大型研究(如ASTER、COMPASS等)相比,主要的区别在于可回收支架组和支架联合抽吸取栓组的患者均90%以上使用球囊导引导管,而且取栓最多操作3次,之后术者决定进一步的补救操作方案(包括抽吸、支架、抽拉结合、血管成形等)。研究结果也证实单纯支架取栓术后仍需更多的补救治疗,之前未使用抽吸导管节约的时间又被消耗在了补救治疗上,最终两组患者的手术操作时间无显著差异。研究的结果提示,支架联合抽吸取栓确实可能对获得血管完全再通更有效,但这种效果在可回收支架组通过补救治疗后,最终无明显的差异性。随着介入设备的迭代和更新,将会有更多新型取栓装置,包括综合不同取栓方式的联合装置出现。在为EVT寻找最优硬件设备的同时,也应该关注为不同的取栓方式寻找最合适的人群。
6 各有千秋——无症状颈内动脉狭窄的非药物治疗
颈动脉狭窄最常见的部位是颈内动脉起始处,规范化药物治疗可降低此类患者的卒中风险,但对于重度(70%~99%)颈动脉颅外段狭窄的患者,即便给予标准化药物治疗,仍有部分发生致残性甚至致死性卒中。目前,颈动脉支架置入术(carotid artery stenting,C A S)是除颈动脉内膜剥脱术(c a r o t i d endarterectomy,CEA)外治疗颈动脉颅外段狭窄最重要的治疗手段。在过去几十年间,随着CAS材料与技术的不断进步,其围手术期风险也明显降低。不过,目前对CEA和CAS的选择仍然难分伯仲。既往的临床研究多聚焦于症状性颈动脉重度狭窄患者,对于无症状性颈动脉重度狭窄者,CAS与CEA的临床效果探索较少,现有证据仅局限于登记研究和样本量有限的临床研究[41-42]。
2021年,Halliday教授[43]牵头进行的一项多中心随机对照试验——ACST-2在Lancet杂志上发表了其研究结果。该研究历经12年,主要评价无症状性颈动脉颅外段狭窄患者CAS与CEA治疗后临床结局的差异。研究共纳入来自全球130家大型医院的3625例无症状性(在过去6个月内该处狭窄未引起神经功能缺损)颈动脉颅外段重度狭窄(超声评估狭窄>60%)且具有CAS或CEA手术指征的患者,其中1811例患者被随机分入CAS组,1814例患者被随机分入CEA治疗组,术后1个月及随后的每年均随访一次,平均随访时间5年。结果显示,两组患者术后30 d全因死亡和致残性卒中的发生率(CAS 0.9%vs. CEA 1.0%,P=0.77),以及非致残性卒中(mRS 0~2分)的发生率(CAS 2.7%vs. CEA 1.6%,P=0.77)差异均无统计学意义(表3)。Kaplan-Meier生存曲线估计,两组5年的死亡和致残性卒中发生率为2.5%,全部卒中的发生率在CAS组为5.3%,在CEA组为4.5%(RR1.16,95%CI0.86~1.57,P=0.33)。同时该研究荟萃分析了既往比较CAS与CEA临床结局的试验数据,显示无论对于症状性还是无症状性颈动脉颅外段重度狭窄的患者,CAS与CEA所有的非围手术期卒中的发生率相似(RR1.11,95%CI0.91~1.32)。该研究提示,对于无症状性颈动脉颅外段狭窄的患者,CAS与CEA术后的严重并发症均不常见,且两组患者在5年随访期间致死或致残性卒中的发生率也基本一致。
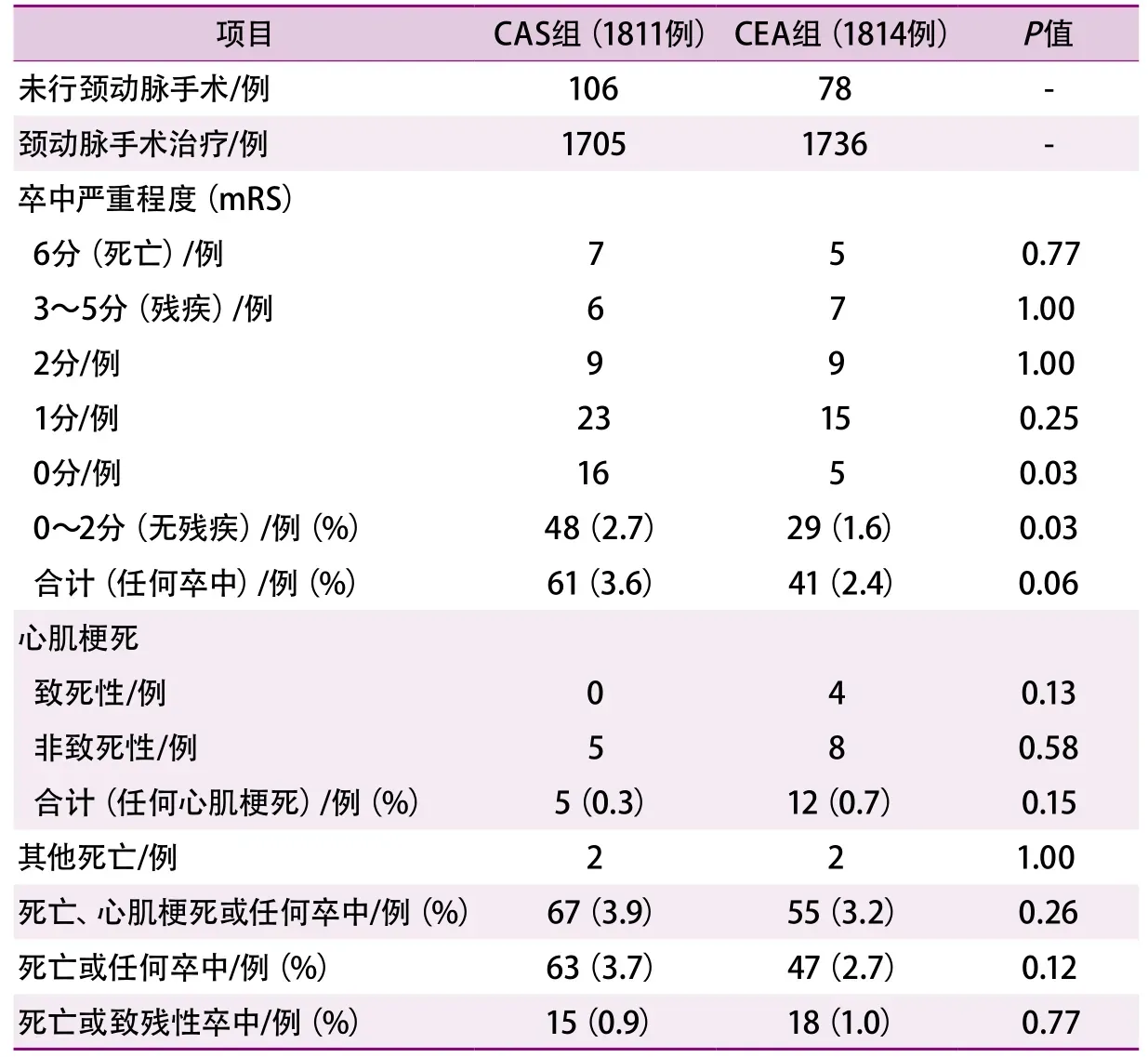
表3 ACST-2研究中CAS与CEA围手术期安全性比较[43]
对于无症状性颈动脉颅外段重度狭窄患者,包含ACST-2在内的多项研究证据表明,虽然CEA的临床结局略优于CAS,但是差异没有统计学意义,这个结论与症状性颈动脉颅外段狭窄患者的CEA和CAS治疗研究结论相似。我们期待ACST-2研究后期的随访结果以及其他临床研究来验证CAS与CEA在改善颈动脉颅外段狭窄患者临床结局方面的差异性,为今后的临床治疗提供理论基础。
7 持之以恒——隐源性卒中的长程心电监测
近年来的研究已证实了长程心电监测(包括体外及植入式设备)可显著提高隐源性卒中患者心房颤动的检出率[44-45],同时研究发现亚临床房性快节律可增加患者缺血性卒中和系统性栓塞的风险[46]。然而针对整体缺血性卒中人群,尚缺乏明确长程心电监测能否提高心房颤动检出率的随机对照试验;此外心房颤动检出率提高是否会增加临床抗凝药物的使用,进而减少卒中复发,改善患者结局也缺乏充分的证据支持。
2021年,众多学者着手于植入式心电监测(insertable cardiac monitor,ICM)与传统心电监测对缺血性卒中患者心房颤动检出率的比较,发表了几项有代表性的研究。
STROKE-AF研究纳入了492例发病10 d内的大动脉粥样硬化性卒中和小血管闭塞性卒中,1∶1随机分入ICM组或常规监测组(包括十二导联心电图、动态心电监测、移动传感器、事件记录仪等)[19]。结果显示,ICM组心房颤动的检出率显著高于对照组(12.1%vs. 1.8%,HR7.4,95%CI2.6~21.3),其中在小血管闭塞性卒中患者中,这种差异更加显著(HR13.8,95%CI1.8~111.1)(图8)。不过该研究无法证明发现的这些心房颤动是病因性的,也无法验证提高的心房颤动检出率对预防卒中的临床意义。
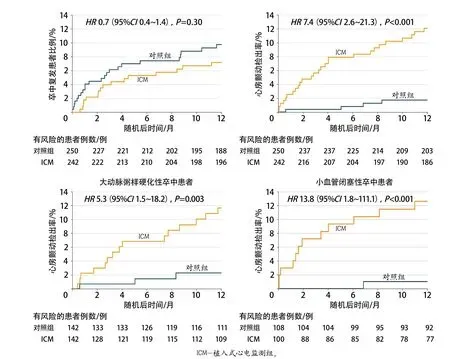
图8 STROKE-AF研究中心房颤动检出率和卒中复发情况[19]
另外一项来自加拿大的PER DIEM研究纳入了300例发病6个月内且无明确心房颤动病史的缺血性卒中患者,1∶1随机分为ICM组(持续12个月)和体外事件记录仪组(持续30 d),主要结局为随访1年发现持续≥2 min的新发心房颤动[47]。研究结果显示,ICM组心房颤动检出率显著提高(15.3%vs. 4.7%,RR3.29,95%CI1.45~7.42,P=0.003)。研究的结论为:①对于无明显心房颤动病史的缺血性卒中患者,ICM监测(12个月)可显著提高心房颤动的检出率;②尚需进一步的研究比较两种监测方式对临床结局的影响及其成本效益。
有学者对STROKE-AF和PER DIEM研究进行了比较:两项研究设计基本一致,均为随机、开放标签、平行对照设计,ICM设备均来自同一厂家;但两组的对照组设计有所不同,STROKE-AF研究没有规定对照组心电监测的具体方式,而PER DIEM研究则统一应用30 d触发式的心电记录仪进行心电监测[48]。两项研究的最终结果基本趋于一致,进一步证实了ICM对提高心房颤动检出率的优势(表4)。

表4 STROKE-AF和PER DIEM 研究设计对比[48]
MonDAFIS研究试图回答提高心房颤动检出率与临床抗凝决策的相关性问题,研究纳入了3465例急性缺血性卒中和TIA患者,1∶1随机分配至对照组(常规监测组)和干预组(住院期间给予7 d动态心电监测),主要结局为1年后患者口服抗凝药物的比例。研究发现,虽然干预组新发心房颤动的检出率显著提高(5.8%vs. 4.0%,HR1.4,95%CI1.0~2.0,P=0.024),但1年时13.7%的干预组患者及11.8%的对照组患者使用口服抗凝药物,两组抗凝药物使用比例差异无统计学意义(OR1.2,95%CI0.9~1.5)。研究者认为,尽管系统性中心化判读的长程心电监测可行且提高了心房颤动的检出率,然而对于实际口服抗凝药的使用率并未产生显著影响,因此,对于缺血性卒中和TIA患者,仍需探索其他提高抗凝治疗率和改善患者结局的策略[49]。
综合解读关于监测缺血性卒中患者心房颤动的研究结果发现,尽管目前研究已证实了长程心电监测可显著提高心房颤动的检出率,但什么类型的心房颤动(持续时间、合并危险因素等)值得筛查,筛查出的哪些心房颤动需要抗凝治疗,进而改善患者结局仍是未来研究的方向。
8 上行下效——卵圆孔未闭封堵手术长期随访结果
国内外多项研究表明,卵圆孔未闭(patent foramen ovale,PFO)与不明原因性卒中相关,美国学者于2020年正式提出PFO相关性卒中这一概念。2017年,N Engl J Med上发表了CLOSE、Gore REDUCE和RESPECT的研究结果;2018年,在亚洲人群中治疗高危
PFO的DEFENSE研究结果公布,上述研究一致表明经导管封堵PFO术在降低不明原因卒中复发风险方面优于单纯药物治疗。基于上述研究结果,多个国家和地区相继更新了PFO治疗指南或专家共识,经导管封堵PFO术已经成为预防高风险PFO合并不明原因卒中患者卒中复发的一线治疗措施。
Gore REDUCE试验是上述研究中比较重要的一项,共纳入664例伴有PFO和右向左分流的隐源性卒中患者,2∶1随机分入PFO封堵组(441例)和单纯抗血小板治疗组(223例),2017年其3.2年随访的结果显示,PFO封堵术可显著降低患者卒中复发的风险(OR0.23,95%CI0.09~0.62,P=0.002)。2021年3月,Gore REDUCE试验发表了其5年随访的结果,共有20例患者缺血性卒中复发,其中PFO封堵组8例(1.8%),单纯抗血小板治疗组12例(5.4%),差异有统计学意义(HR0.31,95%CI0.13~0.76,P=0.007)[50]。两组严重不良事件包括死亡、大出血、深静脉血栓或肺栓塞的发生率差异无统计学意义。在延长的随访期内,无封堵器相关的血栓栓塞发生,也没有发现封堵器断裂或对周边组织的侵蚀。上述结果进一步证实了导管PFO封堵术的有效性和安全性,夯实了该治疗方式在高风险PFO合并不明原因卒中治疗中的地位。
虽然PFO封堵术总体上降低了卒中复发的风险,但对于患者个体来说,PFO封堵术是否为最佳选择仍不明确。2021年12月,JAMA发表了一项荟萃分析的结果,该研究汇总了6项比较单独药物治疗与药物治疗联合PFO封堵术的随机对照试验,共纳入3740例患者[51]。研究结果显示,在57个月的中位随访期中,药物治疗组的卒中年化发病率为1.09%,PFO封堵组卒中年化发病率为0.47%,差异有统计学意义(HR0.41,95%CI0.28~0.60)。该研究还通过采用反常性栓塞风险(risk of paradoxical embolism,RoPE)评分(表5)和PFO相关卒中因果可能性(PFO-associated stroke causal likelihood,PASCAL)分类系统(表6)对纳入人群进行了亚组分析,以评估不同亚组中PFO封堵术的获益情况。分层评估的结果显示,对于RoPE评分<7分的患者,封堵术预防卒中复发的HR为0.61(95%CI0.37~1.00),而在RoPE评分≥7分的患者中,封堵术预防卒中复发的HR为0.21(95%CI0.11~0.42),获益更加明显。根据PA S C A L分类系统,在被归类为不太可能、可能和很可能的亚组中,封堵术预防卒中复发的HR分别为1.14(95%CI0.53~2.46)、0.38(95%CI0.22~0.65)和0.10(95%CI0.03~0.35),提示封堵术预防卒中在“不太可能”亚组中没有获益。此外,在不太可能的、可能和很可能的PASCAL类别中,2年卒中复发的绝对风险降低分别为-0.7%(95%CI-4.0%~2.6%)、2.1%(9 5%C I0.6%~3.6%)和2.1%(95%CI0.9%~3.4%)。该荟萃分析的结果说明,PFO封堵术在减少卒中复发方面具有人群异质性,而针对性的评分和分类系统具有指导个体化治疗决策的潜力。
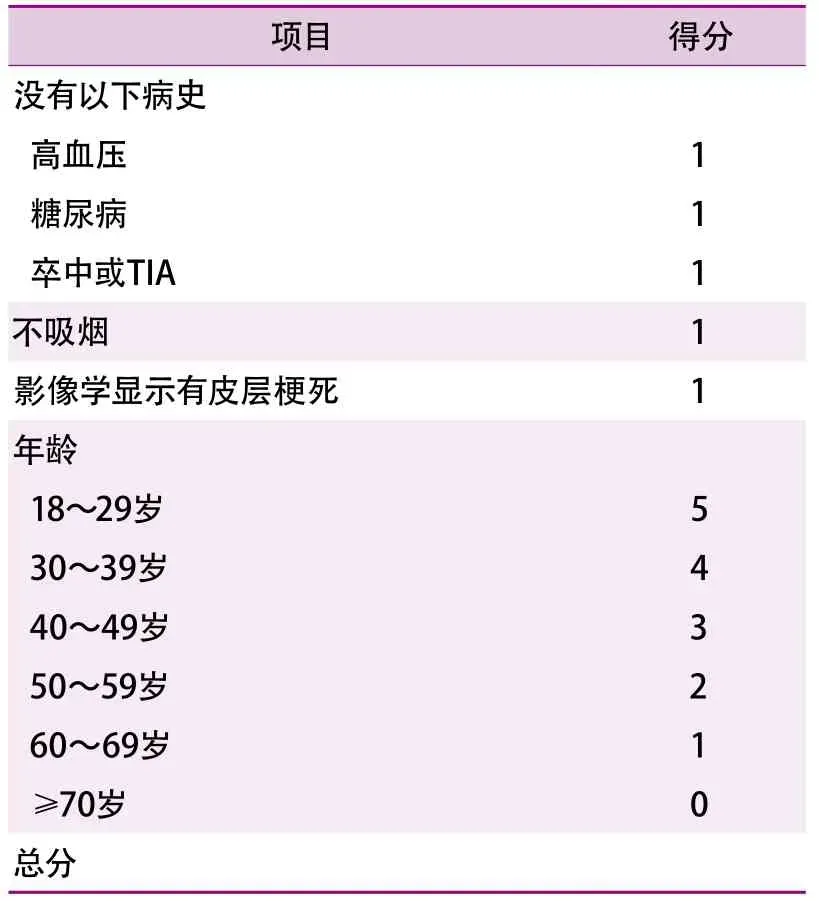
表5 反常性栓塞风险评分表[单位:分]

表6 卵圆孔未闭相关卒中因果可能性分类系统
有研究表明约90%的非瓣膜病心房颤动的血栓来自于左心耳,因此通过外科手术或经皮左心耳封堵术对左心耳进行干预也是目前非瓣膜病心房颤动患者预防卒中的研究热点。2021年5月,LAAOS Ⅲ研究的结果发表在N Engl J Med上[52]。该研究旨在明确在外科手术的同时干预左心耳(包括切除和缝合、吻合器缝合、双层直线缝合)能否降低卒中风险,研究纳入行其他心脏手术且具有高危卒中风险的心房颤动患者,随机进行左心耳封堵术。数据分析发现,左心耳封堵术组和未行封堵术组平均随访3.8年的卒中或系统栓塞发生率分别为4.8%(114/2379)和7.0%(168/2391),差异有统计学意义(HR0.67,95%CI0.53~0.85)。两组的围手术期出血、心力衰竭或死亡的发生率差异无统计学意义。需要指出的是,多数(76.8%)患者在随访期间服用了抗凝药物,因此该研究未进行左心耳封堵术与抗凝治疗的对比分析,另外,因为外科手术的创伤大、风险高,因此仅在因其他原因接受外科手术治疗的患者中可考虑同时进行左心耳封堵治疗。
经皮左心耳封堵术作为一种创伤小、操作简单、耗时少的治疗方法,近年来在国内得到了蓬勃发展。但目前该治疗有效性的证据有限,国内外指南均将该技术的适应人群主要限定为有抗凝治疗禁忌证、高危出血风险和规范抗凝治疗下仍出现栓塞事件的心房颤动患者。2021年发表了一项关于经皮左心耳封堵与口服抗凝药物对比的观察性登记研究,结果发现,接受左心耳封堵的患者主要终点事件(卒中、严重出血、死亡)发生率更低(HR0.57,95%CI0.49~0.67),严重出血率(HR0.62,95%CI0.49~0.79)和全因死亡率(HR0.53,95%CI0.43~0.64)也更低,不过,两组的缺血性卒中发生率差异无统计学意义(HR1.11,95%CI0.71~1.75)[53]。该研究初步回答了经皮左心耳封堵术与直接口服抗凝药物孰优孰劣的问题,但该结论尚需高质量的前瞻性随机对照试验进一步确认。另外,接受经皮左心耳封堵术后的抗栓治疗方案目前尚无定论;部分中心的“一站式”手术,即进行心房颤动消融手术的同时行左心耳封堵治疗的模式缺乏长期随访结果,尚需进一步研究来确认其安全性和有效性。
9 精益求精——精准医学改变联合抗血小板治疗格局
2013年,CHANCE研究的发表奠定了对非致残性脑血管事件高危人群(high-risk with non-disabling cerebrovascular events,HR-NICE)进行短程、双联抗血小板治疗的基础[8]。之后,全球又先后发表了4项以阿司匹林为基础的双联抗血小板治疗的临床研究结果:FASTER[54]、POINT[55]、PRINCE[56]和THALES[17]研究。其中PRINCE研究是在我国开展的Ⅱ期临床研究,THALES研究是美国、中国、法国和西班牙共同设计的Ⅲ期临床研究。在目前发表的这5项最重要的双联抗血小板治疗研究中,中国的研究者主导了半数,在针对HR-NICE人群的抗血小板治疗领域,中国学者已经成了领导者。
2021年,加拿大的研究者对上述5项研究进行了meta分析,在所有被纳入的22 098例小卒中或TIA患者中,5517例接受了阿司匹林联合氯吡格雷治疗,5859例接受了阿司匹林联合替格瑞洛治疗,单用阿司匹林药物的患者有10 722例[57]。汇总后的结果显示,在预防卒中复发和死亡方面,与单用阿司匹林相比,阿司匹林联合氯吡格雷的有效性增加26%(HR0.74,95%CI0.65~0.84),阿司匹林联合替格瑞洛的有效性增加21%(HR0.79,95%CI0.68~0.91);阿司匹林联合氯吡格雷与阿司匹林联合替格瑞洛两种方案的有效性未见显著差异(表7)。基于这5项研究的结果,2021年欧洲[58]、美国[59]和加拿大[60]的缺血性卒中诊疗指南再次进行了更新,均将HR-NICE患者的短程、双联抗血小板治疗方案作为最高级别的推荐。其中欧洲卒中组织(European Stroke Organisation,ESO)和加拿大的指南均推荐阿司匹林联合氯吡格雷治疗持续21 d后改为阿司匹林单独抗血小板治疗,但AHA/ASA的指南在CHANCE研究的基础上加入了POINT研究的证据,推荐的是双联抗血小板治疗21~90 d后再改为阿司匹林单独抗血小板治疗。
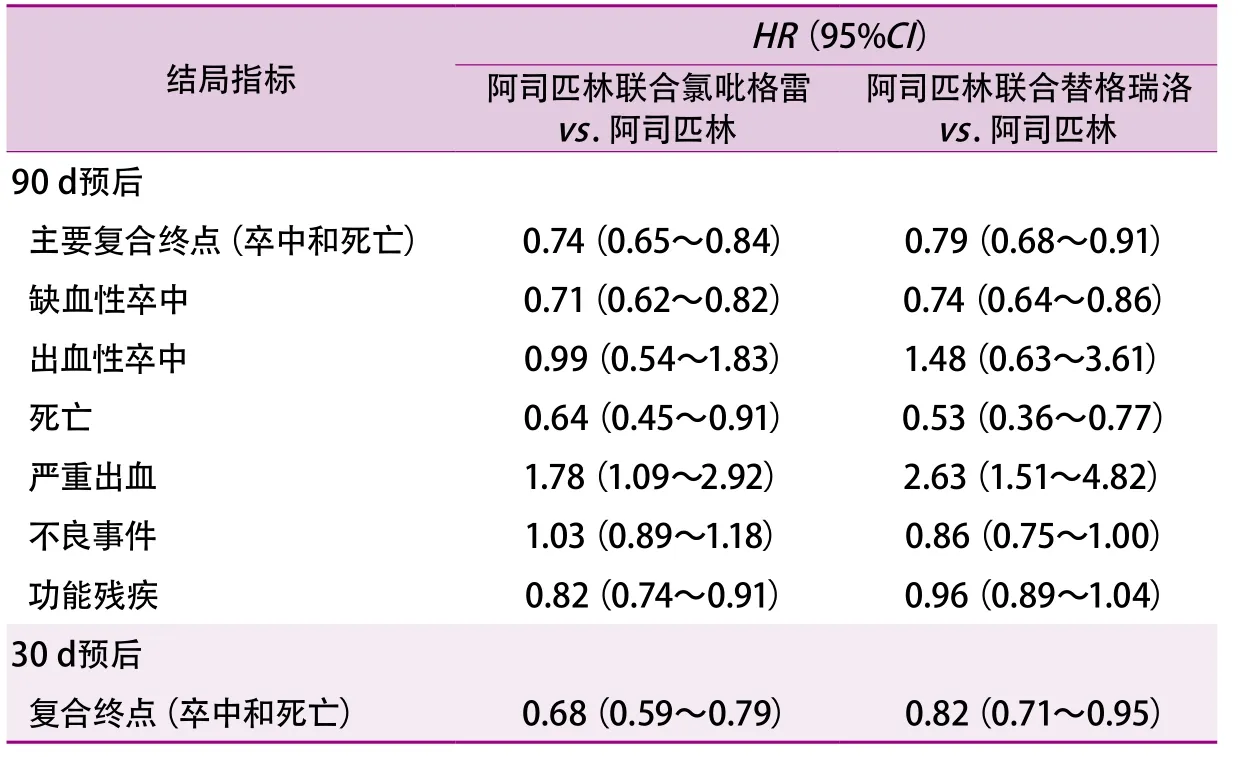
表7 CHANCE、FASTER、POINT、PRINCE和THALES研究的meta分析结果[57]
虽然目前国际上已逐渐将短程、双联的CHANCE方案作为治疗HR-NICE患者的“金标准”,但氯吡格雷在体内的代谢易受多种基因的影响,从而降低了该方案对某些基因型患者的疗效,这个问题尚未得到解决。对氯吡格雷的代谢影响最大的基因是CYP2C19。首都医科大学附属北京天坛医院国家神经系统疾病临床医学研究中心团队2016年发表在JAMA上的研究显示,携带CYP2C19丧失功能(loss of function,LoF)等位基因可使氯吡格雷的疗效降低20%[61]。由于CYP2C19LoF等位基因的携带者较多,特别是在中国汉族人群中,携带者比例高达58.8%,所以设计绕行基因的抗血小板治疗方案是十分必要的。
2021年,基于基因的精准抗血小板治疗研究CHANCE-2在世界卒中大会上作为最重要的研究报告被推出,同一天在N Engl J Med上正式发表[62]。CHANCE-2是一项随机、双盲、安慰剂对照的多中心Ⅲ期临床研究,在与CHANCE同样的HR-NICE人群中,通过快速基因检测筛选出CYP2C19LoF等位基因携带者。CHANCE-2的治疗方案同样是21 d内短程、双联抗血小板治疗,入组患者在发病24 h内,随机给予替格瑞洛(首日180 mg,次日起每次90 mg,每日2次,持续90 d)联合阿司匹林21 d或氯吡格雷(首日300 mg,次日起每次75 mg,持续90 d)联合阿司匹林21 d治疗。主要终点为90 d出血性或缺血性卒中复发,次要终点包括30 d内卒中复发、90 d内缺血性卒中复发等;主要的安全性终点为致死性出血和颅内出血。
CHANCE-2共纳入6412例患者,其中氯吡格雷联合阿司匹林组3207例,替格瑞洛联合阿司匹林组3205例。最终的数据统计显示,替格瑞洛联合阿司匹林组与氯吡格雷联合阿司匹林组相比,可显著降低携带CYP2C19LoF等位基因的HR-NICE患者90 d卒中复发的风险(HR0.77,95%CI0.64~0.94,P=0.008)(图9)。在次要终点事件中,替格瑞洛联合阿司匹林组的30 d内卒中复发风险(HR0.75,95%CI0.61~0.93)和90 d缺血性卒中复发风险(5.9%vs. 7.4%,HR0.78,95%CI0.65~0.95)均显著降低。在安全性终点方面,两种治疗方案发生致死性出血和颅内出血的风险差异均无统计学意义,但替格瑞洛联合阿司匹林组的全部出血风险和轻度出血的风险高于氯吡格雷联合阿司匹林组(表8)。

图9 CHANCE-2研究累积卒中发病率(主要终点)[62]

表8 CHANCE-2研究临床结局[62]
综合以上数据,CHNACE-2的研究结论为:对于携带CYP2C19LoF等位基因的HRNICE患者,与氯吡格雷联合阿司匹林治疗相比,在发病24 h内给予替格瑞洛联合阿司匹林治疗可显著降低患者的卒中复发风险,且不增加中、重度出血的风险,该研究为替格瑞洛联合阿司匹林治疗方案提供了高质量的阳性临床证据。出于CHANCE-2研究对抗血小板治疗独创的研究思路,以及结合基因进行精准治疗在脑血管病治疗领域的划时代突破,CHANCE-2研究在世界卒中日当天被评为2021年国际最重要的五大临床研究之一。值得注意的是,CHANCE-2还是全球第一个基于药物基因的脑血管病大型临床研究,期待在2022年,CHANCE-2继续为改写国际指南贡献中国力量。
10 另辟蹊径——迷走神经刺激成为卒中康复新选择
康复治疗是卒中治疗的另一热门板块,迷走神经刺激术(vagus nerve stimulation,VNS)是近年来在康复领域备受关注的干预方式。VNS最早应用于治疗难治性癫痫,其安全性和有效性已得到了验证。卒中后上肢功能的恢复一直是康复治疗的难点与热点。既往在大鼠缺血性卒中模型中的研究表明,VNS可通过增加大鼠运动皮层神经元的突触连接,提高大脑皮质的可塑性,改善前肢的运动功能[63]。2016年第一个将VNS应用于缺血性卒中亚急性期治疗的研究证明,将VNS与康复训练相结合是安全可行的[64];2018年发表的一项针对缺血性卒中患者的随机对照试验表明,VNS组治疗90 d后的运动功能较对照组有显著改善[65]。2021年VNS这种康复治疗方式已经获得美国食品和药品管理局批准。
2021年英国发起的VNS-REHAB研究结果发表在Lancet杂志上,该研究采用随机对照设计,探讨了VNS对缺血性卒中亚急性期和慢性期患者上肢功能的康复效果,再次为VNS提供了临床研究的支持[66]。VNS-REHAB研究纳入发病9个月~10年的单侧幕上梗死患者108例,其中VNS组53例,在康复治疗基础上采用植入式VNS设备进行迷走神经刺激;对照组55例,进行一般康复治疗,两组的治疗均持续6周。治疗前后采用Fugl-Meyer量表上肢部分(Fugl-Meyer assessment-upper extremity,FMA-UE)评定上肢运动功能的变化。结果显示,治疗6周后VNS组FMA-UE评分均值提高5.0分,对照组FMA-UE评分均值提高2.4分,治疗组的康复效果优于对照组(组间差异2.6分,95%CI1.0~4.2);治疗90 d后,治疗组的FMA-UE评分改善也优于对照组(5.8分vs. 2.8分,组间差异3.0分,95%CI0.8~5.1,P=0.0077),且VNS组的上肢功能改善率高于对照组(47%vs. 24%,组间差异24%,95%CI6~41,P=0.0098)(图10)。
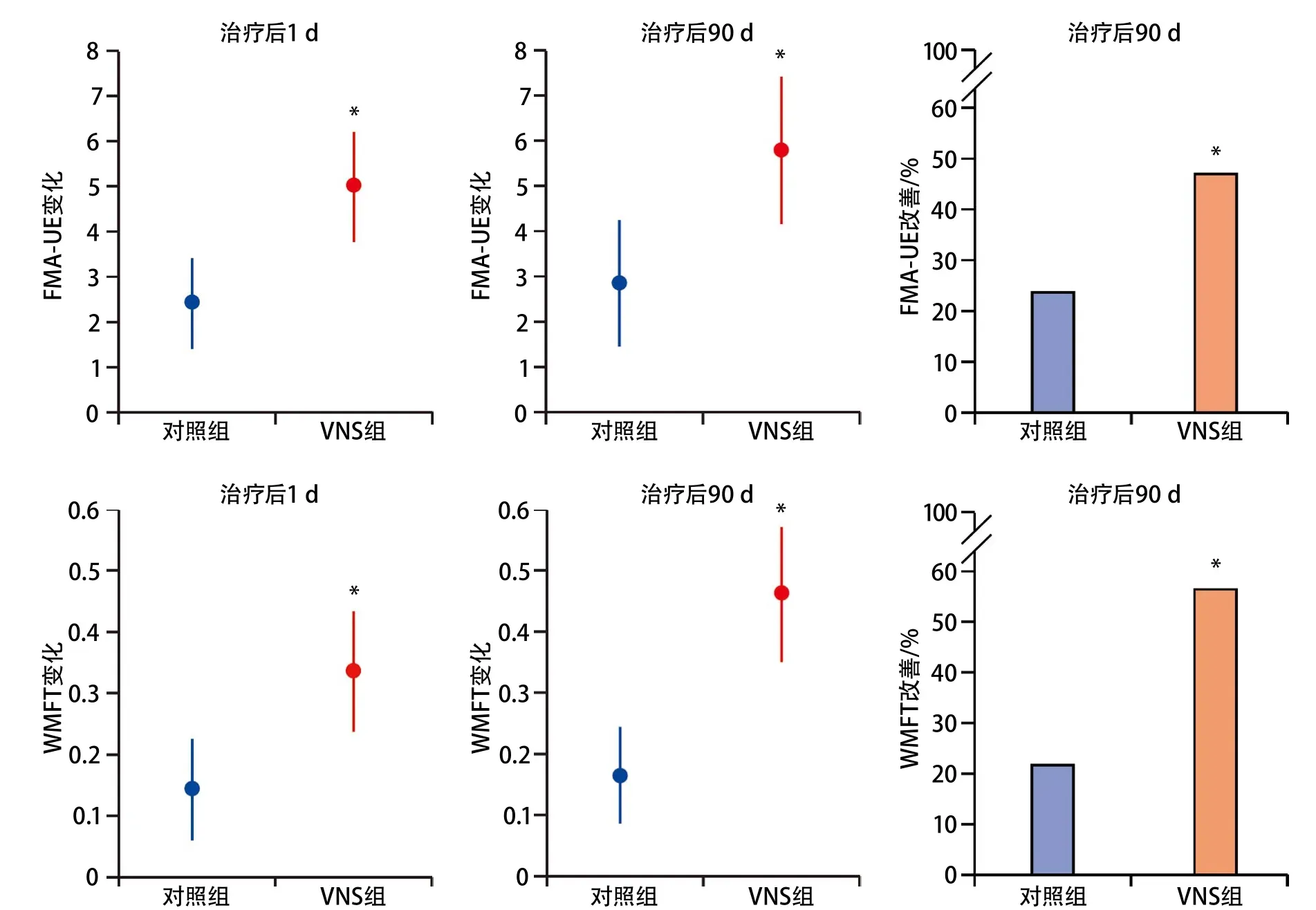
图10 VNS-REHAB研究结局提示迷走神经刺激术可促进肢体运动功能恢复[66]
同期发表的述评指出,VNS-REHAB试验证实VNS对缺血性卒中的康复具有良好的治疗效果,为缺血性卒中的康复治疗开辟了新思路;另外,此项研究的重大意义还在于提示卒中事件发生多年后,患者的运动功能仍有可能改善,其潜在机制可能为刺激迷走神经能促进神经递质释放和突触连接形成,但其疗效的机制和持续性仍需进一步的研究来探索和证实[67]。值得注意的是,尽管该研究样本量较小,但仍受到了国际卒中及康复领域的重视,被认为是2021年卒中研究领域的重大进展,这间接反映了国际同行对新型装置和新型治疗方法的期待。
回眸2021年,在受到新型冠状病毒肺炎疫情波及的情况下,全球脑血管病领域的研究者们仍坚持不懈地努力,在卒中急性期急救模式探索、再灌注治疗时间窗拓展和治疗方式验证、隐源性卒中的监测和PFO治疗、基于基因的抗血小板治疗方案选择、发展新的神经康复技术等方面取得了显著进步,这值得我们骄傲。
2021年也是中国的一个“超级航天年”,首次火星探测任务取得圆满成功,空间站建造进入全面实施阶段,首颗探日卫星“羲和号”发射成功等,带领我们进入更广阔的空间领域,也向世界展示了中国稳定、踏实的前进步伐。同样,在脑血管病研究领域,我们中国的研究也正在向世界展示其蓬勃的发展势头。期望2022年国际脑血管病研究领域凯歌再响,更期望我们中国的研究越来越多地发表在重要的学术期刊上,发出更响亮的中国声音!
附录:本文涉及研究的缩写及中文全称
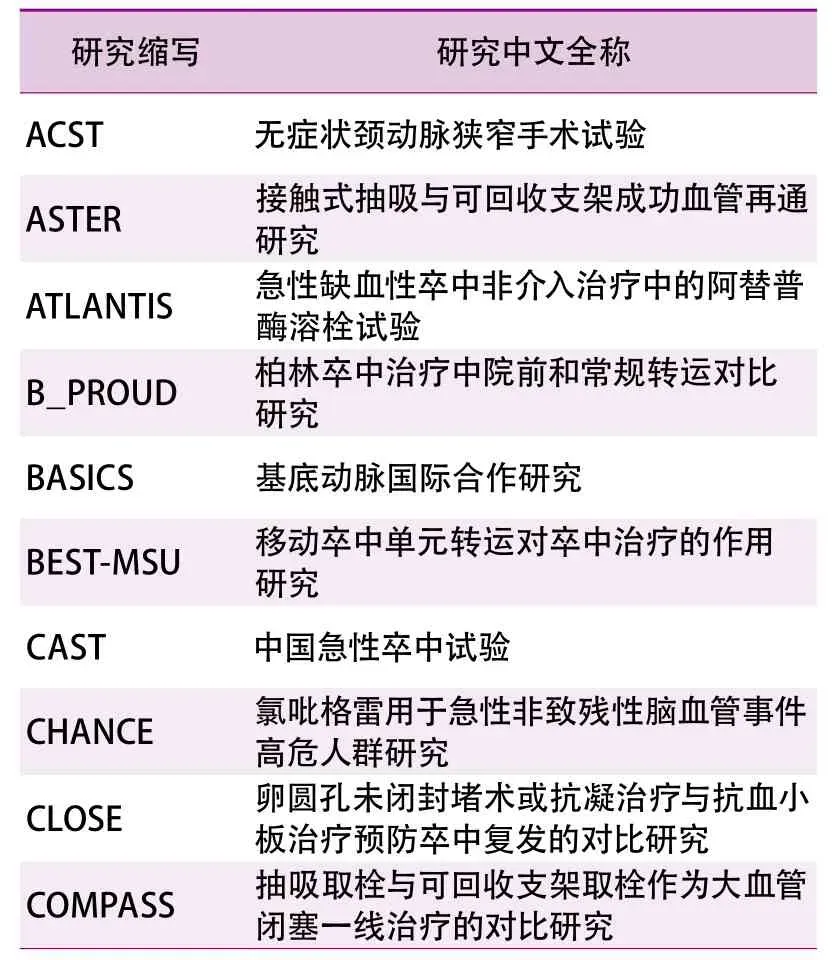
研究缩写 研究中文全称ACST 无症状颈动脉狭窄手术试验ASTER 接触式抽吸与可回收支架成功血管再通研究ATLANTIS 急性缺血性卒中非介入治疗中的阿替普酶溶栓试验B_PROUD 柏林卒中治疗中院前和常规转运对比研究BASICS 基底动脉国际合作研究BEST-MSU 移动卒中单元转运对卒中治疗的作用研究CAST 中国急性卒中试验CHANCE 氯吡格雷用于急性非致残性脑血管事件高危人群研究CLOSE 卵圆孔未闭封堵术或抗凝治疗与抗血小板治疗预防卒中复发的对比研究COMPASS 抽吸取栓与可回收支架取栓作为大血管闭塞一线治疗的对比研究
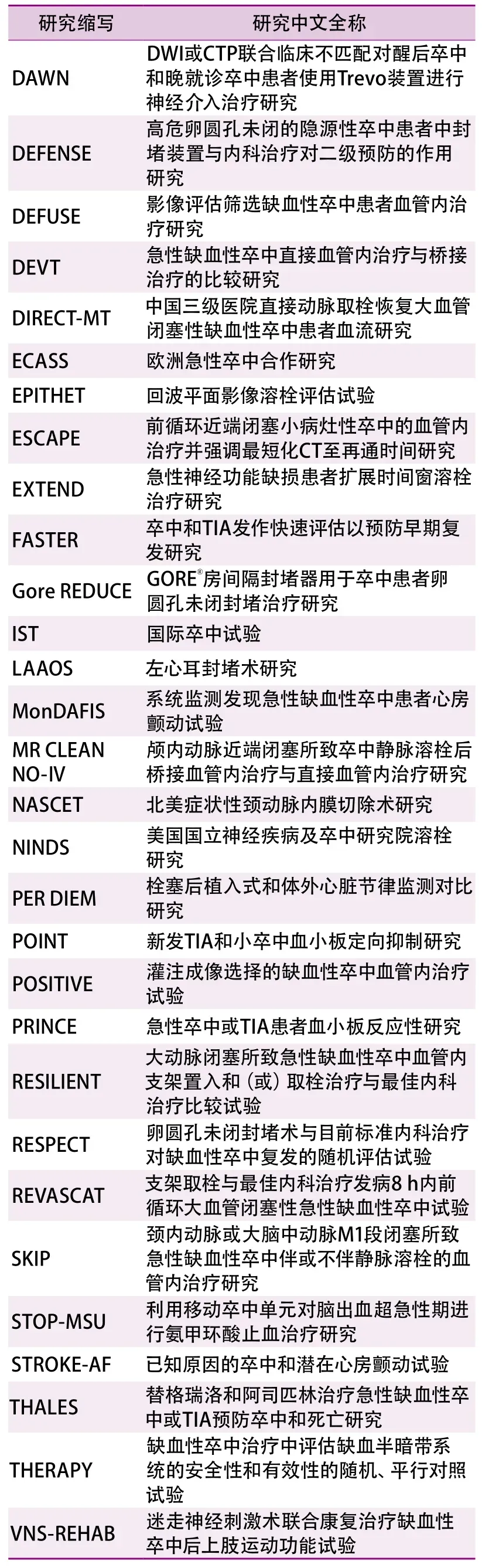
续表

