盐酸羟考酮在腹腔镜下子宫肌瘤剜除术后镇静镇痛中的应用及对患者疼痛介质水平的影响
马媛媛, 贺 亮, 陆富钊, 冯华锋, 彭凌云
(1.桂林医学院附属医院麻醉科, 广西 桂林 5410012.南方医科大学第五附属医院麻醉科, 广东 广州 510000)
子宫肌瘤是子宫平滑肌组织增生形成的肿瘤,临床无明显症状,部分患者存在月经异常、下腹坠胀、白带异常等症状,在育龄妇女中的发病率可达25%[1]。对于药物治疗无效的患者,临床多采用手术治疗,腹腔镜下子宫肌瘤剜除术是临床治疗子宫肌瘤常用的方法,具有手术创伤小、术后恢复快等特点,但该类手术术后会出现切口痛、内脏痛等疼痛刺激,若未及时干预,会增加患者术后并发症的发生风险,不利于术后康复。有效的术后镇痛是促进患者康复,改善其预后的重要措施,当前临床主要使用阿片类药物以达到术后镇静、镇痛的作用[2]。盐酸羟考酮(oxycodone hydrochloride,OH)是μ、κ受体双重激动剂,具有较强的镇痛、镇静作用,不仅对手术切口有良好的镇痛作用,还能有效抑制术后内脏痛,临床应用广泛[3]。目前有关OH在子宫肌瘤剜除术中应用研究已有报道,但OH在子宫肌瘤剜除术中应用的最适剂量还缺乏相关研究[4]。本研究分析了不同剂量OH在腹腔镜子宫肌瘤剜除术后镇静、镇痛中的应用效果,并与吗啡比较,旨在为临床腹腔镜下子宫肌瘤剜除术术后的镇静、镇痛提供参考。
1 资料与方法
1.1一般资料:选取2019年5月至2021年5月于本院择期行腹腔镜下子宫肌瘤剜除术的134例患者为对象,采用简单随机法将患者分为三组:OH1组(n=45)、OH2组(n=46)和对照组(n=43)。纳入标准:①临床检查符合腹腔镜下子宫肌瘤剜除术指征,均为首次接受子宫肌瘤剜除术治疗;②患者年龄≥18岁;③美国麻醉医师协会(American Society of Anesthesiologists,ASA)分级为Ⅰ~Ⅱ级;④患者知情同意,均签署知情同意书。排除标准:①合并其他恶性肿瘤、血液性疾病、自身免疫性疾病和重要脏器功能障碍患者;②存在阿片类药物过敏史、慢性疼痛病史患者;③长期服用镇痛药物患者;④存在认知功能障碍,难以配合研究患者。本研究经医院伦理委员会批准,各组患者的年龄、身体质量指数(body mass index,BMI)、ASA分级和手术时间等一般临床资料比较,差异无统计学意义(P>0.05),具有可比性,见表1。
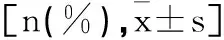
表1 各组患者一般临床资料比较
1.2方法:所有患者均在全身麻醉下行腹腔镜下子宫肌瘤剜除术,术前常规禁食禁饮,入室后采用心电监护仪常规监测患者心电图、心率、血压、平均动脉压和血氧饱和度等;给予患者鼻导管吸氧,氧流量为2L/min;建立静脉通路,行桡动脉穿刺监测有创血压。所有患者均于麻醉诱导前10min给予0.01mg/kg盐酸戊乙奎醚(国药准字H20051948,成都力思特制药股份有限公司)。麻醉诱导采用靶控输注,静脉注射1.0mg/kg丙泊酚(国药准字J20130163,Corden Pharma S.P.A.)+0.4 μg/kg舒芬太尼(国药准字H20054172,宜昌人福药业有限责任公司)+0.15 mg/kg苯磺酸顺式阿曲库铵(国药准字H20060869,江苏恒瑞医药股份有限公司)。气管插管行间歇正压通气,控制潮气量为7~10 mL/kg,呼吸频率为8~12次/min,呼气末二氧化碳分压为35~40mmHg。插管完成后4min行麻醉维持,静脉输注0.1~0.2μg·kg-1·min-1)瑞芬太尼(国药准字H20030197,宜昌人福药业有限责任公司)+丙泊酚3~5mg·kg-1·h-1,复合吸入1%~1.5%七氟醚(国药准字H20080680,山东新时代药业有限公司)。术毕连接镇痛泵行静脉自控镇痛(Patient-controlled Intravenous Analgesia,PCIA),OH1组配方为OH 20mg(国药准字H20090228,北京华素制药股份有限公司)+昂丹司琼8 mg(国药准字H10960148,宁波天衡药业股份有限公司)+0.9%氯化钠注射液,共100 mL;OH2组配方为OH 30 mg+昂丹司琼8 mg+0.9%氯化钠注射液,共100 mL;对照组PCIA配方为吗啡50 mg(国药准字H21021995,东北制药集团沈阳第一制药有限公司)+昂丹司琼8 mg+0.9%氯化钠注射液,共100 mL;参数设置:负荷剂量2 mL,背景计量2 mL/h,PCA剂量2 mL/次,锁定时间15 min;当视觉模拟评分(visual analogue scales,VAS)≥3分时,按压PCA键,必要情况下静脉注射双氯芬酸钠进行补救镇痛。所有操作均由同一位高年资麻醉医生完成。
1.3观察指标:①术后疼痛情况和镇静程度:分别术后6 h、12 h和24 h采用VAS评分法对患者术后的疼痛情况进行评价,该评分法总分为0~10分,分值越高,表明患者疼痛越明显[5];采用Ramsay镇静评分法对患者术后的镇静程度进行评估,该评分法总分为0~10分,分值越高,表明患者镇静程度越高[6]。②疼痛介质水平:分别于麻醉诱导前15min、术后6h、12h和24h取患者静脉血5mL,3000r/min离心10min,分离血清后低温保藏待测;采用放射免疫分析法检测疼痛介质水平,包括前列腺素E2(Prostaglandin E2,PGE2)和神经生长因子(nerve growth factor,NGF)。④术后镇痛补救率和PCA按压次数:记录两组患者术后48 h内的镇痛补救率和PCA按压次数。⑤不良反应发生情况:记录两组患者镇痛期间恶心呕吐、头晕嗜睡、皮肤瘙痒、低血压、窦性心动过缓、呼吸抑制、镇静过度等不良反应发生情况。
1.4统计学处理:采用SPSS20.0统计软件对数据进行分析。计量资料以表示,多组间年龄、BMI、手术时间、PCA按压次数比较采用单因素方差分析,进一步两两比较采用SNK-q检验;多组间不同时间点VAS评分、Ramsay评分、PGE2、NGF水平比较采用重复测量方差分析,同时间点各组间比较采用LSD-t检验;计数资料以n(%)表示,ASA分级比较行χ2检验,镇痛补救率、不良反应发生率比较行Fisher确切概率检验,检验水准α=0.05;两两比较时采用Bonferroni法对显著性进行校正,校正后的检验水准α=0.0325。
2 结 果
2.1不同时间点各组患者疼痛情况和镇静程度比较:各组患者VAS评分、Ramsay评分随时间推移而不同,不同时间、不同组间的差别及时间与分组的交互作用均有统计学意义(P<0.05)。术后6h,各组患者的VAS评分和Ramsay评分比较,差异无统计学意义(P>0.05);术后12h、24h,OH1组和OH2组的VAS评分和Ramsay评分均明显低于对照组(P<0.05),OH1组和OH2组的VAS评分和Ramsay评分比较无明显差异(P>0.05),见表2。
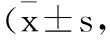
表2 术后不同时间点两组患者疼痛情况和镇静程度比较分)
2.2不同时间点各组患者疼痛介质水平比较:各组患者疼痛介质水平随时间推移而不同,不同时间、不同组间的差别及时间与分组的交互作用均有统计学意义(P<0.05)。麻醉诱导前15min,各组患者的PGE2、NGF水平比较,差异无统计学意义(P>0.05);术后6h、12h、24h,OH1组和OH2组的PGE2、NGF水平均低于对照组(P<0.05),OH1组和OH2组的PGE2、NGF水平比较无明显差异(P>0.05),见表3。
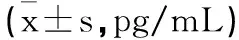
表3 不同时间点各组患者疼痛介质水平比较
2.3术后48h内各组患者镇痛补救率和PCA按压次数比较:术后48h内,OH1组和OH2组患者的镇痛补救率均低于对照组,PCA按压次数均少于对照组(P<0.05);OH1组和OH2组的镇痛补救率、PCA按压次数比较,差异无统计学意义(P>0.05),见表4。
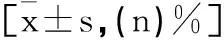
表4 术后48h内各组患者镇痛补救率和PCA按压次数比较
2.4镇痛期间各组患者不良反应发生情况比较:镇痛期间,两组患者均未出现低血压、窦性心动过缓、呼吸抑制等不良反应;三组的皮肤瘙痒、镇静过度比较无明显差异(P>0.05)。三组患者的恶心呕吐、头晕嗜睡发生率比较,差异有统计学意义(P<0.05),且OH2组患者的恶心呕吐、头晕嗜睡发生率均高于OH1组和对照组(P<0.0325),OH1组和对照组的恶心呕吐、头晕嗜睡发生率比较无明显差异(P>0.05),见表5。
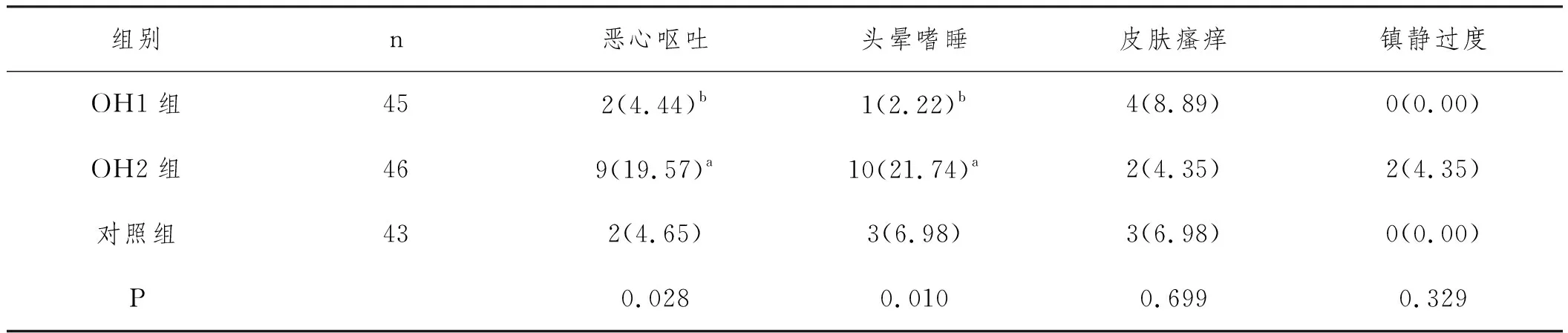
表5 镇痛期间各组患者不良反应发生情况比较n(%)
3 讨 论
3.1腹腔镜下子宫肌瘤剜除术后应给予合适的镇痛治疗:接受腹腔镜下子宫肌瘤剜除术的患者,由于术中的创伤性操作会引起机体应激反应,释放大量炎性递质,导致中枢及外周神经元敏感化从而引发术后剧烈疼;此外,术后缩宫素的使用还会引发较为强烈的内脏痛,进一步影响患者的术后恢复。因此,合适的术后镇痛是减少术后并发症、加速患者康复的关键。作为半合成的纯阿片受体激动剂,OH可动或拮抗不同受体,通过降低炎性因子水平、维持细胞因子平衡等方式减轻患者术后疼痛。刘清仁等[7]比较了羟考酮与吗啡在腹腔镜全子宫切除术后镇痛中的应用,发现羟考酮较之吗啡在腹腔镜全子宫切除术后静脉镇痛中可以起到更好的镇痛效果。
3.2OH在腹腔镜下子宫肌瘤剜除术后具有良好的镇静、镇痛作用:本研究研究结果显示,术后12h、24h,OH1组和OH2组的VAS评分和Ramsay评分均明显低于对照组,OH1组和OH2组的VAS评分和Ramsay评分比较无明显差异,提示OH在腹腔镜下子宫肌瘤剜除术后的镇静、镇痛方面效果优于吗啡,且20mg、30mg的OH效果相当。OH可作用于中枢神经系统突触前末段细胞膜上的μ受体,发挥镇静、镇痛的作用,还可以激动平滑肌κ受体,缓解术后内脏痛[8]。此外,在等效剂量下,血脑屏障对OH的主动转运效率高于吗啡,中枢神经浓度可迅速达到阈值,加快起效速率,从而发挥更强的镇痛效应[9]。
3.3OH可降低腹腔镜下子宫肌瘤剜除术后患者疼痛介质水平:研究表明,术后疼痛的产生与部分血清细胞因子关系密切。PGE2是一种由花生四烯酸被催化后产生的典型疼痛刺激因子,其表达水平升高可降低人体疼痛阈值,使得痛觉增强;还可导致血管痉挛,促进血小板的释放,使得中枢及周围神经系统敏感化,增加患者主观疼痛感受[10]。NGF是影响神经元亚群的生长和增殖的重要物质,当与原肌球蛋白受体激酶A结合后,可激活多种疼痛信号通路,从而扩大疼痛反射,还可增强邻近痛觉神经元对炎症反应的敏感性,加深痛觉感受[11]。本研究发现,术后6h、12h、24h,OH1组和OH2组的PGE2、NGF水平均低于对照组,OH1组和OH2组的PGE2、NGF水平比较无明显差异,提示OH能更好地抑制患者疼痛介质的合成,从而达到缓解疼痛的目的。张金立等[12]发现,在腹部闭合性损伤开腹手术中应用OH超前镇痛,可显著降低患者疼痛介质水平,进一步表明OH的良好镇痛作用与抑制疼痛介质分泌有关。
3.4OH可降低腹腔镜下子宫肌瘤剜除术后镇痛补救率和PCA按压次数,安全性较高:本研究发现,术后48h内,OH1组和OH2组患者的镇痛补救率均低于对照组,PCA按压次数均少于对照组,进一步表明OH具有良好的镇痛作用,可减少补救镇痛次数与止痛药使用量,从而有利于患者术后恢复。本研究还发现,镇痛期间皮肤瘙痒、镇静过度发生率比较无明显差异,但OH2组患者的恶心呕吐、头晕嗜睡发生率均高于OH1组和对照组,提示高剂量的OH可能会增加患者术后不良反应的发生风险。分析原因可能是OH2组患者的OH血药浓度达到了可影响呼吸及血流动力学的阈值,从而使术后不良反应增加。因此,低剂量的OH安全性更高,可安全地用于腹腔镜下子宫肌瘤剜除术后镇静、镇痛中。
综上所述,OH用于腹腔镜下子宫肌瘤剜除术术后镇静、镇痛较吗啡效果好,可有效减轻患者痛觉感受,低剂量OH的不良反应发生率更低,安全性更高。

