腹腔镜下辅助LAM对直径>10cm子宫浆膜下肌瘤患者的效果分析
肖冰冰
(安徽省界首市人民医院, 安徽 界首 236500)
子宫肌瘤为常见的一种良性肿瘤,属于一种雌孕激素依赖的肿瘤,常发病人群为育龄期妇女,发病率占75%[1]。直径>10cm子宫肌瘤过大会影响手术野的暴露,医疗风险及手术难度加大,手术治疗中多采用剖腹手术进行治疗,但传统的开腹手术切口由于切口较大,往往会出现感染等术后并发症的发生[2]。随着腹腔镜设备的不断完善,利用腹腔镜辅助下腹壁小切口子宫肌瘤剔除术(laparoscopically assisted myomectomy,LAM)方案治疗,可有效降低损伤,且此方法具有小切口、小损伤的优点。目前该技术应用较为成熟,可规避因脏器过度暴露而引起术后并发症等风险的发生,使手术质量得到提高[3]。本文根据手术治疗方式的不同,观察并分析腹腔镜下辅助LAM对直径>10cm子宫浆膜下肌瘤患者的效果及影响,为临床直径>10cm子宫浆膜下肌瘤治疗方案提供数据参考。
1 对象与方法
1.1研究对象:本文选取2017年11月至2020年11月在我院就诊的直径>10cm子宫浆膜下肌瘤患者80例,年龄29~54岁,病程1~6年,身高146~173cm,体重55~86kg,肌瘤部位:前壁30例,后壁20例,宫底18例,峡部7例,阔韧带5例;按照随机数字表法分为常规组(39例)和观察组(41例)。两组患者一般资料比较,差异无统计学意义(P>0.05),具有可比性,见表1。纳入标准:①所有患者均符合《实用妇产科学》中关于直径>10cm子宫浆膜下肌瘤的诊断标准[4];②均经超声影像学及宫颈细胞学确诊的患者;③本文研究患者及其家属均知情,签署知情同意书,经过我院伦理委员会批准。排除标准:①伴有其他子宫疾病的患者;②伴有双侧卵巢异常的患者;③伴有盆腔器官疾病的患者;④伴有心肝肾等脏器功能异常的患者;⑤伴有其他恶性肿瘤的患者;⑦伴有严重哮喘高血压病、糖尿病的患者。
表1 两组患者临床基线资料的比较
1.2手术方法:两组患者在手术前均要禁食6h,进行全麻或者持续硬膜外麻醉。常规组采用传统开腹方案进行治疗,嘱咐患者取平卧位置,于腹部正中选取纵向或者横向进行切口,选取耻骨联合处将皮肤逐层分开,随后入腹腔对子宫肌瘤所处具体大小及位置进行探查(图1)。于基底部注射10mL的垂体后叶素(陕西发展医药有限公司,H34022977)6U+0.9%氯化钠注射液(辰欣药业股份有限公司,H37022336),切开肌瘤外包膜,然后剔除肌瘤结节,采用可吸收缝合线连续缝合切口,闭合瘤腔与腹腔(图2)。观察组采用腹腔镜下辅助LAM进行治疗:嘱咐患者取膀胱截石位置,于脐窝上缘约1cm处横向进行切口,建立气腹后置入5mm腹腔镜进行探查(图3),观察肌瘤有无粘连、解剖关系、个数及位置大小,在耻骨联合处,横向切开4cm,随后逐层进腹,将子宫位置进行调整,暴露肌瘤的位置且处于切口下方,在包膜内注射10mL的垂体后叶素6U+0.9%氯化钠注射液,将肌瘤表面假包膜打开,然后进行逐步碎瘤,将所有可触及肌瘤结节逐个剔除(图4)。使用1-0号可吸收线,进行8字缝合肌瘤蒂部的血管,分层连续缝合子宫切口(图5)。
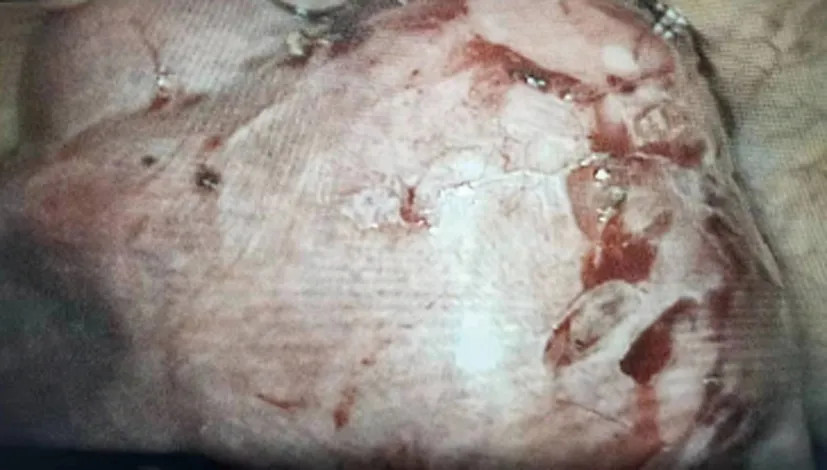
图1 耻骨处将皮肤逐层分开探查肌瘤大小及位置
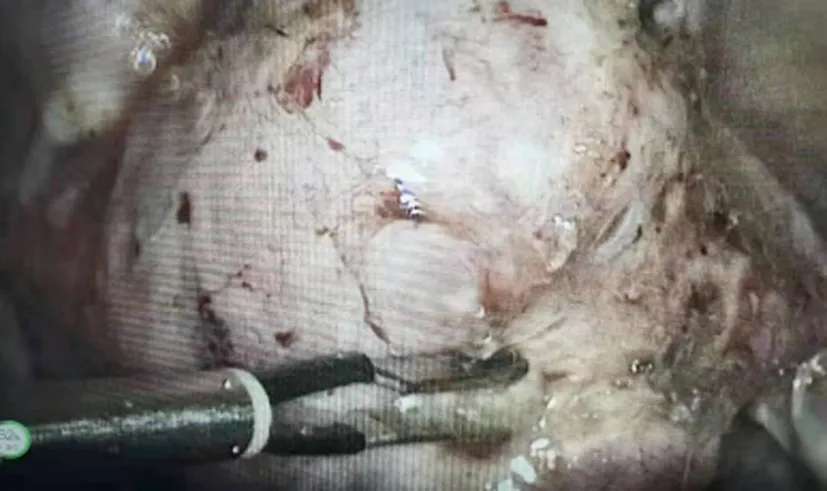
图2 切开肌瘤外包膜剔除肌瘤结节
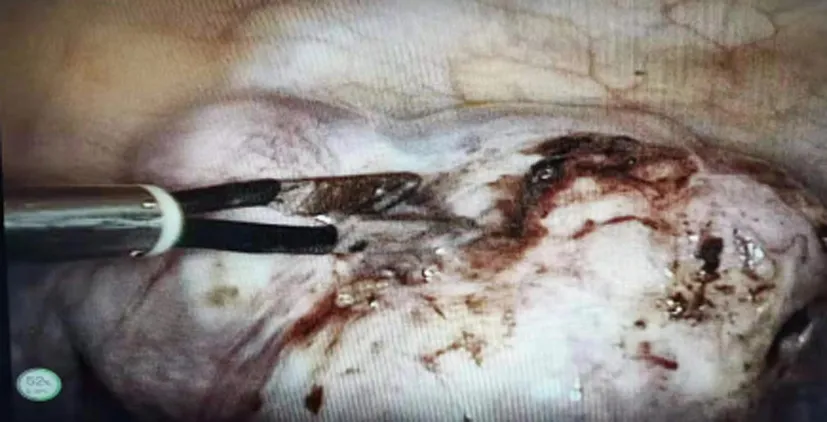
图3 脐窝上缘进行横向切口,腹腔镜探查
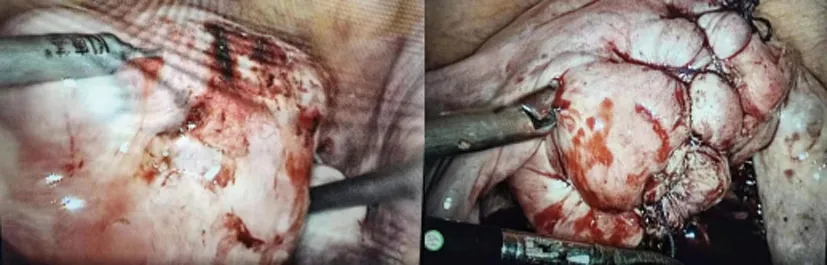
图4 观察肌瘤整体情况,将所有可触及肌瘤结节逐个剔除
腹腔镜下辅助LAM手术图片(注:图片顺序同上述手术操作步骤一致)
1.3观察指标
1.3.1术中及术后指标检测:观察并记录两组患者手术时间,术中及术后的恢复情况,术中出血量,术后并发症,术后排气时间、住院时间、手术时间。采用微循环检测仪(郑州天益健生物科技有限公司,ZL103)检测两组患者在术前及术后1d、7d毛细血管管径、血流灌注、血液流态积分。
1.3.2疼痛评分、术后疼痛消失时间、肌瘤体积:采用VAS评估表对患者疼痛情况进行评分,患者分数越高说明疼痛程度也会逐渐增加,VAS评分是通过患者主观的疼痛感觉进行评分,一端0是代表没有疼痛感觉,另一端10代表疼痛严重,此评分是由患者根据自己疼痛程度进行评分的。肌瘤体积:按公式πabc/6cm3计算,a、b、c(B超测量肌瘤的三维切面最大径线,多发性肌瘤按照最大肌瘤体积计算);观察并记录两组患者术后疼痛消失时间。
1.3.3统计手术治疗效果及术后并发症发生情况:根据《子宫肌瘤的诊治中国专家共识》[5]中患者临床症状评价治疗效果,显效:患者临床体征、症状及子宫肌瘤均完全消失;有效:患者临床症状及体征明显改善;无效:患者临床症状及体征无改善;治疗总有效率=(显效例数+有效例数)/总例数×100%。观察两组患者在手术过程中术后并发症发生情况,主要包括:切口感染、皮下气肿、过性发热,并作组间比较。
2 结 果
2.1两组患者的手术指标的比较:观察组术后排气时间、住院时间、术中出血量低于常规组,手术时间高于常规组,差异有统计学意义(P<0.05),见表2。
表2 两组患者的手术指标的比较
2.2两组患者手术前后宫颈局部微循环水平的比较:两组术前毛细血管管径、血流灌注及血液流态积分,差异无统计学差异(P>0.05)。两组患者术后1d、7d毛细血管管径、血流灌注低于两组术前,血液流态积分高于两组术前,差异均有统计学意义(P<0.05),见表3。
表3 两组患者手术前后宫颈局部微循环水平的比较
2.3两组患者VAS评分、术后疼痛消失时间、肌瘤体积的比较:两组术后1d、7d VAS评分高于两组术前,差异均有统计学意义(P<0.05),观察组术后1d VAS评分低于常规组,观察组术后7d VAS评分低于常规组,观察组术后疼痛消失时间低于常规组(t=6.230,P=0.001),观察组术后肌瘤体积低于常规组,差异均有统计学意义(P<0.05),见表4。
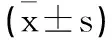
表4 两组患者VAS评分术后疼痛消失时间肌瘤体积的比较
2.4两组患者临床疗效的比较:观察组治疗总有效率高于常规组,差异具有统计学意义(P<0.05)。见表5。
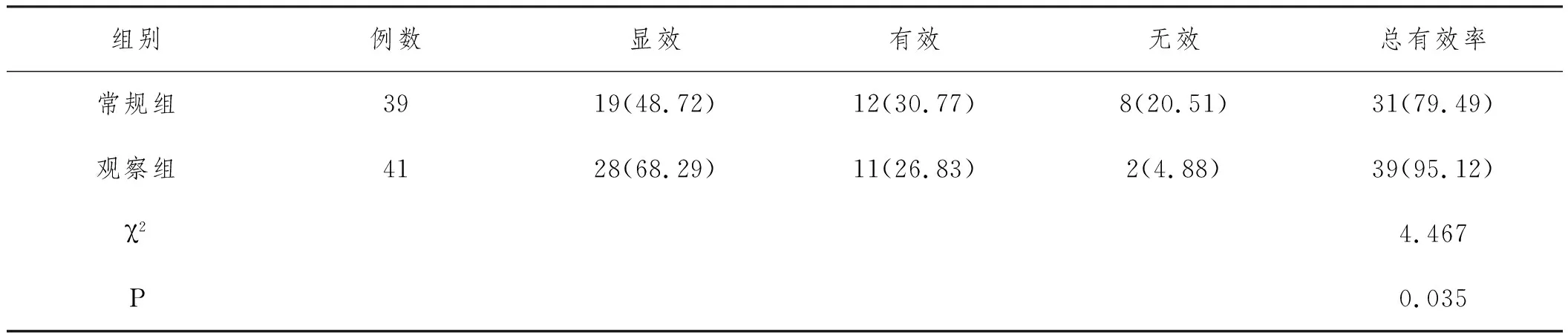
表5 两组临床疗效比较n(%)
2.5两组患者术后并发症比较:与常规组相比,观察组术后并发症发生率较低,差异有统计学意义(P<0.05),见表6。
表6 两组患者术后并发症比较
3 讨 论
子宫肌瘤常以往常常采用传统开腹手术方法治疗,因其具有较广的适应性,不受肌瘤大小、数目及所处位置的限制,技术难度较低并且疗效确切[6]。但是传统开腹手术对于患者腹腔干扰、损伤较大且还容易造成患者体内环境发生紊乱,增加切口感染等术后并发症风险,导致患者术后恢复情况较差。
腹腔镜下辅助LAM手术是在保留了腹腔镜微创化的基础上,同时还具有开腹手术的优点,二者完美结合能够实现优势互补的效果,该技术在目前是较为成熟的一种技术[7]。本文研究显示,腹腔镜下辅助LAM能够缩短直径>10cm子宫浆膜下肌瘤患者术后排气时间、住院时间及手术时间,减少术中出血量,从而有利于患者术后的恢复。Asgari Z等[8]研究中发现,腹腔镜下辅助LAM手术是根据肌瘤大小选择脐窝上缘约1cm处横向进行切口,置入腹腔镜进行探查,以保证手术视野足够大便于操作,从而使其与子宫血管吻合支的方向保持一致,从而减少术中的出血量。而毛细血管管径、血流灌注、血液流态积分能够综合反映患者集体的血供情况,从而了解患者术前和术后的整体状况。在本文研究中,腹腔镜下辅助LAM能够升高直径>10cm子宫浆膜下肌瘤患者毛细血管管径、血流灌注,降低血液流态积分,从而改善患者微循环功能。MacKoul P等[9]研究中腹腔镜下辅助LAM术在实施过程中对患者腹腔部位产生的不良影响较小,其在清除肌瘤的同时还能有效控制机体内微循环状态,本文研究结果与其一致。
腹腔镜下辅助LAM借助腹腔镜进行探查,可有效扩大手术的视野且获得较为清晰的影像学资料,同时对患者机体邻近组织损伤较小,利用电凝止血减少术中出血量,减轻患者疼痛感。在本文中,采用腹腔镜下辅助LAM能够降低直径>10cm子宫浆膜下肌瘤患者VAS评分及肌瘤体积,缩短术后疼痛消失时间,从而有效减轻患者的疼痛。MacKoul P等[10]研究中发现,对于临床症状的育龄期患者,采用腹腔镜下辅助LAM手术首选的手术方法,其与传统开腹手术相比,其对患者术后疼痛程度及干扰较小。而传统开腹手术容易影响术后恢复进程,增加患者切口感染等术后并发症的风险。在本文研究结果中,腹腔镜下辅助LAM能够提高直径>10cm子宫浆膜下肌瘤患者治疗总有效率,减少术后并发症的发生。腹腔镜下辅助LAM手术是在可视条件下严格按照无菌化操作,采用较小的手术范围,能够缩短患者术后排气时间,降低切口感染的发生及加快患者术后的恢复,缓解患者术后疼痛,其在手术操作过程中一定要注意观察肿瘤边界,并对出血位置及时控血,避免伤口感染事件的发生。
综上所述,腹腔镜下辅助LAM能够减少直径>10cm子宫浆膜下肌瘤患者术中出血量,缩短患者术后排气时间、住院时间、术后疼痛消失时间及手术时间,减小肌瘤体积,减轻患者术后的疼痛,改善患者微循环功能,疗效显著。

