甘蔗糖蜜酶法澄清技术的研究
张洛铫,尚红岩*,杨凤婷,郑毅锋,付金亿,陈秀丽,黄泽彬,钟靖琪,曹嘉亮,郑子鑫,殷德运
(1广东轻工职业技术学院食品与生物技术学院,广东广州 510300;2广东省科学院南繁种业研究所,广东广州 510316)
0 前言
糖蜜是制糖工业副产物,富含蔗糖、还原糖等可发酵性糖,广泛应用于食品、发酵、饲料等行业[1-4]。但糖蜜中还含有胶体、无机盐灰分和色素等,其中胶体约占10%左右,主要来源于甘蔗原料中果胶和含氮有机物[5]。果胶是以半乳糖醛酸和还原糖聚合成复合多糖类,在糖蜜中形成胶体溶液,增大糖蜜粘度。目前国内糖蜜大部分用于发酵生产酵母、酒精和发酵制品,糖蜜中的胶体不能被发酵微生物利用,并且会抑制酵母等微生物的繁殖和发酵,糖蜜利用前必须进行澄清处理[6-7]。
目前糖蜜澄清方法多采用添加酸、碱、钙盐或絮凝剂等化学方法处理。化学方法处理原理是将糖蜜中的胶体和灰分沉降,沉降后的有机物成为工厂废渣,仍然需要处理才能排放,并且加进糖蜜中的酸碱会将过多的阴离子或阳离子残留在糖蜜中,给糖蜜在食品发酵中应用带来安全隐患[8-11]。本研究采用生物酶解方法澄清糖蜜,采用果胶酶等酶制剂将糖蜜中的胶体水解成小分子糖,酶法澄清后糖蜜还原糖浓度明显提高。
1 材料与方法
1.1 原料及试剂
糖蜜85°Bx,广西凤糖生化股份有限公司;酿酒活性干酵母,广西丹宝利酵母有限公司;过磷酸钙、硫酸铵、酚酞等均为分析纯,广州化学试剂厂;浓硫酸,重庆长鹏化工有限公司;氢氧化钠,天津华东试剂厂;果胶,分析纯,Sigma公司。
果胶酶100000 U/g[酶活(U):1 g酶在50℃,pH 5.0的条件下,1 h分解果胶产生1 mg半乳糖醛酸为一个酶活单位],广州瑟烨生物科技有限公司。
1.2 仪器及设备
PHS-3精密酸度计,上海大普仪器有限公司;FA224电子分析天平,上海舜宇恒平科学仪器有限公司;UV-520紫外可见分光光度计,上海元析仪器有限公司;DK-98-II电热恒温水浴锅,郑州长城科工贸有限公司;98-1-C数显控温电热套,天津市泰斯特仪器有限公司;DHP-9162电热恒温培养箱,上海恒科科学仪器有限公司;酒精浓度计,河北省武强县同辉仪表厂;移液枪,济南欧莱博技术有限公司。
1.3 试验方法
1.3.1 糖蜜无酸澄清
称取200 g糖蜜,加水稀释到50°Bx,加入过磷酸钙0.3%,硫酸铵0.6%,果胶酶19 U/g到糖蜜后,平均分成 5组,分别搅拌加热到 30、40、50、60、70℃,分别自然沉降40 min,离心分离沉降物,澄清糖液降温至30℃,分析每组锤度。
1.3.2 糖蜜酶法澄清工艺研究
称取500 g糖蜜,加水稀释到50°Bx,分析其还原糖浓度。加过磷酸钙0.3%,硫酸铵0.6%,加热到50℃,平均分成5组,每组分别按每克糖蜜加入果胶酶10、13、15、17、19 U/g(即上述5组糖蜜分别加入果胶酶 0.01、0.013、0.015、0.017、0.019 g),搅拌混合均匀后再平均分成5组,每组分别自然沉降20、30、40、50、60 min,分别离心分离排除沉降物,降温至30℃,分析每组澄清糖液的锤度和总还原糖浓度。
1.4 检测方法
1.4.1 糖锤度的测定
采用阿贝折光仪测定糖锤度:取待检溶液数滴,置于折光棱镜面上,合上盖板,使溶液均匀分布在棱镜面。将仪器进光窗对向光源,调节视度圈,读取明暗分界线对应刻度读数,即为糖锤度。
1.4.2 酒精度测定
采用酒精计法测定酒精度[12]。
1.4.3 还原糖测定
采用 3,5-二硝基水杨酸比色法(DNS法)测定还原糖的含量[10]。
1.5 数据处理与分析
每组实验重复3次,实验结果取平均值,采用Excel软件对实验数据进行统计和绘图。
2 结果与讨论
2.1 温度对果胶酶酶解后糖锤度的影响
将稀释到50°Bx的糖蜜分别在不同温度下澄清,离心分离排除沉降物,分析澄清糖液的锤度,实验结果如表1,澄清后锤度随温度变化如图1所示。
由表1和图1可以看出,随着温度的升高,果胶酶将糖蜜中果胶水解成小分子糖越多,糖锤度相应升高。在温度50℃时果胶酶活性最高,糖锤度达到峰值,温度过高,果胶酶活性降低,糖锤度相应降低。同时也验证了果胶酶最适温度为50℃[13],接下来实验将对果胶酶升温到50℃酶解。
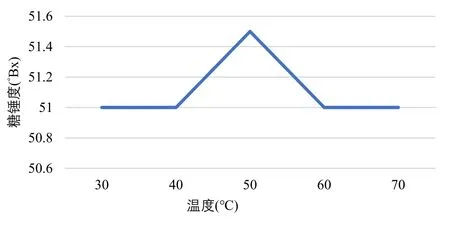
图1 温度对果胶酶酶解后糖锤度的影响

表1 温度对果胶酶酶解后糖锤度的影响
2.2 果胶酶不同添加量对糖蜜澄清的影响
称取500 g糖蜜,加水稀释到50°Bx,DNS法测定分析其还原糖浓度为30.11 g/100mL。
2.2.1 果胶酶用量10 U/g时,沉降时间对糖蜜澄清效果的影响
当果胶酶用量为10 U/g时,分析每组澄清糖液的锤度和总还原糖变化,如表2所示,分别做糖锤度和还原糖随澄清时间变化趋势,如图2所示。
从表2和图2可以看出,开始时随澄清时间延长,糖锤度和还原糖都在升高,澄清时间在40 min时,糖锤度和还原糖浓度达到峰值。澄清时间过长,酶解的糖可能被灰分和胶体吸附到沉淀物中,造成糖损失。因此果胶酶用量为10 U/g时,最佳澄清时间是40 min。

表2 果胶酶10 U/g时糖蜜不同澄清时间下的澄清效果

图2 果胶酶10 U/g时糖锤度和总还原糖随澄清时间变化趋势
2.2.2 果胶酶用量13 U/g,沉降时间对糖蜜澄清效果的影响
当果胶酶用量为13 U/g时,分析每组澄清糖液的锤度和总还原糖变化,如表3所示,分别做糖锤度和还原糖随澄清时间变化趋势,如图3所示。从表3和图3可以看出,开始时随澄清时间延长,糖锤度和还原糖都在升高,澄清时间在40 min时,糖锤度和还原糖浓度达到峰值。澄清时间过长,糖会被灰分和胶体吸附到沉淀物中,造成糖损失。因此果胶酶用量为13 U/g时,最佳澄清时间是40 min。

表3 果胶酶13 U/g时糖蜜不同澄清时间下的澄清效果

图3 果胶酶13 U/g时糖锤度和总还原糖随澄清时间变化趋势
2.2.3 果胶酶用量15 U/g时沉降时间对糖蜜澄清效果的影响
当果胶酶用量为15 U/g时,分析每组澄清糖液的锤度和总还原糖变化,如表4所示,分别做糖锤度和还原糖随澄清时间变化趋势,如图4所示。
从表4和图4可以看出开始时随澄清时间延长,糖锤度和还原糖都在升高,澄清时间在40 min时,糖锤度和还原糖浓度达到峰值。澄清时间过长,糖会被灰分和胶体吸附到沉淀物中,造成糖损失。因此果胶酶用量为15 U/g时,最佳澄清时间是40 min。

表4 果胶酶15 U/g时糖蜜不同澄清时间下的澄清效果

图4 果胶酶15 U/g时糖锤度和总还原糖随澄清时间变化趋势
2.2.4 果胶酶用量17 U/g,沉降时间对糖蜜澄清效果的影响
当果胶酶用量为17 U/g时,分析每组澄清糖液的锤度和总还原糖变化,结果如表 5所示,分别做糖锤度和还原糖随澄清时间变化趋势,如图5所示。从表5和图5可以看出,开始时随澄清时间延长,糖锤度和还原糖都在升高,澄清时间在40 min时,糖锤度和还原糖浓度达到峰值。澄清时间过长,糖会被灰分和胶体吸附到沉淀物中,造成糖损失。因此果胶酶用量为17 U/g时,最佳澄清时间是40 min。

表5 果胶酶17 U/g时糖蜜不同澄清时间下的澄清效果

图5 果胶酶17 U/g时糖锤度和总还原糖随澄清时间变化趋势
2.2.5 果胶酶用量19 U/g时沉降时间对糖蜜澄清效果的影响
当果胶酶用量为19 U/g时,分析每组澄清糖液的锤度和总还原糖变化,结果如表6所示,分别做糖锤度和还原糖随澄清时间变化趋势,如图6所示。
从表6和图6可以看出,开始时随着澄清时间的延长,糖锤度和还原糖都在升高,澄清时间在40 min时,糖锤度和还原糖浓度达到峰值。澄清时间过长,糖会被灰分和胶体吸附到沉淀物中,造成糖损失。因此果胶酶用量为19 U/g时,最佳澄清时间是40 min。

图6 果胶酶19 U/g时糖锤度和总还原糖随澄清时间变化趋势

表6 果胶酶19 U/g时糖蜜不同澄清时间下的澄清效果
2.3 果胶酶最适添加量研究
糖蜜添加果胶酶澄清,综上实验所示,果胶酶添加量从10 U/g到19 U/g,最佳沉降时间均为40 min。糖蜜添加果胶酶澄清后,还原糖浓度是糖蜜食品发酵应用最核心的指标,将上述实验中沉降时间固定为40 min,果胶酶添加量从10 U/g到19 U/g,澄清后还原糖浓度数据整理到表7中,分析糖蜜澄清后还原糖浓度随果胶酶添加量不同变化趋势,如图7所示。
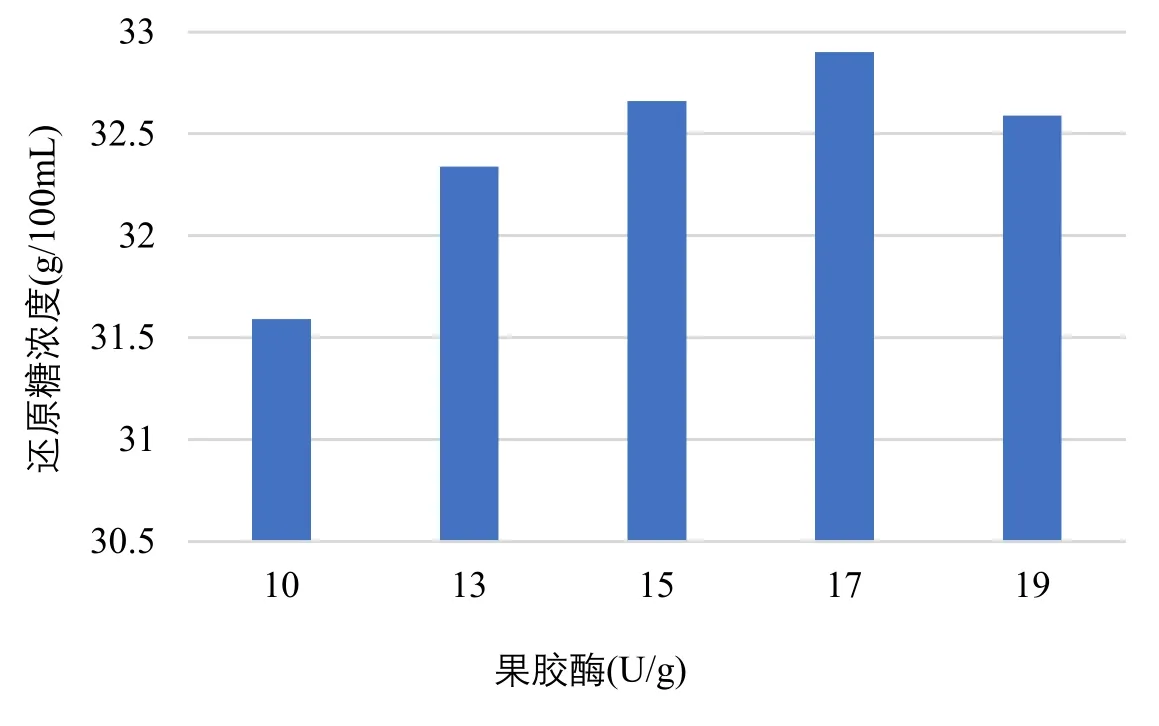
图7 果胶酶不同添加量糖蜜澄清后还原糖浓度变化趋势

表7 不同果胶酶添加量下糖蜜澄清后还原糖浓度
从表7和图7可看出,随果胶酶添加量增加,糖蜜澄清后还原糖不断升高,果胶酶用量为17 U/g时,还原糖浓度达到峰值32.90 g/100mL,比未加酶糖蜜还原糖浓度30.11 g/100mL提高了9.3%。因此糖蜜最佳澄清条件为:糖蜜稀释到 50°Bx, 加热到50℃,然后沉降40 min,果胶酶最佳添加量是17 U/g。
3 结论与讨论
本实验研究了添加果胶酶对糖蜜澄清效果的影响,首先对糖蜜进行稀释,添加过磷酸钙、硫酸铵和果胶酶,加热升温至不同温度后自然沉降,分析澄清糖蜜锤度,实验研究出最适合的澄清温度。然后将糖蜜稀释添加不同浓度果胶酶,每组糖蜜分别自然沉降不同时间,分析澄清糖液的锤度和总还原糖,研究最适澄清时间。最后根据实验数据,分析出果胶酶最佳添加量。最终实验得出的糖蜜最佳澄清条件为:糖蜜稀释到50°Bx,加热到50℃,果胶酶最佳添加量是17 U/g,自然沉降时间为40 min,澄清后糖蜜还原糖浓度为32.90 g/100mL,比未加果胶酶的糖蜜还原糖浓度提高了9.3%。因此糖蜜添加果胶酶澄清能够明显提高还原糖浓度,有利于糖蜜应用于食品发酵工业后提高产品得率。

