伴有皮质下梗死和白质脑病的常染色体隐性遗传性脑动脉病的临床特点(附1例报告)
段立晖,张克忠,孙婧
伴有皮质下梗死和白质脑病的常染体隐性遗传性脑动脉病(CARASIL)是一种罕见的常染色体单基因遗传性疾病,以脱发、反复缺血性卒中、认知障碍及腰痛为其特征性表现[1-2]。本病于1965年由日本学者Maeda初次报道,1995年由Fukutake教授正式命名[3]。其后各地相继报道了CARASIL患者五十多例,并且主要来自日本[1,4-5]。大多数患者在30岁前出现临床症状,如脱发、腰痛、脑白质病变等[6-7]。30岁后起病的患者可能出现其他的症状,如认知障碍、假性延髓性麻痹、步态障碍、锥体或锥体外系症状、缺血性卒中等,严重者表现为痴呆[7-8]。Hara等[1]首次发现CARASIL的致病基因是定位于10号染色体上的丝氨酸蛋白酶1(HTRA1)基因。本研究小组现报告1例经基因测序确诊的老年期起病的CARASIL的临床资料,并结合文献分析该病临床特征,以期提高对CARASIL的认识和诊断分析水平。
1 临床资料
1.1 病例 患者,女性,55岁,因“运动迟缓、腰腿疼痛伴双下肢乏力1年,记忆力减退2个月”于2021年3月入院。患者1年前无明显诱因下出现行动迟缓,自觉双下肢乏力,迈步困难,行走需有人搀扶,伴左侧膝关节疼痛及腰腿痛,活动后加重,休息后缓解。至我院骨科门诊查膝关节MRI示左膝关节滑车发育不良,左膝关节周围软组织稍肿胀,左膝关节腔少许积液。予口服“依托考昔片”后疼痛好转,但双下肢仍有乏力,不能独立行走。2个月前出现记忆力下降,表现为近事遗忘,外院查头颅CT示脑内多发腔隙性脑梗死灶,轻度脑萎缩,两侧脑室旁及额顶叶脱髓鞘改变可能,未予特殊处理。为求进一步诊治收入我科。患者平素体质一般,2年前曾诊断为“脑梗死”。否认高血压、糖尿病、冠心病史,无肝炎、结核或其他传染病等病史及其密切接触史,2014年在当地医院行子宫肌瘤切除术,无外伤史,无血制品输注史,无食物、药物过敏史,预防接种史不详。入院查体:体温36.3 ℃,脉搏86次/min,呼吸16次/min,血压169/94 mmHg (1 mmHg=0.133 kPa)。神志清楚,精神可,言语清,记忆力、计算力、理解力等正常。双耳听力、双眼视力无明显异常,双侧眼睑无下垂,眼球运动正常,未见明显眼震,双眼瞳孔等大等圆,直径约3 mm,对光反射存在。额纹对称,口角不歪,下颌居中,伸舌居中,双侧软腭上抬可,悬雍垂居中,双侧咽反射存在。四肢肌力、腱反射无明显异常,下肢肌张力增高。双手对指、握拳、轮替稍慢,双侧指鼻试验、跟-膝-胫试验不稳准,双侧深浅感觉正常,病理征(-)。入院初步诊断:(1)帕金森综合征;(2)脑梗死。患者外院CT示脑内多发腔隙性脑梗死灶,读片后考虑为脑小血管病变引起的“血管性帕金森综合征”可能性大,记忆力下降考虑与脑血管病变相关,完善头颅MRI及MRA评估脑实质及脑血管情况,结果示双侧颈内动脉颅底段稍粗细不均(粥样硬化可能)、脑内多发腔隙性梗死、脑白质疏松(图1)。完善风湿三项、免疫五项、血沉、抗核抗体、抗ENA抗体、抗中性粒细胞抗体、血小板聚集功能等检查,结果均未见明显异常,排除风湿免疫疾病或血小板功能障碍导致脑血管病变的可能。进一步完善双下肢血管超声,双侧下肢动脉血流未见明显异常,双侧下肢深静脉未见明显血栓。患者腰腿痛,完善腰椎正侧位X线片结果示L2-L3、L3-L4、L4-L5椎间隙变窄;L4椎体向前滑脱(Ⅰ°);腰椎退变(图2)。
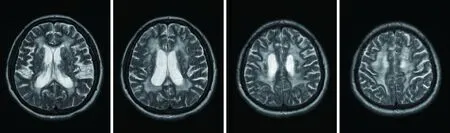
图1 头颅MRI检查(2021-03)示脑内多发腔隙性梗死、脑白质疏松
患者脑血管病变引起帕金森综合征诊断明确,考虑既往无高血压、糖尿病等病史,无吸烟等动脉粥样硬化危险因素。追问家族史,其哥哥有脑梗死史,行相关遗传学检查明确脑血管病变病因,该样本在HTRA1存在一处杂合变异c.754G>A(p.A252T),HGMDpro数据库报道为致病变异。家系验证示其女儿杂合携带该变异。据美国医学遗传学和基因组学学会指南,该变异可评级为疑似致病性变异(图3)。
根据Fukutake[4]及何志义[9]总结既往病例提出的诊断标准,患者出现下述症状时可诊断为CARASIL:(1)早期发病的白质脑病,有锥体和锥体外系症状,存在广泛脑白质病变;(2)青少年期出现脱发;(3)早年反复出现急性腰痛,或腰椎影像学检查显示脊柱退行性改变和椎间盘病变;(4)具有符合常染色体隐性遗传特点的家族史。若临床高度怀疑CARASIL,确诊需进一步行HTRA1基因检测。梳理患者既往检查结果发现其2018年(发病前2年)即出现脑白质损害(图4),至2021年脑白质损害明显加重,且出现多发皮质下梗死(图1)。2021年检查颈胸腰椎MRI均提示椎体退变(图5)。根据基因检查结果,结合脑白质早发病变、椎体退变病史,明确诊断为CARASIL。

图2 腰椎正侧位片 L2-L3、L3-L4、L4-L5椎间隙变窄;L4椎体向前滑脱(Ⅰ°);腰椎退变 图3 基因检查结果
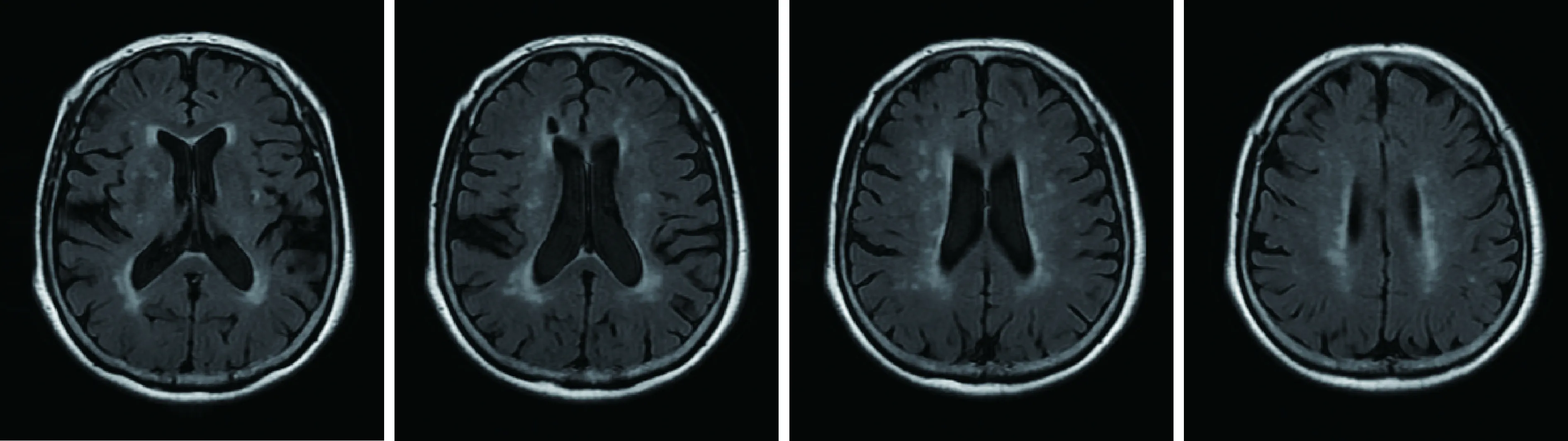
图4 2018年头颅MRI检查示脑白质损害
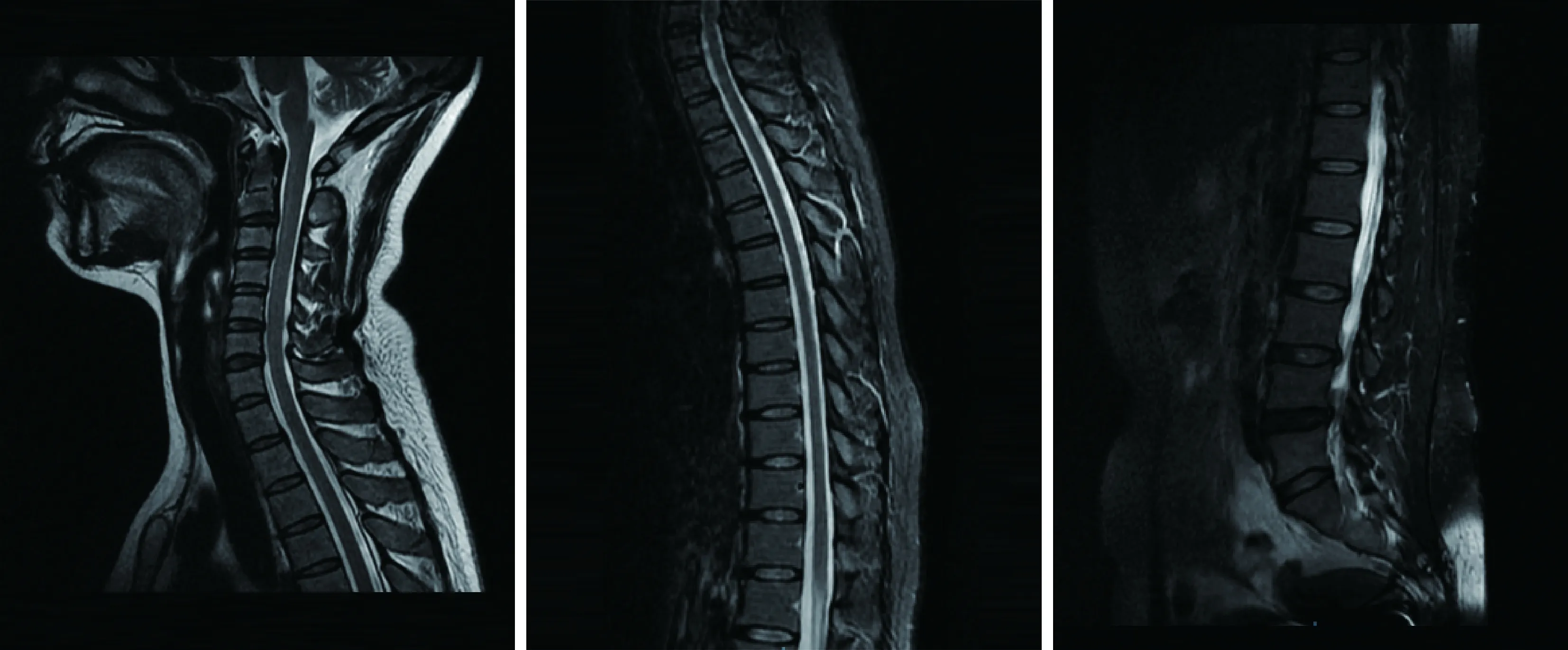
图5 颈胸腰椎MRI 椎体退变
考虑患者帕金森综合征是由脑血管病变所引起,记忆力下降亦与脑血管病变相关。治疗上调整抗帕金森药物剂量为美多芭剂量,3次/d以及金刚烷胺剂量,3次/d,加用阿司匹林抗血小板、瑞舒伐他汀调节血脂稳定斑块、丁苯酞软胶囊建立侧支循环、思尔明改善脑循环,同时加用艾地苯醌片、多奈哌齐片改善认知,并辅以经颅磁刺激治疗改善患者行动迟缓等症状。经综合性积极对因对症治疗,患者感行动迟缓、记忆力减退、腰腿疼痛、下肢乏力等症状均较前有所改善。
1.2 文献复习
1.2.1 检索策略 以“伴有皮质下梗死和白质脑病的常染体隐性遗传性脑动脉病”、“cerebral autosomal recessive arteriopathy with subcortical infarcts and leukoencephalopathy”为主题词,检索万方数据库、中国知网、PubMed上报道的CARASIL病例,检索时间至2022年4月,排除急性脑血管意外患者。
1.2.2 一般资料 见表1。共26篇文献30例加本例。男16例(51.61%),女15例(48.39%);年龄24~59岁,平均(39.03±10.37)岁;亚裔83.87%。

表1 经基因检测证实的CARASIL患者临床特征(包含本例)文献诊断年龄(岁)性别国家突变位点/氨基酸改变临床表现(发病年龄)脱发偏头痛腰痛脑白质损害步态障碍精神障碍认知障碍尿潴留Tikka等[10]54男日本c.904C>T(p.R302X)16-1628----Kawata等[11]46女日本c. 224 G>C(p.R75P)14-2931----Oide等[12]51女日本c.904C>T--3440----Hara等[1]44女日本c.1108C>T(p.R302X)18-21现患病50女日本c.889G>A(p.V297M)未知----33男日本c.889G>A(p.V297M)16-39未知31-50-Nshimoto等[5]44女日本c.821G>A(p.R274Q)14-33未知29-33-Mendioroz等[13]43男西班牙c.883G>A(p.Gly295Arg)--203944-44-Wang等[14]27女中国c.1091T>C(p.L364P)18--34343435-Chen等[15]26女中国c.854C >T(p.P285L)27-252726-26-Menezes等[16]45男葡萄牙c.496C>T(p.R166C)自出生开始进行性脱发-2326232424-Khaleeli等[17]35男巴基斯坦c.517G>A (p.A173T)青少年期-3345----Bayrakli等[18]29女土耳其c.1108C>T(p.R370X) 未知35-未知333535-Bianchi等[19]29女罗马尼亚c.961G>A (p.Ala321Thr)未知-272927---Cai等[20]28男中国c.161_162delAG (p.Gly56Alafs*160)--142924---Preethish-Kumar等[21]26男印度c.739delG (p.E247Rfs) 18-2828----24男印度c.830_831delAG (p.E277Vfs)自出生开始进行性脱发--23232323-33女印度c.502A>T (p.K168ter)--2121212121-Gündüz等[22]26男土耳其c.983C>A (p.Ser328* )自出生开始进行性脱发24243233---Cao等[23]59男中国c.497G>T(p.Arg166Leu)-20202630303030Wen等[24]43女中国c.508 A>C(p.N170H, chr10:124248453)---5759595958Tan等[25]44男高加索c.904C>T(p.Arg302Ter) 43--4242-42-Oluwole等[26]39男加蓬p.G283R20--4545近40岁近40岁-陈莉等[27]49男中国C.267C>A--323232323232朱飞奇等[28]58男中国c.404C>A (p.A135D)-444444-4444-Hou等[29]36男中国c.971A>G(p.N324S)---55555555-Bougea等[30]31男希腊c.496C>T23--36363636-刘楠等[31]33女中国c.854C>T(p.Pro285Leu)2129-31--31-李伟新等[32]36女中国c.589C>T30-303328-33-李务荣等[33]34女中国c.524T>A(p.Val175Glu)5-3236--36-本例55女中国c.754G>A(p.A252T)31未知29343434--
1.2.3 临床表现 见表1。本组中21例(67.74%)存在脱发,发病年龄为0~43岁,平均(18.76±11.49)岁;6例(19.35%)偏头痛,发病年龄20~44岁,平均(31.0±8.58)岁;22例(70.97%)反复腰痛,发病年龄为14~55岁,平均(28.59±9.36)岁;所有患者均出现白质损害,发现白质病变年龄为21~57岁,平均(36.1±9.46)岁;22例(70.97%)出现步态障碍,发病年龄为21~55岁,平均(34.68±10.82)岁;14例(45.16%)出现焦虑、抑郁等情绪障碍,发病年龄为21~59岁,平均(37.21±12)岁;21例(67.74%)有认知损害,发病年龄为21~59岁,平均(37.29±10.7)岁;3例(9.68%)出现尿潴留,发病年龄为30~58岁,平均(40.0±15.62)岁(注:自出生即出现症状按0岁计,青少年按16岁计,现患病但发病年龄不详按就诊时年龄计)。平均18岁开始脱发,31岁出现偏头痛,最早14岁出现腰痛,脑白质损害出现的平均年龄为36岁,步态障碍约于34岁出现,焦虑、抑郁等精神障碍于37岁出现,平均于37岁出现认知功能障碍,于40岁出现尿潴留症状。
1.2.4 基因突变分析 见表1。经基因检测确诊的CARASIL病例有31例,共发现26个HTRA1基因突变位点。
2 讨论
CARASIL属于遗传性脑小血管病[34],发病机制与HTRA1基因突变有关。HTRA1基因位于染色体10q上的2.4 Mb区[1],HTRA1具有至少1个C-末端PDZ结构域和高度保守的类胰蛋白酶样丝氨酸蛋白酶结构域。HTRA1是调节血管生成和血管内稳态的一种调节因子,在转化生长因子(TGF)-β信号通路中发挥重要的作用[35],而TGF-β1信号在CARASIL脑动脉病变中非常关键。HTRA1基因的3~6号外显子是酶活性的关键区,属于HTRA家族丝氨酸蛋白酶,具有分子伴侣和丝氨酸蛋白酶的双重活性。HTRA1通过在内质网中结合并切割TGF-β1的前体以减少成熟TGF-β1的数量。HTRA1基因除了导致隐性遗传性脑小血管病外[33],还可以导致显性遗传性脑小血管病[32,36-37]。CARASIL中的基因变异主要为HTRA1基因突变导致的HTRA1酶活性丧失,导致不能抑制TGF-β家族信号,从而使纤维连接蛋白EDA结构域和多功能蛋白聚糖在患者的脑小动脉内膜中累积、增厚,进而引起脑血管管腔狭窄、动脉硬化,最终导致缺血性脑小血管疾病。TGF-β也调控头发毛囊的发育和骨骼的形成,导致脊椎病和脱发[38]。
1995年Fukutake等[3]报道了17例青年期发病并伴有脱发和腰痛且无高血压病的动脉硬化性白质脑病患者,发现了本病呈常染色体隐性遗传,并将其命名为CARASIL。CARASIL的临床特点为青年期起病的卒中、痴呆、腰痛和脱发,不伴有脑血管病常见的危险因素,且家族中多有近亲结婚史,其中精神障碍和运动异常平均在三十岁左右发病,痴呆、步态障碍均在三十余岁发生,脱发、腰椎间盘病变、反复急性腰痛和关节退化多在青少年时期至二十岁左右发生[2-3,34,39-42]。既往报道的CARASIL病例均为日本人,故有学者将日本人作为其临床特点之一[41],但如今已排除该特点。
CARASIL的病理改变主要累及基底节小动脉和脑白质,类似于小动脉硬化,病理可见壁细胞外基质减少,中膜严重玻璃样变,内膜纤维化增厚,脑小动脉外膜明显变薄,平滑肌细胞大量脱失。脑白质区存在明显的髓鞘苍白,但保有皮质下U型纤维[42]。
CARASIL最具特征性的影像学表现为基底节区及丘脑的腔隙性梗死灶和脑白质高信号,早期表现为双侧弥漫性脑白质病变,主要分布于皮质下白质,随疾病的进展,病变逐渐累及基底神经节、丘脑、脑干和小脑[4]。头颅MRA检查及血管造影检查多无明显异常。头颅MRI异常征象可出现于患者有临床症状前[43]。CARASIL进展期可以累及脑桥小脑束,脑桥到小脑中脚的弧形白质高信号为该时期特征性的MRI表现[43],同时该时期可有全脑弥漫性脑萎缩及分布于大脑皮质、小脑和丘脑区的散在微出血灶[44]。患者于三十岁左右行脊椎MRI检查可见椎间盘退行性变及不同程度的椎管狭窄[43]。
本例患者以记忆力减退为首发症状,合并运动迟缓、腰腿疼痛及双下肢乏力等症状,头颅MRI发现多发性腔隙性脑梗死、脑白质疏松,因此该患者可以诊断为脑小血管病。患者无糖尿病、高血压、冠心病等病史,因此患者脑白质损害因高血压等脑血管病危险因素所致脑小血管病的可能性小,同时患者有相关家族史(患者哥哥有脑梗死病史),因此该患者应该首先考虑遗传性脑小血管病。患者脑白质损害逐渐加重,且为皮质下梗死,因此本研究小组初步排除脑淀粉样脑血管病。采用全外显子测序明确病因,排除其他遗传性脑小血管病非常必要。本例患者最后通过基因测序证实为HTRA1突变所致的CARASIL。
目前,还没有有效的或针对性的治疗和管理CARASIL的方法,临床上主要采用对症支持治疗。杨任民等[45]报道,CARASIL患者一般在出现神经症状后的10年内死亡,也有患者的生存期达20年以上。Favaretto等[46]研究发现,单一杂合子突变致病HTRA1基因仅局限于CNS疾病,其与典型的CARASIL不同,该型发病患者的多数脑卒中发作和认知损害出现较晚,且多无脱发和脊椎病等神经系统外症状。对于有家族史或临床疑似的患者,应行HTRA1基因突变检测以早期确诊。
随着基因功能分析与研究的发展,CARASIL将被更广泛的发现。重视基因诊断、从分子生物学角度诊断CARASIL可以减少临床误诊和漏诊率,提高临床确诊率,给CARASIL的治疗带来希望。

