渤海湾典型闸控入海河流水体N2O释放研究
李肖正,岳甫均,2*,周 滨,王欣楚,胡 健,陈赛男,李思亮,2
渤海湾典型闸控入海河流水体N2O释放研究
李肖正1,岳甫均1,2*,周 滨3,王欣楚1,胡 健4,陈赛男1,李思亮1,2
(1.天津大学地球系统科学学院,天津 300072;3. 天津市环渤海地球关键带科学与可持续发展重点实验室,天津 300072;2.天津市环境保护科学研究院,天津 300191;4.中国科学院生态与环境研究中心,北京 100085)
为探究弱水动力条件下,典型滨海地区水体N2O释放通量及其主控因素,于2019年7月和8月(夏季)和11月(冬季初期)对以大清河-独流减河-北大港湿地为代表的渤海湾弱水动力条件河流开展水样采集与分析工作.结果表明:N2O浓度变化范围为0.4~184.5nmol/L,N2O饱和度的变化范围为7.2%~2740%,其中近90%的样品处于过饱和状态,表明该研究区是潜在的N2O释放源.N2O水-气界面释放通量为-0.3~6.7μmol/(m2·h),夏季水体N2O的释放通量高于冬季.降雨前后N2O浓度出现明显波动,相同点位降雨前后N2O浓度的变化值为-15.2~63.9nmol/L,独流减河上游农业区N2O浓度的平均增加量(22.1nmol/L)显著高于下游(1.3nmol/L),降雨驱动了流域氮素的运移,促进了水体N2O释放.相关性分析表明,水体N2O的浓度受反应物浓度、水体盐度共同调控.通过计算得到该滨海地区弱水动力条件下河流N2O的排放因子为0.0073,表明气候变化委员会(IPCC)默认值0.0026可能低估了该地区间接N2O释放.
N2O;滨海地区;弱水动力河流;渤海湾;排放因子
氧化亚氮(N2O)作为全球氮循环中重要的活性氮分子,其百年增温潜势是CO2的265倍[1].N2O还会消耗平流层臭氧,造成臭氧层破坏,危害人体健康[2].因此,大气中N2O升高对气候的影响可能远比它的直接温室效应复杂,探究大气中N2O产生机制对气候的影响具有深远的意义.
自工业革命以来,人类对全球氮循环的干扰,显著增加了陆地和水生生态系统N2O的释放[3-4],水生生态系统作为N2O的重要来源,其释放通量约占全球N2O释放总量的25%~30%[1,5].为估算全球河流N2O的释放量,政府间气候变化专门委员会(IPCC)提供了地下水和排水渠(EF5-g)、河流(EF5-r)、河口区(EF5-e)等水生生态系统N2O释放系数.尽管IPCC对排放因子的默认值做了多次修改(现行的推荐值为
0.0026)[6],但由于环境条件的可变性,单个排放因子默认值往往忽视了时空的差异性,在对特定河流进行评估时往往存在一些不确定性[7].如Wang等[8]对北京城市河流的研究表明,河流N2O排放因子的平均值为0.001,低于IPCC默认值.Beaulieu等[2]在对美国受农村和城市共同影响的河流研究中发现EF5-r值为0.0075,为IPCC默认值的3倍.使用IPCC默认值来预测所有河流的N2O释放显然是不合适的,需要进行更多的研究来确定EF5-r.
滨海地区作为陆地和海洋生物地球化学循环的关键过渡地带,受海陆交互作用影响,形成了复杂变异的多种环境梯度.近年来由于闸坝的修建,导致原有河流连通性被改变,形成相对封闭的水体环境,呈现流速较缓的水文特征,改变了原有的水动力条件,势必对N2O的形成及转化过程产生影响[9-12].早期针对滨海地区N2O释放的研究主要集中在欧洲地区[13-14],且越来越多的证据表明,不同的滨海地区往往会存在较大的区域及环境差异,特别是N2O释放的主要控制因素往往也有所不同[15-16].随着人口的增加及工业化进程的加快,亚洲滨海地区在全球N2O的释放评估中扮演着越来越重要的角色,探究受闸坝影响的弱水动力条件下滨海地区河流及湿地N2O的产生对全球N2O的评估具有重要的意义[16].
以往有学者对不同人为干扰的河流及湿地开展了研究[5,17],发现水体N2O的产生受到水质的强烈影响,农村河流N2O的转化过程比较复杂,但针对河流中N2O产生的生物地球化学过程与季节之间的响应关系,及强降雨事件对河流氮素的运移及N2O释放强度影响的研究还不够充分.基于此,本研究选取了渤海湾典型闸坝控制型河流,大清河水系下游河段-独流减河-北大港湿地区域,于2019年进行了4次样品采集工作,并对水体营养盐浓度及N2O浓度开展分析,以探究不同季节N2O的时空分布及降雨对N2O释放的影响,厘清滨海地区N2O释放的主控因素,评估滨海弱水力条件下N2O的释放系数及N2O释放通量的水平,为科学评估滨海地区N2O源汇效应提供理论参考.
1 材料与方法
1.1 研究区概况
天津市位于华北平原北部,东临渤海,北靠燕山,由环线公路将天津市划分为市区和农村[5].作为世界上人口最多的沿海城市之一(近1500万人口),伴随着京津冀一体化建设,经济的发展及人口的增加极大地改变了河流水环境.独流减河位于天津市区南部,是滨海新区海河水系南部下游地区最大的河流,全长67km,是承接大清河泄洪的主要入海通道.天津市北大港湿地自然保护区位于渤海湾沿岸,湿地总面积约348.9km2,分为核心区,缓冲区和实验区,有湖泊、河流、海岸滩涂、沼泽4种湿地类型,是天津市面积最大的“湿地自然保护区”.研究区地处半湿润大陆性季风型气候区,夏季炎热多雨,冬季寒冷干燥,年平均气温为14.8℃,年平均降雨量为520~ 660mm.降水年际变化较大,年内分配不均,总降水量的75%发生在6, 7, 8月份.独流减河属于典型的“闸坝控制型”河流,径流量小,流速慢,近年来由于沿岸工农业的影响更是导致水体水质变差[18].
1.2 样品采集与分析
于2019年7月(分别在降雨量67mm事件前后进行样品采集)、8月(高水位期样品采样,主要在大清河,独流减河上游以及独流减河下游加密采集)、和11月(冬季)对以大清河-独流减河-北大港湿地为代表的河流-滨海湿地进行了共4次水样采集工作(图1).其中,K1~K5为北大港湿地样品,K6为团泊洼水库样品,R1~R11为独流减河样品,R12为大清河样品.利用分层采水器采集表层样品(0.5m),并将水样缓慢加入250mL血清瓶中.为避免气泡的产生,将水样持续溢流约瓶体积的1.5~2倍,并使瓶口形成凸液面,迅速加入0.5mL饱和HgCl2溶液以抑制微生物活动,然后用带聚四氟乙烯内衬的橡胶塞和铝盖压盖密封,样品低温避光保存,运回实验室后尽快完成测定[19].利用水质参数仪(德国wtw: Multi 3630 ),现场测量水温()、pH值、溶解氧(DO)、电导率(EC)和盐度(SAL)[20].使用营养盐连续流动分析仪(SAN++SA5000)测试硝酸盐氮(NO3--N)、亚硝酸盐氮(NO2--N)、铵氮(NH4+-N)、可溶性总氮(DTN).其中NO3--N的测定方法为镉柱还原法,检出限为0.01mg/L;NO2--N的测定方法为N-(1-萘基)-乙二胺光度法;NH4+-N的测定方法为次氯酸钠氧化法,检出限为0.02mg/L;溶解态总氮(DTN)经过硫酸钾紫外消解后利用镉柱还原法测定,检出限为0.02mg/L.可溶性有机氮(DON)采用计算公式DON=DTN-NO3--NO2-- NH4+得到[21].
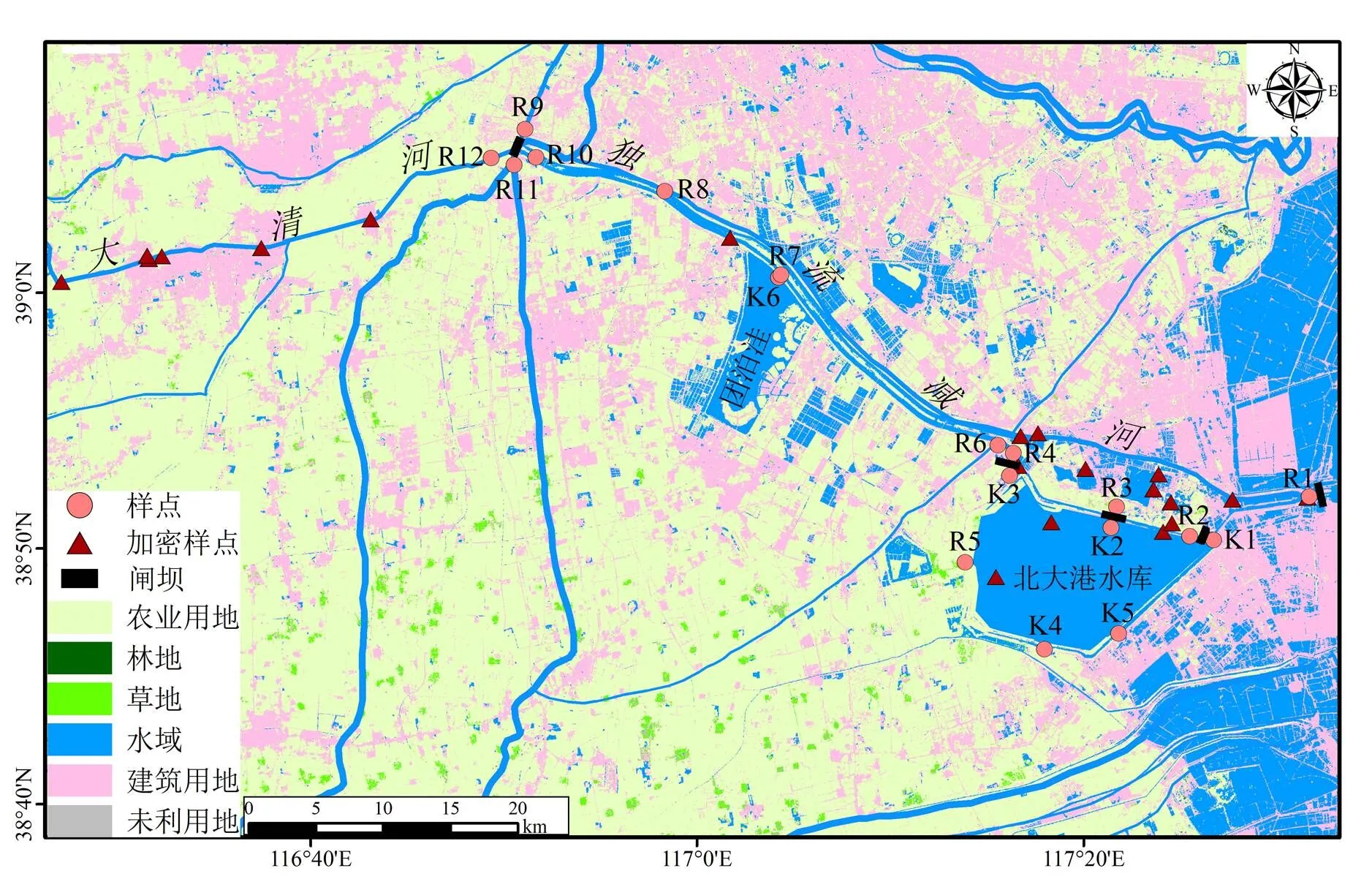
图1 研究区域采样点分布及其土地利用方式
其中样点在4次采样期间均采集了水样,加密样点仅在8月采集了水样,图中不同颜色代表不同土地利用类型.R1~R6 (包括K1~K5)之间点位为独流减河下游样品,K6~R11之间样品为独流减河上游样品,R12为大清河样品
水中溶解的N2O浓度采用顶空平衡法测定[22-23],具体步骤为:向装满水样的玻璃瓶中注入40mL高纯N2,同时置换出等体积水样.将置换完水样的玻璃瓶置于恒温振荡器中振荡40min,随后静置3h,使得玻璃瓶中气液两相达到平衡.抽取液面上方气体1mL,使用Agilent 7890B气相色谱仪测定N2O含量,根据测定样品的色谱峰面积计算出玻璃瓶顶空中N2O浓度.气相色谱仪配备电子捕获检测器(ECD检测器)和Pompak Q填充柱,进样口、柱温箱和检测器的温度分别为200, 70和300℃,以高纯He为载气,95% Ar+5% CH4(体积比)为尾吹气,柱流速和尾吹气流速分别为25和30mL/min.
1.3 水体N2O浓度、饱和度及释放通量的计算
利用Weiss等[24]提供的溶解度数据及公式,将气相中N2O浓度换算成水样中溶解的N2O浓度,具体计算方法如下所示:
N2O浓度计算
1=G·0/(·) (1)
式中:1为顶空中N2O的浓度, μmol/L;G为顶空中N2O的摩尔分压;0为标准大气压, 1.01325´105Pa;是理想气体常数, 8.314´103Pa·L/(mol·K);为热力学温度, K.
玻璃瓶液体中N2O的浓度可根据Weiss等[24]提供的气体溶解度公式计:
2=G·(2)
式中:2为平衡后玻璃瓶内水体中溶存N2O的浓度, μmol/L;G为顶空中N2O的摩尔分压.其中的计算公式如下:
ln=1+2(100/)+3ln(/100)+4(/100)2+
[1+2(/100)+3(/100)2] (3)
式中:是溶解系数;表示玻璃瓶内的热力学温度, K;是水体的盐度, ‰;和是关于计算的常数,具体如表1.

表1 关于D计算的不同参数值[24]
将顶空气体和玻璃瓶内水体溶存N2O的浓度根据下列公式换算为平衡前水样中温室气体的浓度:
w=(1·1+2·2)/2(4)
式中:w为水样中温室气体的实际浓度, μmol/L;1和2分别代表顶空气体体积和瓶中水样体积, mL.
N2O饱和度计算:
=w/eq´100% (5)
式中:为N2O的饱和度, %;w为水样中温室气体的实际浓度, μmol/L;eq为大气与自然水体处于水气平衡时水中N2O的理论浓度, μmol/L,可根据实际的水温、盐度和大气中温室气体的年均体积分数,利用Weiss等[24]提供的溶解度计算公式计算.
N2O释放通量计算[25-27]:
=(w-eq) (6)
=600(c/600)-2/3(7)
600=2.07+(0.215101.7) (8)
c=2141.2-152.56+5.89632-0.124113+
0.00106554(9)

式中:为水-气界面N2O的释放通量, μmol/(m2·h);为N2O在水体的扩散系数, cm/h;c为水中N2O气体的施密特系数;是水温,℃,通过现场测得,取值范围为-2~40℃.U为水体上方m处的风速,10是水面上方10m风速, m/s,采样期间风速在1.8~2.5m/s之间,夏季风速为2.2m/s,冬季风速为1.8m/s,数据由公式10转化.C10为10m时的阻力系数, 取0.0013,为Von Karman常数,取0.41.
河流N2O释放系数[28]:
EF5-r=[N2O-N]/[NO3--N](11)
式中: EF5-r是河流N2O的释放系数,[N2O-N]是河流溶存N2O的浓度, μg N/L;[NO3--N]是河流NO3-浓度, μg N/L.
1.4 数据分析方法
采用SPSS 22.0和Excel 2019进行数据统计分析,采用Origin8.0进行图形绘制,数据间的关系采用Spearman进行相关分析.
2 结果与分析
2.1 水质参数及氮素形态特征
表2概述了水样主要理化性质包括水温、DO、盐度、pH值以及不同形态氮素的平均值及变异系数(CV),、DO、盐度的季节变化差异明显.虽然冬季和夏季水温的差异性很大,但由各季节的变异系数发现,每次采样期间,水温在空间上的变化范围不大.在冬季和夏季降雨前测得最高和最低DO含量,分别为13.1和9.4mg/L,每次采样期间DO在空间上的变化较小.受雨季闸坝调蓄影响,河流水位显著降低,加速了海水入侵的趋势,河水在7月降雨前呈现较高盐度(9.4‰)特征,而降水后由于雨水的稀释作用,导致盐度降低(8.4‰).受集中降雨期影响,8月份盐度较7月份更低(5.6‰).冬季受闸坝关闭及河道蓄水双重影响,改变河水与海水间的水位差异性,盐度表现为最低2.5‰.结合变异系数以及图2a、2b发现,盐度具有明显的空间差异性,独流减河下游河水具有较高的盐度,而下游湿地由于闸坝的拦截,河流与湿地之间的连通性较差,湿地水样中盐度含量较低;独流减河上游以及大清河受渤海的影响较小,盐度平稳且含量较低.雨前、雨后、8月及冬季采样期间水体pH值分别为8.4, 8.6, 8.4, 8.7,变异系数为4%、3%、5%、3%,pH值时空差异不明显,且降雨对河水pH值影响不显著.
不同季节3种无机氮的含量差异显著, NH4+-N在冬季含量最高为0.21mg/L,而雨前、雨后及8月采样期间NH4+-N的含量均接近0.1mg/L.水体NO2--N含量在3种无机氮中占比最低,采样期间除8月高于0.05mg/L外,其余3次NO2--N含量均低于0.05mg/L.NO3--N是水体最主要的活性氮赋存形态,在冬季含量最高为0.48mg/L,其余3次采样期间NO3--N浓度在0.26mg/L左右,基本保持一致. NO3--N在空间上变化差异显著(表2,图2c,2d),降雨后大清河和独流减河上游部分点位NO3--N浓度出现显著增高,而独流减河下游在降雨后水体NO3--N含量出现了降低.水体中DON的含量高于可溶性无机氮(DIN),其中8月采样期间DON的含量最高.相比于DIN,DON在空间上变化较稳定,差异性不明显.4次采样期间,DTN波动范围较大,其中冬季采样期间含量最高为1.38mg/L,降雨前水体DTN含量最低为0.83mg/L.

表2 采样期间水体理化性质变化
注:右上角带a数据为平均值,下方百分数据为对应采样期间变异系数CV.

图2 盐度和NO3--N含量的沿程变化
DQR为大清河,UDLR为独流减河上游,DDLR为独流减河下游
2.2 N2O浓度及饱和度的时空变化
如图3所示, N2O的浓度具有明显的时空变异性,范围在0.4~184.5nmol/L之间,平均值为32.5nmol/L.夏季降雨前N2O的平均浓度为18.5nmol/L,降雨后N2O的平均浓度增到27.4nmol/L,相同点位降雨前后N2O的变化值为-15.2~ 63.9nmol/L.8月采样期间河流N2O的平均浓度为37.8nmol/L,冬季河水具有最高的N2O平均浓度(40.4nmol/L).空间分析发现,除冬季采样期大清河-独流减河上游-独流减河下游N2O平均浓度基本一致外,其余3次采样期间大清河和独流减河上游N2O的平均浓度均高于下游.
N2O的饱和度在7.2%~2740%之间,平均值为405.9%,其中90%的样品处于过饱和状态,河流将作为大气中N2O的源对大气N2O的浓度起到升高作用.降雨后水体N2O的饱和度明显升高(图3).与N2O浓度变化不同的是,虽然冬季N2O的平均浓度远高于夏季,但冬季N2O的平均饱和度(255.9%)却显著低于夏季(354.8%).对N2O饱和度进行空间分析发现,与其它点位相比,R8号点位N2O饱和度出现显著升高.
2.3 研究区水体N2O释放通量的变化
4次采样期间N2O释放通量(式6~10)在-0.3~6.7μmol/(m2·h)之间,均值为0.8μmol/(m2·h).无论在季节还是空间尺度上,N2O的释放通量都存在较大的差异(图3).冬季N2O的平均释放通量处于最低水平为0.35μmol/(m2·h),8月采样期间N2O的平均释放通量达到最高值为1.07μmol/(m2·h).与降雨前N2O的平均释放通量(0.48μmol/(m2·h))相比,降雨后N2O的平均释放通量的(0.84μmol/(m2·h))提高了1.8倍.对4次采样期间N2O的释放通量进行空间分析发现,大清河及独流减河上游N2O的平均释放通量为1.37, 1.22μmol/(m2·h),而独流减河下游N2O的平均释放通量为0.47μmol/(m2·h),上游N2O的平均释放通量远高于下游.

图3 水体N2O浓度(a)和(b)、饱和度及释放通量(c)和(d)的时空变化
模向虚线表示饱和度,N2Osat100%即N2O饱和度为100%
3 讨论
3.1 研究区河流N2O排放因子
通过对4次采样期间EF5-r进行计算(式11),得到夏季降雨前EF5-r平均值为0.0014,降雨后EF5-r的平均值为0.0038,8月采样期间EF5-r的平均值为0.014,冬季EF5-r的平均值为0.0035,这与之前对不同季节EF5-r的研究结果相一致[28-29],表明不同季节及极端降雨事件的发生均会显著影响对N2O释放的预测.研究区水体水动力条件较弱,水体中NO3--N浓度较低为0.31mg/L,导致4次采样期间EF5-r的平均值较高,为0.0073,高于IPCC规定的EF5-r值(0.0026).利用IPCC默认值可能会低估弱水动力条件下滨海地区河流N2O的释放.

表3 不同研究中c[N2O-N]:c[NO3--N]值的比较
结合先前的研究结果发现,不同研究区域EF5-r值往往是不同的(表3).例如Outram等[30]通过对受农业影响的瑟恩河上游研究发现,该区域河水中N2O的浓度约是本研究中N2O浓度的1.9倍.但该区域河水中NO3--N浓度是本研究区(0.31mg/L)的5倍,较高浓度的NO3--N导致瑟恩河上游EF5-r值(0.0011)小于IPCC默认值.此外,Wang等[31]对受城市污染的南淝河的研究表明,区域主要受NH4+-N (12.54mg/L)污染,河水中N2O的浓度约是本研究区4.5倍, NO3--N(0.51mg/L)的含量却与本研究区相似,两者间较大的差异倍数,导致该河流N2O的排放因子(0.0745)远高于IPCC规定的默认值.综上,不同河流EF5-r值可能会存在较大的差异,且与季节、水动力条件、氮污染类型、氮素浓度有关.使用一个排放因子评估的方法将导致评估结果的不确定性变大[28,32-33],需要综合考虑各因素对N2O释放的影响,加深对河流N2O释放机理的研究,降低全球N2O释放量预测的不确定性.
3.2 滨海河流弱水动力条件下的低N2O释放强度
对4次采样期间N2O释放通量分析发现,夏季N2O释放通量高于冬季.夏季采样期间水温较高,风速较大,N2O在水体的扩散系数(=3.9)高于冬季(=1.4),从而更有利于N2O的释放.降雨后N2O释放通量增加了1.8倍,其中上游水体N2O释放通量的变化值是下游水体变化值的11倍.强降雨与大量施用农业氮肥的结合,增加了水体中N2O的含量,进而显著增强了河流N2O的释放能力.降雨后为河流N2O释放的关键时刻,需深入开展更多N2O释放机制的研究,以降低滨海地区N2O收支的不确定性.
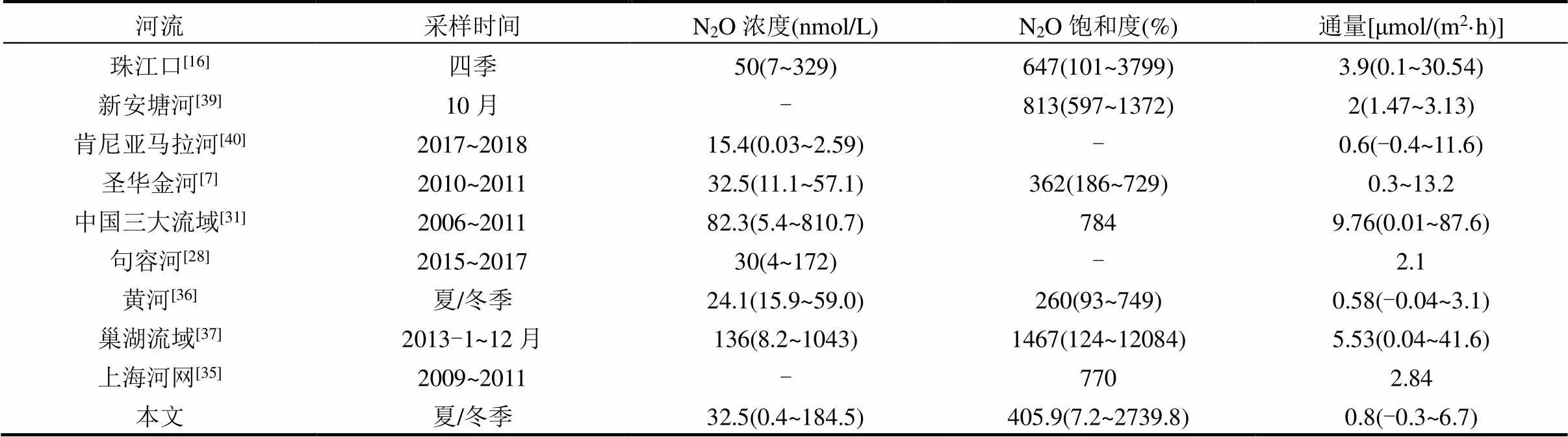
表4 不同河流水体N2O释放强度的比较
注:括号外数据代表平均值、括号内数据表示范围(只有平均值无范围则不加括号); -表示无相关数据.
将河流N2O的释放情况与之前的研究相比较,结果如表4所示:不同区域类型河流N2O释放通量的范围为-0.4~87.6μmol/(m2·h).与其它河流相比,该研究区域N2O的释放略高于一些低营养化的河流,如黄河下游[36],而低于一些污染较为严重的城市河流,如珠江口、巢湖流域等[16,37].N2O的释放受到水体流速、风速及N2O饱和度等的影响[28,36].Xiao等[28]通过对河流、池塘以及水库的研究指出:对于慢生态系统(池塘、水库),由于水体流动的速度较慢,N2O的释放主要受风力作用的影响.与N2O浓度相近的句容河相比,本研究中的滨海地区由于受到闸坝拦截的影响,水体水动力条件较弱,N2O释放受到水流影响较小,N2O的释放通量远低于句容河[28].总体来说,尽管该区域是大气中N2O的源,但由于该研究区河流N2O的饱和度较低,水动力条件较弱,与大气气体交换能力不强[38],N2O的释放仍处于一个较低水平.
3.3 典型滨海地区河流N2O影响因素及产生机制
已有研究表明河流中N2O的产生受到多种因素的影响,如氮负荷、盐度、降雨、温度、pH值、DO及水力滞留时间等,多个环境变量可以一起预测河流N2O浓度,但当单独考虑时,它们中没有一个能作为N2O的最佳预测因子[41-42].为判断影响河流N2O产生的主导因素,将各变量与河流中N2O浓度进行相关性分析,结果如图4、5所示.无论考虑季节变化还是河流类型,NO3--N与N2O浓度(=0.53,<0.01)之间均呈现显著正相关.如具有较高NO3--N浓度的R8,表现出了较强N2O浓度,河流N2O浓度可以通过NO3--N的动态水平来预测(图4和图5).而由于河流中NH4+-N的浓度较低,与N2O浓度之间的相关性不明显(=0.10).结合现有研究结果,N2O可以在水体及沉积物中通过硝化和反硝化作用产生[43],DIN作为硝化作用及反硝化作用的底物,其浓度的高低对水体N2O的产生具有重要的影响[11,28].分析水体氮含量、DO、水动力条件以及各变量之间的相关性关系,可以对水体中N2O的主要产生途径进行解析:由DON和DO浓度可知,较高浓度的DON在有氧水体中会进行持续的矿化作用产生NH4+-N[10,44],产生的NH4+-N又会在有氧条件进行持续的硝化作用[11-12,45],使河水中NH4+-N减少, NO3--N和N2O浓度增加,再结合NO3--N与N2O浓度之间的相关性关系,可以看出硝化作用在水体N2O产生中占据重要地位.但值得注意的是,由于闸坝的建立,导致独流减河径流量变小,流速减慢[18],形成弱水动力条件.这种弱水动力条件,将导致DIN在水体中的滞留时间延长,表层水体中的DIN更容易向深层转移,在水-沉积物界面由于存在富氧和缺氧区域的不断变化[45],有利于耦合硝化-反硝化作用的发生[7,46],产生更多的N2O.因此,弱水动力条件下水-沉积物界面存在的耦合硝化-反硝化作用应当引起关注.

盐度梯度作为滨海地区水体特有特征,在影响N2O产生中起着重要作用.对研究区水体N2O浓度分析发现:上游低盐度区域N2O浓度较高,而下游高盐度区域N2O浓度较低,相关性分析结果表明水体N2O的浓度与盐度之间呈现显著负相关(=-0.44,<0.01),这与之前的研究相一致[16,47].盐度作为影响硝化和反硝化作用的因素之一,当盐度升高时会抑制河流中相关微生物的活性[16],导致N2O的产生速率降低,从而使河流中N2O的浓度下降[48].降雨作为影响河流氮含量及水动力条件的重要因素,对水体N2O浓度的影响是不容忽视的.如图3所示,降雨后大清河-独流减河上游河水中N2O的浓度出现显著增高,这与先前的研究相一致[28,42].结合土地利用类型发现(图1),该区域农业土壤分布较广,雨水会冲刷农业区土壤NO3--N进入河流,造成河流NO3--N含量的升高[42,49-50],高浓度的NO3--N会刺激反硝化作用及相关N2O的产生[40,42].降雨的发生也会导致地下水位改变,高水位使土壤和地下水等其它来源的N2O直接输入到河流导致水体中N2O浓度的升高[2,51],8月较7月水体测得更高N2O浓度可能受到降雨的强烈影响(7月降雨后到8月采样前累计降雨量为299.5mm).降雨可以通过促进水体扰动,增强水动力条件,从而促进河流N2O的排放[28].与独流减河上游(平均增加22.1nmol/L)相比,由于雨水的稀释作用,独流减河下游水体中N2O浓度(平均增加1.3nmol/L)的增加量较小,R4、R6点位在降雨后还出现了N2O浓度降低的情况.结合水体DIN含量分析发现,在降雨后R4、R6点位NO3--N含量出现了显著的降低,NO3--N含量的变化可能是引起水体N2O浓度减小的原因[31].由此看出,降雨事件驱动了流域氮素的运移,为N2O的产生提供反应物,导致水体N2O浓度的升高.
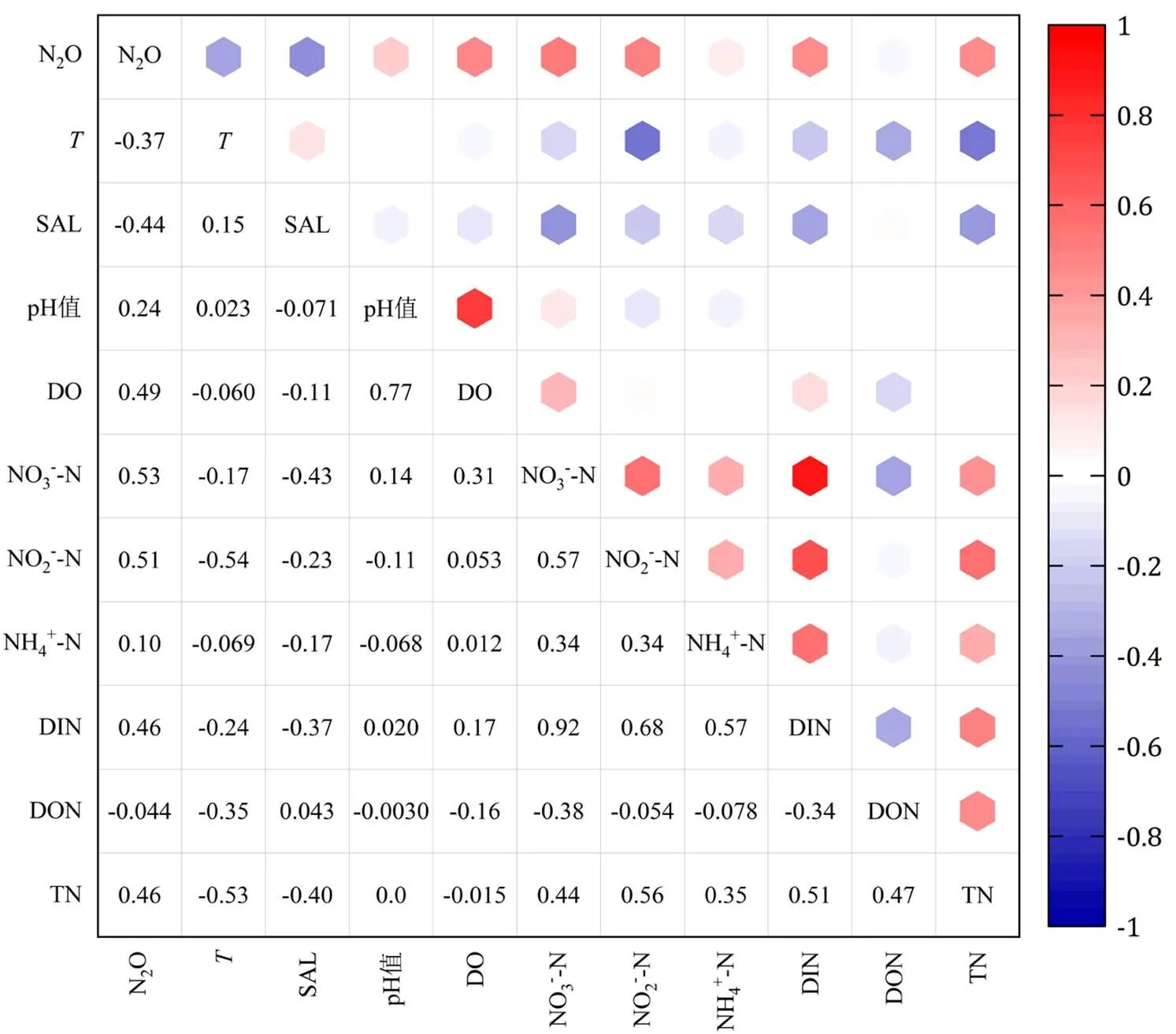
图5 各变量之间相关性分析
为消除底物浓度的影响,将与[N2O-N: NO3--N]进行相关性分析,结果表明与[N2O-N: NO3--N]之间呈较弱的负相关(=-0.09),这与之前的研究有所不同[52].一般认为温度对水体N2O浓度的影响是双向的,温度升高会增强微生物的活性,使水体N2O的产生量增加[53].但随着温度的升高,N2O在水体中的饱和溶解度会随之降低,有利于水体N2O向大气中释放,从而导致河流N2O浓度的降低[54].4次采样期间水温在空间上的差异性较小,但N2O浓度在空间上的差异性较大(表2),因此水温可能不是该研究区驱动水体N2O浓度变化的主要原因,N2O浓度的季节性变化可能受其它因素的影响[49].研究区冬季水体中测得DIN的含量高于夏季,进而为N2O的产生提供充足的反应物,从而促进了N2O产生和低温条件下的溶解[11,28],高DIN含量可能是促使河流N2O产生的更重要原因[28,31].N2O的浓度与DO含量之间呈显著正相关(=0.49,<0.11),进一步说明了硝化作用在水体N2O的产生过程中起着重要作用[5,11].由DO与pH值之间的相关性发现,DO和pH值之间呈现显著的正相关,这可能是由于DO和pH值都会随着藻类光合作用的进行而逐渐增加[55].河流中N2O的产生受多因素的影响,总体来说该滨海地区N2O的产生主要与河流NO3--N和盐度的含量息息相关,河流中N2O的生成受硝化作用的影响强烈.
4 结论
4.1 本研究以我国北方典型受闸坝控制河流-湿地水生生态系统为研究对象,通过对水化学参数及氮素浓度分析发现,该区域水体溶存N2O浓度处于过饱和状态,表现为大气的源,N2O浓度呈现明显空间和季节性差异,上游水体中N2O的平均浓度是下游水体的1.9倍.
4.2 对N2O产生机制及影响因素分析发现,该区域河流N2O的产生受到反应物浓度、水体盐度的共同调控,硝化作用在水体N2O产生中占据重要作用.夏季受强降雨的影响,驱动氮素向水生生态系统的运移,河流N2O的浓度较高,诱发N2O的快速释放,是研究区N2O释放的热点时刻.
4.3 通过计算得到EF5-r的平均值为0.0073,高于IPCC默认的N2O排放因子,使用IPCC默认值会低估该类型滨海河流水体N2O释放.
[1] IPCC. Climate change 2014: synthesis report. contribution of working groups I, II and III to the fifth assessment report of the intergovernmental panel on climate change [M]. Cambridge: Cambridge University Press, 2014:86-87.
[2] Beaulieu J J, Tank J L, Hamilton S K, et al. Nitrous oxide emission from denitrification in stream and river networks [J]. Proceedings of the National Academy of Sciences of the United States of America, 2011,108(1):214-219.
[3] Garnier J, Cébron A, Tallec G, et al. Nitrogen behavior and nitrous oxide emission in the Tidal Seine River Estuary (France) as influenced by human activities in the upstream watershed [J]. Biogeochemistry, 2006,77(3):305-326.
[4] Ivens W P, Tysmans D J, Kroeze C, et al. Modeling global N2O emissions from aquatic systems [J]. Current Opinion in Environmental Sustainability, 2011,3(5):350-358.
[5] Liu X L, Bai L, Wang Z L, et al. Nitrous oxide emissions from river network with variable nitrogen loading in Tianjin, China [J]. Journal of Geochemical Exploration, 2015,157:153-161.
[6] IPCC. 2019 Refinement to the 2006 IPCC Guidelines for National Greenhouse Gas Inventories. Volume 4: Agriculture, Forestry and Other Land Use. Chapter 11: N2O Emissions from Managed Soils, and CO2Emissions from Lime and Urea Application [M]. IPCC, Switzerland, 2019:35-37.
[7] Hinshaw S E, Dahlgren R A. Dissolved nitrous oxide concentrations and fluxes from the eutrophic San Joaquin River, California [J]. Environmental Science & Technology, 2013,47(3):1313-1322.
[8] Wang G Q, Xia X H, Liu S D, et al. Distinctive patterns and controls of nitrous oxide concentrations and fluxes from urban inland waters [J]. Environmental Science & Technology, 2021,55(12):8422-8431.
[9] Crump B C, Hopkinson C S, Sogin M L, et al. Microbial biogeography along an estuarine salinity gradient: combined influences of bacterial growth and residence time [J]. Applied and Environmental Microbiology, 2004,70(3):1494-1505.
[10] Beaulieu J J, Nietch C T, Young J L. Controls on nitrous oxide production and consumption in reservoirs of the Ohio River Basin [J]. Journal of Geophysical Research: Biogeosciences, 2015,120(10): 1995-2010.
[11] Liang X, Xing T, Li J X, et al. Control of the hydraulic load on nitrous oxide emissions from cascade reservoirs [J]. Environmental Science and Technology, 2019,53(20):11745-11754.
[12] Maavara T, Lauerwald R, Laruelle G G, et al. Nitrous oxide emissions from inland waters: Are IPCC estimates too high? [J]. Global Change Biology, 2019,25(2):473-488.
[13] Bange H W, Rapsomanikis S, Andreae M O. Nitrous oxide in coastal waters [J]. Global Biogeochemical Cycles, 1996,10(1):197-207.
[14] Barnes J, Upstill-Goddard R C. N2O seasonal distributions and air-sea exchange in UK estuaries: Implications for the tropospheric N2O source from European coastal waters [J]. Journal of Geophysical Research:Biogeosciences, 2011,116:G01006.
[15] Harley J F, Carvalho L, Dudley B, et al. Spatial and seasonal fluxes of the greenhouse gases N2O, CO2and CH4in a UK macrotidal estuary [J]. Estuarine Coastal and Shelf Science, 2015,153:62-73.
[16] Lin H, Dai M H, Kao S J, et al. Spatiotemporal variability of nitrous oxide in a large eutrophic estuarine system: The Pearl River Estuary, China [J]. Marine Chemistry, 2016,182:14-24.
[17] 胡蓓蓓,谭永洁,王东启,等.冬季平原河网水体溶存甲烷和氧化亚氮浓度特征及排放通量[J]. 中国科学:化学, 2013,43(7):919-929.
Hu B B, Tan Y J, Wang D Q, et al. Methane and nitrous oxide dissolved concentration and emission flux of plain river network in winter [J]. Science China: Chemistry, 2013,43(7):919-929.
[18] Han Z L, Xiao M, Yue F J, et al. Seasonal variations of dissolved organic matter by fluorescent analysis in a typical river catchment in Northern China [J]. Water, 2021,13(4):494-513.
[19] 程 芳,丁 帅,刘素美,等.三峡库区及其下游溶解氧化亚氮(N2O)分布和释放[J]. 环境科学, 2019,40(9):4230-4237.
Cheng F, Ding S, Liu S M, et al. Distribution and emission of nitrous oxide (N2O) in Three Gorges Reservoir and downstream river [J]. Environmental Science, 2019,40(9):4230-4237.
[20] Yan W J, Yang L B, Fang W, et al. Riverine N2O concentrations, exports to estuary and emissions to atmosphere from the Changjiang River in response to increasing nitrogen loads [J]. Global Biogeochemical Cycles, 2012,26:GB4006.
[21] 田琳琳,王 正,胡 磊,等.长江上游典型农业源溪流溶存氧化亚氮(N2O)浓度特征及影响因素[J]. 环境科学, 2019,40(4):421-431.
Tian L L, Wang Z, Hu L, et al. Characteristics of the dissolved nitrous oxide(N2O) concentrations and influencing factors in a representative agricultural headwater stream in the upper reach of the Yangtze River [J]. Environmental Science, 2019,40(4):421-431.
[22] Manjrekar S, Uskaikar H, Morajkar S. Seasonal production of nitrous oxide in a tropical estuary, off western India [J]. Regional Studies in Marine Science, 2020,39:101418.
[23] Wang R, Zhang H, Zhang W, et al. An urban polluted river as a significant hotspot for water–atmosphere exchange of CH4and N2O [J]. Environmental Pollution, 2020,264:114770.
[24] Weiss R F, Price B A. Nitrous oxide solubility in water and seawater [J]. Marine Chemistry, 1980,8(4):347-359.
[25] Wanninkhof R. Relationship between wind speed and gas exchange over the ocean revisited [J]. Limnology and Oceanography: Methods, 2014,12(6):351-362.
[26] Cole J J, Caraco N F. Atmospheric exchange of carbon dioxide in a low-wind oligotrophic lake measured by the addition of SF6 [J]. Limnology and Oceanography, 1998,43(4):647-656.
[27] 唐 晨,杨 平,展鹏飞,等.河口区养殖塘水-气界面N2O扩散通量比较 [J]. 中国环境科学, 2021,41(3):1074-1085.
Tang C, Yang P, Zhan P F, et al. Comparison of floating chamber and diffusion model methods in determining diffusive N2O fluxes across water-atmosphere interface in estuary aquaculture ponds [J]. China Environmental Science, 2021,41(3):1074-1085.
[28] Xiao Q T, Hu Z H, Fu C S, et al. Surface nitrous oxide concentrations and fluxes from water bodies of the agricultural watershed in Eastern China [J]. Environmental Pollution, 2019,251:185-192.
[29] Hiscock K M, Cooper R J, Hama-Aziz Q. Indirect nitrous oxide emission factors for agricultural field drains and headwater streams [J]. Environmental Science & Technology,2017,51(1):301-307.
[30] Outram F N, Hiscock K M. Indirect nitrous oxide emissions from surface water bodies in a lowland arable catchment: a significant contribution to agricultural greenhouse gas budgets?[J]. Environmental Science & Technology, 2012,46(15):8156-8163.
[31] Wang J N, Chen N W, Yan W J, et al. Effect of dissolved oxygen and nitrogen on emission of N2O from rivers in China [J]. Atmospheric Environment, 2015,103:347-356.
[32] Tian L L, Zhu B, Akiyama H. Seasonal variations in indirect N2O emissions from an agricultural headwater ditch [J]. Biology and Fertility of Soils, 2017,53(6):651-662.
[33] Beaulieu J J, Arango C P, Hamilton S K, et al. The production and emission of nitrous oxide from headwater streams in the Midwestern United States [J]. 2008,14(4):878-894.
[34] Liu X L, Li S L, Wang Z L, et al. Nitrous oxide (N2O) emissions from a mesotrophic reservoir on the Wujiang River, southwest China [J]. Acta Geochimica, 2017,36(4):1-13.
[35] Yu Z J, Deng H G, Wang D Q, et al. Nitrous oxide emissions in the Shanghai river network: implications for the effects of urban sewage and IPCC methodology [J]. Global Change Biology, 2013,19(10): 2999-3010.
[36] Cheng F, Zhang H M, Zhang G L, et al. Distribution and emission of N2O in the largest river-reservoir system along the Yellow River [J]. Science of the Total Environment, 2019,666:1209-1219.
[37] Yang L B, Lei K. Effects of land use on the concentration and emission of nitrous oxide in nitrogen-enriched rivers [J]. Environmental Pollution, 2018,238:379-388.
[38] 谭永洁,王东启,周立旻,等.河流氧化亚氮产生和排放研究综述[J]. 地球与环境, 2015,43(1):123-132.
Tan Y J, Wang D Q, Zhou L M, et al. Review on the production and emission of nitrous oxide from rivers [J]. Earth and Environment, 2015,43(1):123-132.
[39] Xia Y Q, Li Y F, Li X B, et al. Diurnal pattern in nitrous oxide emissions from a sewage-enriched river [J]. Chemosphere, 2013,92(4):421-428.
[40] Mwanake R M, Gettel G M, Aho K S, et al. Land use, not stream order, controls N2O concentration and flux in the upper Mara River basin, Kenya [J]. Journal of Geophysical Research: Biogeosciences, 2019,124(11):3491-3506.
[41] Harrison J, Matson P. Patterns and controls of nitrous oxide emissions from waters draining a subtropical agricultural valley [J]. Global Biogeochemical Cycles, 2003,17:1080.
[42] Zhao Y Q, Yong Q, Xia B L, et al. Influence of environmental factors on net N2and N2O production in sediment of freshwater rivers [J]. Environmental Science & Pollution Research, 2014,21(16):9973-9982.
[43] Kuypers M, Marchant H K, Kartal B. The microbial nitrogen-cycling network [J]. Nature Reviews Microbiology, 2018,16(5):263-276.
[44] 赵彦龙,李心清,丁文慈,等.水中有机质矿化作用的生物地球化学室内模拟研究[J]. 地球与环境, 2007,35(3):233-238.
Zhao Y L, Li X Q, Ding W C, et al. Laboratory biogeochemical study on mineralization of organic matter in water [J]. Earth and Environment, 2007,35(3):233-238.
[45] 夏星辉,杨 腾,杨 萌,等.中国江河氧化亚氮的排放及其影响因素[J]. 环境科学学报, 2020,40(8):2679-2689.
Xia X H, Yang T, Yang M, et al. A review of nitrous oxide efflux and associated controls in China’s streams and rivers [J]. Acta Scientiae Circumstantiae, 2020,40(8):2679-2689.
[46] Xia X H, Jia Z M, Liu T, et al. Coupled nitrification-denitrification caused by suspended sediment (sps) in rivers: importance of sps size and composition [J]. Environmental Science & Technology, 2016, 51(1):212-221.
[47] Mueller D, Bange H W, Warneke T, et al. Nitrous oxide and methane in two tropical estuaries in a peat-dominated region of northwestern Borneo [J]. Biogeosciences, 2016,13(8):2415-2428.
[48] Jia J, Bai J H, Wang W, et al. Salt stress alters the short-term responses of nitrous oxide emissions to the nitrogen addition in salt-affected coastal soils [J]. Science of the Total Environment, 2020,742:140124.
[49] Yang L B, Yan W J, Ma P, et al. Seasonal and diurnal variations in N2O concentrations and fluxes from three eutrophic rivers in Southeast China [J]. Journal of Geographical Sciences, 2011,21(5):820-832.
[50] 夏妍梦,李 彩,李思亮,等.天津海河氮动态变化对夏季强降雨的响应过程[J]. 生态学杂志, 2018,37(3):743-750.
Xia Y M, Li C, Li S L, et al. Response of nitrogen dynamic change to heavy rainfall events during summer in Haihe River of Tianjin City [J]. Chinese Journal of Ecology, 2018,37(3):743-750.
[51] Garnier J, Billen G, Vilain G, et al. Nitrous oxide (N2O) in the Seine river and basin: Observations and budgets [J]. Agriculture Ecosystems & Environment, 2009,133(3):223-233.
[52] Beaulieu J J, Shuster W D, Rebholz J A. Nitrous oxide emissions from a large, impounded river: the ohio river [J]. Environmental Science & Technology, 2010,44(19):7527-7533.
[53] Harold F, Hemond A P, Du R. Fluxes of N2O at the sediment-water and water-atmosphere boundaries of a nitrogen-rich river [J]. Water Resources Research, 1989,25(5):839-846.
[54] 韩 洋,郑有飞,吴荣军,等.南京典型水体春季温室气体排放特征研究[J]. 中国环境科学, 2013,33(8):1360-1371.
Han Y, Zheng Y F, Wu R J, et al. Greenhouse gases emission characteristics of Nanjing typical waters in Spring [J]. China Environmental Science, 2013,33(8):1360-1371.
[55] Mishima I, Masuda S, Kakimoto T, et al. Assessment of nitrous oxide production in eutrophicated rivers with inflow of treated wastewater based on investigation and statistical analysis [J]. Environmental Monitoring and Assessment, 2021,193(2):1-13.
N2O release from the water bodies of typical gate controlling tributaries of Bohai Bay.
LI Xiao-zheng1, YUE Fu-jun1,2*, ZHOU Bin3, WANG Xin-chu1, HU Jian4, CHEN Sai-nan1, LI Si-liang1,2
(1.School of Earth System Science, Tianjin University, Tianjin 300072, China;3.Tianjin Key Laboratory of Earth’s Critical Zone Science and Sustainable Development in Bohai Rim, Tianjin 300072, China;2.Tianjin Academy of Environmental Protection Sciences, Tianjin 300191, China;4.Research Center for Ecology and Environmental Sciences, Chinese Academy of Sciences, Beijing 100085, China)., 2022,42(1):356~366
To explore the spatiotemporal variation in N2O in typical coastal zone and its main controlling factors under weak hydrodynamic conditions, water samples were collected from coastal rivers and wetlands (Daqing River-Duliujian River-Beidagang wetland) in July and August (Summer) and November (the beginning of Winter) in 2019. The results show that the concentration of N2O varied between 0.4~184.5nmol/L. The saturation of N2O ranged from 7.2%~2740%, and 90% of the samples were oversaturated, indicating that the study area was a potential source of N2O. The N2O release flux at the water-gas interface ranged from -0.3~6.7μmol/(m2·h), while the N2O exchange flux in summer was higher than that in winter. The study also found that the N2O concentration fluctuated significantly before and after rainfall, and the variation in N2O ranged from -15.2~63.9nmol/L at same sites before and after rainfall. The average increase in N2O concentration was significantly higher in the upper reaches (22.1nmol/L) than in the downstream (1.3nmol/L), indicating that rainfall drove the transportation of nitrogen species and accelerated N2O release. The salinity and NO3--N concentration had significant effect on N2O concentration. The N2O emission factor of the tributaties under the weak hydrodynamic conditions in coastal zone was estimated to be 0.0073, higher than the default value of 0.0026 defined by IPCC. Therefore, the N2O budget in the coastal zone may underestimate the indirect N2O emissions by using the IPCC threshold value.
N2O;coastal zone;weak hydrodynamic river;Bohai Bay;emission factor
X16
A
1000-6923(2022)01-0356-11
李肖正(1997-),男,山东聊城人,天津大学硕士研究生,主要研究方向为流域水环境质量监测与评估.
2021-05-28
国家自然科学基金资助项目(42073076,41925002);国家重点研发计划(2019YFC1805805);天津市科技计划项目(18ZXSZSF00130);天津大学创新基金(2021XYF-0037)
* 责任作者, 副教授, fujun_yue@tju.edu.cn

