铁磁性纳米材料的制备及对17b-雌二醇的选择性富集——基于分子印迹技术
管安浙,赵旭东,张婷婷,李 易,李建生,陆 锐
铁磁性纳米材料的制备及对17b-雌二醇的选择性富集——基于分子印迹技术
管安浙,赵旭东,张婷婷,李 易,李建生,陆 锐*
(南京理工大学环境与生物工程学院,江苏 南京 210094)
将铁磁性分离与分子印迹技术结合,以四氧化三铁纳米颗粒为核,以17β-雌二醇(E2)为模板分子,3-氨基丙基三乙氧基硅烷(APTES)为功能单体, 利用表面聚合法制备了E2分子印迹纳米材料(MIPs)和不含E2的非印迹纳米材料(NIPs).通过傅里叶变换红外光谱(FT-IR)、X射线衍射(XRD)、X射线光电子能谱(XPS)和扫描电镜(SEM)等方法对MIPs和NIPs进行分析和表征,显示MIPs形状规则呈球状粒径统一在790nm左右.选择吸附实验中,MIPs和NIPs对E2的饱和吸附量分别为9.69,6.25mg/g,说明材料具有较好的选择性.对静态吸附数据进行Freundlich线性拟合,结果证明MIPs具有良好的吸附能力.同时,MIPs表现出优秀的可重复利用性,7次吸附-解吸后吸附损失量仅为3%.
分子印迹;磁性纳米材料;表面聚合;17β-雌二醇
17β-雌二醇(E2)是一种天然的雌激素,广泛应用于畜牧业,起到促进动物生长,增强脂肪沉积,增加原料奶产量的作用[1].E2可以通过食物链在人体内富集[2-4].小剂量E2可治疗功能性子宫出血等疾病,缓解骨质疏松症.然而,过量摄入E2会扰乱内分泌系统,导致子宫内膜异位症、卵巢癌、睾丸癌和前列腺癌等疾病[5-6].因此对E2环境残留量检测分析意义重大,但环境样品中E2通常以低浓度存在,且存在干扰组分,检测需要对E2进行分离富集.
分子印迹技术是指制备出能对目标分子进行选择性识别的聚合物的技术,其制备原理是模板分子与功能单体先进行预聚合[7-8],再在交联剂[9]、引发剂的作用下,形成含有模板分子的高分子聚合物[10],最后破坏预聚合物间的作用力将印迹分子洗去[11],得到分子印迹聚合物(MIP).这种人工合成材料的识别性能与酶、抗体等天然物质相似[12],同时还具有协同识别能力、稳定性和制备成本低等优势[13],被广泛应用于手性分离、固相萃取、模拟酶、化学传感器等领域[14-16].然而,传统的MIP具有识别点位分布不均和非特异性识别等缺点.随着对分子印迹技术的研究的深入,表面印迹技术的出现则有效改善了这些问题.表面印迹法,即在固相基质表面进行印迹聚合反应.本文选择纳米材料作为固相基质,是因为纳米颗粒尺寸小,比表面积高[17],可以加快结合模板分子的动力学[18],有效提高印迹分子的洗脱-吸附速率.本文将分子印迹技术与磁性纳米材料结合,以Fe3O4@SiO2纳米粒子为核,1,2-二(三乙氧基硅基)乙烷(BTESE)为交联剂、3-氨基丙基三乙氧基硅烷(APTES)为功能单体,通过表面印迹法制备17β-雌二醇磁性分子印迹纳米材料.同时,对制备的纳米材料进行了傅里叶变换红外光谱(FT-IR)、X射线衍射(XRD)、X射线光电子能谱(XPS)、扫描电镜(SEM)和动态光散射(DLS)等一系列仪器分析和吸附动力学、选择性吸附、再生吸附等实验研究.
1 材料与方法
1.1 实验试剂
六水合氯化铁(FeCl3×6H2O)、无水乙酸钠(NaAC)、氨水,均为分析纯试剂,购于南京化学试剂有限公司;正硅酸四乙酯(TEOS,AR)、乙二醇(AR)和十六烷基三甲基溴化铵(CTAB,AR)由国药集团化学试剂有限公司提供;1,2-二(三乙氧基硅烷)乙烷(BTESE,CP)、3-氨基丙基三乙氧基硅烷(APTES,CP)和17β-雌二醇(E2,BR)购自上海麦克林生化有限公司;冰乙酸(AR)购于南京晚晴化学试剂有限公司.
1.2 合成Fe3O4@SiO2纳米微球
Fe3O4纳米粒子的制备:将1.35g FeCl3×6H2O, 3.60g NaAC溶解在50mL乙二醇并搅拌均匀,再将混合溶液转移至特氟龙不锈钢高压反应釜中,在200℃下反应6h,制得的Fe3O4依次用水、乙醇各洗涤3次后,真空干燥备用.
制备硅烷化的Fe3O4纳米颗粒:取100mg上一步骤中制得的Fe3O4,溶于20mL水中,超声使溶液分散均匀后,再加入115mL乙醇和2mL氨水,超声15min,然后缓慢地滴加2mL TEOS,室温下快速搅拌12h.制得的产物在外加磁场的辅助下,用乙醇和水反复洗涤,以除去未反应的TEOS,45℃真空干燥过夜.
1.3 基于Fe3O4@SiO2的表面分子印迹聚合物的制备
取0.5465g CTAB溶解于20mL的水和10mL乙醇的混合液中,再加入100mL水,然后将3mL氨水(28%,质量分数)、3mL BTESE(交联剂)、235μL APTES(功能单体)和70mg E2(模板分子),加入至上述混合液中,超声分散均匀后,于室温下搅拌1h, 使模板分子和功能单体进行预组装.然后加入80mg Fe3O4@SiO2,超声使其分散均匀后,在室温下搅拌聚合6h.反应完成后,在外加磁场的辅助下分离产物,得到含有模板分子的印迹聚合物.再以甲醇溶液(含2%(体积分数)冰乙酸)为洗脱剂去除聚合物中的模板分子,用高效液相色谱检测洗脱液,直至洗脱液中检测不到17β-雌二醇为止,最后将Fe3O4@SiO2@MIPs置于55℃真空干燥箱中烘干,用于后续实验.制备流程见图1. Fe3O4@SiO2@NIPs的制备过程与MIPs的制备条件相同,只是不加入模板分子E2.

图1 E2磁性分子印迹聚合物的制备流程
1.4 实验设备
实验使用的仪器主要有X-射线衍射仪(XRD, D8Advance,德国-Bruker)、Zeta电位-粒径分析仪(美国-Brookhaven)、扫描电子显微镜(SEM, Quante 400FEG,美国-FEI)、高分辨Zeta电位及粒度分析仪(Zeta PALS,Brookhaven)综合物性测量系统(PPMS- 9TM,美国-Quantum Design)、傅里叶红外光谱仪(FT-IR,Nicolet iS10,美国-Thermo Fisher)、X射线光电子能谱(XPS,ESCALAB 250Xi,美国-Thermo Fisher)以及高效液相色谱仪(HPLC,E2695,美国-Waters).
1.5 吸附性能研究
1.5.1 静态吸附实验 探究了E2初始浓度变化对吸附性能的影响.分别称取适量MIPs和NIPs,浸入5mL不同浓度的E2溶液中(1~200mg/L),然后于室温下振荡吸附6h,在外加磁场的作用下分离上清液,用高效液相色谱检测上清液中E2的浓度.
1.5.2 吸附动力学实验 分别称取适量的MIPs和NIPs,分别置于25mL具盖样品瓶中,加入10mL 70mg/L的E2溶液,在30℃恒温振荡,取不同时间段(1,2,3,4,5,6,7,8h)的上清液,用高效液相色谱测定上清液中E2的浓度吸附后溶液中残留的E2浓度.
1.5.3 选择性吸附实验 首先配置70mg/L 的E2、雌三醇(E3)、双酚A(BPA)和3,4-苯并芘(BaP)的乙醇溶液,其中E3、BPA为E2的结构类似物,BaP为非结构类似物.然后分别称取适量MIPs和NIPs,浸入5mL上述溶液中,室温下振荡至吸附平衡后,取上清液,用高效液相色谱检测上清液中E2、E3、BPA和BaP的浓度.
1.5.4 吸附再生实验 分别称取适量MIPs和NIPs浸入5mL 70mg/L的E2溶液中,室温下振荡至吸附平衡后,在外加磁场的作用下分离上清液,用高效液相色谱检测上清液中E2的浓度.然后用甲醇(含2%(体积分数)冰乙酸)溶液洗脱吸附后的MIPs和NIPs,同样用高效液相色谱检测洗脱液中E2的浓度.洗脱后的MIPs和NIPs真空干燥后,重复7次上述吸附-解吸过程,探究MIPs的循环使用情况.
2 结果与讨论
2.1 表征结果与分析
由图2a可知Fe3O4呈球状结构且大小均一;图2b为Fe3O4@SiO2的扫描电镜图,表面硅烷化的Fe3O4的粒径明显增加,并从明暗程度可清晰看出核-壳结构纳米颗粒的形成;图2c、d为MIPs和NIPs的扫描电镜图,Fe3O4@SiO2表面明显包覆了一层物质,粒径略有增加.

图2 Fe3O4 (a)、Fe3O4@SiO2 (b)、MIPs (c)和NIPs (d)的SEM图
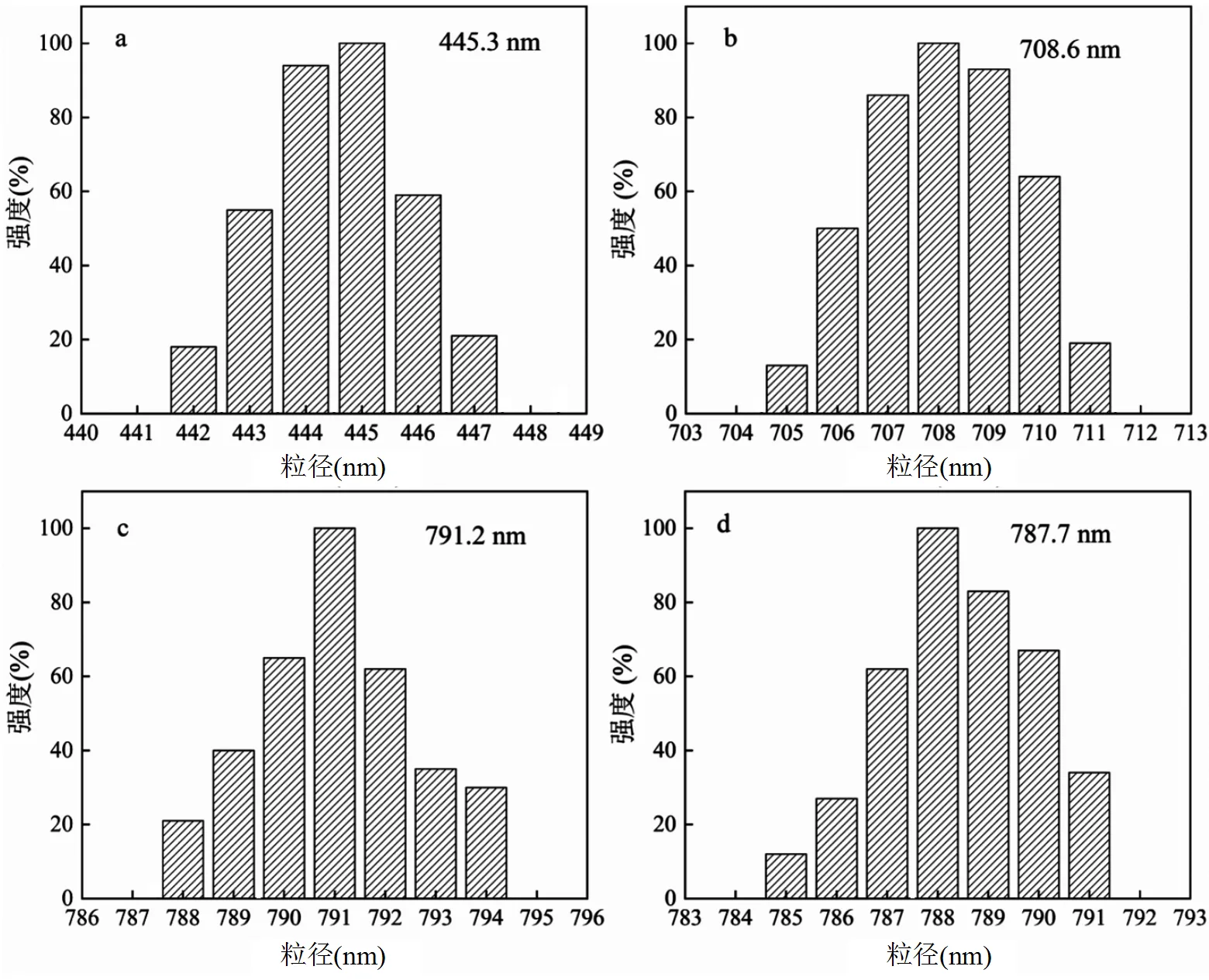
图3 Fe3O4(a)、Fe3O4@SiO2(b)、MIPs(c)和NIPs(d)的动态光散射图
由图3可知,4种粒子的直径分别为445.3, 708.6, 791.2和787.7nm,其中,SiO2层的平均厚度在125nm左右;MIPs和NIPs层的平均厚度为40nm左右,DLS的结果与SEM观测结果一致.制备的印迹材料形状规则,粒径均一.
如图4所示,710.76和532.48eV位置处的峰对应Fe 2p和O s1的特征峰,证明有效合成了Fe3O4.在包覆SiO2后,可以观察到102.85eV处的Si 2p峰,且710.76eV处的Fe 2p峰强大幅度降低,这是由于SiO2较厚造成的.表面印迹聚合后,MIPs和NIPs中都可以观察到405eV的N 1s峰(图4e),N元素来源于功能单体中的氨基,证明材料按照预想制备成功.

如图5所示,这4种纳米材料在570cm-1处都存在明显吸收峰,对应的是Fe3O4中Fe-O伸缩振动;包覆SiO2后,765, 904和1021cm-1处的峰分别对应于Si-O的弯曲振动,Si-OH的对称伸缩振动和Si-O不对称伸缩振动;包覆聚合物后,1635cm-1处为BTESE中C=O的伸缩振动特征峰,2882和2983cm-1对应于APTES中长链烷基的伸缩振动.这些峰的出现说明聚合物成功包覆在Fe3O4@SiO2表面.

图5 Fe3O4(a)、Fe3O4@SiO2(b)、MIPs(c)和NIPs(d)的FT-IR图
如图6所示,这4种样品中,都能在2值为30.15, 35.49, 43.24, 53.72, 57.22和62.84°处观察到明显的衍射峰,这些峰位置与Fe3O4的晶面指数(220)、(311)、(400)、(422)、(511)和(440)相对应.在SiO2和聚合物依次包覆后,Fe3O4衍射峰强度有所降低,但峰位置没有发生偏移.说明成功制备出Fe3O4,且Fe3O4的晶体结构没有发生变化,纳米材料具有良好的磁性.

图6 Fe3O4、Fe3O4@SiO2、MIPs和NIPs的XRD图
如图7所示,Fe3O4的磁化强度值为80.47emu/g, SiO2包覆后强度有所降低,降低至61.18emu/g,MIPs和NIPs包覆后,磁化强度值分别降至31.28 和26.86emu/g.与Fe3O4相比,MIPs和NIPs纳米颗粒的磁性降低,但仍然具有足够的磁场强度实现在外加磁场下快速分离.
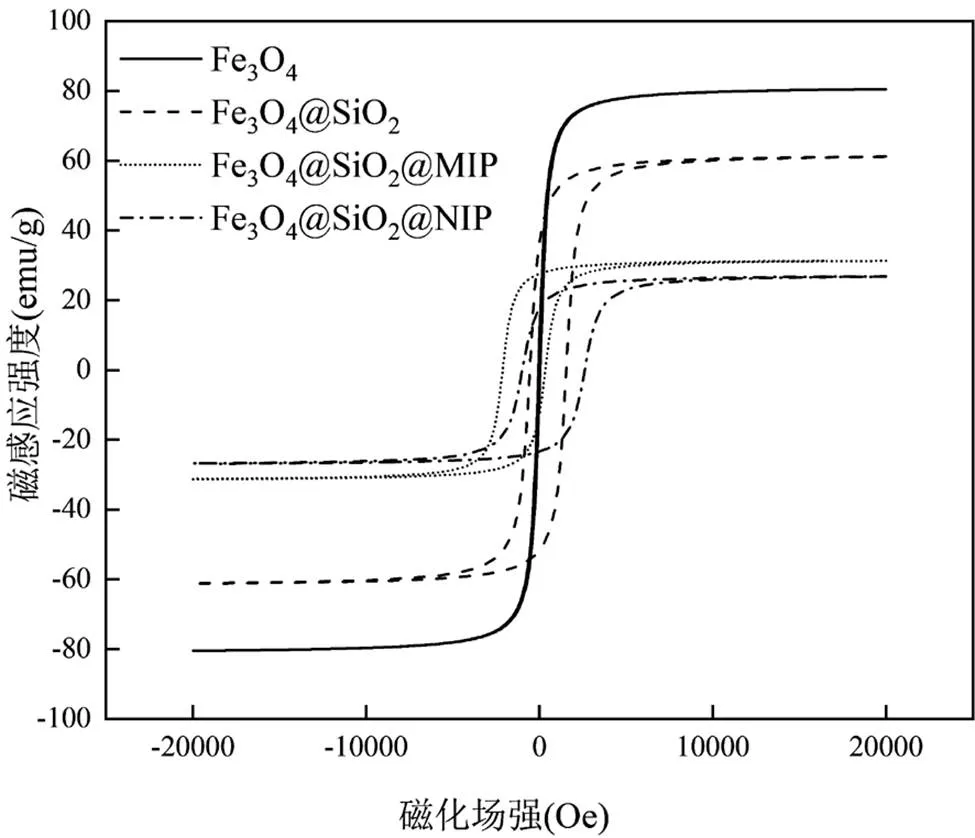
图7 Fe3O4、Fe3O4@SiO2、MIPs和NIPs的磁滞回线测试(VSM)图
2.2 吸附等温线
探究MIPs和NIPs对E2的结合性能,测定了室温下MIPs和NIPs对E2初始浓度在0~200mg/L浓度范围内的吸附容量,绘制了吸附等温线(图8)从图中可以看出,随着E2浓度增加,MIPs和NIPs对E2的吸附量也随之增加,且MIPs对E2的吸附量明显高于NIPs,这表明MIPs对E2存在选择性吸附,对E2的识别能力强,吸附容量大.
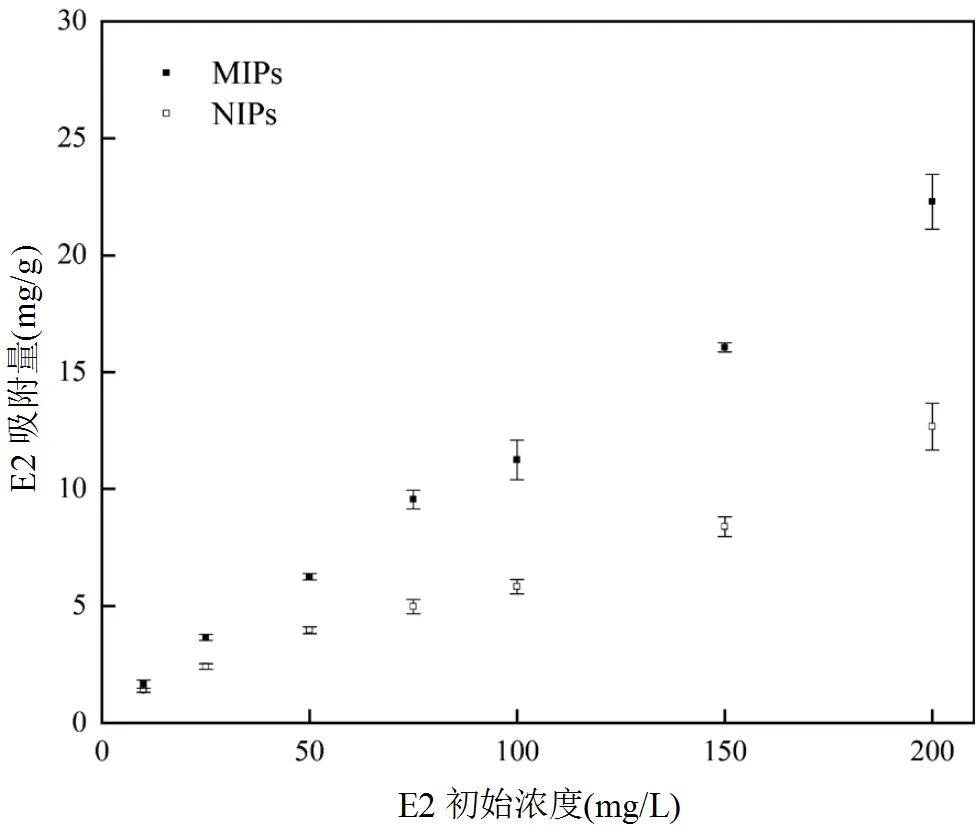
图8 MIPs和NIPs的吸附等温线
为了更加直观地表达MIPs和NIPs对E2吸附性能的差异,利用Freundlich吸附等温模型对吸附数据进行分析.
MIPs和NIPs的拟合结果见表1和图9.MIPs的f值远远高于NIPs的f值,说明MIPs对E2的吸附能力强;MIPs的1/值小于NIPs的1/值,说明MIPs对E2的吸附比NIPs更容易进行.结合图8可知,MIPs具有优秀的选择性吸附性能.

表1 MIPs和NIPs的Freundlich等温线拟合参数
注:f是Freundlich结合常数,是吸附剂吸附能力的指标;表示吸附过程的支持力,1/值越小表示模板分子越易吸附.
2.3 吸附动力学

图9 MIPs (a)和NIPs (b)的Freundlich线性拟合图
e为平衡吸附量, mg/g;e为吸附平衡时E2的溶液浓度, mg/L

图10 MIPs和NIPs的动态吸附曲线
在吸附动力学实验中,E2初始浓度为70mg/L,于30℃下振荡吸附,每隔一段时间取1.5mL上清液测定E2的含量.结果如图10所示,随着吸附时间的增加,MIPs和NIPs对E2的吸附量逐渐增加并趋于平衡.在3h内,吸附速率上升较快,在4h后吸附量基本趋于平衡,在5h之后基本达到平衡.并且,MIPs的平衡吸附量明显大于NIPs的吸附量,说明MIPs对E2具有较好的吸附动力学性质.
2.4 选择性吸附
如图11所示,与其他化合物相比,MIPs和NIPs对E2的吸附量最大,分别为9.69和6.25mg/g,表现出明显的选择性.对结构类似物E3、BPA的吸附容量次之,分别为4.05, 1.39mg/g和3.73, 1.57mg/g.对结构非类似物BaP的吸附量最少,低至0.67和0.60mg/g.同时,MIPs对4种物质的吸附量都大于NIPs.以上结果表明,MIPs对模板分子及其结构类似物具有较好的选择性能.
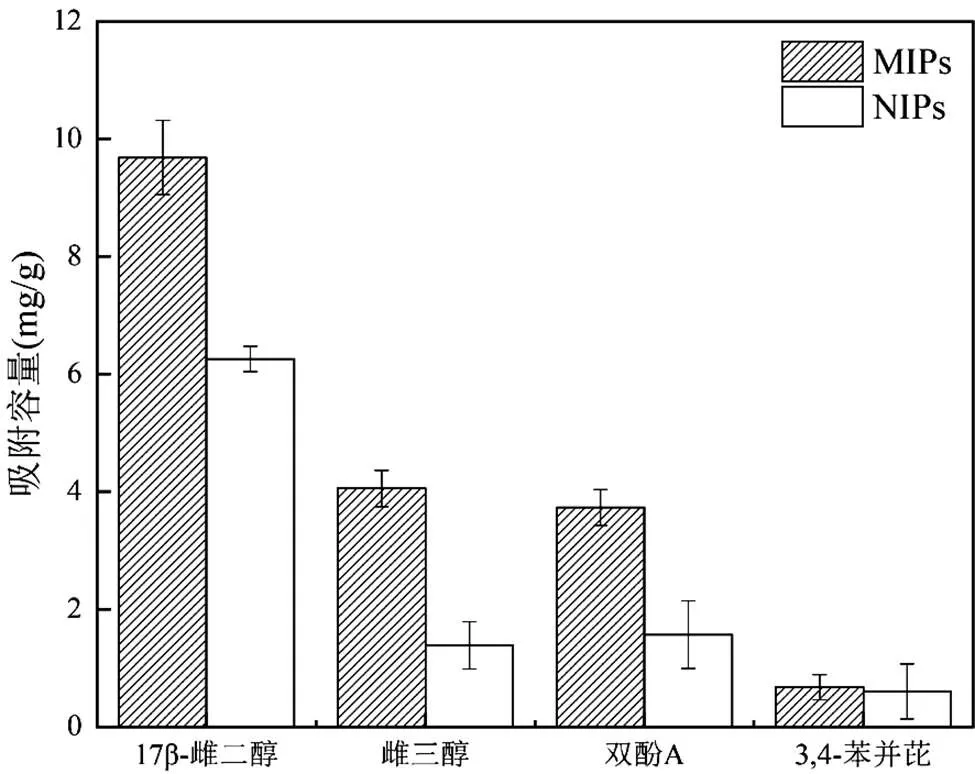
图11 常温下MIPs和NIPs对E2、E3、BPA和BaP的选择性吸附
2.5 吸附再生
从图12中可知,经过7个循环后,MIPs和NIPs的吸附性能并未产生明显变化,MIPs稳定在9mg/g上下,NIPs稳定在6mg/g上下.图13为MIPs每次循环对E2的吸附量和解吸量变化,吸附损失量约3%.表明MIPs在具有良好吸附能力的同时,表现出优秀的可重复利用性.综上可知,本文制备的MIPs具有较好的化学稳定性和使用寿命长的优点,可用于E2的快速分离富集.

图12 MIPs和NIPs循环使用后的吸附量

图13 MIP的吸附和解吸量
3 结论
3.1 成功制备出Fe3O4@SiO2@MIPs,且纳米材料大小均匀、形状规则.
3.2 对MIPs进行一系列吸附试验,得出MIPs对E2具有良好的选择识别能力和吸附能力,MIPs和NIPs对E2的饱和吸附量分别为9.69mg/g,6.25mg/g.
3.3 MIPs具有优秀的物理化学稳定性,使用寿命长,7次吸附-解吸后吸附损失量仅为3%.
3.4 结合Fe3O4的磁性可实现印迹聚合物快速地回收再利用,有效简化E2检测前的预处理工作.
[1] Malekinejad H, Scherpenisse P, Bergwerff A. Naturally occurring estrogens in processed milk and in raw milk (from gestated cows) [J]. Journal of Agricultural and Food Chemistry, 2006,54(26):9785-9791.
[2] Courant F, Antignac J, Lille J, et al. Exposure assessment of prepubertal children to steroid endocrine disruptors. 2. Determination of steroid hormones in milk, egg, and meat samples [J]. Journal of Agricultural and Food Chemistry, 2008,56(9):3176-3184.
[3] Gao Q, Luo D, Bai M, et al. Rapid determination of estrogens in milk samples based on magnetite nanoparticles/polypyrrole magnetic solid-phase extraction coupled with liquid chromatography-tandem mass spectrometry [J]. Journal of Agricultural and Food Chemistry, 2011,59(16):8543-8549.
[4] Gao R, Hao Y, Zhang L, et al. Core-shell nano-sized magnetic molecularly imprinted solid phase extractant coupled with HPLC for the selective isolation and determination of 17β-estradiol in a lake water sample [J]. Analytical Methods, 2014,6(24):9791-9799.
[5] Mao Y, Zhang Y, Qu Q, et al. Cancer-associated fibroblasts induce trastuzumab resistance in HER2 positive breast cancer cells [J]. Molecular Biosystems, 2015,11(4):1029-1040.
[6] Zhen Y, Li F, Gui Y, et al. Label-free aptamer-based electrochemical impedance biosensor for 17β-estradiol [J]. Analyst, 2012,137(4):819- 822.
[7] Ze H, Li N, Yan P, et al. Imprinted monoliths: recent significant progress in analysis field [J]. Trac Trends in Analytical Chemistry, 2017,86:84-92.
[8] Gao D, Wang D, Zhang Q, et al. In vivo selective capture and rapid identification of luteolin and its metabolites in rat livers by molecularly imprinted solid-phase microextraction [J]. Journal of Agricultural and Food Chemistry, 2017,65(6):1158-1166.
[9] Zheng X, Lian Q, Yang H, et al. Surface molecularly imprinted polymer of chitosan grafted poly(methyl methacrylate) for 5- fluorouracil and controlled release [J]. Scientific Reports, 2016, 6(1):99-100.
[10] Ncube S, Kunene P, Tavengwa N T, et al. Synthesis and characterization of a molecularly imprinted polymer for the isolation of the 16US-EPA priority polycyclic aromatic hydrocarbons (PAHs) in solution [J]. Journal of Environmental Management, 2017,199:192- 200.
[11] González G P, Hernando P F, Alegria J S, et al. An optical sensor for the determination of digoxin in serum samples based on a molecularly imprinted polymer membrane [J]. Analytica Chimica Acta, 2009, 638(2):209-212.
[12] Ulbricht M, Oechel A, Lehmann C, et al. Gas-phase photoinduced graft polymerization of acrylic acid onto polyacrylonitrile ultrafiltration membranes [J]. Journal of Applied Polymer Science, 1995,55:1707-1723.
[13] Davis M E, Katz A, Ahmad W R. Rational catalyst design via imprinted nanostructured materials [J]. Chemistry of Materials, 1996, 8(8):1820-1839.
[14] Gao D, Zhang Z, Wu M, et al. A surface functional monomer-directing strategy for highly dense imprinting of TNT at surface of silica nanoparticles [J]. Journal of the American Chemical Society, 2007, 129(25):7859-7866.
[15] Xie C, Liu B, Wang Z, et al. Molecular imprinting at walls of silica nanotubes for TNT recognition [J]. Analytical Chemistry, 2008,80(2): 437-443.
[16] Zhou H, Xu Y, Tong H, et al. Direct synthesis of surface molecularly imprinted polymers based on vinyl-SiO2nanospheres for recognition of bisphenol A [J]. Journal of Applied Polymer Science, 2013,128(6): 3846-3852.
[17] Xue X, Lu R, Liu M, et al. A facile and general approach for the preparation of boronic acid-functionalized magnetic nanoparticles for the selective enrichment of glycoproteins [J]. Analyst, 2019,144(2): 641-648.
[18] 刘 冰,王德平,黄文旵,等.溶胶-凝胶法制备核壳SiO2/Fe3O4复合纳米粒子的研究 [J]. 无机材料学报, 2008,23(1):33-38.
Liu B, Wang D P, Huang W C, et al. Preparation of core-shell SiO2/ Fe3O4composite nanoparticles by sol-gel method [J].Journal of Inorganic Materials, 2008,23(1):33-38.
Preparation of ferromagnetic nanomaterials based on molecular imprinting technology and their performance for selective enrichment of 17β-estradiol (E2).
GUAN An-zhe, ZHAO Xu-dong, ZHANG Ting-ting, LI Yi, LI Jian-sheng, LU Rui*
(School of Environment and Biological Engineering, Nanjing University of Science & Technology, Nanjing 210094, China)., 2022,42(1):102~108
Ferromagnetic separation and molecular imprinting technology were combined together. Ferromagnetic oxide nanoparticles were used as core, while 17β-estradiol (E2) was used as the template molecule and (3-Aminopropyl) triethoxysilane was used as the functional monomer E2 molecularly imprinted polymer (MIPs) and non-imprinted polymer (NIPs) were prepared by surface polymerization. Then E2MIPs and NIPs were characterized by FT-IR, XRD, XPS, SEM and other methods. The results showed that MIPs have a regular spherical shape, and the particle size is uniform at about 790nm. In the selective adsorption experiment, the saturated adsorption capacity of MIPs and NIPs for E2 is 9.69 and 6.25mg/g, respectively. These results indicated good selectivity of the material. Freundlich linear fitting was performed on the static adsorption data, and the results proved that MIPs have good adsorption capacity. Meanwhile, MIPs showed excellent reusability as the adsorption capacity only lost 3% after 7 adsorption-desorption processes.
molecular imprinting;magnetic nanomaterials;surface polymerization;17β-estradiol(E2)
X56
A
1000-6923(2022)01-0102-07
管安浙(1998-),男,安徽合肥人,南京理工大学硕士研究生,主要从事分子印迹及拉曼光谱研究.
2021-05-27
江苏省自然科学基金资助项目(BK20191294);中央高校基本科研业务费专项资金资助(30919011214);环境污染控制与废弃物资源化利用安徽省重点实验室(2020EPC03)
* 责任作者, 副教授, rlu@njust.edu

