单孔胸腔镜肺减容在治疗老年慢性阻塞性肺疾病中的应用
杨彦辉 李季 王毅 罗雷 成欣 钟霖 谢晓阳
慢性阻塞性肺疾病(chronic obstructive pulmonary disease,COPD)是常见的呼吸道疾病,具体病理生理指肺内与终末细支气管相通的空腔持久异常扩大,并伴有肺泡壁的破坏。肺泡壁破坏,呼吸气腔非均匀性增大,肺泡及其结构排列紊乱,甚至消失。COPD病史长,病程反复,内科治疗效果差,严重影响患者的身心健康及生活质量[1-3]。外科手术多采用肺减容术(lung volume reduction surgery,LVRS),其机制为切除过度通气、无功能靶区肺组织,从而改善余肺通气血流比,提高肺功能。传统开胸手术创伤大,应激反应严重;伴随胸腔镜器械及技术飞速发展,三孔、两孔及单孔法胸腔镜应运而生且可覆盖大部分以往传统开放术式[4-6]。特别在解剖性肺段及肺叶切除术研究方面,涉及单孔胸腔镜技术的诸多研究及学者报道日益增加[7-8]。但目前对于胸腔镜LVRS,尤其单孔法的报道相对少见。内江市第一人民医院胸外科自2012年开展胸腔镜微创手术,2015年开始尝试单孔法胸腔镜手术,目前科室单孔术式占比80%。本研究采用单孔胸腔镜LVRS治疗老年COPD患者,总结具体手术方式、围手术期管理、术后随访等经验,以期更好地指导临床实践。
资料与方法
一、一般资料
回顾性分析2016年1月至2020年12月内江市第一人民医院胸心外科收治的47例行单孔胸腔镜LVRS患者的病例资料,包括术前、术后5 d、术后1个月、术后3个月肺功能[第1秒用力呼气容积(forced expiratory volume in one second,FEV1)、残气量(residual volume,RV)]、动脉氧分压PO2、6 min步行试验(6-min walking test,6MWT)、慢性阻塞性肺疾病评估测试(Chronic Obstructive Pulmonary Disease Assessment Test,CAT)评分。47例患者均为男性,其中30例术前合并气胸急诊入院安置胸引管,所有患者术前行胸部CT提示双肺弥漫性分布,主要病灶位于上叶者32例,中、下叶者15例;术前合并哮喘1例,既往1年内外伤病史合并术侧肋骨骨折1例,对有肺部感染患者应用抗生素、祛痰等治疗,合并哮喘患者予以解痉、平喘等治疗,对于吸烟患者给予严格戒烟≥3个月再评估手术。同时改善患者的一般状况,营养差的患者予以营养支持补液,改善肺功能,给予所有患者对手术的信心,并进行心理辅导。
入组标准:①单孔胸腔镜LVRS;②病例资料完整;③心肺功能耐受手术。排除标准:①术中改为两孔、三孔或中转开胸;②检查资料不完善;③心肺功能差难以耐受手术。
二、方法
1.手术方法:患者签署知情同意书,采用全身麻醉双腔气管插管后,取健侧卧位,稍向前倾,健侧单肺通气。切口位于腋前线与腋中线之间,长约3~4 cm,上、中、下叶切除均选择第5肋间隙。主刀医师位于患者腹侧,扶镜手位于患者背侧,主刀医师对侧将胸腔镜镜身尽量固定在单孔切口后缘(T管做弹力牵引),保持镜身及画面稳定性的同时,尽量避免镜身与手术器械的干扰。肺叶切除肺门处理顺序为右肺上叶:后段动脉–支气管–尖前、后动脉–肺静脉–叶间裂;右肺下叶:叶间裂–背段、基底段动脉–静脉–支气管;左肺下叶:叶间裂–背段、基底段动脉–静脉–支气管。非肺叶切除术时,切割闭合器直接切除靶区肺组织,所有断面常规采用划线缝补,同时肺创面试水漏气患者常规心包脂肪垫加固。术毕带气管插管返回胸外科重症监护室。
2.胸引管安置方法:术毕根据余肺漏气量大小安置胸引管。
16F胃管:间隔2~3 cm剪3~5个侧孔,从切口后份安置至胸顶,外接胸引瓶,引流管不留置预留线,切口采用钛合金线皮内缝合。28F引流管:间隔2~3 cm剪3~5个侧孔,从切口后份安置至胸顶,外接胸引瓶,引流管留置预留线,切口采用丝线间断缝合[9]。
三、统计学分析
采用SPSS 19.0分析数据。计量资料采用±s表示,呈正态分布两组间比较采取t检验;计数资料以例(%)表示,采用χ2检验。检验水准α=0.05。P<0.05为差异有统计学意义。
结 果
47例患者无围手术期死亡,均行单孔胸腔镜肺LVRS,其中肺叶切除术8例,右上叶切除术6例,左下肺2例,术后胸腔引流管持续引流时间(11.55±6.81) d,最长引流时间36 d,术后皮下气肿再置管5例,术后出现急性呼吸衰竭再次有创呼吸机辅助通气1例(表1,图1~2)。

图1 患者男性,56岁,吸烟史30+年,右肺行单孔胸腔镜LVRS,术前及术中CT资料

表1 47例肺减容患者术前及术中临床资料
术后随访1~3个月。术前、术后5 d、术后1个月、术后3个月,FEV1、6MWT及CAT评分呈上升趋势;术前与术后5 d、1个月、3个月相比,RV差异均有统计学意义(P<0.05,表2,图3)。

图3 术前及术前3个月FEV1及6MWT比较

表2 所有患者术前和术后肺功能值及6MWT
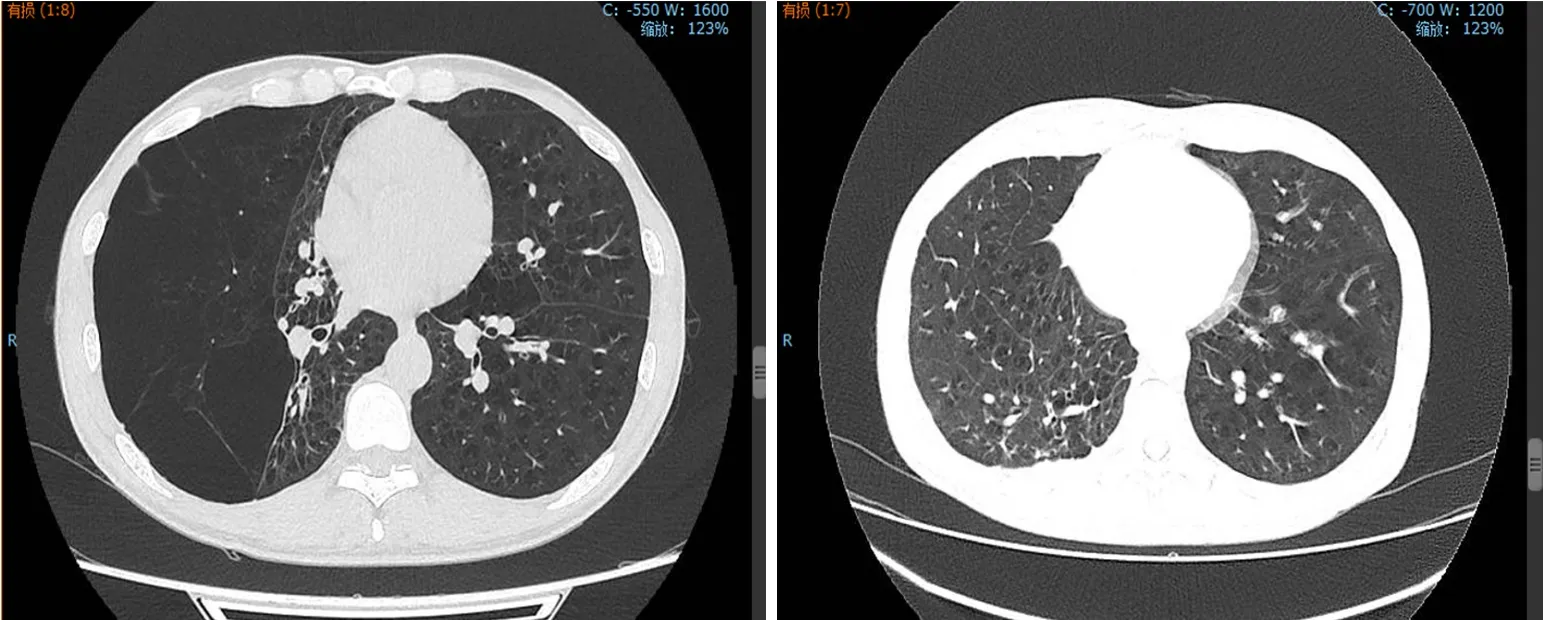
图2 患者男性,68岁,吸烟史40+年,单孔胸腔镜右上肺叶切除+ LVRS术前及术后CT资料
讨 论
COPD临床症状反复,预后差,治疗较为复杂,内科治疗通过抗炎、解痉、平喘及呼吸功能训练等对症处理,在一定程度上可改善轻中度患者症状,但终究无法逆转COPD的病理生理进程。LVRS通过外科手术切除COPD过度通气的靶区,提高余肺功能,改善患者症状及生活质量。随着微创外科的兴起,大量研究证实胸腔镜LVRS安全可行,且可取得与开放手术相同的疗效[10-12]。
本研究入组47例患者均行单孔胸腔镜LVRS,围手术期及术后3个月随访无死亡病例,术后肺功能指标及生活质量明显提高。那么如何有效提高经胸腔镜LVRS治疗COPD的效果,以及降低术后并发症的发生风险,我们的体会是:①右上肺病灶仍为主要靶区,肺叶切除患者耐受程度较高。②双侧弥散性肺大泡不建议同期手术,可优先处理明确靶区或病变较重一侧。③术前合并哮喘患者并非为美国NETT实验所认为手术绝对禁忌,但围手术期积极应用激素平喘并排除哮喘急性期。④术前加强肺部管理,术前予以吸氧营养支持。对于吸烟患者需严格戒烟3个月后再次评估手术。⑤术前对患者进行充分的知识宣教及心理沟通,使患者尽可能接受微创手术理念。⑥但对于病态肥胖及术前合并胸部外伤肋骨骨折史,LVRS的手术病死率及术后并发症发生率较高,对于同时合并肋骨骨折的患者,单孔切口选择注意避免骨折肋间,在单孔操作困难或暴露欠佳时应及时改为多孔或中转开胸。LVRS后并发症高,肺持续性漏气是最常见且长期困扰胸外科医生、限制该手术推广的重要原因,该并发症发生率约为50%。本组患者中,术后最长漏气及引流时间为36 d,术后1例患者出现CO2潴留后再次行有创呼吸机辅助通气。分析主要原因为:①COPD患者肺质量及顺应性差,切割闭合器处理后针眼漏气;②过度膨胀的肺组织切除后,胸腔内压力骤降,手术前后的压力差类似负压作用,促使或加重肺漏气;③在不确定需要处理的靶区肺组织存在反复牵拉器械损伤;④切割闭合器处理过后的切缘未行进一步肺修补和加固;⑤本组患者出现呼吸衰竭二次上机主要原因可能为合并哮喘激素应用不充分,术后动脉血气监测不及时,手术应激造成全身炎症反应。因此,相关预防措施包括:①切割缝合器在处理时尽量避免“钉上成钉”;②如肺残缘漏气可加用胸膜及心包脂肪垫加固或带垫钉仓,可明显减少肺漏气的发生;③残端或可疑漏气针眼处喷洒生物蛋白胶;④麻醉师吸痰鼓肺时压力不宜过大;⑤术后加强呼吸道管理,尽量减少机械通气时间,但是对于合并哮喘患者可适当延长呼吸机辅助通气时间,围手术期足量应用激素(加强龙40 mg,每6 h一次)及抗生素。同时,术后一定动态监测血气变化情况。
Cooper等[13]首次报道胸腔镜肺减容治疗COPD的大样本LVRS研究后,Kotloff等[14]即报道了胸腔镜下LVRS的研究。VATS与传统术式改善肺功能及活动能力的效果类似,但胸腔镜LVRS创伤更小,恢复更快。McKenna等[15]研究359例行LVRS的患者发现,胸腔镜LVRS与常规开胸手术的病死率相同,但胸腔镜术后患者恢复较快。2011年,Gonzalez等[16]首次报道了单孔胸腔镜下右肺上叶切除术,此后陆续有研究报道单孔胸腔镜手术的安全性和可行性,在熟练操作同时,单孔技术较多孔可以显著减轻手术应激反应并减少创伤[17-18]。本组手术时间(94.23±26.39)min,总结经验为:①充分游离术侧肺组织及胸壁粘连;②充分利用膨胀萎陷法证实手术靶区;③术中切记,LVRS并非切除全部病肺,而是获得足够的肺减容来改善呼吸生理机制,提高余肺功能。因此,术中应有效缩短手术时间。
本研究结果显示,单孔胸腔镜LVRS可以有效改善患者的肺功能及6MWT。LVRS术后评分量表有多种,但缺乏对于预后效果判断特异性较高的量表。本研究采用CAT评分量表,单孔胸腔镜LVRS后CAT评分显著改善,部分患者术后3个月可达正常水平;同时,CAT评分量表计算简短实用,可能适合临床推广[19]。
综上所述,COPD是一种慢性进展性疾病,合并气胸,病情危重,须及时处理,但早期有效预防可能需要更多外科医师关注。本研究回顾性分析47例单孔胸腔镜LVRS患者的病例资料,证实单孔胸腔镜LVRS可显著改善患者肺功能及生活质量,手术效果鼓舞人心,但LVRS术后患者住院时间长、抗生素应用强度大,器械耗材需求大,部分患者未能及时得到外科干预,这可能需要更多术者重视。

