不同Kappa角补偿的波前像差引导飞秒激光联合准分子激光原位角膜磨镶术对患者屈光度和视觉质量的影响△
贾寓洁 汝新宇 林淑华 赵 健 王晓伟 贾法力 许文皓 曹婉莹 李英俊
瞳孔光轴与视轴存在的夹角称为Kappa角。个性化的角膜屈光手术中,理想的准分子激光切削中心应与视轴完全重叠,但术中视轴很难确定[1],且通常准分子激光治疗仪配备的主动眼球跟踪系统定位跟踪的是瞳孔(瞳孔中心),术中瞳孔定位跟踪扫描时如不考虑Kappa角的调整,会导致 “手术源性”的偏心切削[2],引起术后高阶像差的增大[3]。
角膜共轴反光点是视轴的角膜切入点。研究表明,角膜共轴反光点是较为理想的切削中心点,不受瞳孔大小及中心位置变化的影响,距视轴平均为 0.02 mm,是距离视轴最近的点[4],因此,Kappa角可以理解为瞳孔中心与角膜共轴反光点之间的距离(P-Dist)[5]。目前可供选择的Kappa角调整只是按瞳孔中心与角膜共轴反光点之间的矢量比补偿的,其输入的值是固定的移心量。但Kappa角不是固定值,随瞳孔中心位置的动态变化而发生改变[6]。
本研究分析瞳孔中心与角膜共轴反光点之间的分布规律及特点,通过75%及100%的Kappa角补偿量,分析不同Kappa角补偿的个性化准分子激光原位角膜磨镶术对中度近视患者的术后屈光度和视觉质量的影响。
1 资料与方法
1.1 一般资料选取2020年5月至8月在延边大学附属医院眼科行飞秒激光联合准分子激光原位角膜磨镶术的中度近视患者322例,均为右眼,其中男157例,女165例。患者一般资料见表1。
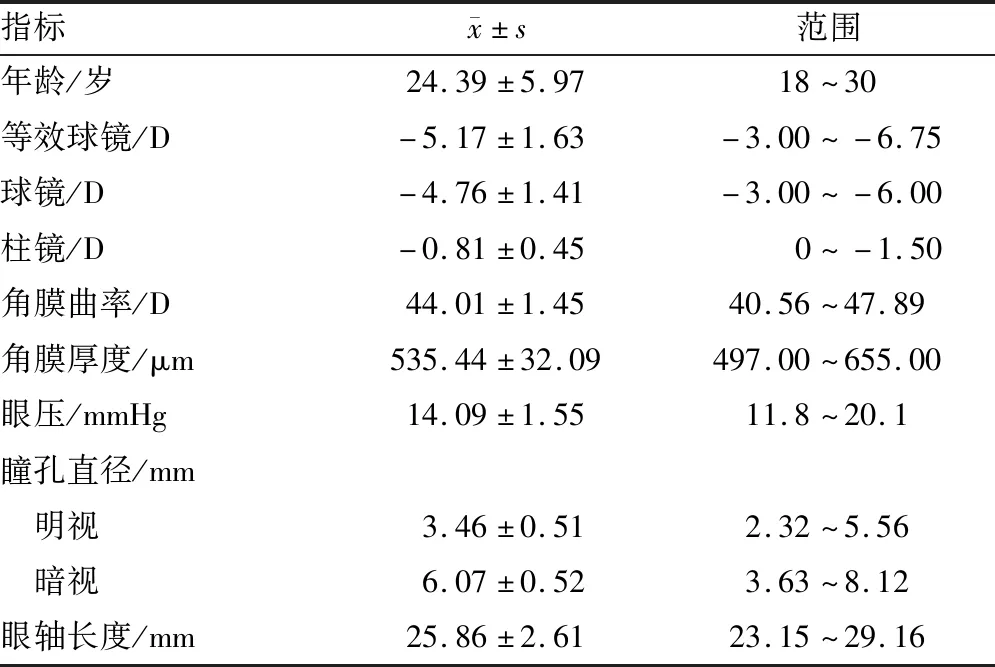
表1 患者的一般资料
纳入标准: (1)双眼术前球镜度数-3.00~-6.00 D,柱镜度数0~1.50 D,两眼等效球镜度数差异≤1.00 D;(2)近2年屈光状态稳定(每年变化小于0.50 D);(3)停戴软性角膜接触镜2周以上或硬性透气性角膜接触镜1个月以上;(4)全身状态良好,术中和术后随访3个月过程中无并发症;(5)术前中央角膜厚度≥480 μm,术后残留角膜基质床厚度≥280 μm;(6)近期内无糖皮质激素、避孕药等服用史。
排除标准:(1)排除角膜病变、圆锥角膜、白内障、青光眼、葡萄膜炎、视网膜疾病等眼部疾病患者;(2)排除糖尿病、高血压病、风湿、甲状腺功能亢进等全身疾病患者;(3)排除妊娠或哺乳期女性。
1.2 方法
1.2.1 分组根据Kappa角补偿量的不同,将患者分为补偿75%组(163眼)、补偿100%组(159眼),术中通过WaveLight鹰视EX500准分子激光系统的X轴和Y轴眼球跟踪调节程序记录患者的P-Dist大小。通过分析P-Dist大小的分布情况,对P-Dist>0.225 mm、P-Dist≤0.225 mm时的补偿75%组和补偿100%组患者进行分析。
1.2.2 手术方法采用德国WaveLight FS200鹰视飞秒激光(200 kHz)制作直径8.5 mm、厚度110 μm的角膜瓣;采用德国WaveLight EX500鹰视准分子激光机(500 kHz)进行波前像差引导的切削程序进行准分子激光切削,目标屈光度设定为0 D。手术步骤:常规消毒术眼,开睑器开睑,取仰卧位,嘱患者注视上方绿色指示灯,术者显微镜下可见角膜顶点的反光点(角膜共轴反光点)和瞳孔中央的红色反光(光轴中心,直角坐标系的原点),调整手术显微镜的调节照明度及室内照明光线,保持瞳孔大小与术前检查时相匹配,通过WaveLight EX500鹰视准分子激光系统的X轴和Y轴眼球跟踪调节程序,记录患者仰卧位时P-Dist大小。将75%和100%的Kappa角调整量完全随机分配,手动输入到准分子激光设备中。将准分子激光切削中心从瞳孔中心移至视轴方向(角膜共轴反光点)。光学切削直径为6.5 mm,按预先设计好的程序进行激光切削,完毕后瓣复位,冲洗瓣下残留物,取下开睑器,术毕。
1.3 检测指标所有患者术前均行裂隙灯、电脑验光和睫状肌麻痹验光、最佳矫正视力、眼压、角膜厚度、眼轴、眼底检查,在术前及术后3个月采用ALLEGRO Topolyzer角膜地形图仪(Wavelight公司,德国)测量瞳孔的大小和中心位置,WaveScan波前像差仪(VISX公司,美国)测量在暗室下正常瞳孔直径5 mm条件下的眼球高阶像差 (包括 3~6阶的总高阶像差、球差、彗差、三叶草像差),不需要散瞳。应用OPTEC 6500视功能检测仪(美国Stereo公司) 在暗室下测定明视(85.0 cpd)无眩光,明视眩光状态下的5种空间频率(1.5 cpd、3.0 cpd、6.0 cpd、12.0 cpd和18.0 cpd)的对比敏感度。所有检查均由同一医师完成。
1.4 统计学方法采用 SPSS 21.0软件进行数据分析。各组数据进行正态性检验和方差齐性检验,并以均数±标准差进行统计学描述。采用两独立样本资料的t检验进行不同P-Dist时各指标的比较,采用配对t检验进行补偿75%组和补偿100%组患者各个指标的比较。检验水准:α=0.05。
2 结果
2.1 适宜角膜屈光手术患者P-Dist的矢量分布情况患者P-Dist为0.012~0.610(0.225±0.108) mm,32%患眼(104眼)≤0.15 mm,86%患眼(277眼)≤0.30 mm,99%患眼(318眼)≤0.45 mm。
P-Dist≤0.225 mm时患眼为173眼(补偿75%组81眼,补偿100%组92眼);P-Dist >0.225 mm时患眼为149眼(补偿75%组82眼,补偿100%组67眼);其中补偿75%组患者P-Dist为(0.215±0.094)mm,补偿100%组患者P-Dist为(0.238±0.122)mm,两组间差异无统计学意义 (t=0.762,P=0.458)。
2.2 术后3个月患者视力及屈光度比较术后3个月,补偿75%组和补偿100%组患者球镜度数、等效球镜度数、柱镜度数、裸眼远视力(UDVA) (logMAR)在不同P-Dist时差异均无统计学意义(均为P>0.05)。两组患者术后3个月屈光度呈现轻度远视漂移,屈光度在+0.50 D以内者占85%(276眼)以上。
P-Dist ≤0.225 mm时,术后球镜度数、等效球镜度数、UDVA(logMAR)、柱镜度数在补偿75%组和补偿100%组间差异均无统计学意义(均为P>0.05)。但P-Dist>0.225 mm时,补偿100%组患者的术后柱镜度数显著高于补偿75%组(P=0.041);补偿75%组和补偿100%组患者UDVA(logMAR)、球镜度数、等效球镜度数差异均无统计学意义(均为P>0.05)(表 2)。
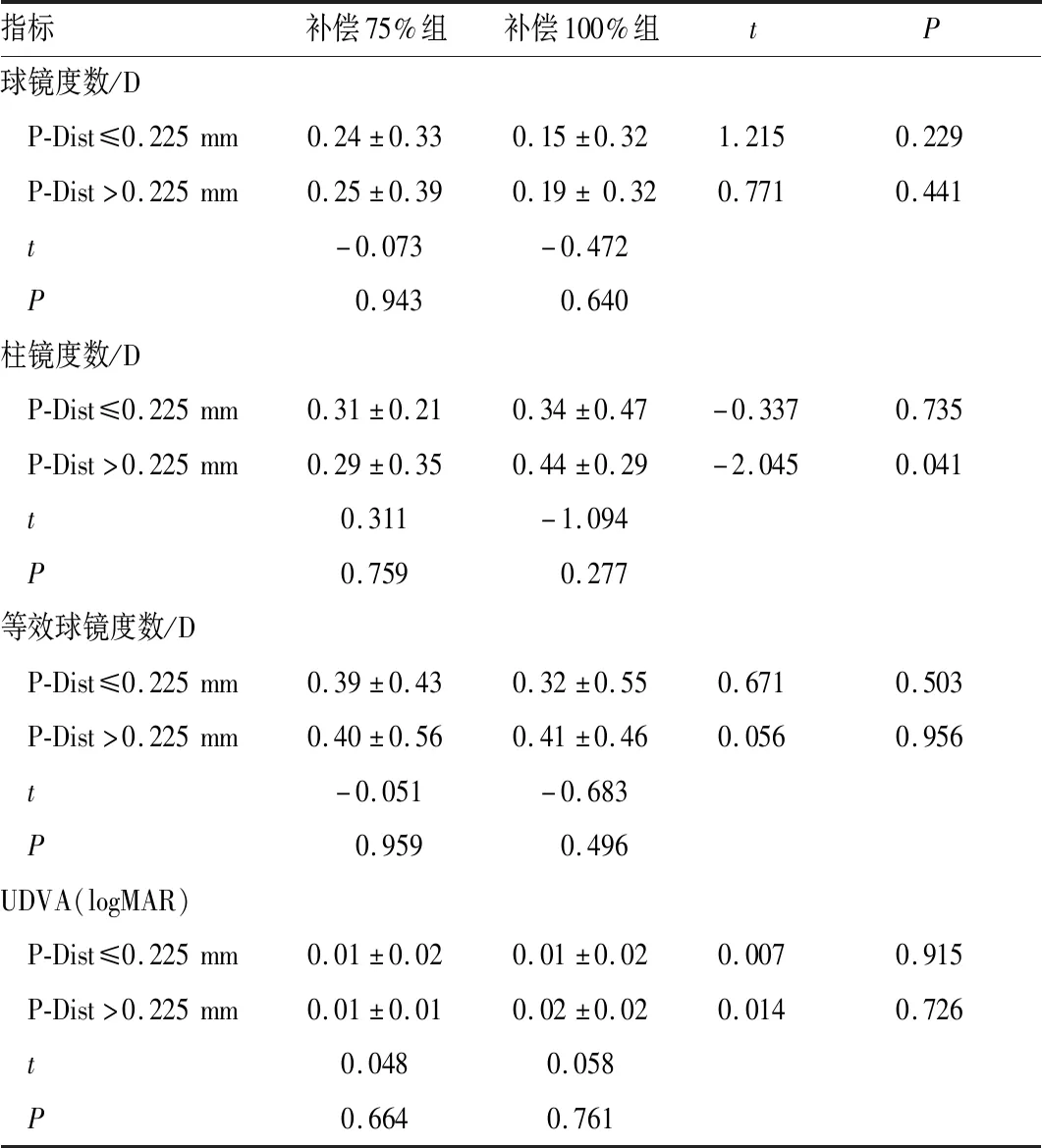
表2 术后3个月不同P-Dist时患者屈光度比较
2.3 术后3个月患者高阶像差比较术后3个月时,补偿75%组和补偿100%组患者总高阶像差、球差、三叶草像差在不同P-Dist时差异均无统计学意义(均为P>0.05)。补偿75%组患者彗差在不同P-Dist时差异无统计学意义(P>0.05),补偿100%组患者彗差在不同P-Dist时差异有统计学意义(P=0.047)(表3)。

表3 术后3个月不同P-Dist时患者高阶像差比较
术后3个月,P-Dist ≤0.225 mm时,补偿75%组患者和补偿100%组患者的彗差差异无统计学意义(P=0.132)。P-Dist > 0.225mm时,补偿100%组患者的彗差明显高于补偿75%组(P=0.023)。
术后3个月,P-Dist ≤ 0.225 mm时、P-Dist >0.225 mm时补偿75%组和补偿100%组患者总高阶像差、球差和三叶草像差差异均无统计学意义(均为P>0.05)。
2.4 术后3个月对比敏感度比较术后3个月,当P-Dist ≤0.225 mm时明视及明视眩光在5个空间频率下,补偿75%组和补偿100%组患者的对比敏感度差异均无统计学意义(均为P>0.05)。但当P-Dist>0.225 mm时,术后明视眩光1.5 cpd空间频率下,补偿100%组患者的对比敏感度显著低于补偿75%组(t=3.677,P=0.038)(表4)。
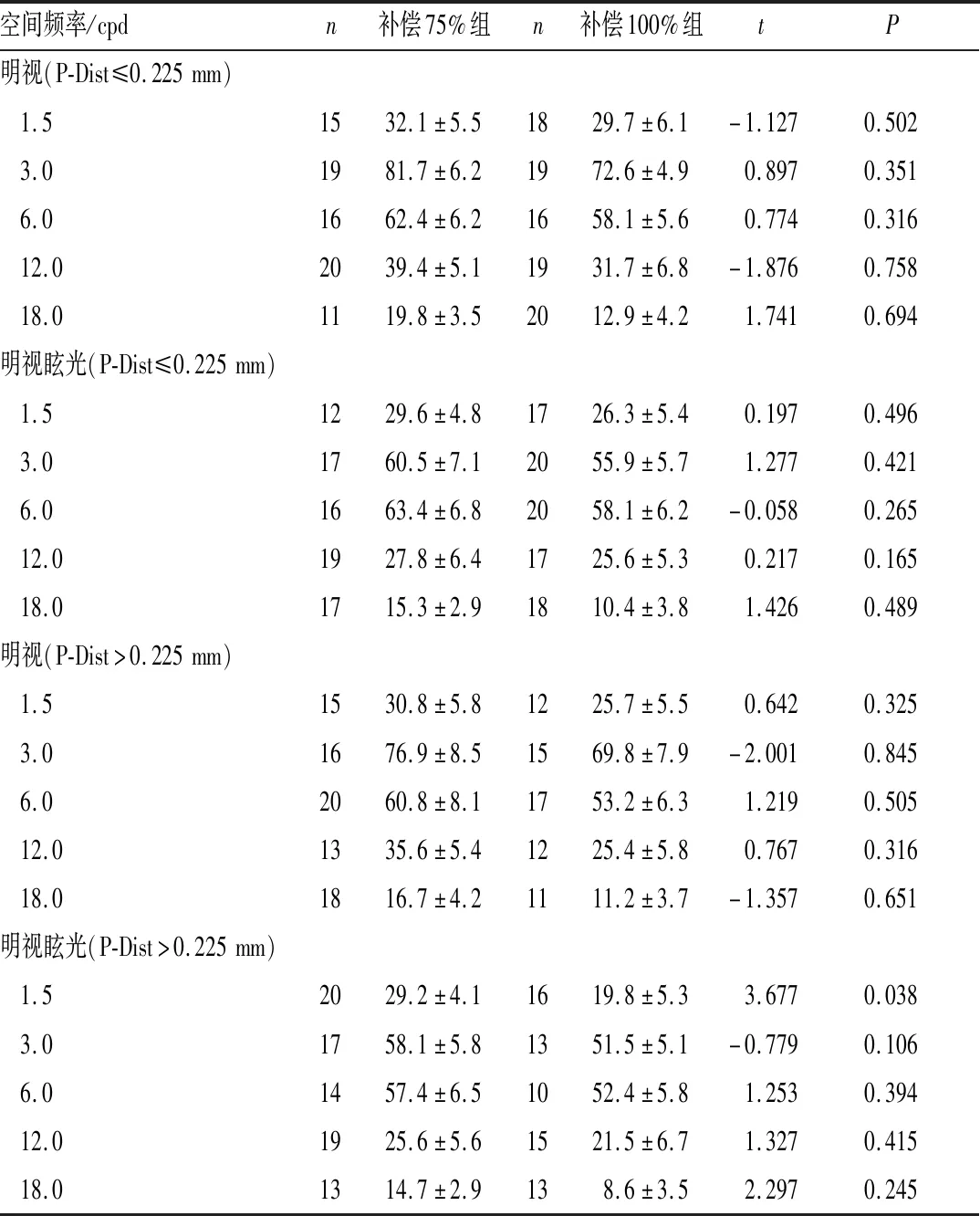
表4 术后3个月明视及明视眩光在5个空间频率下不同P-Dist时患者对比敏感度比较
3 讨论
人的眼睛是一个复杂的光学系统,存在着多条轴线(视轴、光轴、瞳孔轴等)和多个角度(Kappa角、Alpha角等),视轴与光轴存在的夹角称Kappa角[7]。尽管Kappa角补偿联合各种模式的个性化角膜屈光手术具有良好的理论基础,但实际与理想的视觉质量尚存在明显差距[8]。新一代的准分子激光治疗设备多数配有Kappa角调整和眼球跟踪系统,可在准分子激光切削过程中检测眼球的运动,是通过计算瞳孔中心与角膜反射之间的矢量来估计视轴方向的[9],但现有的切削技术只是矫正静态的Kappa角偏移量,并未考虑到瞳孔的动态变化、角膜和晶状体等因素[10]。Kappa角不是静态的固定值,在不同条件下会有所变化[11]。如术中的照明[12]、手术刺激、眼别[13]、情绪紧张[14]、近距离注视指示灯所引起的调节辐辏[15]等因素。如何进行最优化Kappa角的调整百分比以及其对术后屈光度和视觉质量的影响,目前国内外尚无文献报道。
本研究通过分析瞳孔中心与角膜共轴反光点之间的分布规律及特点,探讨不同Kappa角补偿的个性化准分子激光原位角膜磨镶术对中度近视患者的屈光度和视觉质量的影响,我们测量了P-Dist,其分布与Okamoto等[16]的研究报告相似,显示P-Dist为0.012~0.610 mm,平均为0.225 mm,我们根据上述平均值及补偿75%组患者、补偿100%组患者P-Dist大小的分布情况将Kappa角分为P-Dist>0.225 mm(大Kappa角)和P-Dist≤ 0.225 mm(小Kappa角),分别通过补偿75%、100%的矢量百分比,试图验证补偿多少百分比才能获得最佳的视觉质量效果。
本研究结果表明,两组患者的术后视力、等效球镜度数差异无统计学意义,两组患者的残留屈光度均较小,等效球镜呈现轻度远视漂移,+0.50 D内者占85%以上。唐静等[17]在对Kappa角调整与传统 LASIK治疗近视的对比研究中,比较了术后球差和彗差的变化量,结果表明术后变化差异无统计学意义。但在本研究中,我们发现P-Dist > 0.225 mm时,补偿75%组患者的术后残留柱镜度为(0.29 ±0.35)D,补偿100%组患者为(0.44±0.29)D,补偿75%组患者术后残余散光更少。在P-Dist >0.225 mm时,补偿100%组患者的彗差也明显高于补偿75%组。这可能由于补偿100%组患者的切削中心点与视轴的偏移量较补偿75%组患者大,或激光切削中心超过视轴中心,增加了入射的斜光束导致散光的增高从而使术后彗差增大,引起相应的眩光及对比敏感度降低等视网膜成像质量的下降。Mrochen等[18]也报道,亚临床的偏中心切削(≤1.0 mm)是导致术后彗差增大的主要原因,为了最大限度减少高阶像差,需要尽可能地使切削区靠近视轴。
Yeo等[19]认为,Kappa角越大,P-Dist越大,因此,补偿100%Kappa角时,切削中心应更接近视轴[20]。但本研究结果显示,实际与预计的视觉质量尚存在差距。推测术中的照明、情绪紧张、手术刺激、调节辐辏等引起的瞳孔中心位置的动态变化等因素参与其中。本研究进一步证实了准分子激光切削中心点位置的重要性和在不同Kappa角状态下合理定位切削中心的必要性。
本研究探讨了P-Dist分布规律,首次通过补偿75%、100%的Kappa角调整矢量比,比较术后患者的屈光度、高阶像差和对比敏感度。结果显示两组患者均不影响中心视力,等效球镜度数也无差异。但在P-Dist > 0.225 mm时,补偿75%患者的残留散光和彗差更少。综上所述,75%和100%的Kappa角调整量均能有效获得良好的术后视力,但在大Kappa角人群中度近视的个性化准分子激光手术中,选择75%的调整量可能获得更佳的视觉质量效果。本研究也有局限性,由于患者不能完全按随机对照分配,而导致组间分布不均产生混杂偏倚,以及会出现个体变异性,都可能影响研究结果。本研究还有待进一步深入研究其他Kappa角补偿的百分比差异,Kappa角补偿与视觉质量之间的对应关系仍有待于进一步探索。

