外膜内翻并翻转吻合技术的止血效果评价:倾向性评分匹配分析
高洋 史泽鹏 庄熙晶 高峰 刘巍 石磊 王文君 何学志
急性主动脉综合征(acute aortic syndrome,AAS)病情进展迅速,预后凶险,其中急性A型主动脉夹层(acute a-type aortic dissection,AAAD)围手术期死亡率及致死性并发症发生率极高,急诊手术为主要治疗手段[1]。对于主动脉根部及主动脉瓣膜交界受累病人,除加用毡片及应用主动脉瓣膜交界悬吊技术外,常需借助“残存主动脉包裹-右房分流理念”来处理,但因其违背了正常的生理血液引流方向,在存在吻合口持续渗血时,增加右心系统负荷风险。因此,外膜内翻法向内翻折主动脉外膜重塑主动脉根部更为符合主动脉正常的根部解剖对位,缝线对吻合口脆弱主动脉壁的切割力被降低,其操作更为简单易行[2]。本研究对比两种手术方式的止血效果。
对象与方法
一、对象
我院2018年1月1日~2020年4月1日收治的根部受累的急性A型主动脉夹层病人76例。纳入标准:(1)主动脉窦部受累,直径<45 mm;(2)主动脉瓣膜返流为主动脉瓣膜交界受累所致,且其返流为轻、中度;(3)病人主动脉瓣瓣膜结构、功能保存完整。排除标准:同期行其他心脏外科手术;最终拒绝手术,予药物保守治疗后出院;未转入重症监护病房行术后重症监护。所有病人中1例主动脉外膜存在破口,1例瓣膜钙化狭窄严重,7例主动脉瓣重度返流均行Bentall手术;2例病人同期行冠状动脉搭桥;3例病人要求出院;2例病人行术前准备期间死亡。最终纳入研究60例。所有病人均行急诊手术,其中20例(33.3%)应用扩大外膜内翻并翻转吻合技术处理主动脉根部,其余40例(66.67%)采用主动脉瓣膜交界悬吊合并主动脉包裹右房分流技术处理。术前一般资料见表1。本研究经本院伦理委员会批准。

表1 外膜内翻并翻转吻合技术与主动脉包裹-右房分流技术匹配前、后临床资料
二、方法
1.手术方式:所有病人均由同一名资深外科手术医生完成,体外循环采用腋动脉、股动脉及右心房二梯级管;对于循环不稳定者予以股动、静脉插管;右上肺静脉置入左心引流。术中留置心包、纵隔引流管各1枚,术后常规转入ICU行重症监护治疗。(1)外膜内翻并翻转吻合技术[3]:于升主动脉中段横断,于窦管交界水平上方0.5 cm将主动脉内膜环形横断,留存主动脉外膜将其沿三个主动脉瓣膜交界纵向剪开,根据三个主动脉窦形状将三部分主动脉外膜进行修剪,将外膜向内翻转贴敷于主动脉内膜并对位相应的冠脉窦开口,无冠窦部分外膜缝合至瓣环水平,左、右冠窦缝合至冠状动脉开口的上方,对于主动脉瓣膜交界撕脱者,予以主动脉瓣交界复位后行外膜内翻固定。后将人造血管末端外翻插入重塑后的主动脉根部内完成端端吻合(图1~3)。(2)主动脉包裹-右房分流技术:近主动脉根部半横断主动脉,保留主动脉后壁的纵向连续性,对于主动脉瓣膜交界撕脱者,予以主动脉瓣交界悬吊固定,后将人造血管与周径完整部主动脉行内嵌连续缝合,将残存主动脉壁由远心端向近心端缝合包裹人造血管至右心房侧,最后将主动脉囊腔与右心房连通完成最后分流吻合。

图2 外膜向内翻转完成缝合并复位瓣膜交界
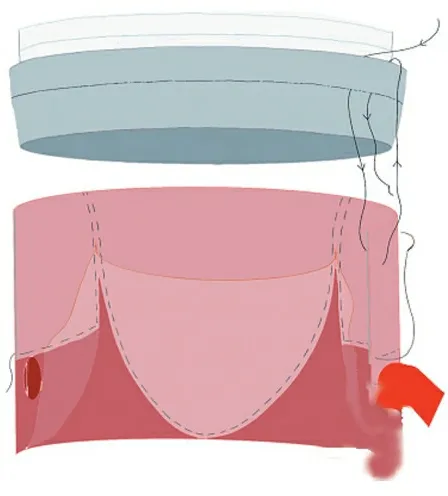
图3 人造血管外翻插入主动脉,行连续缝合
2.评估内容:术前凝血功能有无异常,记录术中体外循环时间,术后24小时内心包、纵隔引流量,围手术期24小时成分输血量、术后24小时止血药物应用等情况。
三、统计学方法
以外膜内翻并翻转吻合技术与主动脉包裹-右房分流技术为1/0二进制处理指标。以手术置换范围,是否存在凝血功能异常作为协同变量,卡钳值为0.05,应用Logistic回归模型进行倾向性匹配,配比度为1∶1,根据Ps行病例匹配,40例包裹组中共20例与外膜内翻组匹配,对比分析匹配后的两组,分析两种手术方法的止血效果。

结果
每组病人术式为:单纯升主动脉置换7例(35%),升主动脉+半弓置换6例(30%),升主动脉+主动脉弓置换+远端支架置入术7例(35%)。两组匹配后病人均无术后24小时内死亡。两组病人的心肌阻断时间、术中停循环时间、主动脉近端处理时间比较,差异无统计学意义(P>0.05)。两组病人围术期各成分输血量、二次开胸止血情况以及术后24小时内止血药物应用情况比较,差异无统计学意义(P>0.05),但外膜内翻并翻转吻合技术组24小时内引流量明显较少,差异有统计学意义(P<0.05)。见表2。24小时内两组病人每小时引流变化据95%可信区间绘制误差棒图(图4),采用非全因子模型析因分析分析其主效应及交互效应,据结果绘制交互效应轮廓图(图5),结果显示,不同手术方式及术后时间对术后24个小时内每小时引流量的主效应均不同(F=1 213.275,P=0.000;F=3 892.397,P=0.000),且手术方式及术后时间两者存在交互效应(F=72.489,P=0.000),即不同手术方式对早期24小时内每小时引流量的影响会随术后时间变化而变化。
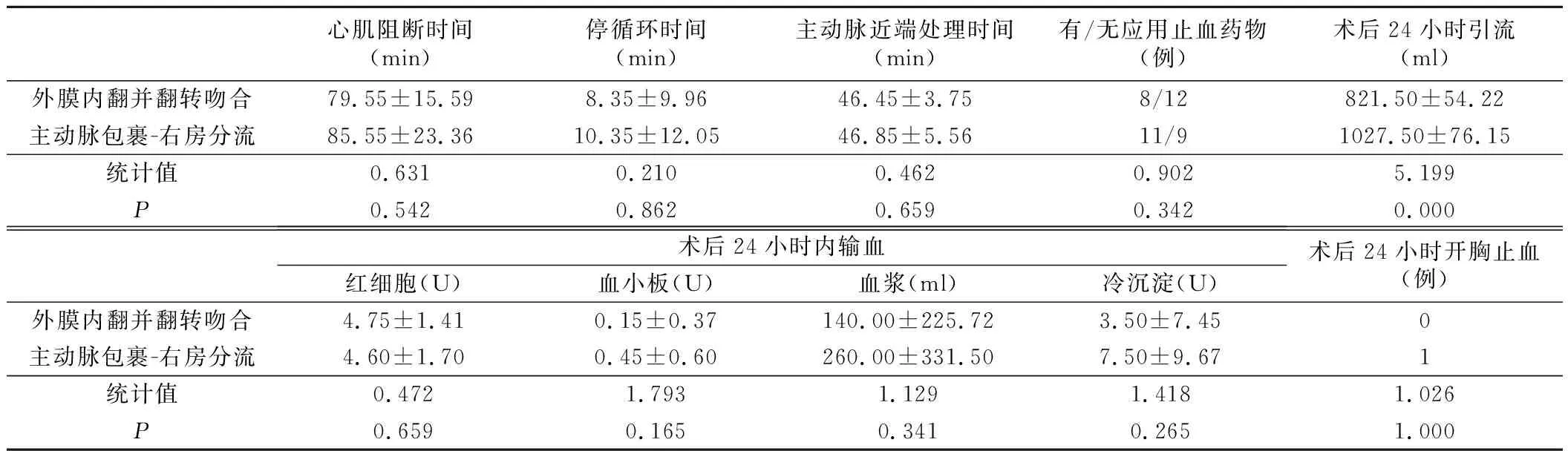
表2 两组手术相关情况
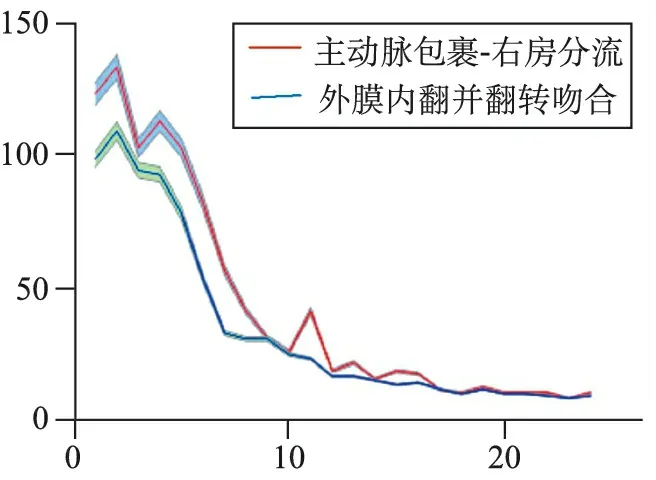
图4 24小时内引流误差棒图
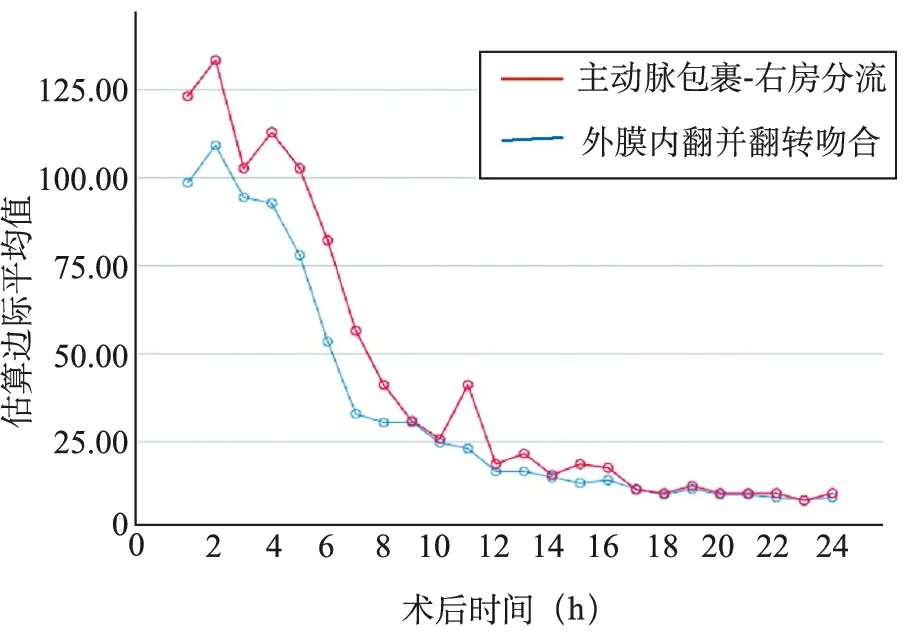
图5 交互效应轮廓图
讨论
AAAD病情凶险,不良预后风险随等待时间延长激增,急诊手术是最有效的治疗手段,但因升主动脉横跨上纵隔,病变累及的差异性使得手术尚无统一定式[3]。据孙立忠等[4]的主动脉夹层细化分型,其中A2型主动脉夹层主动脉瓣膜结构完整,部分功能尚保留,其手术复位效果十分可观,国内多年来以孙氏手术、Cabrol分流、瓣膜交界悬吊等理念相结合的手术治疗方式为主[5]。但人为构建的右房分流管道,在解剖层面并不符合正常的房室血流生理流向。同时,该手术对于主动脉根部的假腔闭合有效率以及主动脉瓣膜复位效果维持率也无法令人满意。
有研究表明,主动脉夹层围术期血小板常呈下降趋势,个体凝血平衡趋向于低凝状态,术中、术后吻合口出血的后果常是灾难性的[6]。为纠正凝血平衡,改善术后低凝状态而快速超负荷成分输血常诱发严重问题,因而强化止血技术,尽最大努力减少术中、术后失血,加强围术期血液保护变得尤为重要[7-9]。受外膜内翻技术启发,我们将翻转的外膜进一步扩大缝合至内膜上,尽可能应用外膜包埋封闭假腔加固脆弱主动脉内膜,增加手术的安全性,降低再手术率,同时借助翻转吻合技术降低缝线对于主动脉根部吻合口主动脉壁的组织切割作用,增大接触面积,有效降低了缝隙性出血的风险。本技术缝合操作简便,出血定位准确,可方便止血,人为增加组织因子(如外膜、管壁组织)的暴露机会可激活外源性凝血途径,通过激活因子X,进而产生凝血酶封闭缝合残腔并促进残留假腔血栓性闭合,同时外膜组织可填补缝合间隙,其安全性及术后效果令人满意[10-11]。
本研究中两组病人术中各成分输血量、术后初期止血药物应用情况未见明显差异,但24小时内心包、纵隔总引流量外膜内翻并翻转吻合组明显较少,提示外膜内翻法处理主动脉根部其术后初期止血效果更为理想。细化分析24小时内引流(图2),两组病人术后0~9小时内每小时引流量95%置信区间完全分开未见交集,提示两者存在显著性差异;9小时后两者置信区间间断重叠,差异变得不再显著。据非全因子模型析因分析结果,单独分析术后时间及手术方式对术后24小时内引流的影响,两种手术方式之间及术后不同时间之间均有统计学差异,即不论术后何时行外膜内翻并翻转吻合手术的病人均较另一组病人引流量少;随术后时间延长,不论何种手术方式其引流量均呈减少趋势。据交互效应轮廓图(图3)分析手术方式及术后时间之间的交互效应,2~4小时此段时间内两组的引流量差距随时间变化存在差异(两者引流量差距先变小后变大);4~7小时随时间变化两组引流量差距相对恒定,7~9小时随着时间延长两类手术方式的引流差距逐步缩小。两种术式曲线走势表明,包裹组心包纵隔引流从术后17小时起逐步平稳,而外膜内翻组则提前至术后7小时起,这也反映了外膜内翻所带来的止血效果更为即时、高效。由于样本量限制,影响术后出血因素较多,有待于扩大样本量的全因子模型进一步评估。
综上,外膜内翻并翻转吻合技术相较于传统主动脉包裹-右房分流处理技术,其主动脉根部止血效果更为理想,外膜向内翻转加固脆弱的主动脉根部内膜组织,翻转吻合削弱缝线切割作用均可有效降低术后初期吻合口的出血风险。

