非小细胞肺癌组织驱动蛋白超家族成员2A、真核起始因子3b的mRNA表达及其临床意义
邴钟兴 郑志博 张家齐
非小细胞肺癌(NSCLC)占所有肺癌组织学类型的80%~85%,预后差,寻找靶向治疗NSCLC的新靶点分子意义深远。相关研究表明,驱动蛋白超家族成员2A(KIF2A)在胃癌等恶性肿瘤组织中表达异常[1]。真核起始因子(eIFs)参与真核翻译起始过程的大多数反应,种类多且复杂,其中eIF3b结构特殊,参与调节多种典型的生物过程,如细胞周期、细胞凋亡、侵袭和迁移等[2]。本研究通过检测NSCLC癌组织中KIF2A、eIF3b mRNA表达,分析KIF2A、eIF3b mRNA表达间的相关性,探讨两者在NSCLC发生发展中的作用及临床意义。
对象与方法
一、对象
2015年1月~2016年12月于我院诊治的NSCLC病人90例。纳入标准:(1)手术达到R0切除,癌组织及癌旁正常组织(距癌周>2 cm)均经明确的细胞学和组织病理学诊断;(2)初次诊治;(3)未接受抗肿瘤治疗;(4)临床病理资料完整,签署知情同意书;(5)术前全身评估无手术禁忌证。排除标准:呼吸道感染等疾病;其他恶性肿瘤;严重的心、肝、肺、肾等脏器功能不全。本研究经本院伦理委员会审核批准。
二、方法
1.收集病人一般资料,包括年龄、性别、吸烟史、肿瘤部位、病理类型、分化程度、肿瘤大小、淋巴结转移、临床分期。
2.实时荧光定量PCR:取液氮速冻且-80 ℃冰箱保存的组织样本约30 mg,Trizol试剂(美国Invitrogen公司)提取组织总RNA;PrimeScriptTM反转录试剂盒(日本TaKaRa公司),反应条件如下:42 ℃逆转录反应20分钟,85 ℃灭活5分钟,逆转录合成cDNA,-20 ℃冰箱保存;实时荧光定量PCR仪(美国伯乐,BIO-RAD CFX96型),SYBR® Premix Ex Taq Ⅱ试剂盒(日本TaKaRa公司),引物(上海启因生物科技有限公司)序列如下,KIF2A正向引物5′-CCTGACCTTGTTCCTGATGAAG-3′,KIF2A反向引物5′-TGCTGAACCAACCACTCTATTATC-3′,eIF3b正向引物5′-CGGTGCCTTAGCGTTTGTG-3′,eIF3b反向引物5′-CGGTCCTTGTTGTTCTTCTGC-3′,内参GAPDH正向引物5′-CGACCACTTTGTCAAGCTCA-3′,内参GAPDH反向引物5′-GGTTGAGCACAGGGTACTTTATT-3′。反应条件如下:95 ℃预变性3分钟,40个循环;94 ℃变性30 s,60 ℃退火1分钟,72 ℃延伸30 s。每个样本重复实验3次,相对循环数(Ct)值方法进行数据分析,2-△△Ct计算KIF2A、eIF3b mRNA相对表达量。
3.随访:病人出院为起始,门诊复查或电话方式,随访至病人死亡或随访终止时间,随访截止时间2020年12月。
三、统计学方法

结果
1.KIF2A、eIF3b表达情况:NSCLC癌组织中KIF2A mRNA相对表达量(3.747±1.388)高于癌旁正常组织(1.424±0.565)(t=14.706,P=0.000);NSCLC癌组织中eIF3b mRNA相对表达量(4.188±1.520)高于癌旁正常组织(1.424±0.565)(t=14.532,P=0.000)。
2.KIF2A、eIF3b表达与病人临床病理特征的关系:NSCLC癌组织中,KIF2A、eIF3b mRNA表达均与病人性别、年龄、吸烟史、肿瘤部位、病理类型无关(P>0.05);KIF2A mRNA表达与分化程度、淋巴结转移及临床分期密切相关(P<0.05),与肿瘤大小无关(P>0.05);eIF3b mRNA表达与肿瘤大小、淋巴结转移及临床分期相关(P<0.05),与分化程度无关(P>0.05)。见表1。

表1 KIF2A、eIF3b表达与病人临床病理特征关系
3.KIF2A、eIF3b表达相关性:Pearson相关系数分析结果,NSCLC癌组织KIF2A mRNA、eIF3b mRNA表达呈正相关(r=0.412,PP<0.05)。
4.KIF2A、eIF3b表达与病人预后的关系:随访期间共有7例病人失访。以KIF2A mRNA相对表达量的均值(3.747)为界,分为KIF2A高表达组(42例)与KIF2A低表达组(41例)。KIF2A高表达组术后5年总生存率为23.81%(10/42),低于KIF2A低表达组60.98%(25/41)(χ2=11.752,PP<0.05)。以eIF3b mRNA相对表达量的均值(4.188)为界,分为eIF3b高表达组(41例)与eIF3b低表达组(42例)。eIF3b高表达组术后5年总生存率为26.83%(11/41),低于eIF3b低表达组57.14%(24/42)(χ2=7.818,PP<0.05)。KIF2A表达与病人预后的关系见图1。eIF3b表达与病人预后的关系见图2。
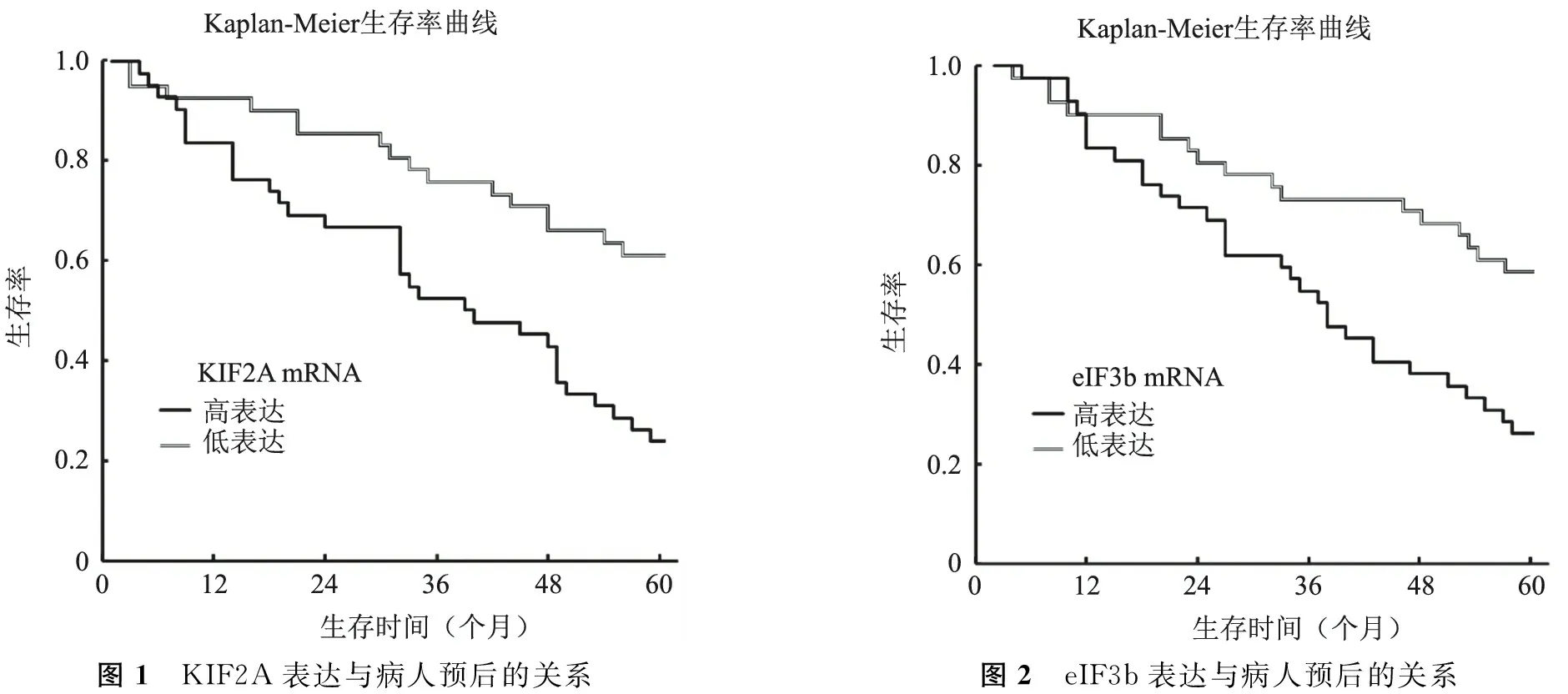
图1 KIF2A表达与病人预后的关系图2 eIF3b表达与病人预后的关系
5.Cox回归模型分析病人预后的影响因素:Cox分析结果显示,临床分期为Ⅲ期、KIF2A mRNA高表达、eIF3b mRNA高表达是病人预后的独立危险因素(P<0.05)。见表2。
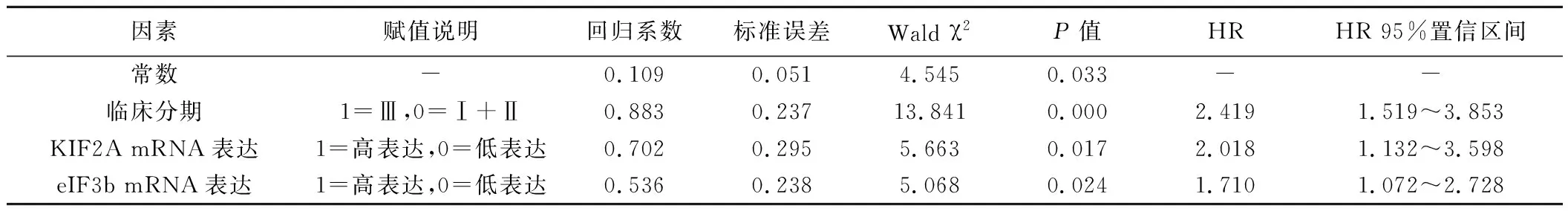
表2 病人预后影响因素分析
讨论
近年来,NSCLC病人生存率得到一定程度的提高,主要归功于分子生物靶向治疗等临床治疗方法的不断革新[3]。寻找靶向治疗NSCLC的新靶点分子,已成为众多学者关注和研究的热点[4]。肿瘤微环境中微管是构成细胞骨架的主要成分之一,其解聚及减少可导致细胞恶变、激发肿瘤恶性潜能。驱动蛋白是微管重要辅助蛋白,是影响肿瘤恶性生物学特性的诸多关键因素之一[5]。KIF2A是驱动蛋白-13家族成员,具有解聚细胞微管的功能,广泛表达于哺乳动物细胞,参与有丝分裂、胞膜运输等过程[6]。研究提示,KIF2A在癌细胞中异常高表达,参与肿瘤细胞进展、浸润及转移等过程[7]。本研究检测出NSCLC癌组织中KIF2A表达水平升高,KIF2A可能与肿瘤周围的局部浸润、侵袭及转移相关,推测KIF2A高表达可能增加微管解聚,造成细胞骨架不稳定,从而增强肿瘤细胞的局部浸润、侵袭特性,如具有抑癌功能的miR-451a靶向降低KIF2A表达,从而抑制肺鳞状细胞癌细胞的侵袭性特征[8]。KIF2A调控NSCLC癌细胞侵袭的分子机制,值得深入探究。
肿瘤细胞恶性转化过程,可能存在翻译调控异常,关于肿瘤发生发展与翻译调控失常的机制,目前尚未明确[9],参与基因翻译进程的关键因子,具有作为新抗肿瘤治疗靶点的潜能,如eIFs分子参与了蛋白翻译和细胞周期的调控及肿瘤的发生发展过程[10]。目前已鉴定12种eIFs分子(eIF1-12),其中eIF3分子量最大且结构最复杂,由13种亚基组成(eIF3a-eIF3m)。研究显示,eIF3可影响细胞周期、调控肿瘤的发生发展过程,如a、b、e和k亚基均可能参与细胞周期调控[11]。实时荧光定量PCR检测发现,eIF3b在NSCLC癌组织中呈高表达状态,与肿瘤大小、淋巴结转移及临床分期相关,揭示eIF3b参与了NSCLC细胞增殖、侵袭及迁移等恶性进展过程。eIF3b是直接参与蛋白合成的关键因子,异常高表达可能参与调控NSCLC细胞增殖、转移过程,此外关于eIF3b调控肿瘤细胞增殖机制,已有研究者证实eIF3b可能参与调控缺氧诱导因子(HIF-1),在胶质母细胞瘤细胞增殖发挥至关重要作用[12],初步推测eIF3b也可能是调控HIF-1促进NSCLC癌细胞增殖。深入研究eIF3b分子调控作用机制,可提供更直接、有效的靶点治疗新策略,是下一步研究的方向。
Kaplan-Meier生存分析显示,KIF2A高表达组、eIF3b高表达组术后5年总生存率较低,肿瘤分化程度、浸润深度、淋巴结及临床分期等多种因素影响NSCLC病人预后[13]。Cox回归模型分析结果表明,KIF2A、eIF3b有望作为预测、判断NSCLC预后的新靶点分子,具有预测病情进展、预后不良的潜能。本研究纳入的病例数较少、来源单一,仍需进行大量样本验证。
Pearson相关分析发现,NSCLC癌组织中,KIF2A mRNA、eIF3b mRNA表达呈正相关性,提示两者在促进NSCLC发生过程中发挥协同促进作用,但因实验条件有限,本研究未对组织样本KIF2A、eIF3b蛋白表达进行检测。后续仍需要进一步研究KIF2A、eIF3b在NSCLC发生发展中的分子机制,为临床靶向药物的开发提供前瞻性研究。
综上,KIF2A mRNA、eIF3b mRNA在NSCLC癌组织表达增加,与病人较差临床病理特征有关,均是影响NSCLC病人预后的危险因素,KIF2A及eIF3b具有作为NSCLC疾病进展及预后评估的新靶点分子的潜力,有望为NSCLC病情进展以及治疗提供新途径。

