不同年龄胆道闭锁患儿行腹腔镜下肝门暴露术的效果及预后比较
蔡久英,王忍,李炳,夏顺林,黄霞,孟红艳
(淮安市妇幼保健院小儿外科,江苏 淮安 223002)
胆道闭锁是一种胆管病变,可累及肝内外胆管,多伴有肝纤维化,随着病情进展最终可导致肝硬化,亚洲发病率约为1∶5 000[1-2]。胆道闭锁是新生儿期发生梗阻性黄疸的主要原因,若未得到及时治疗可能因病情发展为肝硬化甚至肝衰竭,严重威胁患儿的生命安全[3]。目前手术是治疗胆道闭锁的重要手段,肝门空肠吻合术可有效解除胆道闭锁患儿胆道梗阻症状,减缓肝纤维化进程,延长自体肝生存时间,提高患儿生存率,是临床应用较为广泛的术式[4]。肝门空肠吻合术治疗的关键在于手术彻底切除患儿肝门纤维块,但多数患儿因胆道闭锁导致肝脏肿大,肝门暴露较为困难,影响肝门纤维块的分离及切除,手术难度增加,影响疗效,因此术中需要充分应用肝门暴露技术[5-6]。肝门暴露充分可以协助医师正确有效地实施肝门肠吻合术。不同年龄段胆道闭锁患儿手术治疗效果不一,目前临床关于肝门暴露技术对不同年龄段胆道闭锁患儿预后影响的相关研究较少。本研究主要探讨腹腔镜下肝门暴露技术在胆道闭锁婴儿治疗中的效果及对患儿预后的影响。
1 资料与方法
1.1一般资料 选择2012年1月至2020年3月淮安市妇幼保健院收治的66例胆道闭锁患儿为研究对象,均采用腹腔镜下肝门肠吻合术治疗,术中充分应用肝门暴露技术。纳入标准:①经腹腔镜及超声等影像学检查确诊为胆道闭锁;②年龄30~120 d;③体重>2.5 kg,肝功能评级为A级或B级,可耐受手术;④无严重心血管疾病。排除标准:①合并严重血液系统及神经系统疾病者;②伴有门静脉高压及消化系统出血者;③合并其他严重先天性畸形者;④无法配合本研究者。上述按患儿年龄不同分为30~60 d组(20例)、>60~90 d组(28例)、>90~120 d组(18例),三组患儿基线资料比较差异无统计学意义(P>0.05),见表1。本研究通过江苏省淮安市妇幼保健院伦理委员会批准,患儿家属均签署了知情同意书。
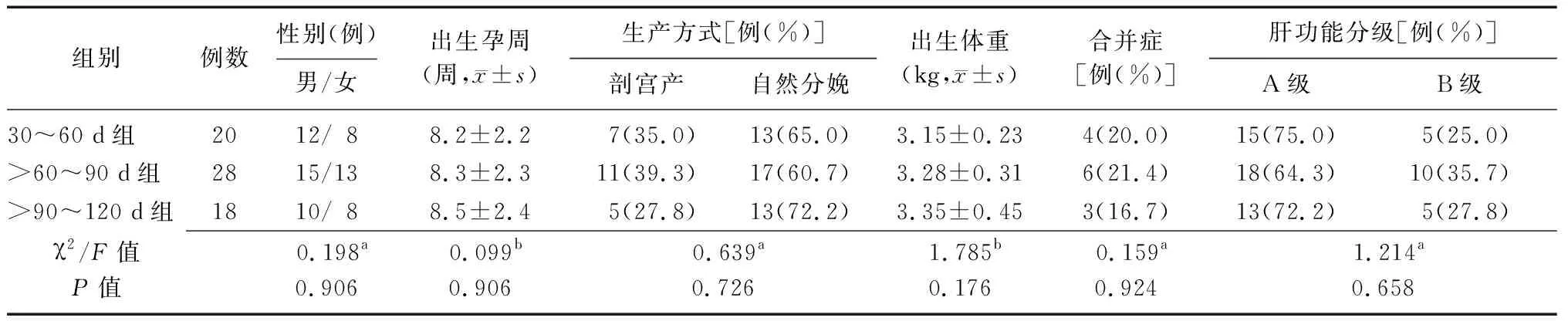
表1 不同年龄段胆道闭锁患儿基线资料比较
1.2治疗方法 患儿取仰卧位,予以气管插管麻醉,于脐部正中做一约5 mm纵向切口,开放式进入腹腔,置入trocar,建立气腹(压力6~8 mmHg)(1 mmHg=0.133 kPa),置入腹腔镜。通过腹腔镜观察患儿肝脏纤维化严重程度、肝门是否出现水肿、胆囊大小及位置等情况。于右上腹肋缘下置入5 mm trocar,在腹腔镜下从trocar孔处将胆囊提出,将胆囊底部切开后,插管固定。将泛影葡胺注入行胆道造影以明确诊断。于右中下腹及左上腹分别置入3 mm trocar,于剑突下以皮缝线将肝圆韧带缝合,提拉缝线将肝脏抬起,将胆囊以电凝钩游离,缝合胆囊床纤维组织,提拉缝线,进一步暴露肝门。若肝脏肿大较为明显,可切除部分肝方叶,游离胆总管以显示肝门纤维块,解剖肝脏周围动静脉,分别游离与离断血管分支(门静脉至肝脏纤维块)。门静脉后缘充分游离后可见其与肝脏表面呈分离状态,采用弹性带在门静脉右支后缘穿过,使其环绕门静脉右支和肝右动脉,最后将弹性带由右中下腹孔穿出体外。门静脉左支及肝左动脉采取同样步骤由左上腹孔穿出体外。上述步骤完成后助手协助牵拉双侧弹性带以充分暴露肝门纤维块,镜下将肝门纤维块彻底切除,以纱布条于切缘压迫止血,肝门纤维块切除后,可见有胆汁溢出。随后将脐部切口扩至约1.5 cm,将空肠近端拉至体外横断空肠(距屈氏韧带约10 cm),并切开空肠使其与近端空肠行端吻合(距封闭端20 cm),吻合完成后将肠管放回腹腔,经结肠将肝支空肠拉至肝门,将肝支空肠的对系膜侧肠壁切开约2.0 cm切口,采用PDS线缝合吻合后壁及前壁,术后不置引流管。
1.3观察指标及评定标准 统计并比较三组患儿手术相关情况,包括手术成功率、手术时间、术中出血量及并发症发生情况。
比较三组肝纤维化程度及胆管反应程度。将术中搜集肝脏组织标本以Masson三色染色法染色,通过光学显微镜观察肝脏纤维化程度,无纤维化为0级;肝汇管区域出现轻度纤维化为Ⅰ级;邻近汇管区域出现轻度纤维化为Ⅱ级;邻近汇管区域呈现重度纤维化则为Ⅲ级;出现肝硬化及肝假小叶为Ⅳ级[7]。采用角蛋白19(鼠抗人细胞角蛋白19抗体,湖南艾佳生物科技有限公司生产)对肝脏病理标本进行染色,光学显微镜下随机保留3张不同区域图像(单张图像面积为0.097 mm2),利用生物分析软件进行分析,获得胆管染色强阳性区域面积与总面积占比,取胆管面积占比平均值表示胆管反应程度[8]。
术后随访6个月,比较各组患儿术后总胆红素水平、黄疸消退率。分别于术前、术后2周及术后6个月抽取患儿外周静脉血3 mL,采用全自动生化分析仪检测患儿血清总胆红素水平。黄疸完全消退:术后总胆红素水平降至20 μmol/L以下。黄疸消退率:各组黄疸完全消退患儿占相应组的比例。

2 结 果
2.1不同年龄段患儿手术相关情况比较 三组患儿腹腔镜下肝门吻合术手术成功率、手术时间、术中出血量及并发症发生率比较差异均无统计学意义(P>0.05),见表2。
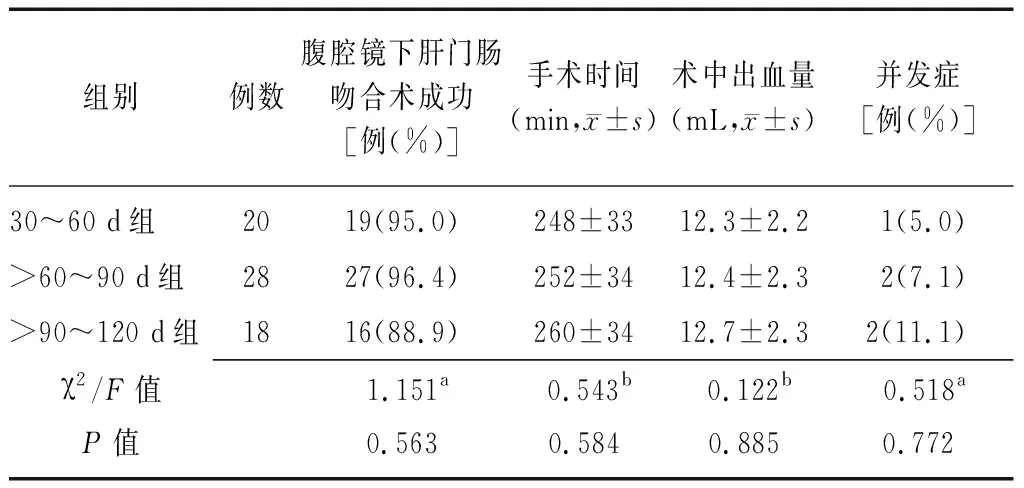
表2 不同年龄段胆道闭锁患儿手术相关情况比较
2.2不同年龄段患儿肝纤维化程度及胆管反应程度比较 三组患儿肝纤维化程度及胆管反应程度比较差异有统计学意义(P<0.01),>60~90 d组和>90~120 d组肝纤维化程度重于30~60 d组(Z=3.267,P=0.008;Z=3.625,P=0.010),>90~120 d组重于>60~90 d组(Z=4.128,P=0.015);>60~90 d组和>90~120 d组胆管面积占比大于30~60 d组(P<0.05),>90~120 d组大于>60~90 d组(P<0.05)。见表3。
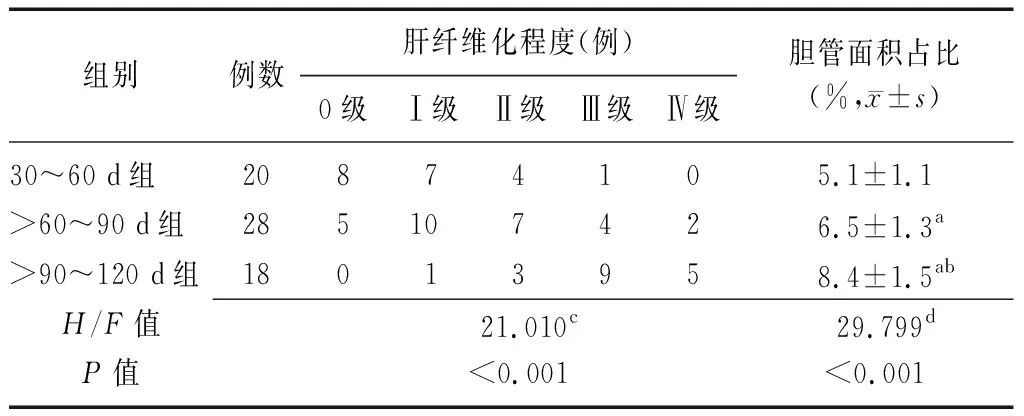
表3 不同年龄段胆道闭锁患儿肝纤维化程度及胆管反应程度比较
2.3不同年龄段患儿术后总胆红素、黄疸消退率比较 总胆红素不同时点间的主效应差异有统计学意义(P<0.01),术前、术后2周及术后6个月三组总胆红素水平呈下降趋势,组间及组间与时间点交互作用比较差异无统计学意义(P>0.05),见表4。术后2周,三组黄疸消退率比较差异有统计学意义(P<0.05),>60~90 d组和>90~120 d组黄疸消退率低于30~60 d组(P<0.05),>90~120 d组低于>60~90 d组(P<0.05);术后6个月,三组黄疸消退率比较差异无统计学意义(P>0.05),见表5。
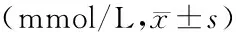
表4 不同年龄段胆道闭锁患儿手术前后总胆红素比较
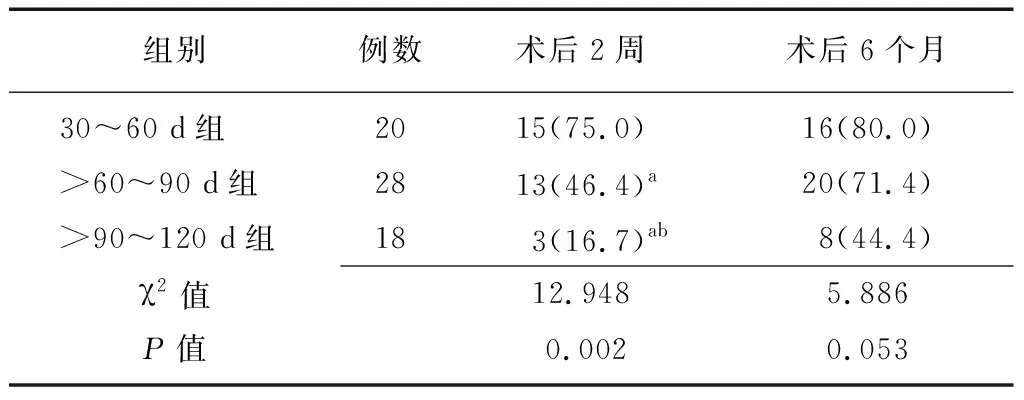
表5 不同年龄段胆道闭锁患儿术后黄疸消退率比较 [例(%)]
3 讨 论
胆道闭锁指肝内、外胆管发育不完整,导致胆汁无法有效排出而淤积,最终造成阻塞性黄疸,早期主要临床表现为严重性黄疸、肝脾大等,目前发病机制尚未完全明确,多与病毒及自身免疫相互作用,基因、胆管发育突变等有关[9-11]。胆道闭锁患儿肝脏病理改变特征明显,在光镜下可见胆汁淤积或形成胆栓,小胆管出现增生反应,汇管区可出现炎症细胞浸润及水肿[12]。若胆道闭锁患儿未得到及时治疗其肝纤维化可最终进展为肝硬化、门静脉高压等,最终导致患儿死亡[13]。肝门空肠吻合术是广泛应用于治疗胆道闭锁的手术方法,可延长患儿自体肝生存时间[14]。但术中门静脉游离或暴露不彻底,可能在切除纤维块时发生出血,吻合困难,因此术中肝门暴露情况仍是手术中的首要问题。
本研究采用腹腔镜下牵拉缝线托举肝脏及充分游离门静脉并牵拉暴露肝门,部分肝脏明显肿大患儿选择切除肝门前部分肝方叶以达到充分暴露肝门的目的,这些暴露肝门技术可最大限度地降低肝门纤维块切除所致的出血风险,便于肝门肠吻合术的实施。其次,腹腔镜手术对患儿机体损伤较小,可提高手术安全性,降低中转手术率[15]。本研究中三组患儿手术成功率、手术时间、术中出血量及并发症发生率比较差异无统计学意义(P>0.05),提示胆道闭锁患儿行腹腔镜下肝门暴露技术安全可行。胆管反应是指胆管细胞增生肿胀,可导致胆管出现分支或管腔增宽,引起胆管面积变大,胆汁淤积,胆间质损害[16-17]。冯佳燕等[18]研究显示,胆管反应程度影响胆道闭锁患儿预后。本研究结果显示,随着年龄增长患儿肝纤维化程度及胆管反应程度逐渐加重,提示肝纤维化程度及胆管反应程度与患儿手术年龄有关,越早进行手术治疗患儿肝纤维化及胆管反应程度越低,与上述研究观点基本一致。故建议胆道闭锁患儿尽早行手术治疗,引流胆汁以减轻胆管反应,从而延缓肝纤维化进展速度,改善患儿预后。
研究表明,90 d内是胆道闭锁患儿行手术治疗的最佳年龄段[19]。但Davenport等[20]研究表明,≥100 d胆道闭锁患儿行手术治疗预后较好,其自体肝生存率约为45%。本研究结果显示,术后6个月三组总胆红素水平低于术后2周,术后2周及术后6个月三组总胆红素水平比较差异无统计学意义(P>0.05);随着年龄的增长黄疸消退率逐渐下降,提示手术治疗中腹腔镜下肝门暴露技术可明显改善总胆红素水平,但不同年龄段患儿差异不明显;本研究结果与李艳阳等[21]的研究观点基本一致。故针对胆道闭锁患儿应及时行手术治疗,进行胆汁引流,提高黄疸消退率,可能逆转患儿胆管反应,延缓患儿肝硬化进程,从而改善患儿预后。
综上所述,胆道闭锁患儿应用腹腔镜下肝门暴露技术有助于完成腹腔镜下肝门肠吻合术,降低中转手术率,胆道闭锁患儿尽早治疗,对其预后有积极作用。但本研究仍有一定不足,如样本量较少,随访时间较短,并未进行远期预后观察,下一步研究将扩大样本量,延长随访时间,并深入探讨胆管反应促进肝纤维化的具体发生机制等,以为胆道闭锁患儿的治疗提供更科学、有效的临床参考依据。

