聚丙烯酰胺(PAM)及有机螯合剂对土壤镉有效性的影响
周 青,谭长银,曹雪莹,郭 瑞,彭 曦,邓月强,柏 佳,杨晶柳
(1.湖南师范大学资源与环境科学学院,湖南师范大学环境重金属污染机理及生态修复重点实验室,中国 长沙 410081;2.长沙学院乡村振兴研究院,中国 长沙 410022)
当前我国土壤环境状况总体不容乐观,部分地区农田土壤污染严重,农产品产地环境质量堪忧。全国土壤环境质量调查公报显示,我国耕地污染点位超标率为19.4%,其中重金属占16.1%,土壤Cd的点位超标率达到7.0%[1]。我国农田主要超标重金属元素为镉 (Cd),且以中轻度污染为主,因此开展中轻度Cd污染稻田的修复研究对保障我国农产品产地环境安全具有重要意义[2]。
从修复原理上看,重金属污染农田土壤有物理、化学和生物修复等技术措施。植物修复被认为是一种环境友好、成本低、不会对土壤肥力造成不良影响的修复技术。但如何提高植物修复效率、缩短污染土壤的修复周期是植物修复过程中亟待解决的重要课题。化学措施对植物修复技术的强化是提高植物修复效率的有效措施之一。在化学改良剂强化植物修复的实践中,有机螯合剂在重金属污染农田土壤修复实践中应用较为广泛。螯合剂进入土壤后,与土壤重金属离子发生螯合作用,形成水溶性金属-螯合剂络合物,从而活化土壤中的重金属,有利于土壤重金属的植物吸收并从土壤中移除[3]。常用的化学改良剂包括柠檬酸(CA)、乙二胺四乙酸二钠(EDTA)、乙二胺二琥珀酸(EDDS)和谷氨酸N,N-二乙酸四钠(GLDA)。CA具有表面活性剂的性能,溶解度高,可被生物降解,还能改善土壤结构[4]。EDTA能够活化Pb,Zn,Cd,Cu,Co及Ni等多种重金属离子,促进植物的吸收,但其生物可降解性差,容易造成二次污染[5]。EDDS作为一种可生物降解且低毒的螯合剂,对土壤Cd有一定的活化效果,但其活化能力远远低于EDTA[3]。GLDA主要作为清洁剂、工业洗涤剂等使用,成本较低,在环境保护方面主要用于废水、工业污泥等方面,具有优良的生物降解性,且不会对生物体构成健康风险[6]。PAM作为一种性能优良的高分子聚合物,具有一定生物降解性且不会造成二次污染,对土壤重金属离子有较强的吸附作用[7]。余高等将高分子聚合物PAM与钝化剂复配来钝化土壤重金属Hg,发现与施用单一钝化剂相比,添加PAM的钝化剂更能有效吸附、固定土壤中的Hg[8]。PAM因其特殊的结构和性能,广泛应用于采收石油、水土保持和土壤改良,作为土壤重金属污染修复材料有广阔的应用前景[9,10]。PAM在土壤重金属污染植物修复领域的研究是国内外学者的研究焦点,PAM施用后对不同重金属与修复植物的差别化效应问题仍待解答[7]。从技术思路上看,重金属污染土壤的修复主要有两个方向,一是对土壤重金属的活化,以利于提高植物修复效率;另一个是通过钝化实现污染土壤的安全利用。因此,PAM及有机螯合剂对土壤重金属的活化或钝化效应研究在理论上可以加深对土壤重金属环境行为的理解,在实践上可以为发展重金属污染土壤的实用修复技术提供指导。
本研究以不同浓度的PAM与几种主要有机螯合剂为材料,筛选出对土壤重金属活化效率最高的有机螯合剂及其最佳施用浓度,为后期植物修复强化技术研究提供依据;同时,PAM与有机螯合剂对土壤重金属Cd的作用效果的比较研究可以为重金属污染农田土壤的安全利用提供技术支撑。
1 材料与方法
1.1 供试材料
供试土样采自株洲市清水塘石峰区,为第四纪红色黏土发育的水稻土(红黄泥)。土壤pH值为4.52。总Cd质量比为2.012 μg·g-1,是国家《土壤环境质量 农用地土壤污染风险管控标准(试行)》(GB15618-2018)风险筛选值(pH≤5.5,Cd 0.3 μg·g-1)的6.7倍[11],土壤Cd污染严重。
供试试剂:PAM(聚丙烯酰胺),CA(柠檬酸),EDTA(乙二胺四乙酸二钠),EDDS (乙二胺二琥珀酸),GLDA (谷氨酸N,N-二乙酸四钠),均为分析纯试剂。
1.2 试验设计
土培实验在湖南师范大学环境重金属污染机理及生态修复重点实验室内进行,试验设计见表1。称取200 g干土(过0.15 mm筛)放入250 mL的烧杯中,按20%的土壤含水率,将试剂溶液与干土混合,搅拌均匀。以不加化学试剂的超纯水作为对照(CK)。综合考虑已有的研究结果和不同螯合剂的性质,确定添加螯合剂的浓度梯度为3,6,12 μmol·g-1[12,13]。为寻求PAM产生效果的最佳浓度区间,增加24,48 μmol·g-1两个浓度。共18个处理,每个处理重复3次,使用塑料薄膜将烧杯封口保存,完成土壤样品的制备。由于土壤样品培养期间水分蒸发旺盛,土壤每7 d补水1次,连续培养42 d,妥善保存土壤样本。采取动态监测取样方法,采样时间为第2天、第5天、第10 天、第15天、第42天结束时。
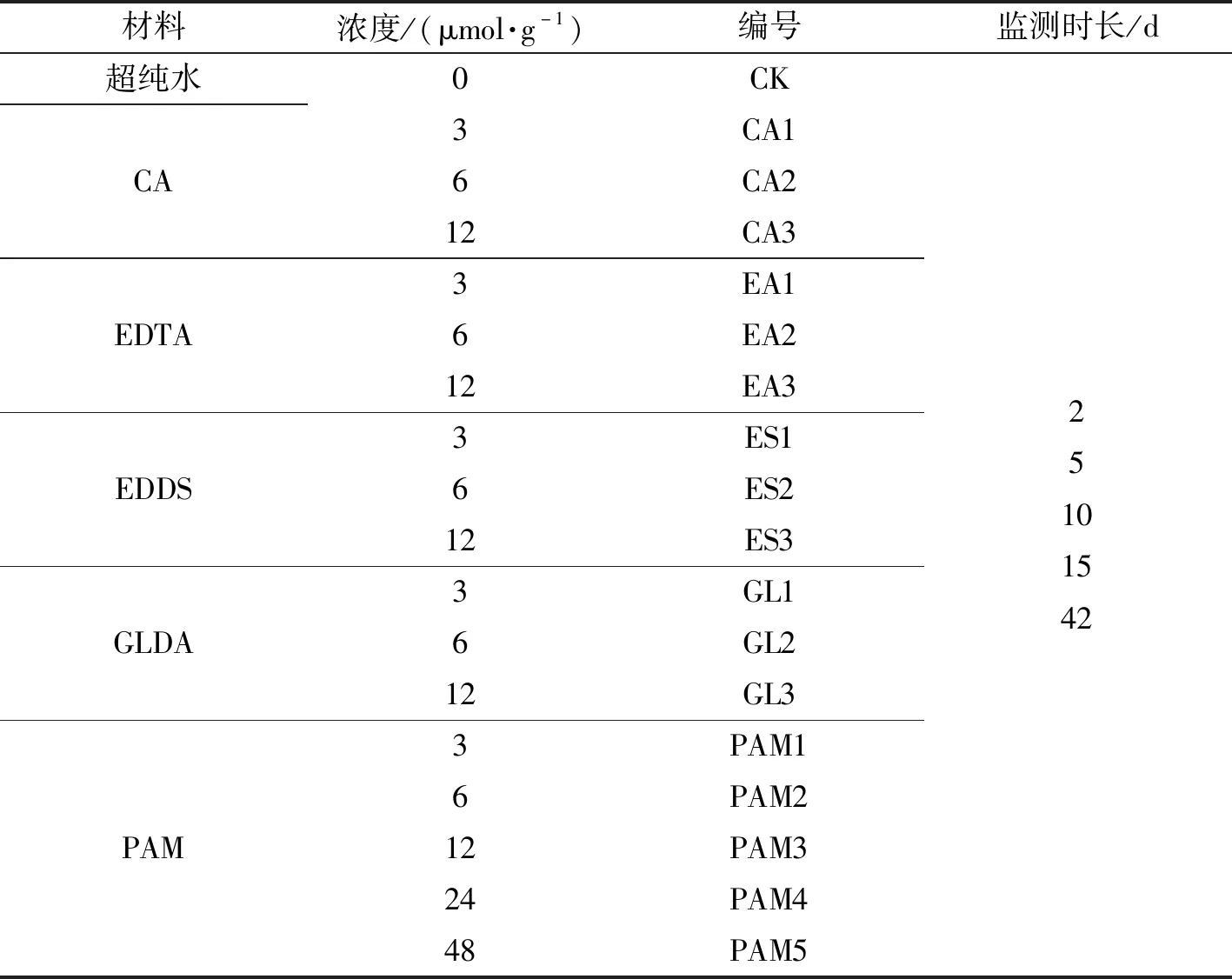
表1 试验设计Tab. 1 Test design
1.3 样品采集与分析
采样之前,将烧杯内的土壤搅拌均匀。使用药匙取用8 g土壤样品于50 mL的烧杯中,用于测定土壤pH值;称量5 g土壤样品于50 mL的离心管,用于测定土壤重金属有效态。
土壤pH以土水比为1∶2.5(g·mL-1)比例配制,采用pHs-4CT型数字酸度计测定[14]。土壤重金属全量测定采用美国EPA标准方法(US EPA3051a)消解,以HNO3和HCl消化土壤样品,微波消解仪(CEM MAR S6,Matthews,NC,USA)中消解。土壤有效态重金属质量比采用0.05 mol·L-1DTPA 浸提法。重金属质量比采用原子吸收光谱仪(PinAAcle 900T)测定,用国家标准物质(GSS-27-1,GBE-361)进行质量控制。
1.4 数据分析方法
应用Microsoft Excel 2010和SPSS 20.0进行数据处理;通过单因素方差分析计算样品pH值与土壤镉有效态的标准差和均值,应用ANOVA中Duncan多重比较评价进行不同处理对土壤pH值的显著性分析;采用Origin 9.0软件绘制图表。
2 结果与分析
2.1 PAM及有机螯合剂对土壤pH值的影响
由表2可知,随着培养时间的增加,第15天各处理的土壤pH值达到峰值,与对照组CK(4.55±0.01)相比均有明显提升;经PAM处理的土壤在第10天pH值达到最小值,与其他培养时间段相比具有显著差异。其他处理的土壤pH值时间差异不明显。
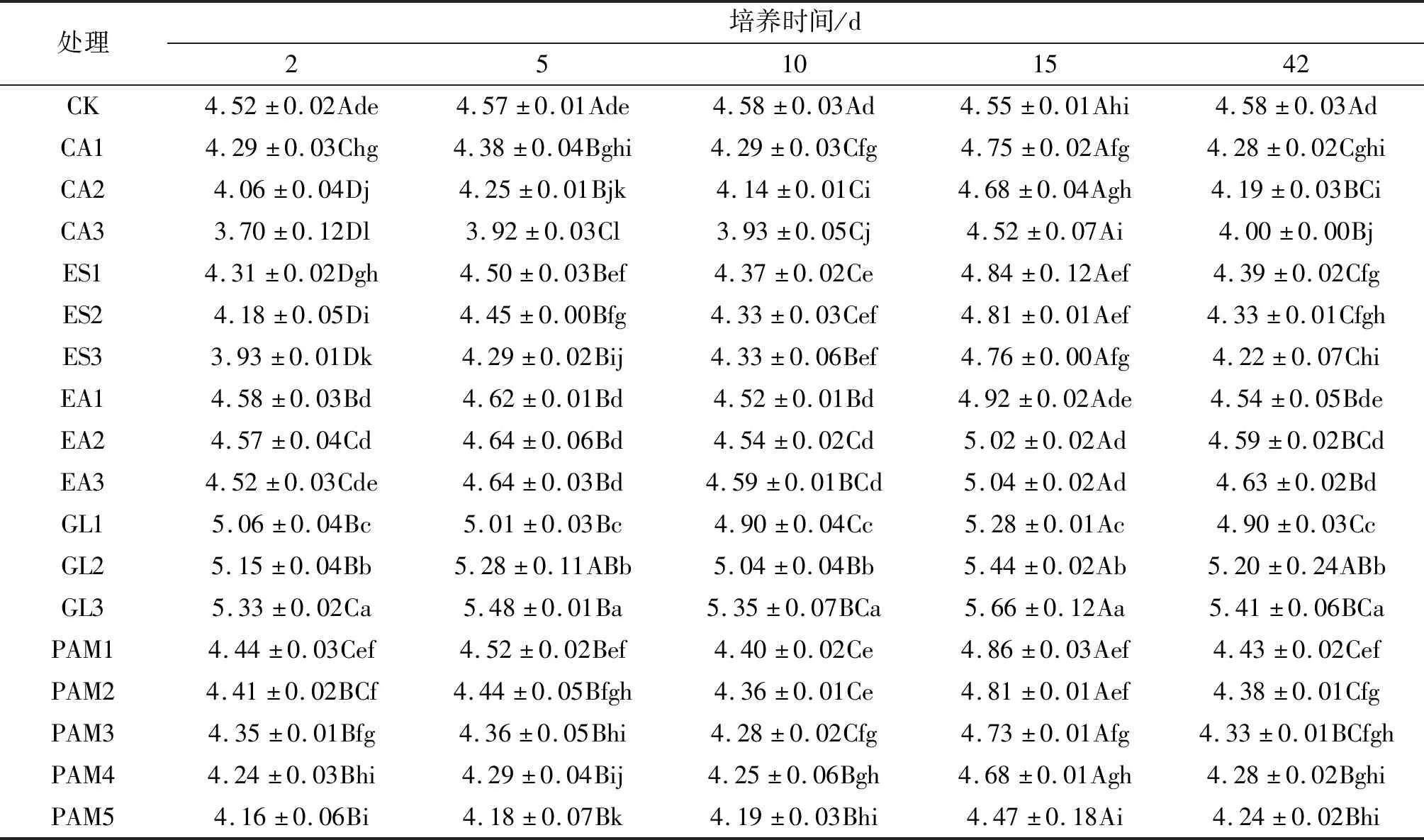
表2 PAM及有机螯合剂对土壤pH值的影响Tab. 2 Effects of PAM and organic chelating agents on the soil pH
与CK相比,CA3和PAM5处理的土壤pH均有显著下降。以培养第10天为例,CA3和PAM5的pH值分别较CK下降0.65及0.39,差异均显著,其中CA3(添加浓度最高)土壤pH值最低,因为CA是一种强酸,在土壤溶液中能够电离出H+离子,从而降低土壤pH值。PAM的分子结构中含有—CONH2,能够与土壤中的OH-离子结合,因此在一定程度上会使土壤pH值降低,但由于—CONH2属于弱电解质,能吸附的OH-离子较少,故酸化作用不及CA明显。这与徐晓春等的研究结论相似,添加PAM不会造成土壤基质pH值的根本性变化[15]。
与CK相比,GL1,GL2及GL3处理的土壤pH均有显著增加。培养第10天,GL1,GL2及GL3的pH值分别较CK增加0.33,0.46及0.77,差异均显著,其中GL3处理(GLDA用量最多)土壤pH值最高,这与卫泽斌等[16]的土壤培养试验结果相似,即施加GLDA后土壤pH值升高。其原因可能是,GLDA分子结构中含有4个羧酸基团(—COO—),能够与土壤中的H+离子结合,因此GLDA的碱性会在一定程度上使土壤pH值升高。
2.2 PAM及有机螯合剂对土壤有效态镉质量比的影响
2.2.1 PAM对土壤有效态Cd质量比的影响 图1所示为不同浓度的PAM处理下土壤中有效态Cd的质量比。由图1可知,在整个培养期间,土壤Cd有效性随PAM添加浓度增加变化幅度较大。观察CK到12 μmol·g-1这一段曲线,与CK相比,第2~10天的Cd有效性下降,说明培养初期PAM对土壤重金属离子起一定吸附作用。添加浓度为3 μmol·g-1时,第5天PAM处理效果显著,与CK相比降低了4.32%;添加浓度为6和12 μmol·g-1时,第2天的处理效果显著,与CK相比分别降低了5.20%和1.32%。第10~42天,土壤Cd有效性上升,其中第42天活化效果最佳,与CK相比增加了8.03%,7.04%及5.42%。当浓度较低(3~12 μmol·g-1)时,PAM呈现钝化效果,随着时间的推移,钝化作用减弱,逐渐变为活化。可能是因为PAM的生物降解,其吸附作用弱化,PAM吸附土壤Cd离子的能力不稳定,培养后期PAM吸附的Cd离子释放到土壤中。
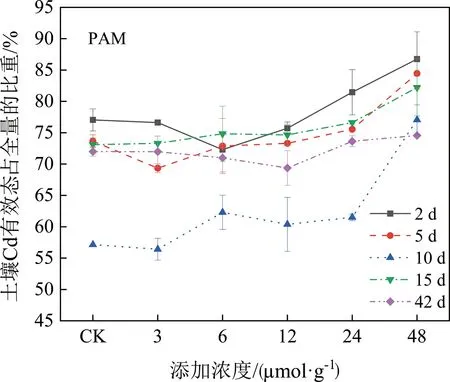
图1 不同浓度的PAM处理下土壤中有效态Cd的质量比Fig. 1 The contents of available Cd in soils treated with different concentrations of PAM
PAM添加浓度为3~12 μmol·g-1时,PAM对有效态Cd起吸附作用,土壤Cd有效性与CK相比分别降低了0.42%,5.20%及1.32%。添加浓度为24和48 μmol·g-1时,PAM对有效态Cd起活化作用,土壤Cd有效性与CK相比增加了4.42%和9.71%。由此可见PAM随浓度的增大由钝化转向活化,且浓度越高,活化效果越强。因此,PAM活化效果最佳的添加浓度为48 μmol·g-1。
综上所述,PAM的吸附能力和活化属性相对复杂,主要受添加浓度和培养时间的影响,且这两个因素存在一定的替代作用,即较短的培养时间、较高的添加浓度与较长的培养时间、较低的添加浓度,这两种条件下的活化作用效果相似。
2.2.2 有机螯合剂对土壤有效态Cd质量比的影响 图2所示为不同浓度的有机螯合剂处理下土壤中有效态Cd的质量比。由图2可知,在培养期前10天,当CA添加浓度较低(3 μmol·g-1)时,对Cd的活化作用不明显,随着CA浓度的增大,对Cd的活化作用加强。当添加CA浓度为12 μmol·g-1时,对Cd的活化效果最佳,与CK相比,分别增加了11.98%,5.41%,6.72%,14.88%及23.41%。
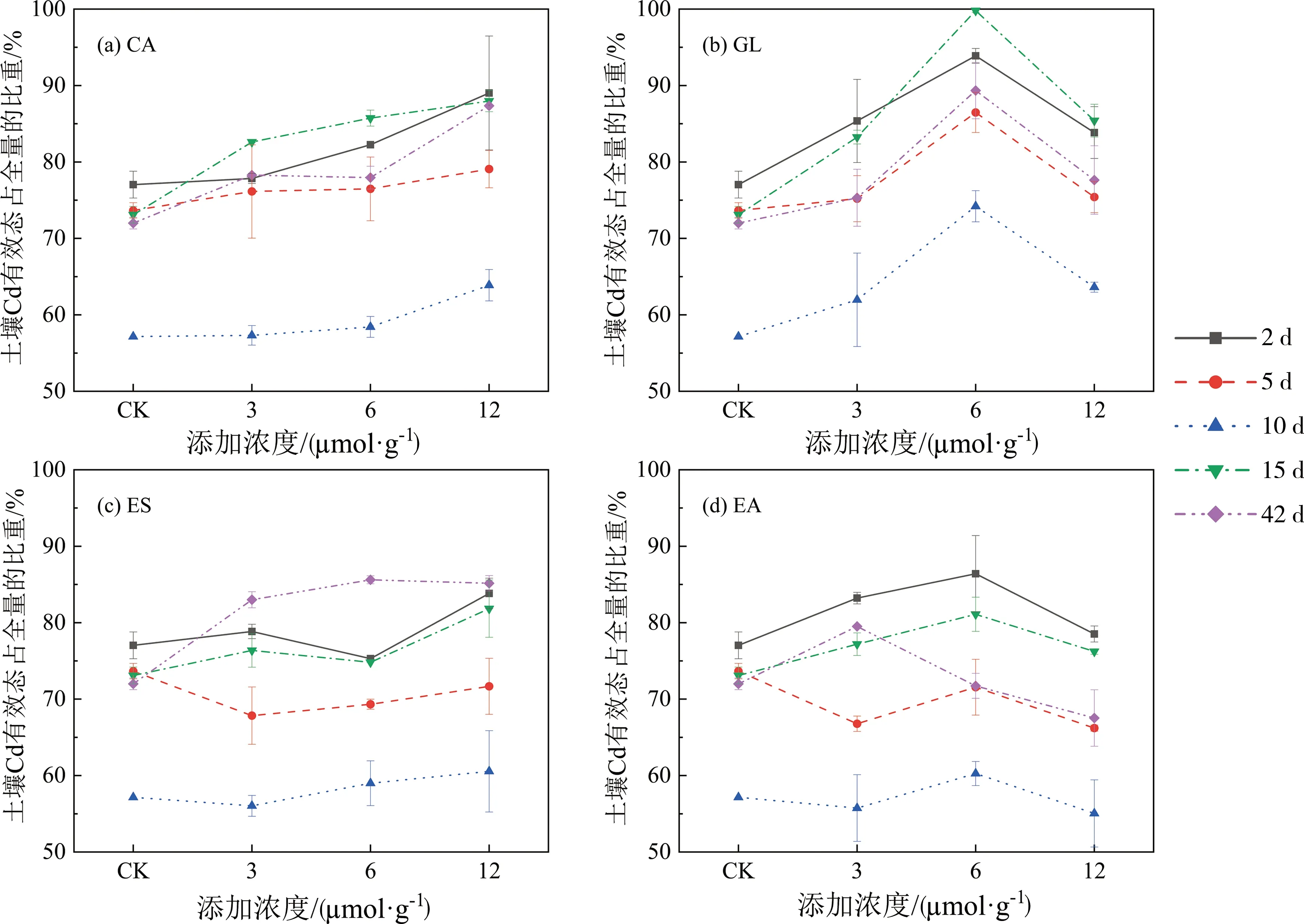
图2 不同浓度的有机螯合剂处理下土壤中有效态Cd的质量比Fig. 2 The contents of available Cd in soils treated with different concentrations of organic chelating agents
在整个培养期间,土壤Cd有效性随GLDA添加浓度的增大呈现先增后减的趋势。在添加浓度为6 μmol·g-1时,土壤Cd有效性达到峰值;继续增大GLDA添加浓度,土壤Cd有效态含量下降。添加浓度为6 μmol·g-1的土壤Cd有效性与CK比较,分别增加了16.85%,12.82%,17.05%,26.71%及25.39%,对Cd的活化效果最佳。
(二)开展生活化问题教学,以此发展学生的数学能力。由于初中数学这门课程中涉及到较多的定理,在这种情况下,就需要教师立足于实际生活,为学生创设问题情境。这样,既能够有效激发学生的学习动机,同时还会促使其学会构建新的知识。
在EDDS处理下,土壤Cd有效性随培养时间的增加而增加,在第42天土壤Cd有效性最高,与CK相比分别增加了19.06%,21.66%及21.21%。土壤Cd有效性整体呈现随着EDDS添加浓度的增大而增大的趋势,添加浓度为12 μmol·g-1的EDDS与CK相比分别增加了6.79%,1.64%,3.39%,8.74%及21.21%,对Cd的活化作用最佳。
Cd的活化量总体呈随着EDTA添加浓度的增大而增大的趋势。当EDTA添加浓度为3 μmol·g-1时,第5天和第10天存在Cd有效性下降的情况,可能是由于作用时间过短还未形成稳定的络合物,但随着时间的增加,Cd有效性呈现上升趋势。当EDTA添加浓度为12 μmol·g-1时,对Cd的活化作用最明显,与CK相比,分别增加了9.36%,3.11%,8%及7.79%。这与陈晓婷等[17]的研究结果是相似的。Cd的提取效率随着EDTA浓度的提高而提高,主要原因是EDTA与重金属之间发生配位作用,在土壤pH<6的条件下,大多数的Cd与EDTA络合形成CdEDTA2-,CdEDTA2-在不同表面电荷的土壤上产生静电作用的非专性吸附,使得表面持有负电荷的土壤对镉吸收受阻,从而降低土壤对镉的吸附,导致镉在土-水界面上的分配减小[18,19]。
2.2.3 PAM与有机螯合剂对土壤中镉活化效果的比较 在不同试剂最佳浓度的条件下对不同的处理进行比较,由图3可知,从整体来看,对Cd的活化强弱顺序:GL2>PAM5>CA3>ES3≈EA3。在整个培养期间,GL2显著增加了土壤Cd有效性,与CK相比分别增加了16.85%,12.82%,17.05%,26.71%及25.39%,差异均达到显著水平。GL2处理随着时间的增加效果愈佳,说明其持久性和稳定性良好,这与廖华[20]的研究相似。在培养期前10天,PAM5处理对土壤Cd的有效态质量比差异达到显著水平,与CK相比,分别增加了12.58%,13.18%及34.64%。培养15和42 d,PAM5处理对增加土壤Cd有效态质量比的效果不佳,可能是因为PAM在土壤中易分解,后期活化作用减弱。除GL2和PAM5处理之外,其他处理的Cd有效态质量比差异不显著。
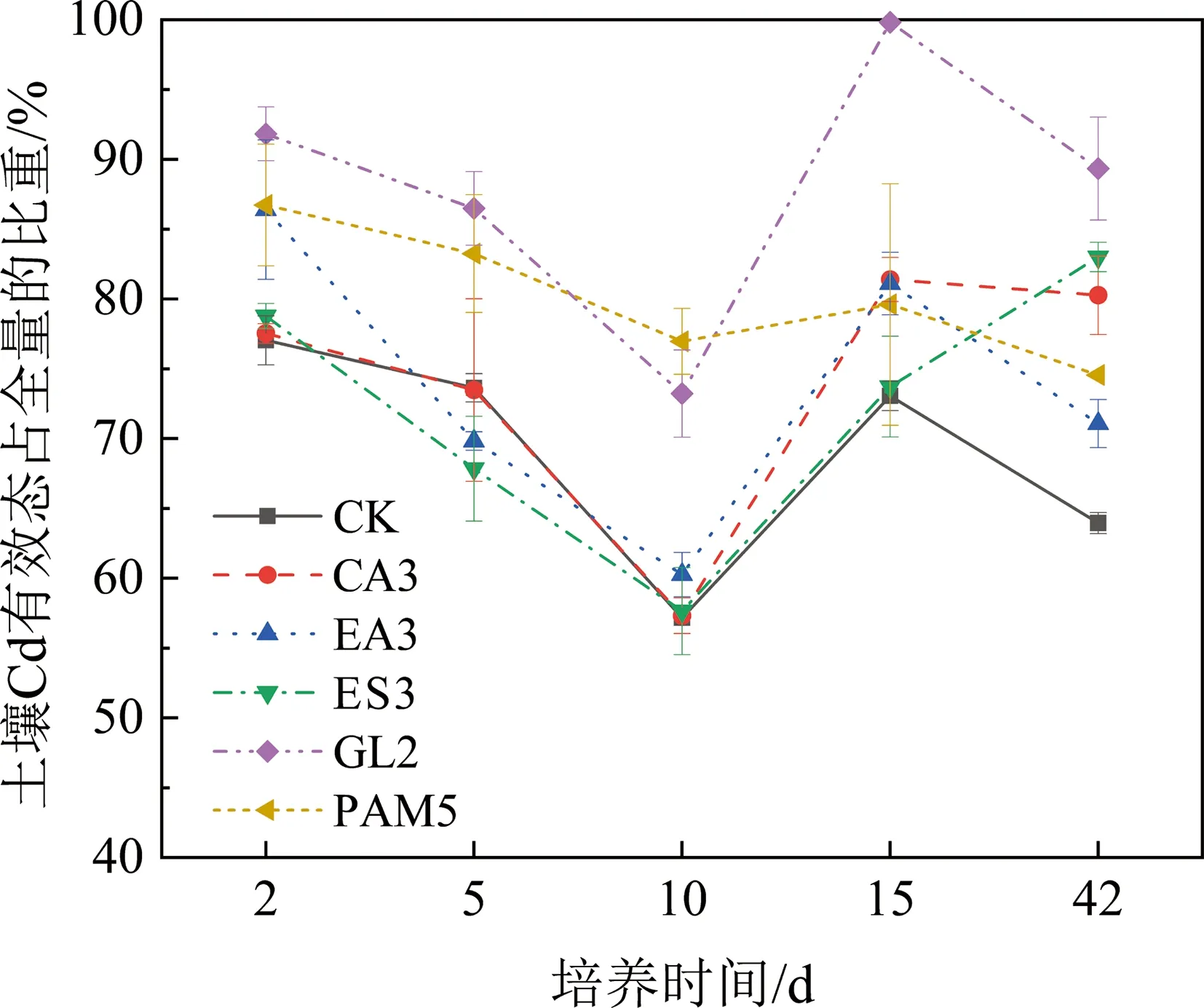
图3 不同处理对土壤Cd有效态质量比的影响Fig. 3 Effects of different treatments on the available Cd contents in soils
3 讨论
3.1 pH对土壤中有效态Cd的影响
土壤pH值能影响各种离子在固相中的吸附水平,从而影响重金属的赋存形态,而重金属在土壤中的赋存形态及各形态所占比例是决定土壤重金属生物有效性的关键[21,22]。许多研究表明,CA,EDDS和PAM能够降低土壤pH值,增强土壤重金属的活性[23,24]。相关性分析结果显示,添加CA,EDDS和PAM能使土壤中的Cd有效态质量比与土壤pH值呈负相关(r=-0.34,-0.43,-0.42),这与曾卉等[25]的研究结果相似,是因为土壤pH值降低使土壤胶体表面的负电荷减少,导致其对重金属离子的吸附容量减少,从而使土壤中重金属的迁移性和生物有效性增强。GLDA的碱性在一定程度上会提高土壤pH值,添加GLDA使土壤的Cd有效态质量比与土壤pH值呈正相关关系,这与Luo等[26]的研究结论相似,螯合剂强化植物提取重金属并不完全取决于土壤pH的变化。
3.2 PAM对土壤Cd的活化效果
在培养初期,当浓度较低(3~12 μmol·g-1)时,PAM呈现钝化效果。Ruehrwein认为,PAM与重金属之间存在表观吸附作用,PAM中的羧基、酰胺基2种活性基团与金属离子形成配位键或氢键,并生成络合物[27],从而降低土壤中的Cd有效态质量比。
本试验中,随着时间的推移,PAM钝化作用减弱,这与孟繁健等[7]的研究结果相似。随着PAM的降解,重金属仍会缓慢释放,并不能永久固定。PAM水溶液随时间、温度、剪切速率及环境因素等发生变化,在土壤环境中长期放置时,一般认为是大分子链在氧化作用下发生降解反应的结果,其粘度逐渐下降,吸附作用弱化,从而影响其应用效果[28]。考虑到实验过程中使用了塑料薄膜将烧杯封口保存,可能PAM在微生物的作用下发生生物降解反应,PAM的降解产物作为细菌生命活动的营养物质,而营养的消耗又促进了PAM的降解[29]。黄峰等[30]利用腐生菌对PAM降解进行研究,结果表明,PAM发生了生物降解,导致其相对分子质量和黏度减小,但是速度极慢,30 d黏度减少不超过12%。
3.3 有机螯合剂对土壤Cd的活化效果
最佳试剂的筛选结果显示,对Cd的活化效果排序如下:GL2>PAM5>CA3>ES3≈EA3。
GLDA对Cd的活化效果最好,具有较强的金属螯合能力。大量研究证明,氨基多羧酸类螯合剂在提取重金属方面的优越性可以归结为其本身较高的羧基和氨基数目[32]。GLDA分子结构中的 4个酸(—COO—)和一个胺(—NRR′)的部分都可作为配体的齿,氮原子和4个氧原子可提供形成配位键的电子对,可以与土壤溶液中的重金属离子结合,形成更稳定的络合物,从而改变重金属在土壤中的存在形态,使重金属由不溶态转化为可溶态,增加土壤中Cd的弱酸提取态和可还原态质量比,大大活化土壤中的重金属[20]。PAM随浓度的增大由钝化转向活化,且浓度越高,活化效果越强。这可能是由于PAM添加浓度均高于其他试剂设置的浓度,使土壤pH值降低,从而增强土壤Cd有效性,活化效率较高。
柠檬酸作为外源质子和有机配体,对胶体表面Cd的解吸会发生一系列复杂的化学反应,其解吸机理可能是质子的溶解作用和有机配体与土壤胶体对重金属的竞争吸附作用[33]。在酸性土壤中,柠檬酸对Cd的活化作用会受到一定程度的抑制。在酸性条件下羟基与羧基不会离解为氧负离子,因而络合能力较弱[20]。
EDTA使土壤中的黏粒、有机质和重金属氧化物对铅的专性吸附减弱,而柠檬酸主要使土壤对Cd的专性吸附减弱,因此EDTA对Cd的活化效率可能比柠檬酸更低[34]。EDDS能够与过渡金属等形成稳定的螯合物,有研究表明,EDDS活化Cd效率与EDTA相似[20],与本试验结论一致。
4 结论
(1)在试验条件下,CA(12 μmol·g-1)和PAM(48 μmol·g-1)处理的土壤pH显著下降(p<0.05),施加GLDA的土壤pH显著增加,均使得土壤有效态Cd质量比显著增加,可见螯合剂强化植物提取重金属并不完全取决于土壤pH的变化。
(2)PAM(48 μmol·g-1)和GLDA(6 μmol·g-1)处理对土壤中Cd的活化效果最好,可显著提高土壤有效态Cd质量比(p<0.05)。
(3)在试验条件下,当PAM施用量较低(3~12 μmol·g-1)时,土壤有效态Cd质量比显著下降;PAM施用量较高(24,48 μmol·g-1)时,土壤有效态Cd质量比显著增加。在利用PAM修复中轻度Cd污染稻田土过程中,建议施用高浓度的PAM以提高有效态Cd质量比,为后期植物修复强化技术研究提供依据。

