我院591 例药品不良反应报告分析
张新娜,李明,李瑞明*,徐东,杨同聚
(1.邹城市人民医院药学部,山东 邹城 273500;2.汶上县人民医院药剂科,山东 汶上 272500)
药品不良反应(adverse drug reaction,ADR)是指合格药品在正常用法用量下出现的与用药目的无关的有害反应[1]。ADR 监测和上报制度的完善,使得ADR 报告的数量越来越多,引起的危害也越来越受到关注。医疗机构内ADR 的监测、收集和上报为确保患者用药安全提供重要依据。本研究对我院2016—2020 年收集的ADR 报告进行分析,旨在了解我院ADR 发生的特点及规律,以期为临床合理用药提供参考。
1 资料与方法
1.1 资料来源
资料来源于我院2016 年1 月—2020 年12 月上报至国家药品不良反应监测系统且系统确认接收的591 例ADR 报告数据,其中男性患者281 例,女性患者310例,年龄2 个月~89 岁,平均年龄(55.75±16.15)岁。纳入标准:监测网中确认上报成功且成功接收;一例ADR 报告中上报为多个药品的只统计怀疑药品;关联性评价为肯定、很可能、可能的。排除标准:ADR 报告信息书写不全的、监测网未接收的。
1.2 方法
收集我院591 例ADR 报告信息,包括ADR 报告类型、报告人职业及科室分布、患者性别及年龄、给药途径、药品种类、累及器官和(或)系统、引发严重ADR 的主要药品及临床表现、ADR 转归等进行统计分析。ADR 填写和判断标准参照《药品不良反应报告和监测管理办法》规定。药品种类参照《新编药物学(第17 版)》[2]进行分类。同一药品不同厂家不同剂型按一个品种计算。
1.3 统计学方法
采用回顾性分析方法,借助Excle 表格对数据进行整理和统计分析,计数资料以(n)和(%)进行描述。
2 结果
2.1 ADR 报告类型
591 例ADR 报告中,“一般的”ADR 报告349 例,占59.05%;“严重的”ADR 报告209 例,占35.36%,“新的一般的”为28 例,占4.74%;“新的严重的”为5 例,占0.85%。“新的和严重的”ADR 报告占比为40.95%。
2.2 ADR 报告的临床资料分析
共591 例ADR 报告中女性多于男性,年龄主要集中于60 岁以上人群;共涉及13 种给药途径,主要为静脉滴注;其中药师上报病例数最多,主要发生于肿瘤科、感染性疾病科、呼吸内科,见表1。
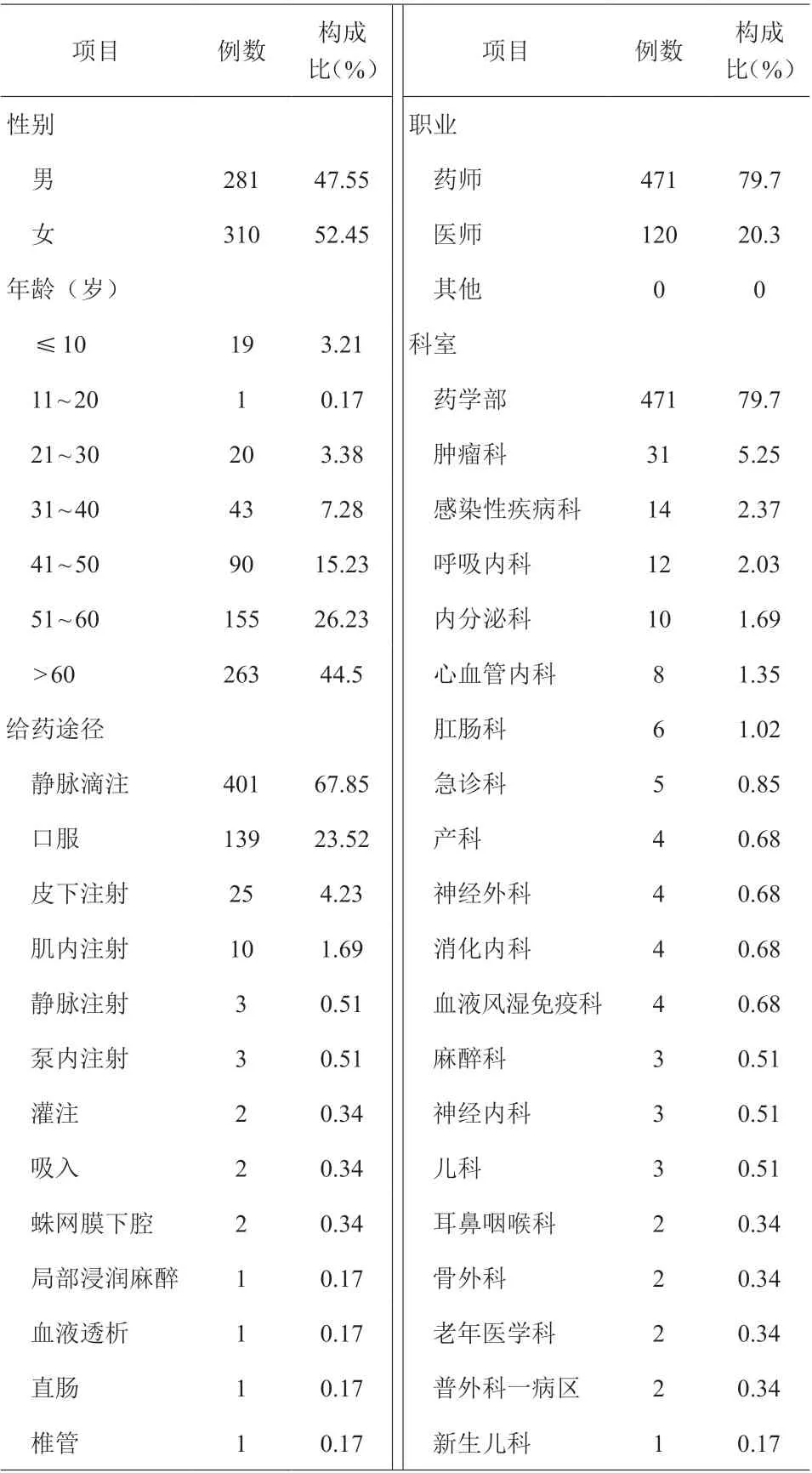
表1 ADR 报告的临床资料
2.3 引发ADR 的药品种类分布
591 例ADR 涉及16 类143 种药品,其中抗肿瘤药引发的ADR 例数最多,共涉及28 种药品,277 例,占46.87%;其次为抗感染药涉及19 种药品,共78 例,占13.2%;其余依次是镇痛药、内分泌系统药、激素类药,见表2。
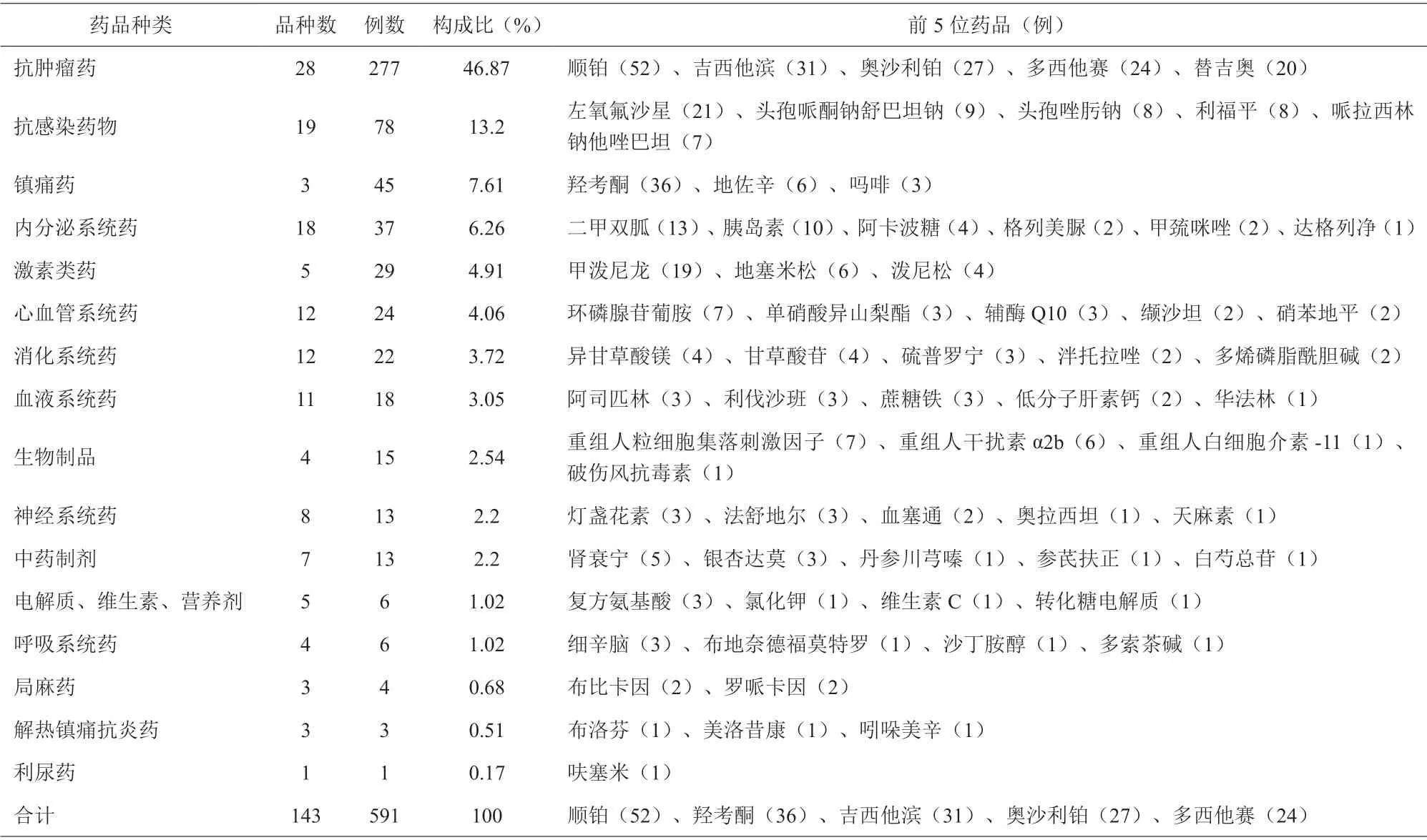
表2 引发ADR 的药品种类分布
2.4 累及器官和(或)系统
591 例ADR 报告中,消化系统损害最为常见,其次为血液系统损害和皮肤及其附件损害,见表3。
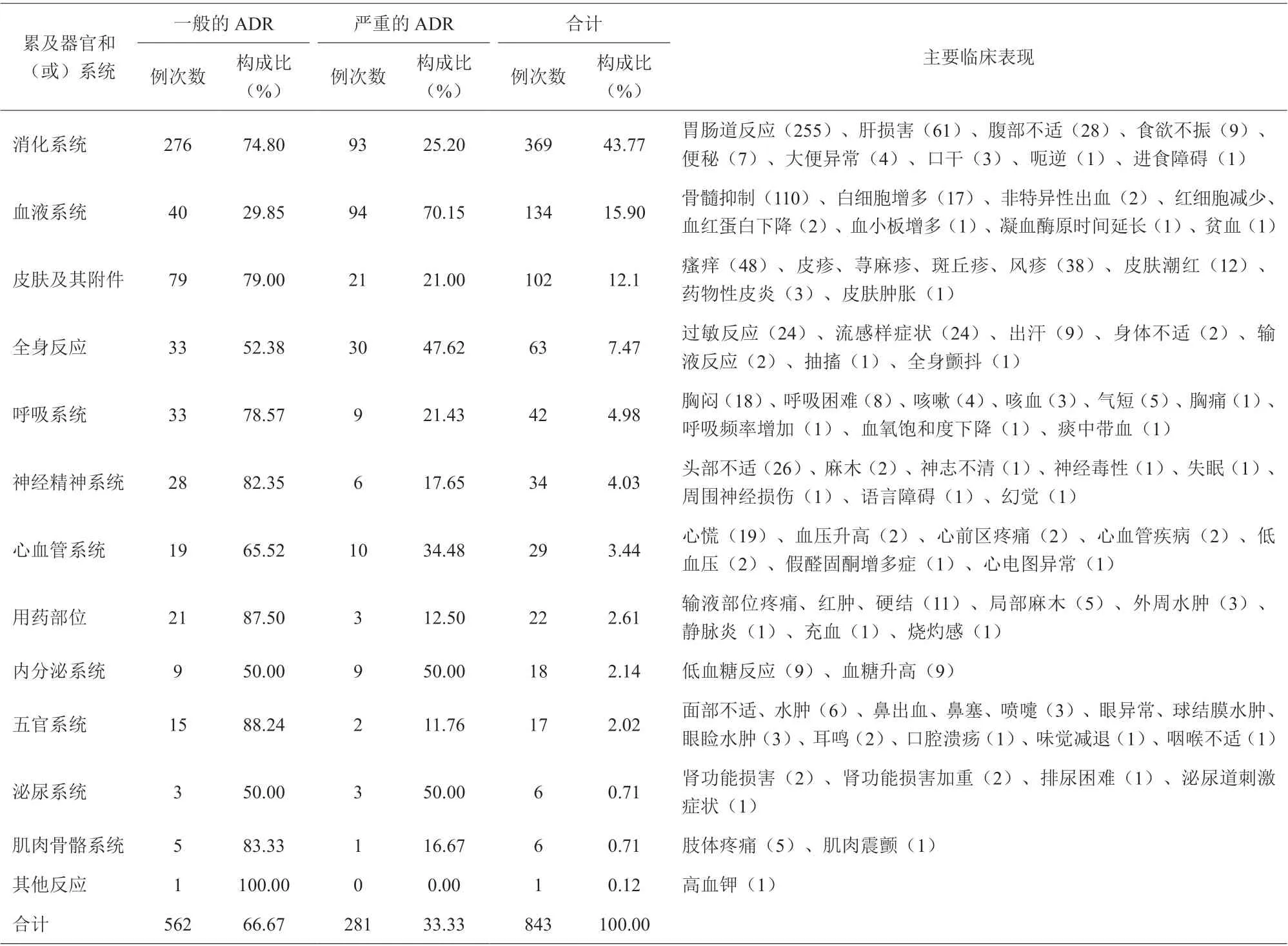
表3 ADR 累及器官和(或)系统
2.5 引发严重ADR 的主要药品及临床表现
严重ADR 的临床表现主要是骨髓抑制,其次为胃肠道反应、肝损害,见表4。
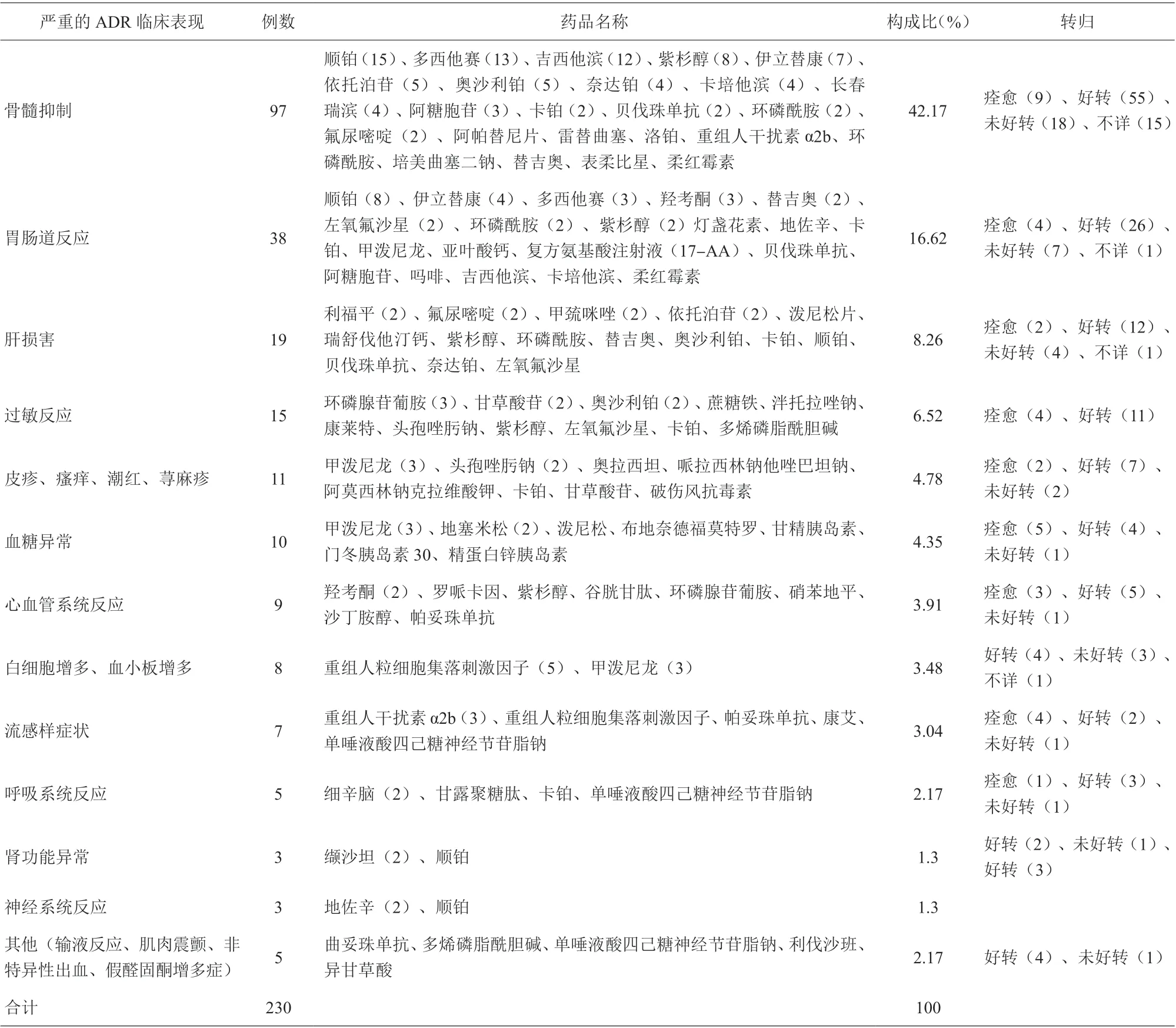
表4 引发严重ADR 的主要药品及临床表现
2.6 ADR 的转归
591 例ADR 报告中,483 例(占81.72%)经相应处理后好转或痊愈。
3 讨论
3.1 ADR 报告情况分析
我院“严重的”ADR 报告占比为35.36%,其数量远高于2020 年国家药品不良反应监测报告的10.0%[3],却远低于2020 年美国严重药品不良反应报告占比62.36%[4]。世界卫生组织(WHO)建议,新的和严重的药品不良反应报告占比30%以上具有警戒信号意义[5],我院“新的和严重的”ADR 报告占比为40.95%,高于2020 年国家药品不良反应监测报告的30.2%,对比数据可知,“严重的”ADR 的数量占绝大多数,而国家公布数据在于“新的”ADR 的数据占多数。因此我院下一步不良反应的上报在关注“严重的”的基础上可重点关注“新的”药品不良反应的搜集。我院严重药品不良反应报告占比高于国家,并不意味着我院药品的安全性水平下降[6],而意味着我院监管部门掌握的信息越来越全面,对药品的风险更了解,对药品的评价更加有依据。
3.2 ADR 报告临床资料分析
本研究中591 例ADR 报告中女性多于男性,与傅瑞春等[7]的报道一致。我院为三级综合医院,收治男女患者均衡,但女性多于男性,可能与女性激素水平有关。我院60 岁以上患者ADR 的发生率最高,主要原因为随着年龄的增长,患者机体各功能趋于衰退趋势,如胃肠蠕动减弱、肝肾功能减退、体内药物清除率降低,加之老年患者常伴有多种基础疾病、用药品种多等易导致老年人群ADR 发生率高[8]。给药途径以静脉滴注为主,与席艳[9]报道一致。主要原因与我院住院患者多采用静脉给药治疗有关;另外,静脉给药药物直接进入血液循环快速起效,静脉输液过程中注射剂的pH值、渗透压、内毒素、微粒、药物滴注速度、配制浓度、溶媒选择、放置时间、人员操作、个体差异等均会引起ADR 的发生[10]。ADR 的上报主要以临床药师为主,这与胡晓燕等[11]的报告一致,我院出现这种情况的原因为临床药师把药品不良反应的上报当做日常重点工作,在药学查房时能敏锐地识别并积极上报。肿瘤科、感染性疾病科、呼吸内科、内分泌科、心内科这些临床科室医师上报的ADR 数量也相对较多,原因是临床药师分布在这些科室,在对科室进行药学查房、医嘱审核时发现了ADR,并督促科室上报。但除临床药师所在的科室外,其他科室医师上报的数量少是因为医师缺乏对ADR 报告工作的认识且存在医患顾虑。因此,在给患者用药时尤其给老年患者,应综合考虑患者的各种因素,用药品种少而精,医务人员加强对老年人的用药指导,反复与患者沟通服药事宜,医务人员在药物治疗过程中坚持“能口服不肌注,能肌注不静滴”的原则,必须静脉给药时严格按照操作流程,我院静脉用药调配中心人员在调配药品时应严格把关,严格按照无菌操作规程调配药品,确保药品配制浓度、溶媒选择无误,当液体配制完毕,尽快安排配送人员配送至病区护士站。护理人员在给患者滴注药品时,按要求控制药品滴速。为了提高其他科室ADR 的上报,需充分发挥我院临床药师的作用,当临床药师在下各临床科室多学科会诊、病历质控时应积极对临床科室做好ADR 的督导和宣传,让医务人员充分了解上报ADR 的必要性。此外,临床药师在药学查房时积极询问患者服药后的反应,并向患者充分普及药品的信息,根据患者对药物的治疗效果提供合理的用药建议,减轻患者因ADR 引起的痛苦,提高我院临床合理用药水平。
3.3 涉及药品种类与品种分析
本研究显示,抗肿瘤药致ADR 最多,这与文献报道[12]一致。主要原因一是恶性肿瘤发病率高,我院收治的肿瘤患者增加,抗肿瘤药物使用量增多且多联合用药;二是抗肿瘤药多有细胞毒性且选择性不强,在杀伤肿瘤细胞的同时,对正常的机体细胞也具有杀伤作用,当机体免疫力低时易致骨髓抑制[13]。
顺铂是我院抗肿瘤药物中发生不良反应最多的药品,这与文献报道[14]一致。顺铂能干扰DNA 复制。主要引起的ADR 为胃肠道反应、骨髓抑制及肝肾损害。其抑制骨髓的程度呈剂量依赖性,好转所需的时间也逐渐延长。用药前临床医师可合用强效止吐药司琼类药物,但部分患者仍可出现不同程度的恶心、呕吐。吉西他滨具有细胞周期特异性,抑制DNA 的合成,可出现胃肠道反应和骨髓抑制现象。奥沙利铂属非周期特异性铂类抗肿瘤药,抑制DNA 的复制和转录。有研究认为其发生过敏反应可能与IgE 抗体介导的超敏反应有关,奥沙利铂进入机体后可诱导产生特异性IgE 抗体,当IgE 抗体达到一定量且再次接触奥沙利铂时,即可产生短暂而迅速的Ⅰ型超敏反应,也有少数患者出现Ⅱ过敏反应和Ⅲ型过敏反应。接受奥沙利铂的化疗方案治疗时,建议止吐方案中包含H2受体拮抗剂和糖皮质激素,发挥止吐和预防过敏作用。鉴于抗肿瘤药物引起的ADR 较多,我院临床药师应做好化疗前预防用药指导和化疗后应对ADR 的治疗工作,医师应综合考虑患者营养状况等因素,合理应用抗肿瘤药,化疗结束后及时监测患者血液学和肝肾功指标,最大减轻患者痛苦。
抗感染药物ADR 仅次于抗肿瘤药物,依次是左氧氟沙星、头孢哌酮钠舒巴坦钠、头孢唑肟钠。除与抗感染药物品种多、用药频度大,抗菌谱广及敏感体质、药品的质量有关外,不合理使用该类药物也是导致ADR高的重要原因,如无指征用药、用药疗程长、联合用药、频繁更换抗菌药物等。不合理使用抗菌药物会导致细菌耐药性发生,导致机体菌群失调。
左氧氟沙星为喹诺酮类抗菌药,抗菌谱广、半衰期长、作用强、不需皮试、与其他抗菌药无交叉耐药被临床广泛应用[15]。英国警示全身和吸入用氟喹诺酮类药物有心脏瓣膜返流的轻微风险,建议有风险的患者首先考虑其他治疗选择[16]。左氧氟沙星化学结构中含有羧基和氟原子,可致消化道反应和光毒性,使机体光照部位皮肤出现瘙痒性红斑。又左氧氟沙星具有脂溶性,因此可引起头痛头晕等中枢神经系统反应。临床中应注意左氧氟沙星的滴注速度不宜过快、滴注时注意避光,滴注期间及用药后3 天之内避免紫外线和日光照射,用药期间多饮水,防止出现结晶尿。头孢哌酮钠舒巴坦钠为广谱抗菌药,临床中用量较大,我院头孢哌酮钠舒巴坦钠引起的主要不良反应是皮疹、瘙痒、过敏等,症状轻微,停药或抗过敏治疗后均好转。这与刘思源等[17]报道一致。引起过敏反应的原因除了与自身结构有关外,还与生产过程中引入的杂质有关[18]。头孢唑肟钠为第三代广谱抗菌药物,主要用于下呼吸道感染、尿路感染、腹腔感染等。不良反应也为皮疹、瘙痒以及过敏反应。因此临床中在使用这两种药物时,应仔细询问患者过敏史,密切关注患者输注期间及输注后症状,一旦出现皮疹、瘙痒等过敏早期症状,立即停药并抗过敏治疗。临床应严格按照《抗菌药物临床应用指导原则》[19]使用抗菌药物,临床药师也应参与抗感染药物治疗方案中,采取用药前干预和事后点评方式,为抗感染治疗提供技术支持。
羟考酮是一种阿片类镇痛药,我院主要用于肿瘤患者晚期癌痛的治疗,因可减弱推进性蠕动致胃排空延迟,肠内容物通过延缓,并能抑制消化液分泌,加之中枢抑制后便意迟钝,可致便秘。因临床中用量较大、不良反应明显,药师对使用麻醉药品的患者逐一回访,因此上报数量较多。对于门诊轻症患者一般建议多食纤维含量高的食物缓解,住院患者建议乳果糖进行对抗。
3.4 累及器官和(或)系统
我院ADR 主要累及消化系统,其次是血液系统,皮肤及其附件等。这与国家药品不良反应监测年度报告(2020 年)[3]大致一致。消化系统损害表现为恶心、呕吐、腹痛、腹泻等,易观察,一般损害较轻微,停药或对症处理后即可缓解。血液系统损害多与肿瘤药物上报数量多有关,大多数抗肿瘤药可以不同程度地损伤骨髓造血干细胞,引起骨髓抑制,一般化疗初期给予升白药物防治该不良反应。皮肤及其附件也较多,主要在于皮肤处主观感受明显,临床表现为瘙痒、皮疹、皮肤潮红等,该类反应难预防,一般发生后立即停药并抗过敏治疗。临床医师应注意观察及询问患者既往用药史、过敏史及用药后的临床表现,一旦发生ADR 及时处理。对于用药后易致骨髓抑制的肿瘤患者,严密监测血常规、肝肾功等,及时发现隐匿的ADR,避免严重后果的产生。
3.5 严重ADR 的临床表现及主要药品
我院引发严重ADR 的药品大多为抗肿瘤药物,主要引起骨髓抑制和胃肠道反应。临床医师可结合患者病情个体化给药,化疗期间根据患者具体情况和反应调整用药,对不合理用药及时干预,促进合理用药。除了抗肿瘤药较易引起严重的骨髓抑制和胃肠道反应外,发现本院其他药物引起的严重不良反应亦应引起重视,如利福平、甲巯咪唑、瑞舒伐他汀、泼尼松、左氧氟沙星等引起的严重肝损害,环磷腺苷葡胺、甘草酸苷、蔗糖铁、泮托拉唑、头孢唑肟、左氧氟沙星、多烯磷脂酰胆碱等引起的过敏反应,甲泼尼龙、头孢唑肟、哌拉西林钠他唑巴坦等引起的皮肤反应,甲泼尼龙、地塞米松、胰岛素等引起的血糖波动,羟考酮引起幻觉,罗哌卡因引起的血压降低,硝苯地平引起心慌,重组人干扰素α2b 引起流感样症状,多烯磷脂酰胆碱注射液引起过敏性休克,细辛脑、甘露聚糖肽引起胸闷呼吸困难,缬沙坦引起肾功能损害加重,地佐辛引起头痛、神志不清,异甘草酸镁引起假醛固酮增多症等严重不良反应应引起重视。对于本院引起严重不良反应的药品,临床应有高度的警惕意识,能快速识别药品不良反应,及时做好防治措施,减轻患者痛苦。
3.6 ADR 的转归
591 例药品不良反应,以痊愈和好转为主。主要在于医务人员发现不良反应后及时采取相应对症措施治疗,降低了不良反应对患者的损伤。
通过对我院5 年来上报的ADR 数据分析,今后我院可重点关注并收集“新的”药品不良反应的上报。下一步可制定ADR 监测和报告的相应文件,实行任务分解制,严格规定各临床科室上报数量,并建立相应的奖惩措施,以提高临床科室的参与度。临床药师在临床科室中应积极宣传ADR 相关知识,加强临床医师和护士对ADR 上报的参与度,加强自身专业技能协助临床科室收集并分析ADR,确保患者安全用药。应重点关注女性、老年人等特殊人群的用药安全。重点监控引起严重ADR 的药品,为临床用药提供参考,不断提高我院合理用药水平。

