2型糖尿病男性患者血清骨膜蛋白水平与骨质疏松的相关性研究
张丹,刘欢,王嘉熙,奚悦
(1.锦州医科大学附属第三医院内分泌及代谢病科,辽宁 锦州 121000;2.葫芦岛市中心医院急诊科,辽宁 葫芦岛 125000;3.锦州医科大学医疗学院,辽宁 锦州 121000)
糖尿病性骨质疏松是在糖尿病的基础上发生的以单位体积骨量减少、骨脆性增加、骨折风险增高为特点的代谢性骨病,是常见的糖尿病慢性并发症之一[1],有报道指出,在我国2型糖尿病骨质疏松的患病率为20%~60%[2],我国50岁以上人群的骨质疏松症总体患病率为19.2%[3],其中男性患病率为6%,而需要进行防治的低骨量人群总体患病率为46.4%,男性骨量减低发生率为46.9 %,但是男性髋部骨折后死亡率至少是同龄女性的2倍[4]。现今骨质疏松症主要依据双能X线骨密度分析仪对骨密度进行检测进而诊断和评估[5],然而这种方法有一定的局限性。因此,临床上寻找一种新的生化标志物可以使我们更早的认识骨的变化,进而预防骨质疏松是必要的。本研究旨在探讨新的影响2型糖尿病男性患者骨质疏松的生化标志物。
1 资料与方法
1.1 受试对象
1.1.1 入选标准:收集2016年3月至2017年3月在我院门诊诊断为2型糖尿病男性病人90例,所有受试者均符合1999年WHO 2型糖尿病的诊断标准,且所选患者及家属均签属知情同意书,并经医院伦理委员会批准备案。另在体检中心健康男性人群中随机选取30例作为正常对照组,且近期均未服用过药物及保健品。年龄≥40岁且≤60岁。
1.1.2 排除标准:年龄>60岁或<40岁;甲状腺及甲状旁腺疾病、库欣综合征、血液病、结缔组织病、骨肿瘤、肾脏疾病、药物等引起的继发性骨质疏松;使用过钙剂、1,25-(OH)2D3、糖皮质激素等影响骨代谢的药物者;严重的肝、心、肾功能不全的病人、自身免疫性疾病、风湿病、长期服用激素及噻嗪类利尿剂等影响钙磷代谢及骨代谢因素者;体重指数(BMI)<18.0 kg/m2或者 BMI>35.0 kg/m2者。
1.1.3 分组情况:所有的受检者均接受双能X线骨密度仪进行检测,分别检测腰椎正侧位(L2~L4)骨密度,取均值,根据1994年WHO骨质疏松诊断标准(DEXA),将受检者按骨密度值分为3组,骨量正常组(30例),骨量减少组(30例)和骨质疏松症组(30例)。
1.2 检测指标
记录患者的年龄、腹围、身高、体重,计算BMI,收集其相关病史资料。所有受试者晚22:00后禁食水8 h以上,于次日晨7:00空腹采肘静脉血,并分别测定甘油三酯(TG)、总胆固醇(TC)、高密度脂蛋白(HDL-C)、低密度脂蛋白(LDL-C)、糖化血红蛋白(HbA1c),血清骨膜蛋白水平。
1.3 骨密度的测量
采用法国MEDILINK公司的双能X线骨密度分析仪检测腰椎正侧位(L2~L4)骨密度,取平均值。仪器测量变异系数为0.9%,每日机器校正后再进行测量。
1.4 统计学方法

2 结 果
2.1 一般资料及生化指标的比较
各组间的年龄、病程、腹围、BMI水平比较差异均无统计学意义(P>0.05)。2型糖尿病3组血清骨膜蛋白水平均较正常对照组升高,其中骨质疏松组最高(P<0.05),且与骨量正常组、骨量减少组比较,差异有统计学意义(P<0.05),见表1。

表1 各组间一般资料及生化指标的比较
2.2 相关性分析
采用直线相关分析对血清骨膜蛋白与各项指标进行相关性分析,结果显示血清骨膜蛋白与年龄、HbA1c、TG正相关,与BMI、HDL-C、骨密度负相关,与TC、LDL-C、钙、磷无明显相关性(见表2)。

表2 血清骨膜蛋白与各因素的相关性
2.3 多重线性回归分析
以骨密度为因变量,年龄、BMI、TG、HDL-C、HbA1c、血清骨膜蛋白为自变量进行多重线性回归分析,得到决定系数R2=0.355,调整后R2=0.344,F=32.155,P≤0.001,模型有统计学意义。结果显示:提示高血糖、血清骨膜蛋白水平升高,为男性2型糖尿病病人骨质疏松的两个危险因素,见表3。
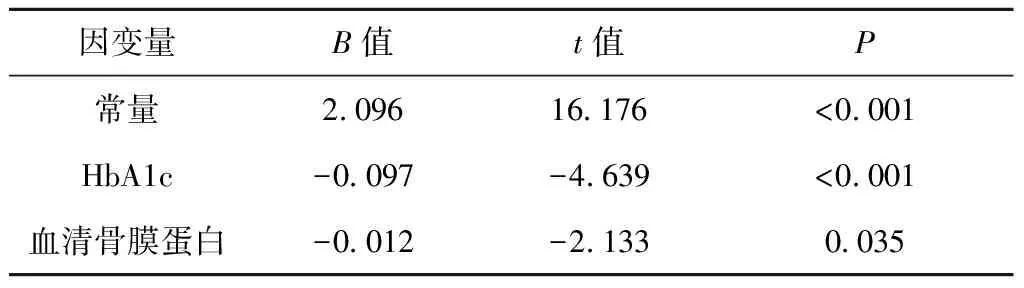
表3 骨密度多重线性回归分析模型参数估计
3 讨 论
骨质疏松(osteoporosis,OP),是一类由多种原因引起的,以单位体积内骨量下降和骨组织的微细结构被破坏为特性,严重者甚至发生骨折的一种全身的代谢性疾病[6],人们称其为“静悄悄的病变”。世界卫生组织估计,全球18岁以上的成年人约4.22亿患有糖尿病,预计到2045年将增长至6.42亿[7]。其发生后展现出高致残率和高死亡率,同时伴随而来的高额医疗费用已成为一种主要公共卫生负担[8]。近年来2型糖尿病与骨密度之间的相关性被广泛探索,有研究者认为糖尿病增加病人骨质疏松和骨折的发生率[9]。高血糖可导致机体渗透性利尿,导致钙、磷等电解质大量排出体外,低血钙刺激甲状旁腺激素的产生,进而增强溶骨作用,导致骨量减少,最终导致骨质疏松症的发生[10]。但是目前2型糖尿病骨密度改变的发病机制仍不十分清楚。在美国,50岁以上男性骨折中由骨质疏松引起的约占1/4,预计到2050年全世界男性髋部骨折会增加310%[11],本试验通过检测男性2型糖尿病病人血清骨膜蛋白水平,与骨密度及生化指标等,为2型糖尿病患者早期预测及治疗骨质疏松症提供新的临床诊疗思路。
近些年来国内外研究显示,1型糖尿病主要是由于胰岛素缺乏导致骨质疏松症,然而2型糖尿病对于骨密度的影响一直存在着不同的论断,可正常、升高或降低[12-13]。本次研究显示,HbA1c是严重影响2型糖尿病患者骨密度的危险因素,这与国内外研究的结果一致[14-15]。HbA1c作为监测T2DM患者血糖控制情况的一项重要指标,可反映近2~3个月血糖的平均水平。长期高血糖对骨的代谢的影响是多样的,有研究表明,高血糖可通过P13K/Akt信号传导途径诱导体内活性氧的产生,阻碍成骨细胞分化,且高渗透性也增加了骨髓脂肪细胞的分化[16]。可能是由于高血糖引起的渗透性利尿,血钙降低,尿钙增高,刺激甲状旁腺素分泌增高,激活了组织中破骨细胞的活性,骨吸收增加进而引发骨密度下降。叶惠成等[17]研究表示,HbA1c与男性2型糖尿病病人的骨密度存在相关性,这与我们的研究结果相一致。本研究显示,伴随年龄的增加,骨密度呈下降趋势。国内外研究报道亦显示,中老年女性的平均年龄每增加1岁,骨密度值下降2.07%[18]。本研究中2型糖尿病骨质疏松组患者的平均年龄超过骨量减少组与骨量正常组,这也进一步说明了血糖及高龄对骨密度的影响。
近年研究发现,骨膜蛋白与骨代谢发生、发展关系密切,其主要病理改变是骨矿含量和骨矿密度下降、骨的微结构紊乱和破坏。骨膜蛋白是由成骨细胞及其前体细胞分泌产生的一种细胞外基质蛋白,具有促进细胞黏附、迁移等功能[19-20]。骨膜蛋白初期又称为骨特异性因子,后续发现其在骨膜中表达,故改名为骨膜蛋白[21-22]。近几年,有研究分析了骨膜蛋白在骨生物学中的作用,并指出骨膜蛋白可能参与了骨的代谢过程。作为具有多功能的细胞外间质蛋白,骨膜蛋白的交互作用主要与整合素受体avβ3、avβ5启动酪氨酸激酶活性受体(RTK)结合触发P13K/Akt及点状黏附激酶(FAK)等信号通路,调节下游基因如硬化蛋白、肌动蛋白、TGF-β1等[23],进而影响成骨细胞的增殖、迁移、修复等,在骨形成和改进过程起重要作用。国外的一项动物实验,通过敲除小鼠血清骨膜蛋白基因,小鼠表现为生长发育迟滞,长骨较短,骨骺形成不良,骨膜的胶原纤维形成不良[24],基因敲除小鼠的成骨细胞,其表现为低增殖、低矿化、低迁移,提示血清骨膜蛋白在骨的发育和重塑过程中具有重要作用[25]。一项进行了7年随访的研究结果提示,血清骨膜蛋白水平与绝经后妇女的骨折风险呈显著相关,且是不依赖骨密度、既往骨折史等的独立危险因素,血清骨膜蛋白水平越高,则骨折风险越高[26]。本次研究结果表明,2型糖尿病骨质疏松组骨膜蛋白水平均高于其余3组,T2DM 3组间血清骨膜蛋白水平比较差异均有统计学意义(P<0.05),提示血清骨膜蛋白可能参与了2型糖尿病骨质疏松的过程,且血清骨膜蛋白与骨密度呈负相关。血清骨膜蛋白于骨代谢的作用机制可能是通过抑制Wnt/β-catenin信号通路结合位点GSK3b[27]。Wnt/β-catenin信号通路在刺激成骨细胞功能和骨形成的过程中都起到了至关重要的作用。抑制Wnt/β-catenin信号通路可导致成骨细胞分化障碍,然而血清骨膜蛋白对骨代谢影响的具体发病机制国内外鲜有报道,需要我们进一步行大样本研究。
综上所述,年龄、BMI、HbA1c、血清骨膜蛋白、TG、HDL水平与2型糖尿病骨质疏松密切相关。血糖控制不佳、血清骨膜蛋白水平增高可能2型糖尿病男性骨质疏松的危险因素。可将血清血清骨膜蛋白的检测列于2型糖尿病男性骨质疏松的预测指标。其检测方法具有简单、易操作的特点,再配合相关生化指标的检测,以降低糖尿病骨质疏松的发病率及骨折的风险。

