枸橼酸托法替布片对不同性别中重度类风湿关节炎患者的疗效评价*
王 丹,张 薇,鲍蕴琦,盖楠楠,白伟莉,贺冬冬
陕西省西安市第五医院风湿免疫科五病区,陕西西安 710082
类风湿关节炎目前在我国的发病率为0.42%,是一种由多种细胞因子引起的自身免疫疾病,病变累及的部位以小关节为主[1]。病变关节主要表现为炎细胞的浸润、滑膜的增生、血管翳的形成以及由此引发的软骨及骨损伤,病情严重时会导致关节变形及活动受限,严重影响患者生活及工作[2]。在全球范围内,类风湿关节炎的对症治疗及规范用药等问题均是研究的热点,部分类风湿关节炎患者在病程中始终存在体内炎性反应,并有高水平的自身抗体,致使用药后仍不能达到缓解标准或使病情稳定[3]。托法替布片是一种新型的口服蛋白酪氨酸激酶抑制剂,也是治疗类风湿关节炎的新型药物,对炎性因子释放有抑制作用,可促进红细胞的沉降,可有效缓解症状,稳定病情[4]。然而,现阶段国内关于枸橼酸托法替布片治疗中重度类风湿关节炎的报道偏少,为进一步了解托法替布片治疗类风湿关节炎的价值,本课题组将本院收治的120例中重度类风湿关节炎患者纳入研究并进行分析,现报道如下。
1 资料与方法
1.1一般资料 选取本院2020年1—12月收治的中重度类风湿关节炎患者120例纳入研究。其中,男性52例,年龄36~78岁、平均(53.26±2.75)岁,病程1~10年、平均(5.23±0.45)年;女性68例,年龄38~76岁、平均(53.69±2.71)岁,病程1~10年、平均(5.20±0.44)年。男性和女性患者间年龄、病程比较,差异无统计学意义(P>0.05)。纳入标准:(1)符合美国风湿病学会(ACR)1987年修订的类风湿关节炎分类标准[5];(2)疾病活动评分(DAS28评分)>3.2分;(3)红细胞沉降率(ESR)、C反应蛋白(CRP)均高于正常值上限2倍以上;(4)类风湿因子(RF)及抗环瓜氨酸多肽抗体(抗-CCP)水平超过正常值上限3倍以上。排除标准:(1)合并系统性红斑狼疮、强直性脊柱炎等结缔组织病;(2)3个月内接受过糖皮质激素治疗;(3)目前正接受生物制剂治疗;(4)妊娠或哺乳期妇女;(5)过敏体质或有严重药物过敏史者;(6)合并心、脑、血液等系统严重疾病;(7)不能配合治疗,如患有精神疾病;(8)正在参加其他药物的临床试验。患者均对本研究知情同意并签署知情同意书。本研究经医院伦理委员会批准通过。
1.2方法
1.2.1患者的治疗 纳入研究的患者均接受健康宣教,以提升治疗依从性。在此基础上,患者口服甲氨蝶呤(上海上药信谊药厂有限公司,国药准字H31020644,规格2.5 mg/片),每次10 mg,每天1次,持续用药12周。口服枸橼酸托法替布片(辉瑞公司,注册证号H20181078,规格5 mg/片)治疗,每次5 mg,每天2次,持续用药12周。
1.2.2观察指标 (1)治疗前后的健康评估问卷残疾指数(HAQ-DI)和DAS28评分:HAQ-DI的评价包括20个问题,如自己能否穿衣、梳头、站起来等,每个问题采用1~4分的计分法,1分为毫无困难,2分为稍有困难,3分为很困难,4分为无法完成;总分0~80分。DAS28评分计算法参照文献[6],评分越高表明疾病活动程度越高。(2)治疗前后的压痛关节数(TJC)和肿胀关节数(SJC)。(3)于患者治疗前后清晨空腹采集血液标本用于检测CRP、ESR、超氧化物歧化酶(SOD)水平,同时记录治疗过程中的不良反应。
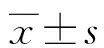
2 结 果
2.1男、女性患者治疗前后HAQ-DI和DAS28评分比较 治疗前,男、女性患者间HAQ-DI和DAS28评分比较差异无统计学意义(P>0.05)。男、女性患者治疗后HAQ-DI和DAS28评分均低于治疗前(P<0.05)。治疗后,男性患者HAQ-DI和DAS28评分均低于女性患者,差异有统计学意义(P<0.05)。见表1。

表1 男、女性患者治疗前后HAQ-DI和DAS28评分比较分)
2.2男、女性患者治疗前后TJC和SJC比较 治疗前,男、女性患者间TJC和SJC比较差异均无统计学意义(P>0.05)。男、女性患者治疗后,TJC和SJC均少于治疗前(P<0.05)。治疗后,男性患者TJC和SJC少于女性患者,差异均有统计学意义(P<0.05)。见表2。

表2 男、女性患者治疗前后TJC和SJC比较个)
2.3男、女性患者治疗前后CRP、ESR、SOD水平比较 治疗前,男、女性患者间CRP、ESR、SOD水平比较差异均无统计学意义(P>0.05)。男、女性患者治疗后,CRP、ESR、SOD水平均低于治疗前(P<0.05)。治疗后,男性患者CRP、ESR、SOD水平均低于女性患者,差异均有统计学意义(P<0.05)。见表3。

表3 男、女性患者治疗前后相关指标比较
2.4男、女性患者不良反应发生率比较 男性与女性不良反应发生率比较,差异无统计学意义(P>0.05),见表4。
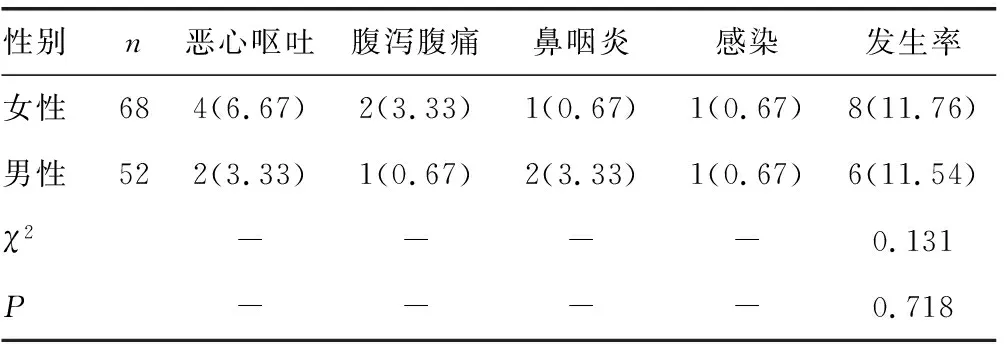
表4 男、女性患者不良反应发生率的比较[n(%)]
3 讨 论
类风湿关节炎是一种表现为慢性滑膜炎症并逐渐导致关节破坏和组织损伤的自身免疫性疾病。B细胞、T细胞、巨噬细胞、软骨细胞、破骨细胞和滑膜细胞的相互作用以及大量细胞因子的释放触发了该病的典型免疫炎性反应过程[7]。类风湿关节炎患者在疾病活动期,体内往往存在高水平的炎性反应;对这些患者进行血清学检测时,其RF及抗-CCP往往也处于高水平,而高水平的RF及抗-CCP是预后不良和关节致残的危险因素。已有的研究证实,抗-CCP及RF水平是预测类风湿关节炎患者关节损伤的重要指标,与骨质侵蚀相关,RF及抗-CCP水平越高则骨质破坏程度越大[8]。一些患者由于及时的治疗及规范用药可逐渐缓解炎症,使病情处于稳定状态。但仍有部分患者在规范应用传统合成甲氨蝶呤、来氟米特及生物制剂等情况下病情始终不能达到缓解标准,甚至自身抗体水平居高不下,这些都将严重影响类风湿关节炎患者的生活质量[9]。因此,必须进一步寻找更为有效的治疗手段。
至今,类风湿关节炎的发病机制并未完全明确,但可以肯定的是细胞因子在其中扮演着非常重要的角色[10]。有研究指出,细胞因子作用于病灶部位,使得滑膜细胞发生变化,引起免疫失衡,诱发炎性反应,导致滑膜增生[11]。另有报道指出,JAK激酶及其下游的效应器、信号转导及转录激活蛋白形成了重要的细胞因子信号传导途径JAK-STAT通路,而该通路是细胞增殖、分化、凋亡等过程的核心,因此在治疗类风湿关节炎时应该将该通路视为新的靶标[12]。托法替布于2017年3月经国家食品药品监督管理总局正式批准用于治疗中度至重度活动性类风湿关节炎,中华医学会风湿病学分会也在《2018年中国类风湿关节炎诊疗指南》中指出,对于使用传统合成型改善病情的抗风湿药物(DMARDs)治疗无法达标的活动性类风湿关节炎患者,推荐使用传统合成型DMARDs联合靶向合成型DMARDs进行治疗(如JAK抑制剂托法替布)[13]。由此可见,托法替布作为类风湿关节炎的靶向治疗药物受到许多学术组织、医生及患者的重视。全球已有多项临床试验证实托法替布与安慰剂组相比可缓解临床症状,但其对病情改善评估指标RF、抗-CCP的作用研究较少。本研究显示,中重度内风湿患者经枸橼酸托法替布片治疗后HAQ-DI和DAS28评分以及TJC、SJC均低于或少于治疗前(P<0.05),说明托法替布片的应用能够减轻关节压痛和肿胀,降低疾病活动度,从而降低对日常生活的影响;男性患者治疗后HAQ-DI和DAS28评分以及TJC、SJC均低于或少于女性患者(P<0.05),说明该药物针对男性患者的效果更好。托法替布片属于JAK通路抑制剂,对多种炎性细胞因子之间的信号传导具有阻断作用,使其能够作用于病灶,促进疾病的逐渐恢复,因此其应用所取得的效果较理想[14]。患者治疗后,CRP、ESR、SOD水平均低于治疗前(P<0.05),表明托法替布片的应用能够促进上述指标的改善。托法替布片是一种新型的用于治疗类风湿关节炎的药物,用药后能够抑制激酶磷酸化,使得患者下游炎性因子的合成减少,进而促进相关炎性因子的水平快速下降,可在短时间内降低ESR[15]。在安全性方面,男性的不良反应发生率与女性相比差异无统计学意义(P>0.05)。托法替布片可以作为治疗类风湿关节炎的理想药物,可以成为其他生物抑制剂反应不佳时的治疗手段。
综上所述,在类风湿关节炎的临床治疗中,枸橼酸托法替布片的应用效果明显,可减轻疾病活动评分,缓解压痛和关节肿胀,促进炎性因子、SOD等指标的改善,具有较高的应用及推广价值。

