基于UPLC-MS/MS白虎汤成分大鼠体内药动学研究
付婷婷, 吕邵娃 ,景梦晓 ,刘紫衡 ,臧玲玲,李永吉*
(1. 黑龙江中医药大学 研究生院, 哈尔滨150040; 2.海南卫生健康职业学院, 海口 570100)
白虎汤为汤剂经典名方,由石膏、知母、甘草以及粳米组成,在《伤寒杂病论》中被张仲景誉为“寒剂之祖方”,用于治疗阳明热症和气分热证,解热效果显著,并能够抑制炎症反应[1].有文献报道[2-4]采用高效液相法测定白虎汤中的成分的含量.也有学者采用超高效液相色谱法研究不同配伍对白虎汤中某一种成分的影响[5-6].基于HPLC法的检测灵敏度低[7],超高效液相色谱串联质谱(UPLC-MS/MS)技术具有灵敏度高、检出限低、样品用量少的优点[8],广泛用于化学成分[9]、药物代谢[10]、杂质鉴定[11]等药物分析中.所以本研究建立测定大鼠血浆中芒果苷、甘草酸铵质量浓度的超高效液相色谱串联质谱法,并研究血药质量浓度及药动学规律,为白虎汤临床药学基础研究提供科学实验依据.
1 实验材料与仪器
炙甘草(批号:170201,安徽广印堂中药股份有限公司);石膏(批号:SAO251安徽广印堂中药股份有限公司);知母(批号:20160512北京本草方源药业有限公司);粳米;芒果苷对照品(批号:DST180513-010成都德思特生物技术有限公司);新芒果苷对照品(批号: DST180630 -017成都德思特生物技术有限公司);甘草酸铵(批号:DST180422-012成都德思特生物技术有限公司);甘草苷(批号:DST180321-014成都德思特生物技术有限公司);磺胺甲噁唑(批号:723-46-6阿拉丁生化科技股份有限公司); ACQUITY UPLC BEH C18(美国Waters公司);甲酸(美国Fisher公司);乙腈(德国Merck公司);甲醇(德国Merck公司).
梅特勒天平(瑞士METTLER公司);SB-5200D-超声波清洗机(宁波新芝生物科技有限公司SB-5200D);UPLC(美国Waters公司); 高速离心机TGL-16C(上海安亭科学仪器厂);HZS-HA 水浴振荡仪(哈尔滨东联电子技术开发有限公司);HgC-12A 型氮气吹扫仪(上海楚定分析仪器有限公司);A110280 涡旋震荡器(南京稼竣生物科技有限公司);T12型体温计(健奥可有有限公司);Waters Xevo TQD型液相质谱联用仪(美国Waters公司).
清洁级SD大鼠(200±20)g,雄性. 购于青岛市动物实验中心(许可证编号:SCXK(鲁) 2014-0001).
2 方法与结果
2.1 溶液的制备
2.1.1 对照品溶液
精密称定芒果苷、甘草酸铵对照品适量,用甲醇溶解配置成对应质量浓度混合对照品作为储备液,芒果苷质量浓度分别为6 250、3 125、1 562.5、781.25、390.62、195.31、97.66、48.83、24.41、12.21、6.10、3.05 ng·mL-1,甘草酸铵也分别配制成6 250、3 125、1 562.5、781.25、390.62、195.31、97.66、48.83、24.41、12.21、6.10、3.05 ng·mL-1相同系列质量浓度溶液.
2.1.2 内标物溶液
另取磺胺甲噁唑适量,用甲醇稀释50 ng·L-1的内标溶液,存放在-20 ℃的冰箱,备用.
2.1.3 供试品溶液
取知母6两(93.75 g),甘草2两(31.25 g),粳米6合(120 mL)于水一斗(1 981 mL)中浸泡30 min,加入生石膏1斤碎(250 g)共同转入砂锅中,武火煮沸后转至文火煎煮40 min,四层纱布趁热过滤得到白虎汤汤液约850 mL.取1 mL白虎汤液,用50%甲醇水溶液溶解并定容于10 mL容量瓶中,超声30 min,4 000 r·min-1离心15 min,取上清液约2 mL,0.22 μm过滤,滤液作为供试品溶液.
2.2 色谱条件及质谱条件
色谱柱:ACQUITY UPLC BEH C18(100 mm×2.1 mm,1.7 μm),流动相 A:乙腈,流动相B:0.1%甲酸,流速0.3 mL·min-1,进样量4 μL.梯度洗脱条件:0~1 min,5%~10%B;1~3 min,10%~14%B;3~5 min,14%~18%B;5~6 min,18%B;6~9 min,18%~19%B;9~12 min,19%~55%B;12~15 min,55%~62%B.
离子源:ESI源,正离子监测模式,离子源温度350 °C,锥孔电压范围2~100 V,碰撞能范围2~80 V,扫描范围m/z:20~1 200,氮气流速:500 L·h-1,扫描方式为多重反应监测(MRM模式),碰撞气体:氦气.内标物锥孔电压28 V,碰撞能8 V;芒果苷锥孔电压34 V,碰撞能22 V;甘草酸铵锥孔电压22 V,碰撞能36 V.
2.3 血浆样品预处理
冻存的大鼠血浆样品自然解冻到室温,取血浆100 μL,加入50 μL内标溶液(50 ng·mL-1磺胺甲噁唑溶液),加入300 μL甲醇溶液除蛋白,涡旋30 s,超声2 min,13 000 r·min-1离心10 min,40 ℃N2吹干,100 μL甲醇复溶,超声2 min,13 000 r·min-1离心10 min,取上清液进样待测.
2.4 专属性考察
在上述色谱和质谱条件下对空白血浆加入芒果苷、甘草酸铵混标的样品及大鼠给药后血浆样品注入UPLC-MS/MS系统中分析,根据结果可见在正离子模式下的芒果苷、甘草酸铵和内标物磺胺甲噁唑的保留时间分别为6.80 、13.31、9.87 min.表明芒果苷、甘草酸铵和内标物在进行离子对提取时,血浆中的内源性物质对毒效成分的无影响.结果见图1、2.
2.5 线性、标准曲线以及定量限
精密吸取芒果苷、甘草酸铵标准溶液100 μL,磺胺甲噁唑50 μL,加入大鼠空白血浆100 μL,按2.3项下操作制备成相应的血药质量浓度的样品,以芒果苷、甘草酸铵与内标物峰面积之比为纵坐标,芒果苷、甘草酸铵质量浓度为横坐标,以最小二乘法进行线性回归获得线性回归方程,及相关系数r,绘制标准曲线.甘草苷标准曲线方程y=0.000 9x-0.010 2,r=0.998 7,线性范围3.05~6 250 ng·mL-1,定量限3.05 ng·mL-1;甘草酸铵标准曲线方程y=0.000 05x-0.013 7,r=0.9955,线性范围18.304~18 750 ng·mL-1,定量限18.304 ng·mL-1.根据《临床前药代动力学指导原则》要求分析物以上制备的QC样品重复测定6次,其准确度(RE)应该在20%之间且相对标准偏差(RSD)小于20%,当信噪比应大于10;芒果苷、甘草酸铵相关系数(r)均大于0.99,各分析物在其相应的质量浓度范围内具有良好的线性关系.
2.6 精密度试验
取含有高、中、低三个标准品质量浓度的血液样品溶液,按照“2.3 血浆样品处理方法”进行处理,每个质量浓度进行平行 6 次进样检测,计算对照品峰面积与内标物峰面积比值的RSD分别为:芒果苷高、中、低质量浓度(781.25 ng·mL-1、97.656 ng·mL-1、12.207 ng·mL-1)RSD值分别为8.214%、7.558%、7.355%.甘草酸铵高中低质量浓度(4 687 ng·mL-1、585.75 ng·mL-1、73.218 ng·mL-1)RSD值分别为8.252%、7.975%、7.814%.

图1 空白血浆中混标物质各成分定量离子对质谱图Figure 1 Quantitative ion pair mass spectrometry of mixed standard substances in blank plasma
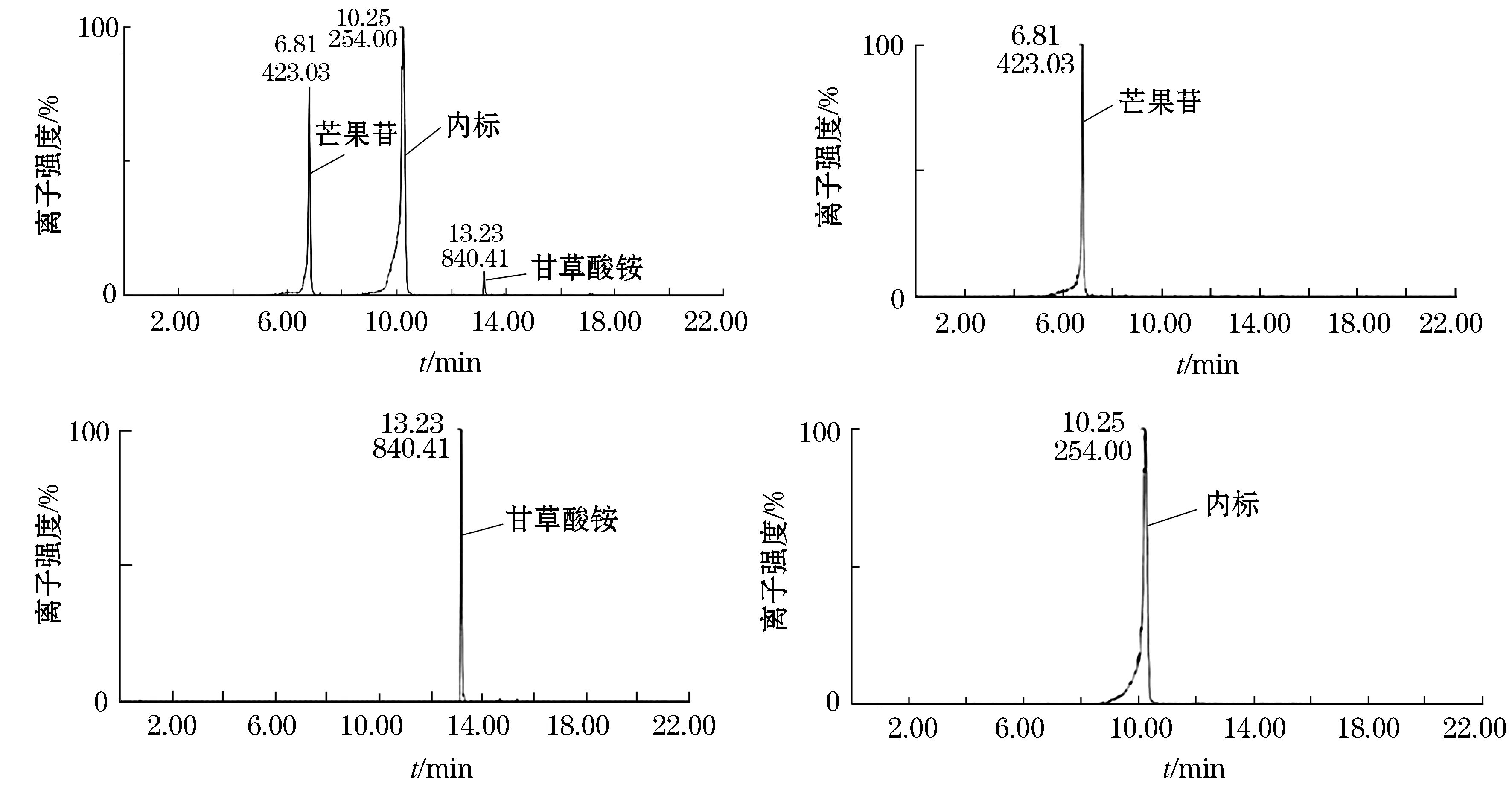
图2 大鼠灌胃给药后血浆样品中物质质谱离子图Figure 2 Mass spectrometry ion map in plasma samples of rats after intragastric administration
2.7 提取回收率
取空白血浆100 μL,加入100 μL高、中、低对照品溶液和50 μL内标溶液,再加入300 μL甲醇溶液除蛋白后,按照2.3项进行处理,进样分析,得色谱峰面积记为A.取空白血浆100 μL,按照2.3项处理方法进行处理,再加入300 μL甲醇溶液除蛋白后,加入高、中、低标准品溶液和50 μL内标溶液,N2吹干,再加100 μL甲醇复溶,超声2 min,13 000 r·min-1离心10 min,进样分析,得色谱峰面积记为B,A/B*100%即为提取回收率.经测定,芒果苷在低、中、高三个质量浓度(12.21、97.66、781.25 ng·mL-1)的提取回收率分别为(87.15±1.93)%,(91.13±3.05)%,(94.05±3.02)%;芒果苷在低、中、高三个质量浓度(73.22、585.75、4687.00 ng·mL-1)的提取回收率分别为(84.97±2.97)%,(94.15±3.11)%,(100.33±3.75)%.
2.8 稳定性试验
取上述含有高、中、低三个标准品质量浓度的血液样品溶液,按照“2.3 血浆样品处理方法”进行处理,于-20 ℃下在 0、6、24 h 放置后分别进样,每个质量浓度平行 6 次进样检测.以质量浓度进行计算,每个质量浓度样品与真实质量浓度的偏差均不超过±13(RE/%),并且同质量浓度测定值的RSD不超过(±12)%.
2.9 药代动力学研究
2.9.1 药动学试验方案
SD 雄性发热模型大鼠12只,随机分2组,每组6只,分别灌胃给药,正常组:生理盐水,3 mL/200 g;白虎汤组:3 mL/200 g.分别于给药后 15 min、30 min、1 h、2 h、3 h、4 h、5 h、6 h、8 h、10 h,于各时间点眼眶取血 1.5 mL,置于EDTA-2Na处理后的抗凝管中,3 000 r·min-1离心 10 min,分离上层血浆,于-80 ℃保存备用.
2.9.2 药时曲线
按2.3项下处理方法将大鼠血浆样品进行预处理,在上述的色谱和质谱条件下,将处理好的血浆样品进入UPLC-MS/MS中分析并记录各待测物的色谱峰面积,以当日的标准曲线计算大鼠血浆中芒果苷、甘草酸铵质量浓度.对每组大鼠的血药质量浓度与时间进行数据处理并绘制血药质量浓度-时间曲线.见图3.

图3 药时曲线Figure 3 Time-concentration curve
2.9.3 药动学参数
上述药-时曲线数据通过DAS 2.0软件处理后,得出白虎汤中的芒果苷和甘草酸铵在大鼠体内的药动学过程属于非房室模型,最终采用统计矩分析方法求算各药动学参数,芒果苷药动学参数分别是AUC(0-t)为(2 292.855±60.13)μg·L-1·h、AUC(0-∞)为(2 363.501±62.561)μg·L-1·h、MRT(0-t)为(4.313±0.036) h、MRT(0-∞)为(4.593±0.06)h、Tmax为5 h、Cmax为(668.749±14.645)μg·L-1;甘草酸铵药动学参数分别是AUC(0-t)为(6 249.021±94.464)μg·L-1·h、AUC(0-∞)为(7 656.155±260.932)μg·L-1·h、MRT(0-t)为(5.079±0.031) h、MRT(0-∞)为(6.751±0.272) h、Tmax为5 h、Cmax为(1 210.931±71.225)μg·L-1.
3 讨 论
3.1 色谱及质谱条件的选择
采用UPLC-MS/MS对指标性成分进行药代动力学研究,色谱条件对各成分的保留时间、峰型、响应值均有较大的影响,分别考察了磷酸缓冲盐-水、乙腈-水、(0.1%)甲酸-水、甲醇-水溶液作为流动相,当选择(0.1%)甲酸-水作为流动相时,色谱峰峰较好,对洗脱梯度进行多次洗脱和优化,确定最终的洗脱条件.为了获得最佳的质谱条件,通过正、负离子模式进行监测,芒果苷、甘草酸铵在正离子模式下响应度较高,优化后的质谱条件具有较好的灵敏度和信号强度,因此确定正离子模式进行检测;优化各种参数后质谱参数能够满足生物样品中有效物质的准确定量的要求.
3.2 内标物的选择
在生物样品的分析中,理想的内标物具有良好的溶解性,与被测样品不起化学反应,且其出峰位置应与分析物的峰相近[12].本课题先后选择对乙酰氨基酚和磺胺甲噁唑为内标物,只有磺胺甲噁唑满足作为内标物的必要条件,对芒果苷、甘草酸铵的测定也有良好的响应,该模式下芒果苷、甘草酸铵出峰时间分别6.80 min、13.31 min,而内标在9.87 min出峰,回收率稳定,因此选择磺胺甲噁唑作为研究选用的内标物.
3.3 血浆样品处理方法的选择
常用的生物样品预处理方法主要有:液-液萃取法(LLE)、固相萃取法(SPE)、蛋白沉积物法(PPT).固相萃取法操作步骤繁琐且萃取小柱价格高昂,加大了成本负担[13].液-液萃取操作人员需要一定的专业技能,不适于临床大批量测定[14].而蛋白沉积物法具有操作简单,提取回收率较好的优势[15].本实验采用甲醇为溶剂进行蛋白沉积物,结果显示甲醇沉积物蛋白的方法简单,去除蛋白效果良好.
3.4 结果分析
本文采用UPLC-MS/MS法测定白虎汤在SD 大鼠体内血浆中药物含量,结果表明,芒果苷药动学存在双峰现象,有可能存在肝肠循环.该方法准确度高、灵敏度强、专属性好,可作为测定白虎汤中芒果苷、甘草酸铵质量浓度的方法,为探讨白虎汤的药动学行为提供方法依据.此前,只有测定白虎汤中一种或几种成分含量的相关研究,未见对白虎汤药动学方面的研究,该实验对白虎汤药动学做出讨论,为白虎汤以后的全面研究打好基础,为经典名方白虎汤的继承和发扬提供帮助.

