双重检测马铃薯X和Y病毒试纸条制备技术研究
张 微 李志新 赵 雪 张金鹏 付春江 于倩倩 刘卫平
(黑龙江省农业科学院克山分院,161600,黑龙江齐齐哈尔)
马铃薯X病毒(potato virus X,PVX)是马铃薯最常见的病毒之一,其感染症状是叶片变小,花叶、叶片上有大小不等的黄绿色斑驳等,可使马铃薯产量降低10%~50%。马铃薯Y病毒(potato virus Y,PVY)是危害马铃薯、烟草等茄科植物的主要病毒之一,其感染症状是重花叶、叶脉坏死和出现褐斑等,可导致马铃薯减产 20%~50%。在田间,PVX与PVY常复合侵染,造成马铃薯严重减产,甚至绝产。我国马铃薯生产受病毒病危害非常严重,在各主要产区如黑龙江、河南等地多为复合侵染[1-3]。目前,马铃薯感染病毒后主要通过电子显微镜、DAS-ELISA(enzyme-linked immunosorbent assay,ELISA)和PCR等方法[4-6]进行检测,但此类方法在生产上的应用具有很大局限性[7]。胶体金免疫层析技术(gold immunochromatography assay,GICA)是将胶体金标记、免疫检测、层析分析、单(多)克隆抗体和新材料等结合在一起的技术,具有操作简便、快速、结果准确、无需特殊设备等优点[8],在医学、动植物检疫、食品安全监督等领域得到广泛应用[9-12]。在马铃薯上已研制出 PVX和PVY单重胶体金检测试纸条[13]。目前,多重马铃薯病毒的检测多使用分子生物学方法[14],而关于多重马铃薯病毒胶体金检测试纸条的研究尚未见报道。为此,本试验研制定性检测PVX和PVY的双重胶体金试纸条,为马铃薯病毒病的田间检测提供一种快速的方法。
1 材料与方法
1.1 试验材料
PVX和 PVY为本研究室从马铃薯上分离得到。病毒分别摩擦接种繁殖于心叶烟(Nicotiana glutinosa)上。马铃薯 S病毒(PVS)、卷叶病毒(PLRV)、M病毒(PVM)和A病毒(PVA)为本研究室保存。供试马铃薯品种为克新13号。
1.2 试剂和仪器
PVX和PVY兔多克隆抗体购买于美国Agida公司,羊抗兔抗体购自北京百奥莱博科技有限公司,氯金酸购自天津市光复精细化工研究所,柠檬酸三钠和牛血清白蛋白购自上海惠世有限公司,硝酸纤维素膜、玻璃纤维膜、样品垫、吸水纸、支持板、三维大平面点膜喷金仪、裁条机和微电脑自动斩切机均购自上海金标生物科技有限公司。DASELISA检测试剂盒购买于美国Agida公司,其他试剂均为国产分析纯。
1.3 胶体金的制备和鉴定
采用常规的氯金酸-柠檬酸三钠还原法制备胶体金。取297mL ddH2O于圆底烧瓶中,加入3mL 1% HAuCl4·4H2O混匀。将圆底烧瓶置于电热套式恒温器中,加入干净搅拌子,低速搅拌加热至沸腾,迅速一次性加入3mL 1%柠檬酸三钠,继续煮沸,观察颜色变化为浅黄色→黑色→紫色→紫红色,当完全转变成红色时,继续煮沸5min后停止加热,补水至原体积。将烧制的胶体金溶液用蛋白核酸分析仪(Gene Spec V,日本日立)进行全波长扫描鉴定,并置于透射电镜(H7650,日本日立)下观察拍照[15]。
1.4 免疫胶体金试纸条制备工艺优化
主要对金标抗体的标记量、反应 pH、封闭时间、离心时间、复溶液和复溶量等进行优化。取8支干净的1.5mL离心管,分别加入1mL胶体金,然后分别加入4μL 1mg/mL PVX与PVY抗体,再分别加入 1、2、3、4、5、6、7、8μL 的 0.2mol/L K2CO3调节pH,混匀后室温静置反应30min,观察颜色变化。根据颜色结果确定免疫胶体金的最适pH。另取8支干净的1.5mL离心管,分别加入1mL胶体金,然后分别加入已确定的最适 pH对应的0.2mol/L K2CO3的加入量,再分别加入1、2、3、4、5、6、7和8μL的1mg/mL PVX与PVY抗体,来调节抗体标记量,混匀后室温静置反应30min,观察沉淀变化。根据沉淀结果确定免疫胶体金的最适抗体标记量。标记了胶体金后的抗体加入 10%BSA,分别设置封闭时间 10、20、30、40、50和60min,观察加入封闭剂后颜色变化,根据颜色变化选择颜色恢复成胶体金颜色1时为最佳封闭时间,设置离心时间10、20、30、40、50和60min,留沉淀弃上清,选择沉淀量最多、沉淀效果最好的为最佳离心条件。分别用复溶液50、60、70、80、90、100、110和 120μL复溶沉淀至合适的比例,用喷金仪器设置喷金量3、4、5、6、7、8和9μL/cm,选择反应颜色容易观察的喷金量为最佳,喷在玻璃纤维纸上,制作金标垫。
1.5 检测线和质控线
将PVX与PVY抗体分别用超滤管(Millipore,10kD)进行浓缩。将硝酸纤维素膜(Nitrocellulose membrane,NC膜)固定贴合于支持板上,使用三维平面点膜喷金仪分别将PVX抗体和PVY抗体浓度设置为 0.5、0.6、0.7、0.8、0.9、1.0、1.1和1.2mg/mL,并划线于NC膜上,作为检测线(testline,T线),T1线为PVX检测线,T2线为PVY检测线。用0.02mol/L磷酸缓冲液(phosphate buffer,PB,pH 7.4)将羊抗兔抗体稀释至0.5、0.6、0.7、0.8、0.9、1.0、1.1和1.2mg/mL,划线于NC膜上,作为质控线(control line,C线),37℃烘干4h。选择反应条带颜色可观察到的最低抗体使用量为最佳。
1.6 试纸条的组装
将样品垫、金标垫和吸水纸组装到附有NC膜的支持板上,然后用切条机切割成 3.5mm宽的试纸条。
1.7 试纸条的质量检测
1.7.1 特异性检测 分别将PLRV与PVS、PVA与PVM、PVM与PVS、PVX与PVA、PVY与PVA、PVX与PVY病毒的阳性材料用2mL的磷酸缓冲盐溶液(PBS缓冲液)混匀,制成样品检测液,将制备好的试纸条置于样品中检测,每2种病毒混合液重复检测3次。
1.7.2 灵敏度检测 取PVX和PVY阳性混合样品进行倍比稀释获得 1、10、102、103、104、105、106和107倍的样品稀释液,分别用试纸条进行灵敏度检测。
1.7.3 准确性检测 分别取马铃薯待检样品93份,分别采用胶体金试纸条与DAS-ELISA进行检测,将结果进行对比分析。
1.7.4 稳定性测试 将试纸条放在装有干燥剂的铝箔袋中,分别密封保存在4℃冰箱中、室温下和敞开保存在室温下;设置不同保存时间,利用阴性样品、只含有PVX、只含有PVY和同时含有PVX和PVY的阳性材料定期检测试纸条的有效性。
2 结果与分析
2.1 胶体金颗粒观测
制备好的胶体金在波长 526nm处有最大吸收峰(图1),金颗粒为圆形,直径20~30nm(图2),表明胶体金质量较好,符合免疫层析试验要求。
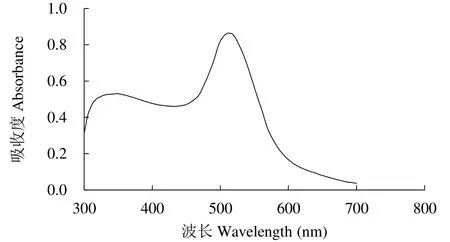
图1 胶体金吸收光谱Fig.1 Colloidal gold absorption spectrum

图2 透射电镜下胶体金颗粒形态(Bar=500nm)Fig.2 Colloidal gold particle morphology under transmission electron microscope (Bar=500nm)
2.2 胶体金试纸条制备条件优化
制备金标抗体的最佳反应条件为加入 2μL 0.2mol/L K2CO3调节pH,PVX抗体加入量为4μL,PVY抗体加入量为5μL,封闭时间40min,离心时间30min,100μL复溶液复溶沉淀。胶体金喷涂量为6μL/cm,T1线的PVX抗体浓度为1mg/mL,T2线的PVY抗体浓度为1.2mg/mL,C线的羊抗兔抗体浓度为1mg/mL,检测线T1、T2与C线划膜量均为1μL/cm。
2.3 试纸条特异性检测
由图3可知,将试纸条分别插入PVX阳性样品与 PVY阳性样品中,相应病毒的检测线及质控线出现明显条带;2种病毒阳性样品混合后,将试纸条插入混样后,2条检测线和质控线均出现明显条带;将试纸条分别插入PLRV、PVS、PVM、PVA的阳性样品中,仅质控线出现条带,说明本试纸条具有非常好的特异性。

图3 试纸条对6种常见病毒的特异性检测Fig.3 Specific detection of six common viruses by strips
2.4 试纸条灵敏度检测
分别将试纸条插入稀释1、10、102、103、104、105、106和107倍的PVX和PVY阳性样品中检测其灵敏度。结果(图4)发现,试纸条可检测稀释至106倍的PVX汁液和105倍PVY汁液。

图4 试纸条检测PVX和PVY汁液Fig.4 Test strips detect PVX and PVY sap
2.5 试纸条与DAS-ELISA检测马铃薯苗带毒情况一致性分析
由表1可知,双重病毒试纸条检出PVX阳性样品12份,PVY阳性样品26份,其中 PVX和PVY同时侵染样品8份,而DAS-ELISA检出PVX阳性样品14份,PVY阳性样品29份,其中PVX和PVY同时侵染样品9份。

表1 2种方法检测结果Table 1 The results of two methods
如表2所示,比对双重病毒检测试纸条和DASELISA检测样品结果,得出2种方法对PVX的检测符合率为97.85%,Kappa值为0.91,判定2种方法符合率非常高;比对双重病毒检测试纸条和DAS-ELISA检测样品结果,得出2种方法对PVY的检测符合率为96.77%,Kappa值为0.92,可见2种方法对PVY检测符合率非常高。
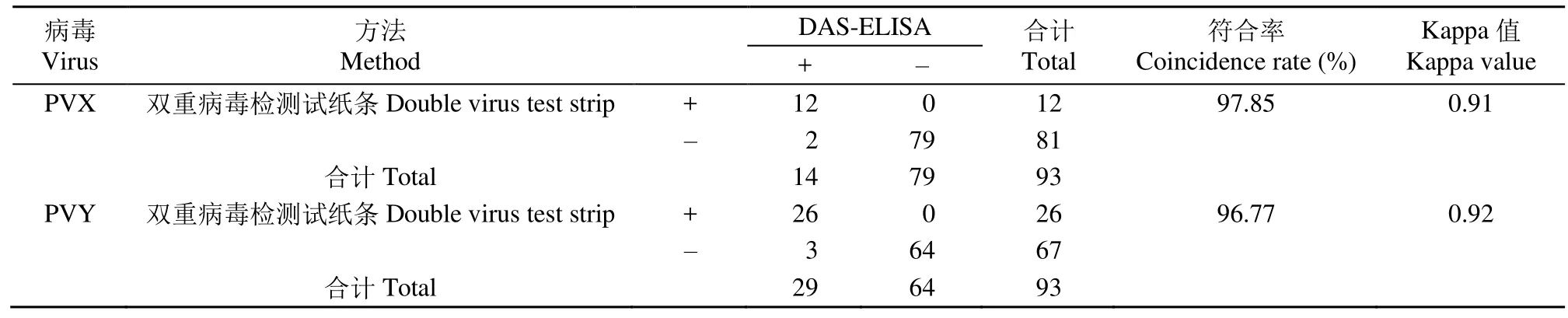
表2 双重病毒检测试纸条与DAS-ELISA检测PVX和PVY的符合性对比Table 2 Comparison of the compatibility between the double virus test strip and DAS-ELISA test for PVX and PVY
2.6 试纸条稳定性检测
如图5所示,将试纸条放在装有干燥剂的铝箔袋中密封,放在4℃冰箱中保存,有效期可达210d,能够保持原有灵敏度;试纸条密封后室温保存,有效期大于120d,检测灵敏度有所下降;试纸条在室温下敞开保存,30d就失去了检测能力。说明在适当条件下保存,本试纸条具有较好的稳定性。

图5 试纸条稳定性测试结果Fig.5 Stability test results of strip
3 讨论
有研究[1,16]表明,2种及以上不相关的病毒复合侵染同一寄主是病毒侵染过程中的常见现象。由于复合侵染时2种病毒的相互作用,包括协生(增加病毒含量)或拮抗(减少病毒含量),会导致寄主产生的症状与单独侵染不同。PVX复合侵染比单独侵染时复制能力增强,病毒含量大幅提高,并造成症状加重,因此对复合侵染病毒的检测方法尤其重要。已有研究[14,17]表明,通过电镜手段和PCR技术可以对PVX和PVY复合侵染进行检测。对多种在烟草花叶病毒(tobacco mosaic virus,TMV)、黄瓜花叶病毒(cucumber mosaic virus,CMV)和PVY上病毒检测试纸条已有研究[18],对3种病毒的特异性、灵敏度和一致性进行了研究分析,但是试纸条的检测时间与稳定性没有提及。对于PVX和PVY双重病毒试纸条研究目前没有相关报道。PVX和PVY是最常见、同时也是对马铃薯危害最严重的2种病毒,常规的检测方法只能在实验室由专业技术人员操作完成,给需要随时检测马铃薯病毒发生情况的田间及试验条件差的基层单位造成不便。而试纸条检测具有使用方便、反应快捷的特点。经过田间取样测试,本试纸条与DAS-ELISA检测结果吻合性非常高,双重病毒试纸条的阳性检出率稍低于DAS-ELISA,可能是由于试纸条检测灵敏度低于DAS-ELISA,但也不排除DAS-ELISA出现假阳性的可能[19-20]。已有研究[15]表明,单一检测PVX和PVY的试纸条检测样品的反应时间在10min之内;马铃薯X病毒试纸条检测烟草病汁液可稀释104倍(W/V),马铃薯Y病毒试纸条检测烟草病汁液可稀释103倍;低温保存时间大于90d,室温保存时间大于30d。本试纸条检测反应快捷,约2min就能得出结果,节约了检测时间。相对于单一检测PVX和PVY试纸条,节约了部分成本。对PVX试纸条检测病毒汁液可稀释106倍(W/V);PVY试纸条检测病汁液可稀释105倍,提高了检测灵敏度。低温4℃保存时间超过210d,室温密封保存时间可达120d,稳定性显著提高。双重病毒试纸条的检测效果基本能够满足田间及口岸一线的检测需求。
4 结论
PVX和PVY双重病毒试纸条具有使用方便、操作简单的优点,无需实验室及专业技术人员,随时随地均可以操作使用,而且反应快捷,几分钟出结果,可以实现现场取样现场出结果,实用性强,适用性广。特别适用于马铃薯田间和试验基础条件差的单位使用。实现了一个试纸条对PVX和PVY同时快速检测,不仅提高了检测效率,且节约了部分成本,可进一步推广应用。

