颈动脉粥样硬化易损斑块超声标志与脑血管疾病关系的研究进展
李怡,何文
《中国卒中报告2019(中文版)》显示,卒中是我国居民的主要死亡原因之一,也是影响全年龄组伤残调整生命年的首位原因[1]。有研究表明约2/3的急性缺血性卒中由动脉粥样硬化易损斑块造成[2]。目前,传统的以颈动脉狭窄程度为缺血性卒中诊疗依据的观点逐渐向综合颈动脉狭窄程度和动脉粥样硬化斑块特点的评估模式转变[3-5]。颈动脉超声是颈动脉动脉粥样硬化的主要检查方法之一,不同模态超声技术可以从不同维度评估动脉粥样硬化斑块的易损性,尤其是斑块负荷、斑块内新生血管、斑块硬度和成分等可作为评估缺血性卒中风险的标志物(图1)[6]。本文综述不同模态超声检查在颈动脉粥样硬化斑块稳定性评估与缺血性卒中诊治中的应用价值,为颈动脉粥样硬化患者的临床管理提供理论依据。
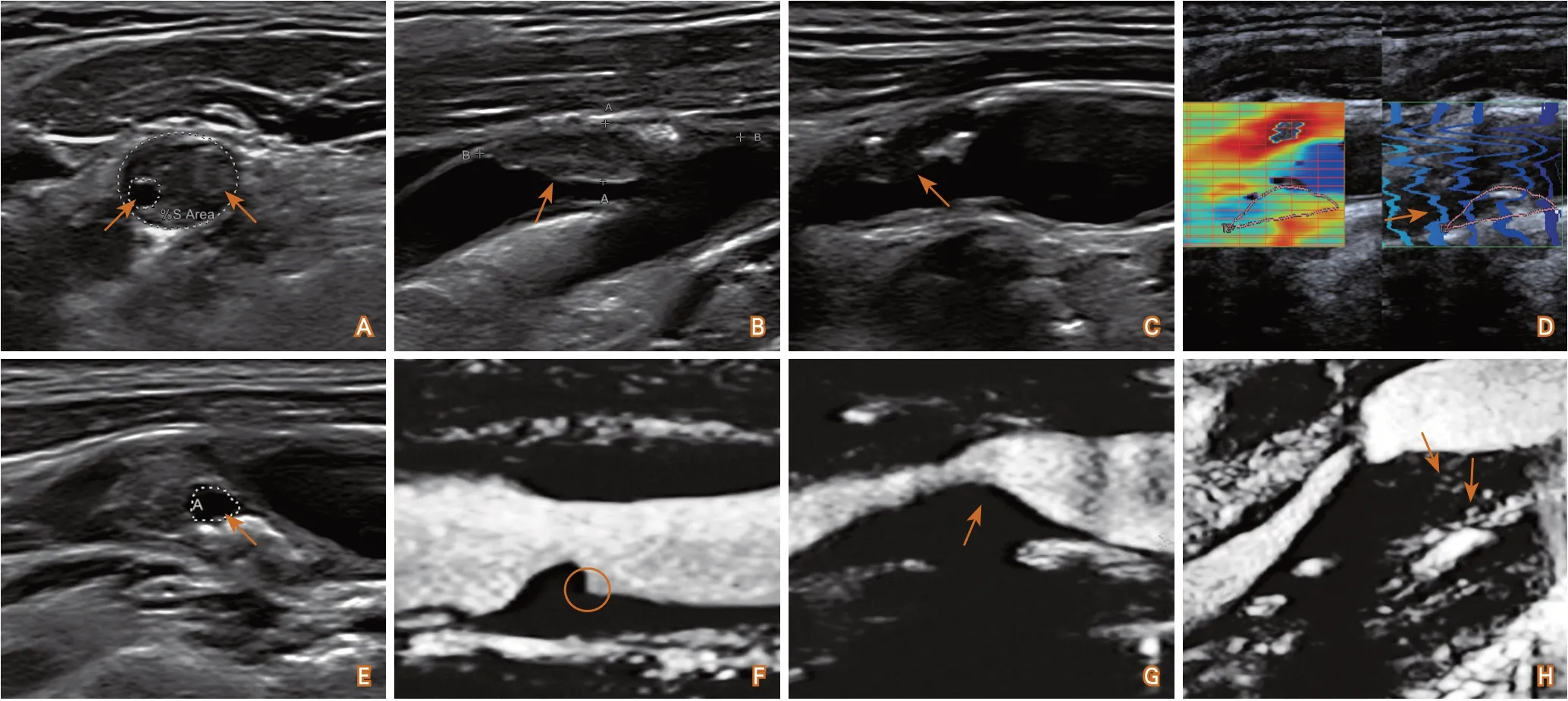
图1 颈动脉粥样硬化斑块的超声影像特点
1 测量颈动脉内-中膜厚度
灰阶超声可对颈动脉内-中膜厚度进行定量测量,具有较高的观察者内部及观察者之间一致性[7]。2011年曼海姆共识将动脉管壁局部内-中膜厚度>1.5 mm定义为动脉粥样硬化斑块[8]。一项基于社区人群的前瞻性研究纳入2190例无心血管事件的动脉粥样硬化患者,超声测量颈动脉内-中膜最大厚度,并对患者进行了中位10.5年的随访,结果有94例首次缺血性卒中事件发生,COX回归分析发现,颈动脉内-中膜最大厚度是首次缺血性卒中的危险因素(HR1.47,95%CI1.28~1.69)[9]。一项纳入2189例患者的前瞻性研究利用超声测量颈动脉粥样硬化斑块的最大厚度,经过平均6.9年的随访,发现斑块最大厚度>1.9 mm是发生复合心血管事件的独立危险因素(HR2.80,95%CI2.04~3.84)[10]。
超声检查不仅可以评估颈动脉是否存在动脉粥样硬化病变,还可以测量颈动脉内-中膜厚度,显示颈动脉粥样硬化斑块数量,从而反映颈动脉粥样硬化的范围和严重程度。
2 评估动脉粥样硬化斑块的面积和体积
颈动脉粥样硬化斑块体积是斑块易损性的潜在风险标志。二维、三维超声可对斑块面积及体积进行定量评估[11]。一项前瞻性研究纳入349例颈动脉粥样硬化患者,基线三维超声评估颈动脉粥样硬化斑块体积,中位随访3.17年,结果显示,斑块体积增大与卒中、TIA及死亡显著相关(P=0.001)[12]。一项前瞻性队列研究纳入100例心脑血管疾病高危患者,在平均24.4月的随访期间,34%的患者发生了复合终点事件(心血管死亡、非致命性心肌梗死或不稳定型心绞痛、非致命性卒中和冠状动脉血运重建术),COX回归分析发现,双侧颈动脉粥样硬化斑块总面积≥69 mm2与心脑血管事件的发生有关,校正混杂因素后HR为5.86(95%CI2.09~16.4,P=0.001)[13]。上述研究提示颈动脉粥样硬化斑块面积或体积作为反映斑块负担的定量指标可以预测心脑血管事件的发生,但尚需统一超声测量标准的大样本临床研究进行验证。
3 检测动脉粥样硬化斑块内的新生血管
动脉粥样硬化斑块内新生血管与斑块活动性有关,斑块活动增加了斑块内出血、炎症及斑块破裂的风险,目前认为斑块内新生血管是斑块易损性的标志[14]。
超声造影可以定量评估颈动脉粥样硬化斑块内新生血管的密度和分布区域,并可以搭载靶向微泡识别斑块内炎症反应[15-16]。一项meta分析纳入7项研究,共507例动脉粥样硬化患者,分析超声造影与病理证实的斑块内新生血管的关系,结果表明,超声造影是检测动脉粥样硬化斑块内新生血管的可靠技术[17]。有观察性研究提示颈动脉粥样硬化斑块内新生血管的密度与卒中发生有关[18]。最近的一项前瞻性队列研究纳入发病7 d内的缺血性卒中患者,对症状侧颈动脉的粥样硬化斑块进行超声造影检查,中位期随访14.1月,有15例卒中复发,COX回归分析发现,超声造影显示的颈动脉粥样硬化斑块内新生血管是卒中复发的独立预测因素(校正HR6.57,95%CI1.66~26.01,P=0.007)[19]。急性轻型缺血性卒中和高危TIA患者90 d卒中复发风险较高,颈动脉粥样硬化斑块的易损性进一步增加了此类患者卒中复发的风险[20]。一项前瞻性研究对91例TIA患者进行了2年的随访,通过超声造影将斑块内新生血管分为5级:0级为动脉壁及斑块内无新生血管;1级为动脉壁外膜增强,无斑块内增强;2级为斑块内点状增强;3级为斑块内线状增强;4级为斑块内弥漫性增强,多因素分析发现颈动脉粥样硬化斑块内线状增强及弥漫增强是缺血性卒中和TIA复发的独立危险因素(OR6.817,95%CI1.58~29.48,P<0.05)[21]。以上研究说明颈动脉粥样硬化斑块内新生血管不仅与缺血性卒中的发生有关,还可以预测卒中复发,为卒中二级预防提供了潜在的干预靶点。
超微血流成像技术是一种用于检测微小血管的新兴超声技术,可更敏感地显示低速血流信号,反映组织微灌注情况,且无须使用超声造影剂[22-23]。Zamani等[24]的研究发现,超微血流成像与超声造影评估动脉粥样硬化斑块内新生血管的数量具有较高的一致性(r=0.911);且超微血流成像显示斑块内新生血管增多与组织学上肉芽组织、炎症和脂质的综合评分增高有关(r=0.494)。Wang等[25]纳入131例缺血性卒中或TIA患者,应用超微血流成像技术评估颈动脉粥样硬化斑块内新生血管的密度,logistic回归分析显示,同侧斑块内中-大量新生血管形成是卒中或TIA的危险因素(OR4.017,95%CI1.351~3.822,P=0.001)。
超声造影虽然可以准确评估颈动脉粥样硬化斑块内的新生血管情况,且与病理结果具有较好的一致性,但目前尚无颈动脉粥样硬化斑块内新生血管超声造影的分级标准。统一、科学和规范的颈动脉粥样硬化斑块内新生血管超声分级标准的制定,有利于临床实践操作和科学研究的开展,是亟待解决的问题。
4 评估动脉粥样硬化斑块的硬度
动脉粥样硬化斑块的稳定性与斑块成分密切相关,斑块硬度可以反映斑块的成分,通常斑块内脂质成分偏软,钙化成分偏硬。剪切波弹性成像技术可无创、定量地评估组织硬度[26]。弹性成像可以提供与动脉粥样硬化斑块成分相关的额外信息,如大的脂质核心和斑块内出血,这些特征均与斑块的稳定性有关[26]。
一项观察性研究纳入44例颈动脉狭窄>30%的患者,应用剪切波弹性成像,以弹性模量评估颈动脉粥样硬化斑块的硬度,结果发现,症状性颈动脉粥样硬化斑块的平均弹性模量显著低于无症状斑块(62 kPavs88 kPa,P=0.01)[27]。Lou等[28]的研究纳入61例患者共271个颈动脉粥样硬化斑块,也发现症状性斑块的平均弹性模量低于无症状斑块(81 kPavs115 kPa,P<0.01)。以上研究证实了剪切波弹性成像测量颈动脉粥样硬化斑块硬度的可行性,且症状性颈动脉粥样硬化斑块的弹性模量显著低于无症状的斑块。最近的一项观察性研究纳入25例颈动脉粥样硬化斑块患者,将剪切波弹性成像与组织病理学进行对照,发现病理学上斑块内出血、血栓形成和泡沫细胞数量增加均与弹性模量降低有关[29]。该研究表明病理学上动脉粥样硬化斑块易损性标志与剪切波弹性成像评估的斑块弹性模量具有较好的一致性,剪切波弹性成像可以作为评估动脉粥样硬化斑块易损性的有效手段。
目前,针对颈动脉粥样硬化斑块弹性成像的研究多是小样本、单中心的回顾性研究,其对斑块稳定性的评估和卒中风险的预测均可能存在偏倚,需要大样本、多中心的前瞻性研究进行验证。此外,随着弹性成像技术的发展,如成像帧频的提高,可以提高对颈动脉粥样硬化斑块易损特征评估的准确性。
5 展望
超声检查可无创性地评估颈动脉的狭窄程度和动脉粥样硬化易损斑块的特点,是颈动脉粥样硬化性疾病的主要检测方法。随着超高速超声成像、超声造影、三维超声、血管内超声、光声成像、弹性成像等新技术的发展,超声定量评估动脉粥样硬化斑块内新生血管和斑块成分更加精准。然而,与CT和MRI相比,超声诊断的准确性仍有待提高[30]。此外,由于操作者依赖性及可重复性等问题,超声影像的纵向研究存在局限性[31]。超声图像的标准化采集及超声诊断的结构化是解决这一问题的必由之路。由于超声影像数据集中包含了大量信息,影像数据呈爆炸式增长,人工智能的发展可能为颈动脉粥样硬化斑块的风险评估开辟新的道路。
目前,基于超声的颈动脉粥样硬化斑块风险标志研究多是单中心的观察性研究,这些风险标志对卒中发生、复发和预后影响的临床价值仍需多中心的前瞻性随机对照研究进一步证实。此外,综合分析各种影像检查手段的优缺点,选择患者最易接受,获益最大,对临床治疗指导价值最高的检查方式仍然是临床应关注的重点[32-33]。
【点睛】超声检查显示颈动脉粥样硬化斑块特点和易损性的准确性虽然较更加直观的CT、MRI等影像技术欠佳,但具有简单、经济、无创等优势。随着超声技术的发展,其在显示动脉粥样硬化斑块成分、血管新生等方面越来越精准,有助于预测缺血性卒中发生和复发的风险,临床价值较高。

