大气等离子喷涂制备SOFC连接体Cu/Mn/Co金属防护涂层
江 舟,文 魁,宋 琛,刘太楷,董 勇,邓畅光,邓春明,刘 敏,杨成浩
1.广东工业大学 材料与能源学院,广东广州510640;2.广东省科学院新材料研究所,现代材料表面工程技术国家工程实验室,广东省现代表面工程技术重点实验室,广东 广州510650;3.华南理工大学环境与能源学院,广东 广州510006
固体氧化物燃料电池(SOFC)因高效、清洁、燃料广泛等诸多优点,已成为当今新能源研究的热点.SOFC单电池由阴极、阳极、电解质组成,通过连接体把若干个单电池组装成电堆,可提高电池的功率输出[1-4].随着固体氧化物燃料电池工作温度降至600~800℃,金属材料代替陶瓷材料作为连接体已成为可能.Crofer22 APU,T 441及SUS430等铁素体不锈钢(Ferritic stainless steel,FSS),因其高电导率、高热导率、低成本等特点,被广泛作为平板式SOFC的连接体材料.但FSS在SOFC工作温度下仍然具有较高的氧化速率,且表面会生成电导率较低的Cr2O3膜层,此外合金中Cr元素不断挥发对电池阴极产生毒化,导致明显的电池性能衰减.研究发现,在FSS表面制备一层导电防护涂层可有效提高FSS的抗高温氧化性能和阻Cr扩散性能[5-10].
(Mn,Co)3O4尖晶石涂层因导电性高、高温稳定性好及与FSS热膨胀系数匹配良好等特点,近些年得到了广泛地研究.但(Mn,Co)3O4尖晶石涂层在工作环境下长时间服役,仍存在电导率不足、Cr挥发改善还不够的问题[11-17].国内外学者尝试在(Mn,Co)3O4尖晶石中掺杂Cu元素以进一步优化其性能.Xiao和Brylewski等人[18-19]研究了Cu掺杂量对粉末电导率的影响发现,Cu掺杂能促进粉末电导率增加,但是Cu原子在(Mn,Co)3O4尖晶石中的固溶度有限,过量的Cu会形成CuO等降低整体电导率的副产物.此外,与MnCo2O4涂层相比,Cu掺杂提高了涂层电导率.Sabato和Molin等人[20-21]研究了Cu掺杂对涂层相结构、热膨胀系数、致密度的影响发现,Cu掺杂能提高涂层致密度、增加热膨胀系数,降低涂层内部相变的程度,从而提高涂层电导率.但Cu掺杂(Mn,Co)3O4尖晶石存在较大的不足:首先,其需要制备出可供喷涂的掺杂粉末,这导致涂层制备效率完全取决于粉末的制备速度,因此效率较低;同时,大规模应用时需要考虑成本问题,采用Cu掺杂(Mn,Co)3O4尖晶石粉末需要采购(Mn,Co)3O4尖晶石原粉,而目前高质量尖晶石粉末价格较贵,不利于该技术的应用.
针对上述问题,提出一种低成本、高效连接体防护涂层制备思路.(Mn,Co)3O4尖晶石是金属Mn和Co氧化形成的复合氧化物,可以先制备金属涂层,随后将之氧化形成尖晶石[24].虽有报道先采用电镀[25]、磁控溅射[26]等工艺制备金属涂层,随后将金属涂层氧化成尖晶石涂层,但这类方法效率极低,所制备的涂层厚度通常不大于5µm,且对基体表面质量要求较高,不适合大规模应用.而大气等离子喷涂技术(APS)可大规模、高效率、低成本制备涂层[2],尤其适合金属涂层的制备,但目前鲜有应用APS进行连接体金属防护涂层制备的报道.因此,拟采用APS直接制备Cu-Mn-Co金属涂层,通过高温氧化形成含Cu-Mn-Co的尖晶石涂层,主要研究不同喷涂工艺参数下涂层氧化过程中的相结构、表面形貌与微观结构演变,并采用四电极法表征涂层电导率,确定最佳喷涂工艺参数,制备出性能优异的涂层.
1 实验部分
1.1 实验原料
实验粉末为低成本的金属Cu,Mn和Co粉的机械混合粉,m(Cu)∶m(Mn)∶m(Co)=17∶50∶33,粉末平均粒径为35µm,其形貌如图1所示.选用T 441不锈钢(30 mm×40 mm×2 mm)和Al2O3圆片(D18.55 mm×1.65 mm)作为喷涂基体.

图1 Cu-Mn-Co金属粉末表面形貌Fig.1 Surface morphology of Cu-Mn-Co metal powder
1.2 涂层制备
采用大气等离子喷涂技术(APS)制备涂层.首先将预先混好的粉末放入70℃恒温烘箱中烘干,直至喷涂前取出.然后用丙酮去除基体表面油污,对基体表面喷砂进行粗化处理,提高涂层与基体的粘附性.最后使用压缩空气清除基体表面多余的砂粒和杂物,其中Al2O3圆片则用酒精超声清洗后干燥处理.表1为喷涂工艺的主要参数.

表1 APS制备金属涂层工艺参数Table 1 Process parameters of metal coatings prepared by APS
1.3 氧化处理
由CuO-MnO和Mn3O4-Co3O4相 图 可 知[27-28],800℃下CuO可与MnO发生固相反应生成CuxMn3-xO4+CuO相,Mn3O4与Co3O4反应生成MnCo2O4相.因此,所制备的涂层均在800℃下进行氧化,以观察尖晶石相的转变情况和电导率变化情况.氧化时间分别选10,20和120 h,其中氧化10和20 h是为了观察涂层微观形貌变化及其电导率的变化,氧化120 h则是为了获得足够稳定的微观组织结构和电导率.
1.4 涂层表征
通过扫描电镜(SEM)、能量色散光谱仪(EDS)及ImageJ软件观察涂层表截面形貌、致密度、结合情况及元素分布,使用X射线衍射(XRD)分析氧化前后涂层相组成变化,采用直流四电极法测定涂层电导率.
首先在Al2O3涂层表面定位出正方形的四个顶点,然后在顶点处蘸取银浆,埋入银线,并放入140℃烘箱中烘50 min,使银浆固化.银浆固化后取出试样,放入管式炉中进行电导率测试.以5℃/min的升温速度升至800℃,通入0.2 A的恒定电流,使用万用表读取电压线上的电压值,记录升温、保温过程中电压随时间的变化结果.涂层电导率ρ=1/(c×R×W),其中:ρ为电导率,单位为S/cm;c为四点法接线系数;R为计算出的电阻,单位为Ω;W为涂层的厚度,单位为cm.
2 结果与讨论
2.1 涂层相结构
图2 为三组涂层喷涂态及800℃氧化处理后的相组成.从图2可见:经氧化后的涂层结晶度明显提高,并形成尖晶石结构;喷涂态涂层由Cu,Co,CuO和MnO相组成,而经800℃氧化10 h或20 h后生 成CuO,Co3O4,MnCo2O4和CuxMn3-xO4(x=1,1.4,1.5)相,延长氧化时间至120 h后,Co3O4衍射峰消失,尖晶石相衍射峰强度明显增强.在试样No.1~No.3中选择峰位、峰强相近的衍射峰(如图2(b)中2θ=48.59°处),并保持测试条件相同,半定量表征其他衍射峰强度变化.从图2(a)可以看到,三种参数的试样的相组成、衍射峰强度、结晶度无明显差异.从图2(b)~图2(c)可见,经800℃氧化10h和20 h后,试样No.2的尖晶石衍射峰强度均高于试样No.1和试样No.3,而CuO衍射峰强度低于试样No.1和试样No.3.从图2(d)可以看到,试样No.1~No.3的尖晶石衍射峰强度无明显差异,而试样No.2的CuO衍射峰较低.这表明,No.2涂层试样含有较少的CuO相,而含有更多的尖晶石相.由此可得,试样No.2的工艺参数能促进尖晶石相的形成,800℃高温氧化可得到CuxMn3-xO4,MnCo2O4和CuO混合相.
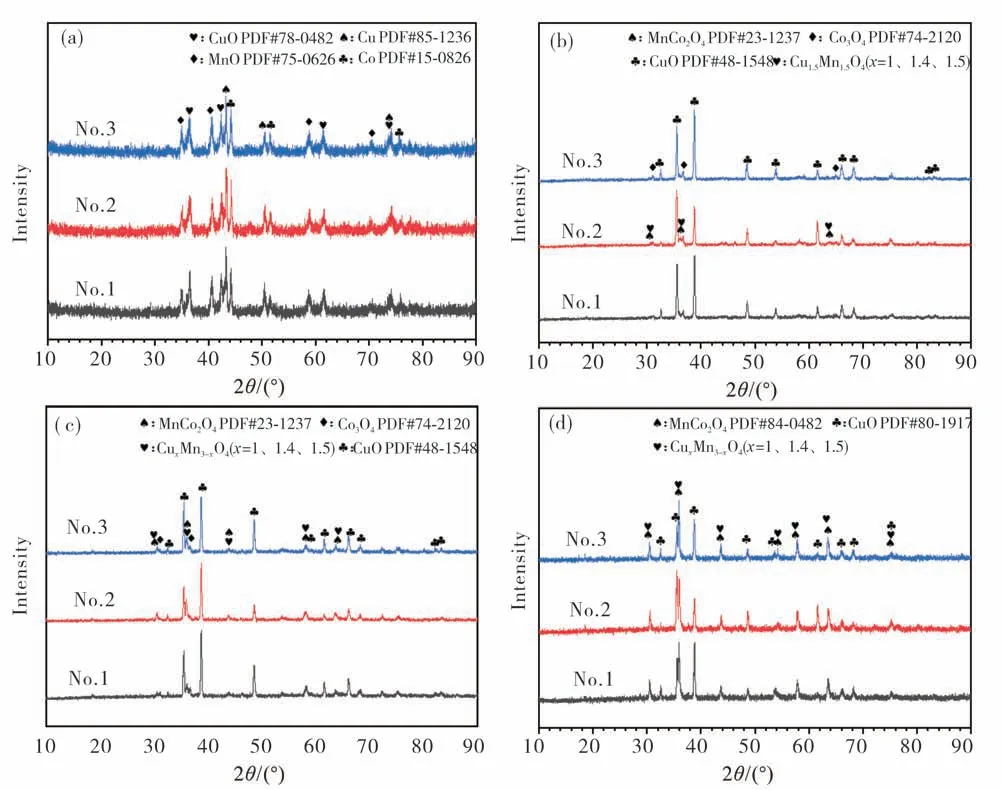
图2 涂层试样的相组成(a)喷涂态;(b)800℃,10 h;(c)800℃,20 h;(d)800℃,120 hFig.2 Phase composition of coating samples(a)sprayed state;(b)800℃for 10 h;(c)800℃for 20 h;(d)800℃for 120 h
2.2 表面形貌演变
对三种喷涂参数涂层氧化前后表面形貌、元素分布进行表征,图3为不同氧化条件下涂层的表面形貌.从图3(a)~图3(c)可见,喷涂态涂层氧化前表面存在凸起颗粒和裂纹空隙.从图3(d)~图3(f)可见,经在800℃下氧化10 h后,涂层表面主要存在平整的四边形和中心凹槽的多面体两种形貌.从图3(g)~图3(l)可见:800℃氧化20和120 h后,表面中心凹槽的多面体逐渐消失,生成“金字塔”形貌的尖晶石相;此外,800℃/120 h,涂层表面出现明显的氧化皮,且氧化皮与涂层之间存在裂缝和孔隙,氧化皮的出现与表层CuO及尖晶石相含量变化有关,部分区域CuO生成尖晶石或氧化层底部生成尖晶石,导致与涂层表面热膨胀系数不匹配,从而产生分层、裂纹.

图3 不同试样在不同氧化条件下涂层的表面形貌(a)~(c)喷涂态涂层;(d)~(f)800℃氧化10h;(g)~(i)800℃氧化20 h;(j)~(l)800℃氧化120 hFig.3 Surface morphology of the coating on different samples under different oxidation conditions(a)and(c)sprayed coating;(d)and(f)oxidation at 800℃for 10 h;(g)and(i)oxidation at 800℃for 20 h;(j)and(l)oxidation at 800℃for 120 h
为确定涂层表面不同形貌的成分,对图3(e)和图3(k)中不同点进行EDS分析,其结果列于表2.由表2可知:图3(e)中的平整四边形(area2)和中心凹槽的多面体(area3)均为富Cu相,暗色区域(area1)为混合尖晶石相;图3(k)中的白色区域为CuO相(area2),暗色区域为混合尖晶石相(area1,area3).由此可知,随氧化时间增加,涂层表面尖晶石相覆盖面积逐渐增大,CuO层覆盖面积逐渐减少.
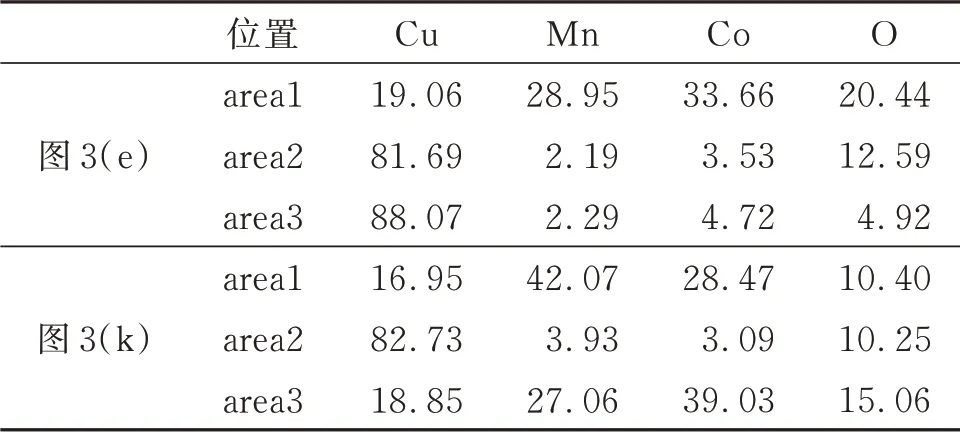
表2 图3(e)和图3(k)中的EDS点分析结果Table 2 EDS pointanalysis results in Figure 3(e)and(k)
2.3 微观结构演变
图4为不同试样喷涂态涂层的截面形貌及涂层的元素分布.从图4(a)~图4(c)可以看到,喷涂态涂层呈现典型的层状结构,层间存在少量的未熔颗粒和缝隙.未熔颗粒的存在与喷涂工艺有关,不同的Ar与H2比例、电流会影响粉末的熔融状态,这决定了材料在到达基体之前是否已经充分熔化;缝隙的存在与熔融液滴的凝固时间有关,由于熔滴的凝固时间非常短,熔滴并不能完全能够在前一个已铺展开的熔滴处形成有效结合,从而导致在铺展的边角区域出现残留缝隙.采用ImageJ软件计算三种涂层的孔隙率,发现No.1~No.3涂层的孔隙率依次为20.84%,19.16%和24.26%,而No.2涂层致密度较高.除此,No.1涂层的厚度大于No.2和No.3的,相同喷涂遍数下No.1的沉积效率更高.对No.1涂层进行EDS面扫(图4(d)~图4(i))后发现,Cu,Mn,Co和O元素分布不均匀,其中部分区域存在Co和Cu金属单质,而Cr元素主要分布于T 441基体.

图4 No.1~No.3喷涂态涂层试样的截面形貌(a~c)及No.1涂层试样的元素分布(d~i)Fig.4 Sectional morphology of No.1-No.3 sprayed coating samples(a-c)and the element distribution of No.1 coating samples(d-i)
图5 为800℃/10 h后No.1~No.3涂层试样的截面形貌及No.1涂层试样的元素分布图.从图5可见,Cu元素向涂层表面扩散并聚集于表面.这因为CuO的生成焓为−0.772 eV而低于MnO和CoO的生成焓−1.979和−1.247 eV[29-31],在同一条件下金属Mn和Co要优先于Cu与氧结合形成氧化物,同时金属Cu的自扩散激活能低于Mn和Co的自扩散激活能且涂层中含有较多的氧化物,因此在氧化过程中金属Cu会优先扩散且被挤出涂层而在涂层底部和面部聚集,同时在原Cu金属位置留下孔隙.底部未扩散的Cu单质在高温条件下氧化吸氧,导致涂层底部出现较多孔隙.随着氧化时间的增加,涂层致密度明显提高,且Mn和Co元素分布逐渐均匀,这与MnCo2O4的大量生成有关.由图5(i)可知,所制备的涂层有效地阻止了Cr的扩散,Cr元素大量富集在基体表面,并以Cr2O3的形成存在.采用ImageJ软件计算三种涂层的孔隙率,依次为8.22%,6.31%和7.72%,其中No.2涂层的致密度较高.

图5 No.1~No.3涂层试样800℃/10h后的截面形貌(a~c)及No.1涂层试样的元素分布(d~i)Fig.5 T he cross-sectional morphology of No.1-No.3 coating samples after 800℃/10h(a-c)and the element distribution of No.1 coating samples(d-i)
图6 为800℃/20 h后No.1~No.3涂层试样的截面形貌及No.1涂层试样的元素分布图.从图6可以看出,涂层中一些较小的孔隙融合形成大的孔洞,且部分区域出现细小的裂纹.对No.1涂层进行EDS分析(图6(d)~图6(i))发现,Mn和Co元素分布更加均匀,涂层中间区域开始出现Cu元素,说明此时Cu元素已经开始从表层向内层扩散,且已经有Cu-Mn尖晶石相生成(图3(j)~图3(l)表面形貌所示).采用ImageJ软件计算三种涂层的孔隙率,依次为15.19%,13.79%和15.97%.

图6 No.1~No.3涂层试样800℃/20 h后的截面形貌(a~c)及No.1涂层试样的元素分布(d~i)Fig.6 (a-c)cross-sectional morphology of No.1-No.3 coating samples after 800℃/20 h and(d-i)element distribution of No.1 coating samples
图7 为800℃/120 h后No.1~No.3涂层试样的截面形貌及No.1涂层试样的元素分布图.从图7可以看出,涂层表层的CuO氧化膜逐渐消失,表层区域更加致密,但靠近底部依旧存在大的孔洞,且与基体结合较差,这可能与喷涂时基体表面粗糙度较高有关.对No.1涂层进行EDS分析(图7(d)~图7(i))发现,更多的Cu元素扩散到涂层内部,且Cu元素分布均匀,由此可推测涂层中含有更多的尖晶石相(CuO可能与MnCo2O4发生固相反应,生成CuxMn3-xO4相).采用ImageJ软件计算三种涂层的孔隙率,依次为7.85%,7.60%和6.87%.综上所述:随氧化时间增加,Cu元素在氧化过程中先扩散到表面,随后因固相反应而向涂层内部扩散;比较三种参数涂层截面致密度发现,No.2涂层更好,但涂层与基体结合问题还需进一步探究.

图7 No.1~No.3涂层试样800℃/120 h后的截面形貌(a~c)及No.1涂层试样的元素分布(d~i)Fig.7 (a-c)cross-sectional morphology of No.1-No.3 coating samples after 800℃/120h and(d-i)element distribution of No.1 coating samples
3.4 涂层电导率测试
对三种参数涂层进行电导率测试,首先将试样放入管式炉中加热至800℃并氧化20 h,使金属涂层氧化转变成尖晶石涂层,随后开始电导率测试.图8为氧化120 h后涂层电导率与表面形貌图.从No.1~No.3涂层试样800℃下电导率随时间的变化曲线图(图8(a))可以看出,随着氧化时间增加电导率逐渐增加,经一定的氧化时间后电导率已达到稳定值,表明此时尖晶石转变基本完全,涂层明显致密化.不同APS参数下所制备的No.1~No.3涂层在800℃下氧化120 h的电导率分别达到59.68,93.55和85.72 S/cm,与APS制备的Mn1.5Co1.5O4涂层(700℃,40 S/cm)[2]和Cu掺杂的Mn1.5Co1.5O4涂层(750℃,27 S/cm)[17]相比电导率得到极大的提升.电导率增加主要来源于涂层中大量生成的MnCo2O4和CuxMn3-xO4(x=1,1.4,1.5)相.由于固相反应生成的尖晶石没有经历等离子喷涂时的高温,所生成的尖晶石杂相少,涂层致密缺陷较少,因此电导率较高.在所制备的三组试样中,No.2涂层试样在管式炉保温期间电导率持续上升,氧化120 h后电导率还有进一步增加的趋势,而No.1和No.3涂层试样的电导率在氧化50 h后基本保持稳定.这是由于800℃下氧化120 h后,所有涂层表面都表现出明显的尖晶石“金字塔”形貌,且局部区域被CuO层覆盖,而CuO层的存在会降低涂层的电导率.从图8(b)~图8(d)可以看出:No.1样品和No.3样品表面均发现了大量的CuO存在,虽然No.2样品也有CuO,但被CuO覆盖的面积明显较少,因此表现出最高的电导率.
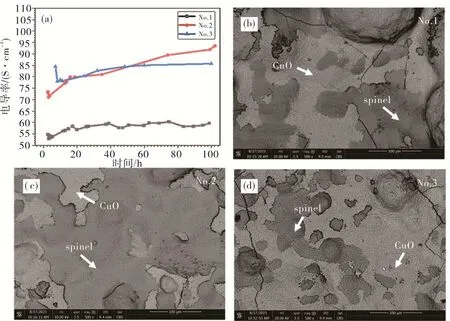
图8 氧化120 h后涂层电导率与表面形貌(a)电导率;(b)No.1试样表面形貌;(c)No.2试样表面形貌;(d)No.3试样表面形貌Fig.8 T he conductivity and surficial morphology of coatings after 120h oxidation(a)conductivity;(b)morphology of sample No.1;(c)morphology of sample No.2;(d)morphology of sample No.3
4 结论
(1)800℃氧化120 h,No.1~No.3涂层试样均生 成 了CuO,MnCo2O4和CuxMn3-xO4(x=1,1.4,1.5).不同喷涂参数下,No.2涂层试样的喷涂参数能加快固相反应进程,涂层中含有更多的导电尖晶石相.
(2)800℃、不同氧化时间下,涂层表面先生成CuO层,随后CuO层中出现金字塔状尖晶石相.当氧化时间达到120 h时,表层CuO层已呈不连续分布,且与涂层分层,产生微裂纹.同时,随着氧化时间增加涂层逐渐致密化,并形成顶部致密、底部多孔的结构.CuO层的演变过程主要与氧化过程Cu元素扩散有关,Cu元素先向涂层表面扩散,随后向涂层内部扩散.
(3)所有涂层都表现出较好的阻Cr扩散效果.氧化后基体中的Cr主要以Cr2O3的形式聚集在基体与涂层的结合处,形成富Cr层,而涂层中未见明显的Cr分布,这说明所制备的金属涂层和高温氧化后生成的尖晶石涂层均能很好地抑制Cr的扩散.
(4)采用四电极法测试No.1~No.3涂层试样的电导率,800℃氧化120 h后,其电导率可分别达到59.68,93.55和85.72 S/cm,其中No.2涂层试样具有更高的电导率.

