响应面优化提取向日葵列当中苯乙醇苷的工艺研究
吕佳佳,张 勇,戴余军*,江 芹,魏帅润喆,蔡树龙,殷 晓
(1.湖北工程学院 湖北省植物功能成分利用工程技术研究中心,湖北 孝感 432000; 2.湖北大学 生命科学学院,湖北 武汉 430062)
向日葵列当(OrobanchecumanaWallr.)俗称独根草、兔子拐棍,为列当科(Orobanchaceae)列当属(Orobanche)一年生全寄生性草本植物,在我国分布很广,主要分布于河北、北京、新疆、山西、内蒙古、黑龙江、辽宁、吉林等省(自治区、直辖市)[1-2]。列当属多种植物在我国部分地区民间已作为药用,其全草可入药,具有强筋壮骨、壮阳补肾、延缓衰老、改善脑组织循环、增强免疫等功效[3-4]。其主要的活性成分为苯乙醇苷(phenylethanoid glycosides,PhGs),是一类由咖啡酸、苯乙醇苷元和糖基组成的天然化合物,其结构特征主要是以β-葡萄糖为母核的并含有酯键及氧苷键,羟基和甲氧基连于苯乙基上,中心葡萄糖基上常连有乙酰基和咖啡酰基[5],其结构式见图1。现代药理研究表明,苯乙醇苷类化合物在抗菌、抗炎、抗氧化、抗病毒、增强免疫力等方面发挥着重要的作用[6-12]。向日葵列当是一种专化性较强的寄生性杂草,由于其自身没有叶绿素,不能进行光合作用,得完全靠从寄主向日葵根部吸取营养而存活,从而影响向日葵的产量和品质[13-15]。所以长期以来,向日葵列当一直被当作农田杂草进行防治根除,其药用价值被长期忽视。

图1 苯乙醇苷基本结构
本研究以向日葵列当全草为原料,采用乙醇加热回流法提取向日葵列当中苯乙醇苷,在单因素的试验结果的基础上,利用响应面法对其工艺条件进行优化,以期为向日葵列当药用资源的开发利用奠定基础。
1 实验方法
1.1 仪器与试剂
T9CS型双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);HH-6型数显恒温水浴锅(常州市亿能实验仪器厂);GTR16-2型高速冷冻离心机(北京时代北利离心机有限公司);PTX-JA2105电子天平(华志电子科技有限公司);超纯水(Milli-Q纯水系统,武汉优普纯水设备有限公司)。向日葵列当于2020年9月购自内蒙古商都县;毛蕊花糖苷标准品(CAS No:61276-17-3,批号:M01101910014 ,HPLC > 99%)购自北京中科质检生物技术有限公司;甲醇(色谱级)和乙醇(分析纯)购自国药集团化学试剂有限公司。
1.2 苯乙醇苷的提取
1.2.1 原料预处理
将一定量向日葵列当洗净后,置60 ℃干燥箱烘干,于多功能粉碎机中粉碎,过60目筛(0.25 mm孔径),密封冷藏备用。
1.2.2 提取工艺流程
向日葵列当粉与一定体积分数的乙醇配制成一定液固比→在一定温度下加热回流一定时间→离心(转速5000 r/min,15 min)→滤渣重复浸提一定次数→合并滤液,得到待测样品溶液。
1.2.3 最大吸收波长的确定
精密量取适量标准品、样品溶液,于200 ~ 800 nm处进行全波长扫描。
1.2.4 样品中苯乙醇苷含量的测定
本研究采用紫外分光光度法测定向日葵列当中苯乙醇苷含量[16]。用乙醇配制毛蕊花糖苷标准液(100 μg/mL),精确吸取1,2,3,4,5,6,7,8,9,10,11,12,13 mL标准液并定容至25 mL,充分混匀。以95%乙醇为空白,在335 nm下测定吸光度值,以毛蕊花糖苷浓度为横坐标,吸光度值为纵坐标,绘制标准曲线。回归方程为:y=0.0289x+ 0.003(R2=0.9999),表明在0 ~ 52 μg/mL范围内毛蕊花糖苷浓度与吸光度值具有良好的线性关系。
样品溶液用95%乙醇溶液稀释至合适浓度,测定335 nm处吸光度值,计算样品中苯乙醇苷含量。苯乙醇苷得率的计算公式为:
式中:Y为苯乙醇苷得率(%),C为样品溶液中苯乙醇苷的含量(μg/mL),V为样品溶液体积(mL),N为稀释倍数,M为样品质量(g)。
1.2.5 影响提取效果的因素试验
1)单因素试验设计
分别对溶剂的种类(乙醇、甲醇、水)、溶剂质量分数(35%,45%,55%,65%,75%)、提取温度(35,50,65,80,85 ℃)、提取时间(30,60,90,120,150 min)、液固比(10∶1,20:1,30:1,40:1,
50:1(mL/g))、提取次数(1,2,3,4,5)进行单因素考察。
2)响应面优化试验
在单因素试验结果的基础上,根据响应面法Central Composite Design设计原理,以单因素结果所选因素为自变量,苯乙醇苷得率为响应值,进行4因素3水平响应面试验,利用Design-Expert 8.0.6软件对试验结果进行多元线性回归方程拟合,检验模型,根据模型进行响应值预测,优化向日葵列当中苯乙醇苷的提取工艺条件,并进行验证试验。
1.2.6 数据处理
所有试验均重复3次,所得数据分别用Excel 2016、Design-Expert 8.0.6软件进行分析处理。
2 结果与分析
2.1 最大吸收波长的确定
由图2可知,标准品和样品均在335 nm处有最大吸收峰,故选择335 nm作为本试验苯乙醇苷的测定波长。

图2 标准品和样品的扫描光谱图
2.2 单因素试验结果
2.2.1 溶剂的种类对苯乙醇苷提取效果的影响
不同的提取溶剂对苯乙醇苷提取效果的影响见图3。由图3可知,3种不同溶剂提取苯乙醇苷得率分别为9.23%(乙醇)、7.70%(甲醇)和4.31%(水),由于乙醇具有低毒性、高渗透性和易挥发性等性质,其在天然活性成分的提取中备受青睐。因此,本研究选用乙醇作为后续实验提取剂。

图3 溶剂种类对苯乙醇苷得率的影响
2.2.2 溶剂质量分数对苯乙醇苷提取效果的影响
不同溶剂质量分数对苯乙醇苷提取效果的影响见图4。由图4可知,当溶剂质量分数在35% ~ 55%时,苯乙醇苷得率随溶剂质量分数的增大而增加,当溶剂质量分数大于55%,随着溶剂质量分数的增大,苯乙醇苷得率反而下降,这可能是较高的溶剂质量分数使苯乙醇苷的溶出率趋于饱和,同时使其他醇溶性物质增多,从而导致苯乙醇苷得率下降。因此选择最佳的溶剂质量分数为55%。

图4 溶剂质量分数对苯乙醇苷得率的影响
2.2.3 提取温度对苯乙醇苷提取效果的影响
温度的高低,会影响苯乙醇苷分子之间的扩散速度。不同提取温度对苯乙醇苷提取效果的影响见图5。由图5可知,随着提取温度的升高,苯乙醇苷提取得率呈现先升高后降低的趋势,在30 ~ 80 ℃时,随提取温度的增加而升高,当提取温度超过80 ℃后,苯乙醇苷提取得率呈下降趋势,这可能是由于过高的提取温度影响了苯乙醇苷的稳定性,因此选择最佳的提取温度为80 ℃。
2.2.4 提取时间对苯乙醇苷提取效果的影响
时间因素是影响工业化产量周期的一个关键性因素,因此常作为工业提取重要的因素考察。不同提取时间对苯乙醇苷提取效果的影响见图6。由图6可知,随着提取时间的延长,苯乙醇苷提取得率呈现先升高后急剧下降至基本稳定的趋势。在60 min时,苯乙醇苷得率最高,这可能是因为在60 min前,原料中的物质在提取溶剂中得到充分溶解。继续延长浸提时间,开始急剧下降最后趋于稳定,这可能是由浸提时间过长导致苯乙醇苷物质的活性发生改变,且较长的时间也会大大影响工业化生产周期。因此选择最佳的提取时间为60 min。
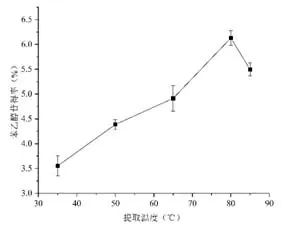
图5 提取温度对苯乙醇苷得率的影响

图6 提取时间对苯乙醇苷得率的影响
2.2.5 液固比对苯乙醇苷提取效果的影响
合适的液固比可以减少原料和试剂的消耗。不同液固比对苯乙醇苷提取效果的影响见图7。由图7可知,随着液固比的增加,苯乙醇苷提取得率随之增大,当液固比为40:1(mL/g)之后,苯乙醇苷得率开始下降,这可能是在苯乙醇苷提取的过程中,需要一定的溶剂渗入原料的孔隙中,进行溶解出苯乙醇苷,当溶剂过多时,溶解出的苯乙醇苷达到饱和后便开始稀释苯乙醇苷溶液,进而导致苯乙醇苷得率降低。因此选择最佳的液固比为40:1(mL/g)。

图7 液固比对苯乙醇苷得率的影响
2.2.6 提取次数对苯乙醇苷提取效果的影响
选择合适的提取次数,既可以最大限度获取苯乙醇苷,也可以在一定程度上节省时间,减少提取剂的浪费。不同提取次数对苯乙醇苷提取效果的影响见图8。由图8可知,随着提取次数的增加,苯乙醇苷提取得率随之增加,提取4次后,苯乙醇苷得率渐渐趋于稳定,说明在提取4次后,苯乙醇苷类物质已基本提出。因此,综合考虑,在优化试验中,将提取次数固定为4次。
2.3 响应面法优化向日葵列当中苯乙醇苷提取工艺
2.3.1 Design-Expert 8.0.6设计及试验结果
在单因素试验结果的基础上,提取次数固定为4次,采用响应面(Central Composite Design)设计原理。以苯乙醇苷得率为响应值(Y),选取溶剂质量分数(A)、提取温度(B)、提取时间(C)、液固比(D)作为自变量,建立4因素3水平共30个试验点的响应面分析试验模型,其中24个为析因点,6个为检验误差的中心点。因素水平表见表1,试验设计和结果见表 2。
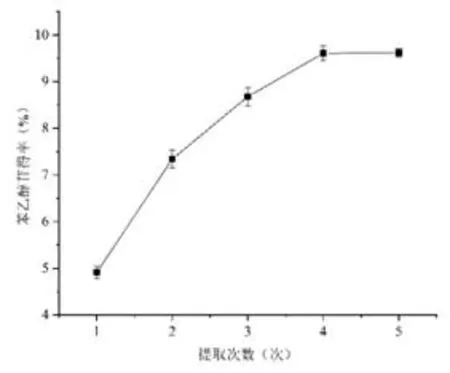
图8 提取次数对苯乙醇苷得率的影响

表1 响应面试验因素水平表

表2 响应面试验设计及结果
2.3.2 响应面方差分析
利用Design-Expert 8.0.6软件对试验结果进行方差分析,结果见表3。由表3可知,模型显著性检验为极显著(P< 0.01),说明模型的建立具有统计学意义。失拟项为不显著(P= 0.3259 > 0.05),说明模型与实验的误差较小,无拟合因子的缺失。F值的大小可直接判断各因素对苯乙醇苷得率的影响程度,F值越大,对苯乙醇苷得率的影响就越显著。F值大小依次为:提取温度 > 提取时间 > 溶剂质量分数 > 液固比。校正决定系数R2=0.9951,说明自变量引起的苯乙醇苷得率变化占99.51%,变异系数为0.15%,说明模型中只有0.15%的变异,进一步印证该模型具有较好的拟合度。
通过模型分析,以苯乙醇苷得率(Y)对A、B、C、D的二次多项式回归方程为:
Y=6.06+0.3A+0.68B+0.18C+0.063D+0.044AB+0.052AC+0.075AD+0.55BC-0.41BD-0.2CD+0.11A2+0.25B2-0.051C2+0.25D2+0.15ABC+0.36BCD-0.41A2B-1.06A2D-0.079AB2+0.85A2B2(R2=0.9951)。
模型中,A、B、C、BC、BD、CD、B2、D2、ABC、BCD、A2B、A2D、A2B2对苯乙醇苷得率的影响为极显著(P< 0.01)。

表3 响应面方差分析表
2.3.3 响应曲面分析
响应曲面可直观反映各因素之间交互的显著性,响应曲面越陡峭,说明因素之间的交互作用越显著,影响越大,反之则影响越小[17]。利用 Design-Expert 8.0.6 软件可以分析各因素对苯乙醇苷得率的影响以及任意2个因素之间的交互作用,响应面曲线见图9。由图9可知,在交互项对苯乙醇苷得率的影响中,当其他因素保持在零水平时,溶剂质量分数的改变对提取温度、提取时间和液固比的显著影响程度不大,反之也是。这说明溶剂质量分数与提取温度、提取时间和液固比之间的交互作用并不显著,但其他因素之间的交互作用显著,这与表3方差分析结果是一致的。

图9 各因素交互作用对苯乙醇苷得率影响的响应面图
2.4 最佳工艺条件的确定及模型验证
为了确定最佳工艺优化参数,利用Design-Expert 8.0.6软件对回归模型方程进行进一步分析,得到向日葵列当中苯乙醇苷提取的最佳工艺参数为:溶剂质量分数为55%,提取温度为85 ℃,提取时间为90 min,液固比为30:1(mL/g),提取次数为4次。在此条件下,模型预测苯乙醇苷得率为10.117%,与试验15号条件一致。为进一步确定其工艺参数的可行性及稳定性,在上述条件下进行验证性试验,平行测定3次,苯乙醇苷平均得率为10.223%±0.03%,与模型预测值相比,相对误差约为0.106%,这说明实际值与模型预测值之间无显著性差异。由此可知,通过此模型来预测向日葵列当中苯乙醇苷的提取工艺是可行的。
3 小结
本研究采用干燥的向日葵列当粉末为原料,乙醇为提取溶剂进行回流提取。通过单因素试验及响应面优化试验确定了向日葵列当中苯乙醇苷的提取工艺:溶剂质量分数为55%,提取温度为85 ℃,提取时间为90 min,液固比为30:1(mL/g),提取次数为4次,在此条件下,苯乙醇苷得率为10.223%±0.03%,与模型预测值相比无显著性差异。通过响应面模型分析,该工艺条件是稳定可行的。

