体外膜肺氧合联合急诊经皮冠状动脉介入术成功抢救急性心肌梗死并心脏停搏一例报道
刘利平,赵文奇,荣小伟,郭胜,张晔
体外膜肺氧合(extracorporeal membrane oxygenation,ECMO)作为一种经皮置入的机械循环辅助技术,近年来在临床上应用于常规生命支持无效的急性呼吸和循环功能衰竭患者[1]。急性心肌梗死并心脏停搏患者由于常规心肺复苏自主循环恢复率较低,无法提供有效的冠状动脉灌注压,常导致急诊经皮冠状动脉介入术(percutaneous coronary intervention,PCI)无法实施,如能早期建立ECMO,迅速恢复患者全身血液循环和血氧供给,使其行PCI时血流动力学维持稳定,血压较为平稳,可提高手术的安全性和有效性[2]。国药同煤总医院心脏中心引进了ECMO设备,由急诊科、心脏中心、ICU和B超室医护人员组建抢救小组,经过技术培训,于2021-01-07运用ECMO联合急诊PCI成功抢救1例急性心肌梗死并心脏停搏患者,现报道如下。
1 病例简介
患者,男,57岁。因“持续性胸痛10 h”于2021-01-07 18:00入住国药同煤总医院。患者10 h前出现持续性胸痛,颜面发绀,全身发冷,多汗。就诊于当地医院,诊断为急性心肌梗死,静脉溶栓后症状缓解,由120救护车转运至国药同煤总医院行急诊PCI。途中出现意识丧失,颜面发绀,肢体抽搐,大动脉搏动消失,心电监护示:心室颤动(ventricular fibrillation,VF)。经电除颤、心肺复苏(cardiopulmonary resuscitation,CPR),心跳恢复,静脉滴注多巴胺以维持血压。既往有糖尿病史8年。体格检查:脉搏119次/min,呼吸16次/min,血压114/66 mm Hg(1 mm Hg=0.133 kPa,多巴胺维持),血氧饱和度57%,浅昏迷,双肺可闻及湿啰音,心音低钝,律齐。心电图检查显示:阵发性室上性心动过速,Ⅱ、Ⅲ、aVF、aVR、V6~V8导联ST段抬高0.1~0.5 mV。心脏彩超检查显示:左心室壁节段性运动异常、左心功能减低,左心室射血分数44%。肌钙蛋白I 27.858 μg/L,肌红蛋白1 709.0 μg/L,N末端脑钠肽前体4 953 ng/L。血气分析显示:酸碱度6.99,二氧化碳分压50 mm Hg,氧分压22 mm Hg,乳酸11.6 mmol/L,实际碳酸氢根12.0 mmol/L,细胞外液碱剩余-19.4 mmol/L,凝血酶原活动度43.0,凝血酶原时间(prothrombin time,PT)-国际标准化比值(international normalized ratio,INR)1.64,凝血酶时间125.5 s,纤维蛋白原0.19 g/L。初步诊断:急性下壁后壁右心室心肌梗死,VF,心脏停搏复苏成功,心源性休克,Ⅱ型呼吸衰竭,Killip分级Ⅳ级,凝血功能异常,代谢性酸中毒。来院后反复发生心脏停搏6次,心电监护仪显示:VF,电除颤6次、CPR 6次,间断静脉推注肾上腺素,每次抢救时间10~20 min,心跳恢复。复苏间歇立即气管插管,连接呼吸机,机械通气,选择压力控制通气模式辅助呼吸,氧浓度100%,潮气量400 ml,呼气末正压10 cm H2O(1 cm H2O=0.098 kPa);经血管活性药物维持血压,左西孟旦改善心功能,冰冻血浆、冷沉淀补充凝血因子,碳酸氢钠纠正酸中毒等对症治疗,入院4.5 h后未出现心脏停搏,病情趋于稳定,心电图转为窦性心律,凝血指标改善,此时由于呼吸、循环功能衰竭导致机体不能维持供氧需求,血流动力学不稳定,不能实施PCI,与家属沟通后采用ECMO治疗。入院后10 h床旁选择右侧股静脉穿刺置入21 F ECMO静脉导管、右侧股动脉穿刺置入17 F ECMO动脉导管,连接ECMO管路,选择V-A模式,转速3 010 r/min,流速3.78 L/min,氧浓度70%,气流2 L/min,辅助心、肺功能。2021-01-08 11:40即入院后17.5 h(静脉溶栓约20.5 h后)在呼吸机、ECMO支持下行冠状动脉造影、急诊PCI。冠状动脉造影结果见图1A~C。对右冠状动脉(right coronary artery,RCA)行介入干预:用2.5 mm×15.0 mm的TREK球囊以12 atm×10 s扩张RCA病变,将3.5 mm×36.0 mm的乐普(GuReater)支架置于病变处,以12 atm×10 s释放支架,用3.5 mm×15.0 mm的NC TREXK球囊以14~20 atm×5 s对支架后扩张整形,重复造影未见残余狭窄,见图1D。手术时间为50 min。术后于床旁行左侧股动脉穿刺并放置动脉鞘管以连接主动脉内球囊反搏(intra-aortic balloon pump,IABP)仪,以心电触发,1∶1反搏,同时联合ECMO用于心源性休克、心力衰竭的治疗。心电图检查显示:窦性心动过速,Ⅱ、Ⅲ、aVF导联ST段抬高0.1~0.2 mV。急诊PCI中和ECMO、IABP治疗期间的机械作用及肝素的使用导致活化的凝血活酶时间为118.4 s,血小板计数为46×109/L,予以静脉输注冰冻血浆、冷沉淀、血小板来改善凝血功能。2021-01-09 14:38患者处于药物镇静镇痛状态,去甲肾上腺素维持血压为109/66 mm Hg,球结膜水肿,全身水肿。心脏彩超检查显示:各房室内径正常,左心室室壁运动整体减低,主、肺动脉内径正常,左心室射血分数52%。动脉血气分析显示:酸碱度7.41,二氧化碳分压27 mm Hg,氧分压225 mm Hg,乳酸1.6 mmol/L,实际碳酸氢根17.1 mmol/L,细胞外液碱剩余-7.5 mmol/L。患者急诊PCI后,闭塞的冠状动脉成功实现血液再灌注,心脏自主神经功能逐渐恢复,左心室射血分数达52%,可以满足机体供氧,为减少并发症的发生,停止ECMO治疗。2020-01-11患者球结膜水肿,全身水肿加重,尿少。胸部X线检查显示:肺淤血征象。行床旁连续性肾脏替代疗法(continuous renal replacement therapy,CRRT)以促进液体排出、减轻心脏负担、改善肺水肿。2021-01-13患者血压119/62 mm Hg,血氧饱和度99%,尿量增加,全身水肿明显,心肌酶明显降低,停用CRRT,改用利尿剂以促进液体排出。2021-01-14患者停用镇静、镇痛、血管活性药物,测血压116/70 mm Hg,意识清楚,拔除IABP。2021-01-16患者通过自主呼吸试验(spontaneous breathing trial,SBT),脱呼吸机,患者问答切题,偶有词不达意及幻觉,继续住院给予心脏、神经功能康复治疗。2021-01-25患者无自觉胸痛、胸闷、心悸等症状,问答切题,无幻觉,好转出院。随访2个月,患者心脏、神经系统功能恢复良好。
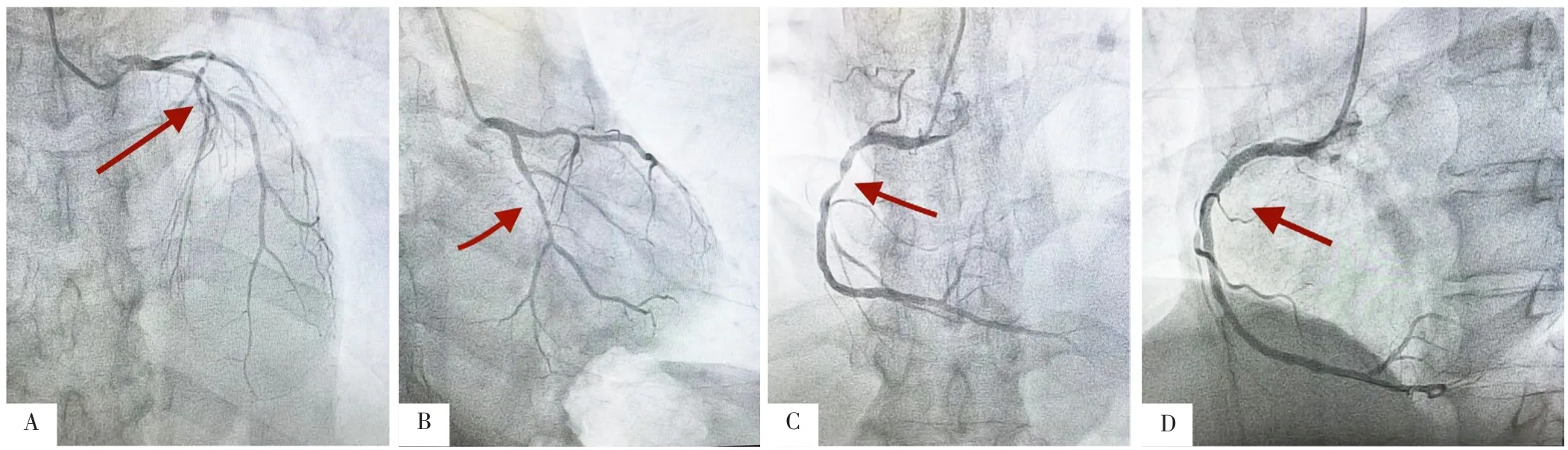
图1 患者冠状动脉造影及急诊经皮冠状动脉介入术结果Figure 1 Results of coronary angiography and emergency percutaneous coronary intervention
2 讨论
ST段抬高型心肌梗死(ST-segment elevation myocaedial infarction,STEMI)是冠状动脉粥样硬化性心脏病中最严重的类型,是猝死的常见病因,具有高发病率、高致死致残率、高花费的特点[3]。早期、快速、完全开通梗死相关冠状动脉并恢复其血供,挽救濒临坏死的心肌细胞是救治STEMI的关键,且PCI、静脉溶栓和外科手术是STEMI患者再灌注治疗的主要措施[4]。其中发病12 h内直接PCI以其可以完全解除冠状动脉狭窄的优势而成为首选治疗方法[5]。患者如就诊于不具备PCI条件的医院,且不能在120 min内完成转运及PCI,根据2017年欧洲指南[6]及2015年我国《急性ST段抬高型心肌梗死诊断和治疗指南》[4],建议在首诊医院于就诊30 min内开始溶栓,溶栓成功后再转运至有PCI条件的医院,使其于溶栓后3~24 h行PCI。早期溶栓可以使PCI时间窗延长,溶栓只是治疗的起点,因为梗死相关动脉破裂斑块只有通过PCI才能消除,只有彻底清除斑块才能避免可能出现的血管再闭塞,由于溶栓后可能出现冠状动脉再闭塞,为了争取心肌再灌注时间,先溶栓再行早期PCI是一个比较好的选择[7]。《2019年中国成人急性ST段抬高型心肌梗死医疗质量控制报告》[8]显示,只有约22.0%的溶栓患者接受药物介入联合再灌注治疗,远不能达到STEMI患者的治疗需求。本例急性心肌梗死患者在当地医院溶栓后症状缓解,转运中出现心脏停搏,可能与血管再闭塞有关,而溶栓为PCI赢得了宝贵的时间,使其在溶栓后20.5 h完成PCI,符合指南要求的溶栓后3~24 h的PCI时间窗。
STEMI后出现心脏停搏属高危PCI患者[4],病死率较高。由于STEMI后心脏停搏的患者需先行CPR,其血流动力学不稳定会影响PCI的实施,此时启用危重症抢救技术ECMO成了最好的选择。ECMO可同时替代肺的气体交换和心脏的泵血功能,可提供4.5 L/min的心输出量,使缺血缺氧的组织器官得到持续稳定的血流和氧供,让心脏得以休息,为冠状动脉再灌注争取时间,是治疗各种急性双心室功能衰竭并呼吸功能衰竭患者的首选方法,尤其适合急性心肌梗死并心脏停搏患者抢救的辅助治疗[9-10]。研究显示,ECMO可提高STEMI后心脏停搏患者的出院存活率[11],STEMI后出现心脏停搏采用ECMO联合PCI抢救患者的存活率为45.9%[12]。本例急性心肌梗死并心脏停搏患者因入院前使用静脉溶栓药物,且多次发生心脏停搏使组织器官缺血、缺氧,造成凝血功能异常,此时建立ECMO存在出血风险,经输注冰冻血浆、冷沉淀补充凝血因子等治疗,凝血功能得以改善,于入院后10 h置入ECMO。在ECMO支持下,使急诊PCI得以顺利进行,罪犯血管开通,STEMI病因去除,患者存活,神经、脑功能逐渐恢复,好转出院。
动脉血乳酸是反映心肌灌注、判断预后的有效指标,血乳酸>8 mmol/L患者的病死率升高[13]。本例患者运用ECMO前病情危重,血乳酸为11.6 mmol/L,PCI后心肌实现再灌注,病情扭转,血乳酸为1.6 mmol/L,预后改善,表明血乳酸可能在预测心脏停搏患者的预后方面具有重要参考价值。
ECMO后常见的并发症是出血,主要是术中应用肝素以及体外血液循环中的血小板损耗所致,其次是感染、肺水肿、肾衰竭等[14],本例患者为减少并发症的发生,停止ECMO,提示ECMO后并发症的发生率较高。
综上,对于急性心肌梗死并心脏停搏患者,在抢救过程中及时建立ECMO,维持血流动力学稳定,早期联合急诊PCI,开通罪犯血管,解除病因,对改善患者预后有重要作用。ECMO在循环衰竭的抢救中具有良好的应用前景,但由于建立ECMO需要特定的装置、专门的救治小组、较高的技术要求,且操作有一定的创伤、并发症发生率较高及治疗费用较高,使其在临床运用率较低,这是今后工作中需要探讨、解决的问题。
作者贡献:刘利平进行文章的构思与设计、文章的可行性分析,撰写论文,进行论文的修订;赵文奇、荣小伟、郭胜、张晔进行文献、资料收集;张晔进行英文的修订,负责文章的质量控制及审校,对文章整体负责、监督管理。
本文无利益冲突。

