碳负载Pd0.8 Fe0.2合金催化剂的氧还原催化性能*
赵东江,马松艳,田喜强,白晓波,郭 齐
(绥化学院 食品与制药工程学院,黑龙江 绥化152061)
铂基催化剂具有高的催化活性,已经成为质子交换膜燃料电池(PEMFCs)阴极氧还原反应(ORR)最有效的电催化剂。然而,铂基催化剂成本高、资源少、耐久性低等问题严重阻碍了PEMFCs的商业化[1]。为了解决这些问题,人们对钯基材料、碳基材料、过渡金属硫族化合物、金属-有机骨架(Metal-Organic Frameworks,MOFs)材料等非Pt催化剂进行广泛研究[2,3]。
在PEMFCs非Pt催化剂研发中,钯基材料作为具有较高催化活性的阴极催化剂受到关注。钯与铂是同一族元素,具有类似的化学和物理性质,是除铂外对ORR电催化活性最高的金属之一,其地球储量比Pt丰富,价格也比Pt低[4]。因此,金属Pd被认为是Pt催化剂一种很有前途的替代材料。然而,纯金属Pd对氧还原催化活性明显低于Pt,为了改善Pd催化剂的性能,进一步提高催化活性和降低成本,采取合金化方法合成Pd基金属合金,能够有效提高催化活性和稳定性。Pd与贵金属Pt、Au、Ag形成的Pd-Pt[5]、Pd-Au[6]、Pd-Ag[7]等合金催化剂,对ORR具有优良催化性能,缺点是成本较高。而Pd与过渡金属形成的合金,既可以降低催化剂价格,又可以改善Pd催化剂氧还原性能,比如,Pd-Fe[8]、Pd-Cu[9]、Pd-Co[10]等Pd基合金的氧还原催化活性超过Pd催化剂,而且稳定性明显提高。在Pd基过渡金属合金催化剂中,Pd-Fe/C纳米材料对ORR具有良好的催化性能,引起研究人员的高度关注。
本文采用回流技术,在1,6-己二醇溶剂中通过Pd(C5H7O2)2与Fe3(CO)12热分解反应制备Pd0.8Fe0.2/C合金催化剂,并利用X射线衍射(XRD)和扫描电镜(SEM)技术表征催化剂物理性能,采用旋转圆盘电极(RDE)技术分析催化剂的ORR的催化性能。
1 实验部分
1.1 试剂与仪器
1,6-己二醇(天津市兴复精细化工研究所);乙酰丙酮钯(Pd(C5H7O2)2上海笛柏化学品技术有限公司);Fe3(CO)12(美国Alfa Aesar公司);浓H2SO4(哈尔滨市新达化工厂),以上均为分析纯;Vulcan XC-72碳黑(美国Cabot公司);Nafion乙醇溶液(美国杜邦公司);医用O2(绥化市氧气厂);高纯N2(绥化市氧气厂)。
S-4800型高分辨场发射扫描电镜(SEM日本日立公司);D8 Advance X射线衍射仪(XRD德国布鲁克AXS公司);CHI660D型电化学工作站(上海辰华仪器有限公司);ATA-1B型旋转圆盘电极(RDE江苏江分电分析仪器有限公司);KQ-50DB型数控超声清洗器(昆山市超声仪器有限公司)。
1.2 催化剂的制备
Pd0.8Fe0.2/C催化剂的制备方法与文献[11]相同,主要操作流程为:按比例(Pd与Fe摩尔比)称取一定量的Pd(C5H7O2)2与Fe3(CO)12反应原料,加入到含有50g 1,6-己二醇溶剂和160mg Vulcan XC-72炭黑的50mL圆底烧瓶中,在搅拌条件下将体系加热至回流温度(约220℃),反应3h,冷却后,加适量乙酸乙酯和超纯水并离心分离,沉淀用乙醚超声清洗3次,所得黑色粉末即为催化剂样品。采用相同方法制备了Pd/C催化剂。
1.3 催化剂的表征
采用XRD进行催化剂样品结构分析,辐射源CuKα,波长0.15418nm;采用SEM分析催化剂的表面形貌,加速电压15kV。采用CHI660D型电化学工作站和RDE分析催化剂的ORR催化性能。
1.4 电化学测试
在三电极电解池中测试催化剂的电化学性能,利用CHI660D型电化学工作站控制。在RDE实验中,玻碳电极(Φ=3cm)为工作电极基底,铂丝为对电极,Hg/Hg2SO4电极用作参比电极,0.5mol·L-1H2SO4为电解液。按照文献[11]方法制备催化剂膜电极:将4.0mg样品加入到1mL超纯水中,超声分散15min得催化剂悬浊液,取该液7.0μL涂在玻碳电极表面,在空气中干燥后,用6.5μL 5%Nafion溶液涂于催化剂表面,再次干燥,制成薄膜型电极。
测试样品催化性能前,在N2饱和电解液(通气30min)中,对工作电极进行电位循环扫描20min,扫描范围为0.80~0.05V(vs.RHE),扫速为25mV·s-1,使电极达到活化状态。电极活化后进行RDE实验,先向电解液通医用O2至饱和(30min),然后利用线性电位扫描(LSV)和循环伏安(CV)技术测试样品的氧还原催化性能,LSV测试从开路电位至0.1V(vs.RHE),扫速10mV·s-1,RDE转速为200~2500r·min-1;CV实验电位范围0.90~0.03V(vs.RHE),扫速25mV·s-1。
2 结果与讨论
2.1 XRD分析
图1为制备的Pd/C和Pd0.8Fe0.2/C催化剂的XRD图谱。
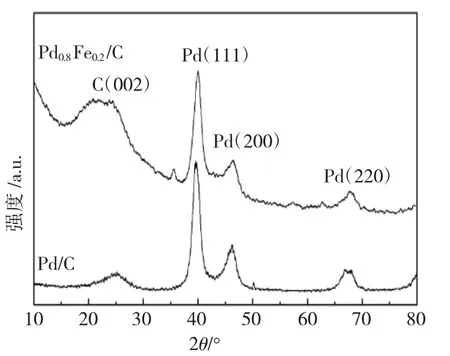
图1 Pd/C和Pd0.8Fe0.2/C催化剂的XRD图谱Fig.1 XRD patterns for the Pd/C and Pd0.8Fe0.2/C catalyst powders
由图1可见,Pd/C催化剂呈现出面心立方Pd晶体结构特征,在25°附近的衍射峰属于XC-72 C(002)晶面,在39.7°、46.2°、66.8°附近的3个衍射峰依次归属于Pd的(111)、(200)、(220)晶面[12]。与Pd/C相比,Pd0.8Fe0.2/C催化剂Pd衍射峰位置发生不同程度的正向偏移,表明Fe原子取代Pd进入了Pd的晶格,与Pd形成Pd-Fe合金。因Fe原子半径比Pd小,进入Pd晶格后导致衍射峰正移,产生晶格收缩,2θ值增大[13]。利用图1中Pd(111)、Pd(200)、Pd(220)衍射峰数据,根据下列Scherrer方程,可计算出晶体颗粒的平均粒径:

式中K=0.89;λ=0.15418nm;β:衍射峰高为1/2处的峰宽;θ:衍射角。
计算得到Pd/C和Pd0.8Fe0.2/C催化剂晶粒的平均粒径分别为4.28和4.03nm,表明原子半径较小Fe元素的加入使Pd晶粒粒径减小。
2.2 SEM分析
图2为Pd0.8Fe0.2/C样品的SEM图像。

图2 Pd0.8Fe0.2/C催化剂的SEM图像Fig.2 SEM micrograph of the Pd0.8Fe0.2/C catalyst
由图2可以看出,Pd0.8Fe0.2/C粉末存在聚集现象,聚集的颗粒较为均匀,在碳载体上催化剂分散较好。采用回流法热分解金属有机化合物制备碳载催化剂,一般都会发生类似聚集现象,催化剂在碳载体上均匀分散可获得较好的催化性能。
图3为Pd0.8Fe0.2/C催化剂的能谱图。
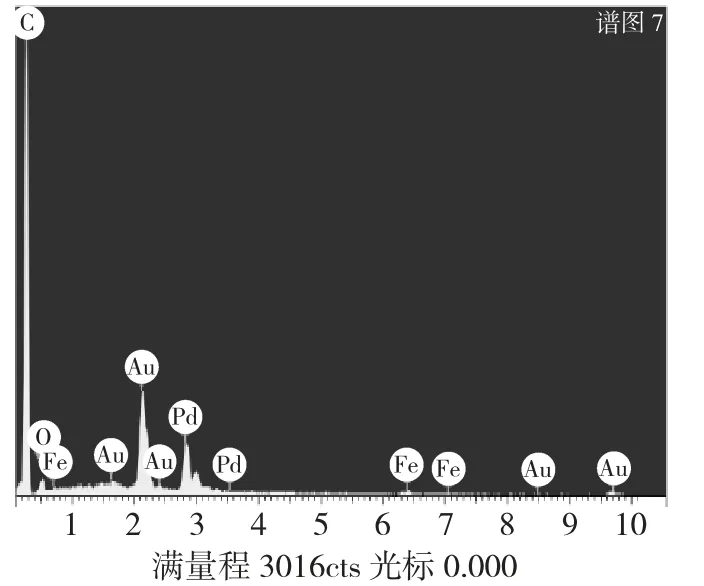
图3 Pd0.8Fe0.2/C催化剂的EDS谱图Fig.3 EDS spectrum of the Pd0.8Fe0.2/C catalyst
处理各种元素在图中峰面积,可以得出Pd与Fe元素的原子比为80.75∶19.25,接近制备催化剂时原料中Pd∶Fe=80∶20的配比值。谱图中的C主要源于催化剂载体材料,同时也有少量的C和O可能是催化剂表面吸附的O2和CO2所致;检测到的Au元素是测试前样品喷金的结果。
2.3 催化性能分析
2.3.1 循环伏安分析 在O2饱和的0.5mol·L-1H2SO4中,测试了Pd0.8Fe0.2/C催化剂样品CV曲线,扫速为25mV·s-1,见图4。

图4 Pd0.8Fe0.2/C催化剂在氧气饱和电解液中的循环伏安曲线Fig.4 Cyclic voltammogram of the Pd0.8Fe0.2/C catalyst in oxygen saturated electrolytes
由图4可以看出,在O2还原电位范围内,电位负向扫描时CV曲线呈现出强还原峰,说明在酸性电解液中催化剂对氧还原有明显催化活性。第1次CV循环的峰电位(Ep)和峰电流(Ip)分别为0.64V和1.27mA·cm-2,第2~4次CV循环的Ep和Ip均为0.65V和0.79mA·cm-2,说明经过第1次电位循环扫描后,催化剂表面趋于稳定,而第1次较大的Ip可能与电极表面吸附氧的还原有关。
2.3.2 催化活性分析 在氧气饱和的0.5mol·L-1H2SO4溶液中,利用RDE测定制备的Pd0.8Fe0.2/C催化剂在不同转速下对ORR的极化曲线,电位扫速为10mV·s-1,见图5。
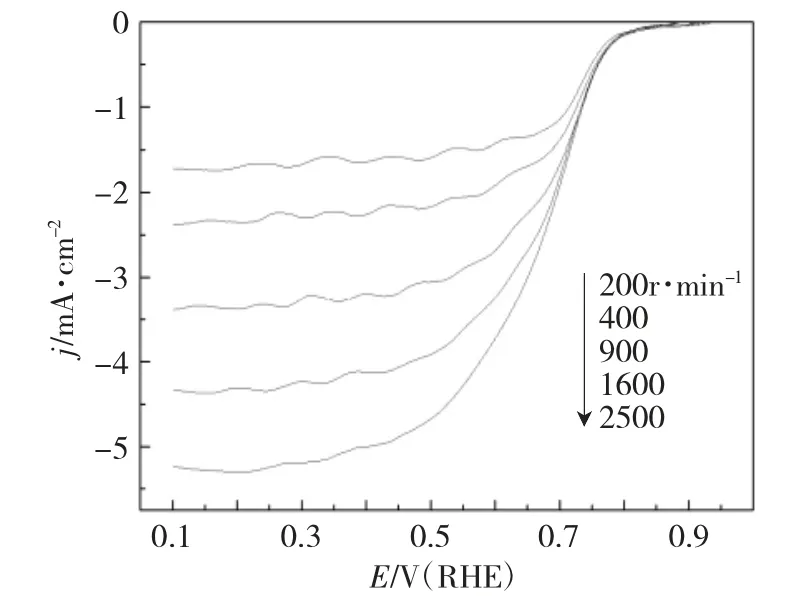
图5 Pd0.8Fe0.2/C催化剂对氧还原的极化曲线Fig.5 Polarization curve of the Pd0.8Fe0.2/C catalyst towards the oxygen reduction
由图5可以看出,样品对氧还原呈现明显的催化活性,随着电极转速增大,催化剂在混合控制区和动力学区的极化曲线基本重合,在扩散控制区的电流密度逐渐增大,且极化曲线比较平缓。
图6为Pd/C和Pd0.8Fe0.2/C催化剂经传质校正的氧还原极化曲线,RDE转速为1600r·min-1,jm为单位质量催化剂电流密度。

图6 在1600r·min-1转速下Pd/C和Pd0.8Fe0.2/C催化剂的ORR极化曲线Fig.6 Polarization curves of the Pd/C and Pd0.8Fe0.2/C catalysts for the ORR at 1600r·min-1 speed
在0.30 V时,Pd/C和Pd0.8Fe0.2/C催化剂的质量活性分别为4.28和5.72mA·mg-1,Pd0.8Fe0.2/C的质量活性是Pd/C的1.34倍,表明在Pd中添加Fe元素能够提高ORR催化活性。根据XRD分析结果,添加的Fe原子进入Pd晶格,形成了Pd-Fe合金,使Pd晶粒减小,改变了Pd的电子状态和晶体结构,降低了氧与Pd结合力,抑制表面Pd的氧化,促进吸附氧的解离和还原,从而提高催化剂对ORR的催化性能[14]。
2.4 催化机理分析
在测定的氧还原极化曲线中,RDE电流jD包括动力学控制电流ik和扩散控制电流id两部分,三者之间关系满足Koutecky-Levich(K-L)方程[15],即

式中 ω:RDE转速,r·min-1;B:Levich斜率。
图7为根据图5实验数据得到的Pd0.8Fe0.2/C催化剂在不同电位下的K-L曲线。

图7 Pd0.8Fe0.2/C催化剂的Koutecky-Levich图Fig.7 Koutecky-Levich plots of the Pd0.8Fe0.2/C catalyst
由图7可见,在0.4、0.5和0.6V电位下,K-L曲线呈现出一组直线,且几乎与四电子氧还原反应的理论曲线平行,说明氧分子还原过程中转移的电子数相近,与氧浓度之间关系服从一级反应规律。对图7中各测试电位下的曲线进行线性化处理,计算出Pd0.8Fe0.2/C催化剂j-1与ω-1/2直线的平均斜率为12.19×10-2mA·cm-2·(r-1·min)1/2,比四电子反应9.41×10-2mA·cm-2·(r-1·min)1/2的理论值大些,与相同条件下Pd/C催化剂的11.11×10-2mA·cm-2·(r-1·min)1/2接近,可能与用电极面积代替粉末催化剂比表面积产生的偏差有关[11]。根据以上结果,氧分子在Pd0.8Fe0.2/C上的还原过程应服从四电子转移机理,即

3 结论
在1,6-己二醇反应介质中,利用回流技术合成了Pd0.8Fe0.2/C催化剂,所得样品呈现面心立方结构,Fe元素进入Pd晶格形成Pd基合金,导致Pd晶粒减小。催化剂样品存在聚集现象,其颗粒大小较为均匀。在O2饱和电解液中,添加Fe对Pd/C催化剂的ORR催化性能有改善作用,催化活性明显提高。氧分子在Pd0.8Fe0.2/C催化剂上按四电子机理还原生成水。Fe对Pd/C催化活性的影响,主要归因于Fe元素进入Pd晶格,改变了Pd的电子状态和晶体结构,降低了氧与Pd结合力,促进吸附氧的解离和还原,提高了Pd0.8Fe0.2/C催化剂对氧还原的催化活性。

