妇科肿瘤铂类药物临床应用指南
中华医学会妇科肿瘤学分会
手术治疗、放射治疗(放疗)和化学治疗(化疗)是妇科恶性肿瘤的三大经典治疗方法,其中化疗属于全身治疗,在综合治疗中占据不可或缺的地位。铂类药物是作用机制独特的广谱抗癌化疗药物,以铂类药物为基础的联合化疗是妇科恶性肿瘤化疗的基本方案。虽然铂类药物在临床上应用广泛,但长期以来,缺乏妇科肿瘤铂类药物临床应用的指南和共识。为此,中华医学会妇科肿瘤学分会专家组在循证医学基础上制订了《妇科肿瘤铂类药物临床应用指南》。
本指南采用以下推荐级别(表1),无特殊说明者推荐级别均为2A类。

表1 推荐级别及其代表意义
1 概述
1.1 铂类药物研发历程和分类
铂类药物的研发始于20世纪60年代。临床上常用的铂类药物包括顺铂(cisplatin)、卡铂(carboplatin)、奈达铂(nedaplatin)、奥沙利铂(oxaliplatin)和洛铂(lobaplatin)。1978年,第一代铂类药物顺铂在美国上市。顺铂抗肿瘤活性强,被广泛用于多种实体瘤的常规治疗。然而,其原发或继发性耐药,以及严重的不良反应等是临床应用需克服的问题[1]。第二代铂类药物研发的主要目标是减少或消除顺铂的严重肾毒性。1986年和1995年,卡铂和奈达铂分别在美国和日本获批上市。经结构修饰后,卡铂在保持抗肿瘤效果基本不变的情况下,毒性大大降低,特别是肾毒性得到较大改善,极大地拓展了适用人群,但卡铂与顺铂存在交叉耐药。第三代铂类药物的研发主要针对其交叉耐药,奥沙利铂和洛铂分别于1996年和2005年在法国和中国上市,与顺铂无交叉耐药。
四价铂、反式铂和铂输送载体研究是铂类药物创新性研发的重要发展方向。
1.2 铂类药物的药理特点、作用机制和适应证
铂类药物为细胞周期非特异性化疗药物。铂类化合物的主要作用机制是跨膜转运进入细胞,在胞内生成水合络离子,形成铂-DNA复合物,引起DNA合成受阻,从而导致细胞死亡。目前应用的第三代铂类药物在药理特点和不良反应方面均有所不同(表2)。

表2 三代铂类药物的药理特点和不良反应比较
1.2.1 第一代铂类药物
顺铂给药后 90% 通过肾脏排泄,不足 10%通过胆道排泄。顺铂的肾毒性、耳毒性、消化道毒性、神经毒性均较强。肾毒性是主要的剂量限制性毒性反应,主要表现为肾小管损伤,可导致血尿素氮和血清肌酐水平升高。肾功能损害通常在用药后 10~20 d达最高峰,多次高剂量和短期内重复使用可导致不可逆性肾损伤,给药前后给予水化增加尿量可减轻肾毒性。顺铂的临床应用广泛,通常与紫杉醇联合应用,也可作为放疗增敏剂,是子宫颈癌的首选铂类药物。
1.2.2 第二代铂类药物
卡铂是顺铂的衍生物,其化学稳定性好,溶解度高。卡铂与DNA作用后,形成交联和解除交联的速度均较顺铂慢。卡铂的血浆清除过程呈双相,清除速度较顺铂慢,其通过尿液排泄较顺铂多。与顺铂不同,卡铂较少与血浆蛋白结合,主要通过肾小球滤过,当肌酐清除率<60 mL/min时应注意调整剂量。卡铂的主要毒性反应为骨髓抑制,尤其以血小板减少最为明显,具有剂量限制性。卡铂的其他非血液学毒性(胃肠道毒性、肾毒性、神经毒性和耳毒性)均低于顺铂。目前卡铂被用于多种联合化疗方案,与紫杉醇联合化疗是卵巢癌的首选方案。
奈达铂水溶性好,肾毒性较顺铂和卡铂降低。奈达铂的剂量限制性毒性为骨髓抑制,以血小板减少较常见。脱发也是其常见的不良反应。
1.2.3 第三代铂类药物
第三代铂类药物与顺铂无交叉耐药。奥沙利铂是第一种对结肠癌有显著疗效的铂类药物。临床上常与5-氟尿嘧啶或卡培他滨联合用于转移性结直肠癌。奥沙利铂是黏液性卵巢癌的首选铂类药物,也是复发性卵巢癌可选择的药物。奥沙利铂可导致较严重的周围神经病变,与顺铂和卡铂相比,其对胃肠道、肝肾功能和骨髓的影响明显减轻。
洛铂水溶性较好,肾毒性、耳毒性、神经毒性均较轻,最常见的剂量限制性毒性是骨髓毒性,特别是血小板减少较为明显。临床应用时通常无需水化。
2 临床应用
妇科恶性肿瘤主要包括子宫颈癌、卵巢恶性肿瘤、子宫体恶性肿瘤、外阴癌和阴道癌,以及滋养细胞肿瘤,化疗是其主要治疗手段之一,以铂类药物为基础的化疗是妇科恶性肿瘤最常用的化疗方案。以下将以前瞻性临床研究结果为主要依据,总结以铂类药物为基础的化疗在妇科恶性肿瘤不同瘤种、不同治疗阶段、不同病理类型中的治疗原则、用药方案等。
2.1 子宫颈癌
子宫颈癌早期以手术治疗为主,中晚期以放疗为主。化疗可用于同步放化疗、新辅助化疗、辅助化疗、晚期和复发病例的挽救性化疗及特殊病理类型的化疗。
2.1.1 根治性同步放化疗
根治性同步放化疗用于ⅠB3~ⅣA期[2018版国际妇产科联盟(International Federation of Gynecology and Obstetrics,FIGO)分期]子宫颈癌。多项随机临床研究表明,在ⅠB3~ⅣA期子宫颈癌中,相较于单纯放疗,含顺铂的同步放化疗治疗方案可降低死亡风险30%~50%[2-7]。GOG120研究结果显示,与顺铂+氟尿嘧啶相比,顺铂单药作为同步化疗方案的毒性较低,且疗效相当[6];也有研究证实卡铂作为同步化疗方案,与顺铂疗效无显著差异且患者耐受性较好[8]。
基于以上证据,根治性同步放化疗的化疗方案首选顺铂单药(1类),每周给药,对顺铂不耐受者可使用卡铂(表3)。

表3 子宫颈癌根治性同步放化疗的化疗方案
2.1.2 新辅助化疗
子宫颈癌新辅助化疗一直存有争议。多中心随机对照临床研究结果显示,在局部晚期(2018版FIGO分期ⅠB3~ⅡB期)子宫颈鳞癌中同步放化疗(顺铂为基础)的5年无病生存率优于新辅助化疗后再行根治性手术[9-10]。子宫颈癌对化疗有较高的反应率(70%~85%),在手术前行新辅助化疗可缩小肿瘤,并减少微转移,以利于后续手术的进行,降低手术风险。与直接手术相比,新辅助化疗后再手术能否改善患者预后目前尚难定论。此外,多项回顾性研究报道新辅助化疗可用于早期子宫颈癌保留生育功能手术之前,以缩小病灶和手术范围,改善妊娠结局。新辅助化疗方案多选用顺铂+紫杉醇,一般 2~3 个疗程。
基于以上证据,仅推荐在临床试验中对局部晚期子宫颈癌应用铂类药物为基础的新辅助化疗,或在缺乏放疗条件的地区应用。
2.1.3 术后辅助治疗
2.1.3.1 辅助同步放化疗
早期子宫颈癌术后辅助同步放化疗的指征包括:①术后病理有以下高危因素之一,淋巴结转移、切缘阳性、宫旁受累(1类);②存在中危因素(宫颈肿瘤大、深层间质浸润、脉管癌栓)的患者,并符合 Sedlis 标准,可选择辅助放疗或辅助同步放化疗(加同步化疗为2B类推荐)。同步化疗的用药方案首选顺铂单药,顺铂不能耐受时可使用卡铂。
2.1.3.2 辅助序贯放化疗
有研究对比了术后TC方案(紫杉醇+卡铂)化疗4个周期后再行放疗(序贯放化疗)与顺铂单药同步放化疗的疗效,结果显示两组患者的生存获益比较差异无统计学意义[11]。国内一项前瞻性随机对照研究发现,序贯放化疗组[TP方案(紫杉醇+顺铂),于放疗前、后分别行2个周期化疗]患者的无复发生存时间优于同步放化疗组和单纯放疗组,且患者耐受性较好[12]。
基于以上证据,对于术后存在病理危险因素的患者采用序贯放化疗时,推荐化疗方案为TP方案,于放疗前、后分别行2个周期化疗。
2.1.3.3 辅助化疗
关于术后单纯辅助化疗的相关临床研究较少。单纯化疗的优势包括减少放疗相关不良反应和并发症,利于保留年轻患者的卵巢功能,提高其生活质量。有文献报道,早期子宫颈癌术后有危险因素的患者,单纯化疗的疗效与放疗或放化疗相当[13-15]。国内一项多中心前瞻性随机对照临床研究(CSEM-002)比较了早期(ⅠB~ⅡA期)子宫颈癌术后辅助放疗与辅助化疗的疗效,结果显示二者的生存结局比较差异无统计学意义[16]。早期子宫颈癌术后单纯辅助化疗尚需更多高级别的临床研究证据。
辅助化疗方案采用TP方案,根据高危因素的多少选择疗程数量(表4)。

表4 早期子宫颈癌术后辅助化疗方案
2.1.4 ⅣB期和复发性子宫颈癌的化疗
以铂类药物为基础的化疗是ⅣB期和复发性子宫颈癌的主要治疗方法。
GOG169研究[17]、GOG179研究[18]分别显示与顺铂单药相比,TP方案、顺铂+托泊替康联合用药的疗效有所改善。GOG204研究比较了含顺铂的多种联合方案(TP方案、顺铂+托泊替康、顺铂+吉西他滨、顺铂+长春瑞滨),各组患者的总生存期(overall survival,OS)比较差异无统计学意义,但客观缓解率(objective response rate,ORR)、无进展生存期(progression-free survival,PFS)、OS在顺铂+紫杉醇组有较好趋势[19]。JCOG0505研究显示TC方案的中位OS不劣于TP方案,接受TC方案的患者耐受性较好[20]。但在既往未接受顺铂治疗的患者中,接受TP方案化疗的患者OS较TC方案化疗者显著延长。GOG240研究显示,与单纯化疗相比,联合贝伐珠单抗显著改善患者OS[21]。另外,一些小型的单臂Ⅱ期临床研究结果显示,奈达铂+紫杉醇、奈达铂+白蛋白结合型紫杉醇、奥沙利铂+紫杉醇在晚期/复发性子宫颈癌中均有一定疗效[22-24]。
基于以上证据,复发或转移性子宫颈癌最常应用的全身治疗方案为顺铂+紫杉醇±贝伐珠单抗(1类)和卡铂+紫杉醇±贝伐珠单抗(既往用过顺铂者为1类,其余为2A类)。对于无法耐受紫杉醇的患者,顺铂+托泊替康可作为选择。其他以铂类药物为基础的联合化疗方案中,可应用奈达铂+紫杉醇(3类)、奈达铂+白蛋白结合型紫杉醇(3类)、奥沙利铂+紫杉醇(3类)(表5)。

表5 ⅣB期和复发性子宫颈癌的挽救/姑息化疗方案
2.1.5 子宫颈神经内分泌癌的化疗
子宫颈神经内分泌肿瘤(主要为小细胞)仅占所有子宫颈恶性肿瘤的2%左右,易发生淋巴结转移和远处转移,预后差。子宫颈小细胞神经内分泌癌是小细胞肺癌的一种肺外变异型,缺乏前瞻性随机对照研究证据,多借鉴小细胞肺癌的治疗方法。目前认为,全身化疗是子宫颈小细胞神经内分泌癌所有分期疾病的重要治疗手段[25]。研究提示早期患者术后行辅助化疗、晚期患者行同步放化疗可改善预后[26-27]。
病变局限于子宫颈者,推荐直接手术或新辅助化疗后行根治性手术,术后应行辅助化疗。对于晚期或无法耐受手术者,推荐行根治性放化疗。化疗方案和剂量多参考小细胞肺癌,已有回顾性研究证实EP方案(顺铂+依托泊苷)是子宫颈小细胞神经内分泌癌最常应用的化疗方案,可改善患者预后[28-30]。也有研究显示,顺铂+伊立替康的化疗方案可使患者的长期生存获益[31]。
基于以上证据,推荐EP方案是子宫颈神经内分泌癌的首选化疗方案,对顺铂不耐受者可考虑使用卡铂。其他化疗方案包括顺铂+伊立替康(2B类)(表6)。
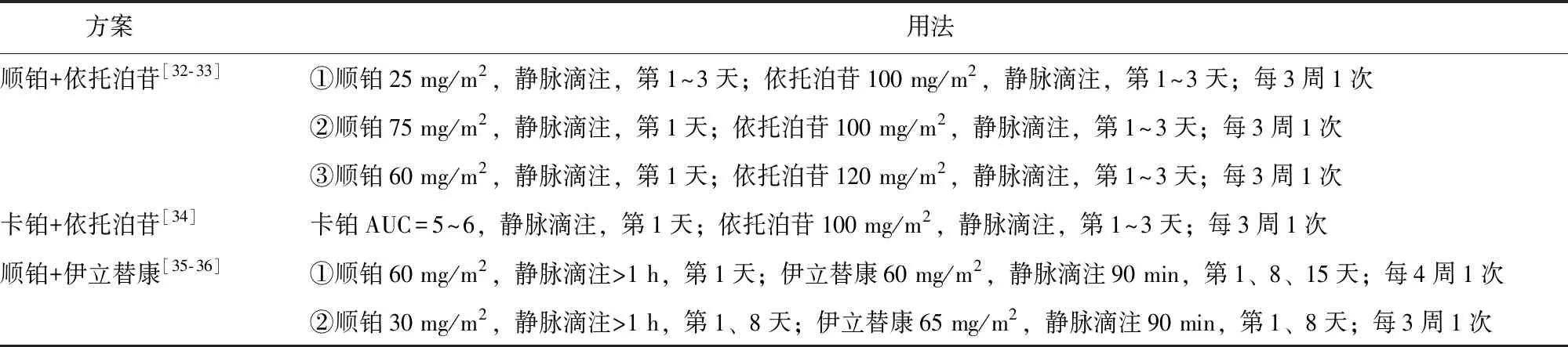
表6 子宫颈神经内分泌癌的化疗方案
2.2 卵巢恶性肿瘤
卵巢恶性肿瘤主要包括上皮性卵巢癌、恶性生殖细胞肿瘤、恶性卵巢性索间质肿瘤和转移性恶性肿瘤四类。总体而言,卵巢恶性肿瘤属于化疗敏感性肿瘤。
2.2.1 上皮性卵巢癌的化疗
2.2.1.1 上皮性卵巢癌的初始化疗
上皮性卵巢癌占卵巢恶性肿瘤的70%左右,患者就诊时70%为晚期,约70%的患者在一线治疗结束后3年内复发。初始标准治疗包括肿瘤细胞减灭术(早期患者全面分期手术)和以铂类药物为基础的联合化疗。20世纪80年代初,顺铂的问世结束了卵巢癌烷化剂化疗时代,PAC方案(顺铂+多柔比星+环磷酰胺)或PC方案(顺铂+环磷酰胺)成为当时的标准化疗方案。此后,GOG111研究[37]和OV10研究[38]显示,与环磷酰胺相比,接受紫杉醇联合铂类药物治疗患者的ORR、PFS及OS均显著改善。从此,开启了铂类药物联合紫杉类药物化疗的新时代。GOG158研究[39]和AGO-OVAR-3研究[40]显示,与TP方案相比,TC方案的安全性和患者生存质量(quality of life,QOL)有所改善,确定了TC方案为首选方案。GOG182/ICON5研究[41]证实,在TC方案中加入第3种化疗药物未能提高患者疗效,且增加毒性,进一步确定了TC方案为上皮性卵巢癌的标准方案。
2.2.1.1.1 早期卵巢癌术后初始化疗
TC方案是首选方案(1类),其他方案包括卡铂+聚乙二醇化脂质体多柔比星(pegylated liposomal doxoru-bicin,PLD)和卡铂+多西他赛。年老(>70岁)、体弱和/或有内科合并症的患者,可考虑使用卡铂单药。根据GOG157研究,一般推荐3个疗程,高级别浆液性癌应给予6个疗程[42]。不推荐早期患者行腹腔化疗。
2.2.1.1.2 晚期卵巢癌术后初始化疗
(1)首选方案:静脉应用TC方案,6个疗程,是晚期上皮性卵巢癌的标准化疗方案。本指南推荐TC方案为首选方案(1类)。
(2)其他方案:SCOTROC1研究证实卡铂+多西他赛与TC方案疗效相当,骨髓毒性虽严重但神经毒性减轻[43]。MITO-2研究证实,卡铂+PLD与TC方案疗效相当,过敏反应、神经毒性和脱发等不良反应发生率降低[44]。本指南推荐此两种方案作为初始化疗的替代方案,特别是合并糖尿病等潜在神经损伤的患者。
(3)含贝伐珠单抗的方案:GOG218研究[45]和ICON7研究[46]证实,晚期卵巢癌在TC方案基础上加用贝伐珠单抗且应用贝伐珠单抗进行序贯维持治疗可延长患者的PFS(平均3~4个月),并能使高复发风险人群(Ⅳ期或Ⅲ期手术未达R0者)的OS明显延长。本指南推荐首选该方案用于晚期上皮性卵巢癌高复发风险人群(1类)。
(4)剂量密集型/周疗方案:JCOG3016研究[47]、GOG262研究[48]、ICON8研究[49]和MITO-7研究[50]比较了标准的3周紫杉醇/卡铂方案与紫杉醇周疗(80 mg/m2或60 mg/m2)+卡铂3周或周疗方案。JCOG3016研究显示周疗方案延长患者的PFS、OS;GOG262研究显示周疗方案可延长未同时应用贝伐珠单抗患者的PFS。ICON8研究和MITO-7研究显示两种方案对患者的PFS、OS改善无显著差异,疗效亦无显著差异。MITO-7研究选用60 mg/m2紫杉醇,该方案肺毒性的发生率较高,但中性粒细胞减少、粒细胞减少伴发热、血小板减少、神经毒性、脱发和呕吐的发生率较低,QOL显著改善。ICON8研究中选用80 mg/m2紫杉醇,该方案中性粒细胞减少、卡铂过敏的发生率较高,QOL降低。
基于以上证据,推荐紫杉醇周疗+卡铂3周方案、紫杉醇周疗+卡铂周疗方案为晚期卵巢癌初始化疗的可选方案,周疗方案中紫杉醇推荐用量为60~80 mg/m2。
(5)腹腔注射联合静脉注射化疗方案:GOG104研究[51]、GOG114研究[52]、GOG172研究[53]证实,腹腔注射联合静脉注射化疗方案可使手术达到满意肿瘤细胞减灭患者的PFS和/或OS延长,但不良反应增加。然而,GOG252研究显示,在紫杉醇+卡铂+贝伐珠单抗联合治疗方案中,与静脉注射相比,无论卡铂还是顺铂经腹腔注射均不能改善患者的PFS或OS,提示含贝伐珠单抗的联合方案中,铂类药物经腹腔注射给药未进一步改善患者预后[54]。
基于以上证据,推荐腹腔注射联合静脉注射化疗用于晚期上皮性卵巢癌手术达到满意肿瘤细胞减灭的患者,铂类药物首选顺铂。
(6)腹腔热灌注化疗(hyperthermic intraperitoneal chemotherapy,HIPEC)方案:M06OVH-OVHIPEC研究显示,对Ⅲ期卵巢癌新辅助化疗后联合中间型肿瘤细胞减灭术,并达到满意减灭后,加顺铂药物的HIPEC,可使患者生存获益[55]。
基于以上证据,推荐HIPEC用于中间型肿瘤细胞减灭术后达到满意减灭(R<1)后的Ⅲ期卵巢癌患者。
(7)老年(>70岁)或有合并症患者的化疗方案:ICON3研究[56]、MITO-5研究[57]、MITO-7研究[50]、GOG273研究[58]等显示,与标准剂量紫杉醇(175 mg/m2)+卡铂方案相比,老年患者对紫杉醇(135 mg/m2)+卡铂3周方案、卡铂单药和卡铂周疗3种方案的耐受性较好且疗效相当。但EWOC-1研究中期分析显示,TC方案的疗效优于卡铂单药[59]。
基于以上证据,推荐老年患者应用TC方案联合治疗。对于无法耐受联合治疗毒性的患者,卡铂单药可作为选择。推荐方案见表7和表8。

表7 晚期上皮性卵巢癌含铂化疗方案

表8 老年晚期上皮性卵巢癌初始含铂化疗方案
2.2.1.1.3 晚期卵巢癌术前新辅助化疗
化疗方案同术后方案,适应证仅限于经评估直接手术难以切净或不能耐受手术者,治疗前需获得组织学证据,一般推荐术前3~4个疗程,且推荐静脉给药。
2.2.1.2 复发性上皮性卵巢癌化疗
卵巢癌复发分为铂敏感复发(platinum-sensitive recurrent,PSR,即一线治疗结束后6个月以上复发)和铂耐药复发(platinum-resistance recurrent,PRR,一线治疗结束后6个月以内复发)。对PSR患者应先进行评估,若预期再次肿瘤细胞减灭术可达到无肉眼残留(R0),应先行手术,术后辅以铂类药物为基础的联合化疗[60-61];若无法达到R0,应优先选择以铂类药物为基础的联合化疗。对PRR患者,原则上选择非铂类药物治疗。若无禁忌证,两种复发均可选择化疗时加用贝伐珠单抗。
2.2.1.2.1 铂敏感复发卵巢癌的化疗
(1)首选方案:ICON4/AGO-OVAR-2.2研究[62]和AGO-OVAR-2.5研究[63]显示,与铂类单药相比,以铂类药物为基础的联合化疗(TC方案、吉西他滨+卡铂)疗效更佳。CALYPSO研究显示,PLD+卡铂方案和TC方案的疗效相当,且患者耐受性好[64]。
OCEANS研究[65]和GOG-0213研究[66]显示,与单纯化疗相比,在以铂类药物为基础的联合化疗(TC方案、吉西他滨+卡铂)基础上联用贝伐珠单抗可改善患者的PFS。AGO-OVAR 2.21/ENGOT-ov 18研究显示,与吉西他滨+卡铂+贝伐珠单抗组相比,PLD+卡铂+贝伐珠单抗组患者的OS、PFS均显著改善[67]。
两项Ⅱ期临床研究报道显示,卡铂+多西他赛的3周方案和其剂量密集型周疗方案的ORR达67%~72%,且安全性良好[68-69]。
基于以上证据,推荐PSR卵巢癌采用含铂联合化疗±贝伐珠单抗治疗,紫杉醇+卡铂±贝伐珠单抗(1类)、吉西他滨+卡铂±贝伐珠单抗(1类)、PLD+卡铂±贝伐珠单抗方案(1类)。卡铂+多西他赛为PSR患者的可选方案。
(2)其他含铂方案:顺铂与吉西他滨有协同作用[70],本指南推荐该方案作为PSR患者的可选方案。卡铂单药的PFS为5.8个月[63];顺铂单药同样有效[62]。奥沙利铂单药治疗患者的ORR为38%~46%,PFS为7.3个月,OS为20.2个月[71-73]。故本指南推荐老年或全身状况差无法耐受联合化疗的PSR患者可使用铂类单药治疗。
(3)其他铂类药物的研究:国内一项回顾性研究显示,奈达铂+紫杉醇方案与TC方案相比疗效相当,患者耐受性较好;治疗结束后6~12个月复发的PSR患者,接受奈达铂+紫杉醇方案治疗的患者PFS较长[74]。一项Ⅱ期临床研究提示,洛铂用于治疗复发性卵巢癌的疗效较好,其中PSR患者的ORR达50%[75]。
PSR卵巢癌含铂化疗推荐方案见表9。

表9 铂敏感复发卵巢癌含铂化疗方案
2.2.1.2.2 铂耐药复发卵巢癌的化疗
奥沙利铂单药是唯一可推荐用于PRR患者的铂类药物[71-73]。此外,国内小样本研究报道,多西他赛+洛铂化疗患者的中位PFS为5个月,与PSR患者相当[76]。但仍需进一步研究验证。推荐方案见表10。

表10 铂耐药复发卵巢癌含铂化疗方案
2.2.1.3 少见上皮性卵巢癌的化疗
少见上皮性卵巢癌包括癌肉瘤、透明细胞癌、低级别浆液性癌、子宫内膜样癌、黏液性癌。可根据化疗指征,采用以铂类药物为基础的联合方案。对于部分少见肿瘤类型,推荐其他治疗方案。推荐术后治疗原则和方案见表11~13。

表11 Ⅰ期上皮性卵巢癌术后管理推荐
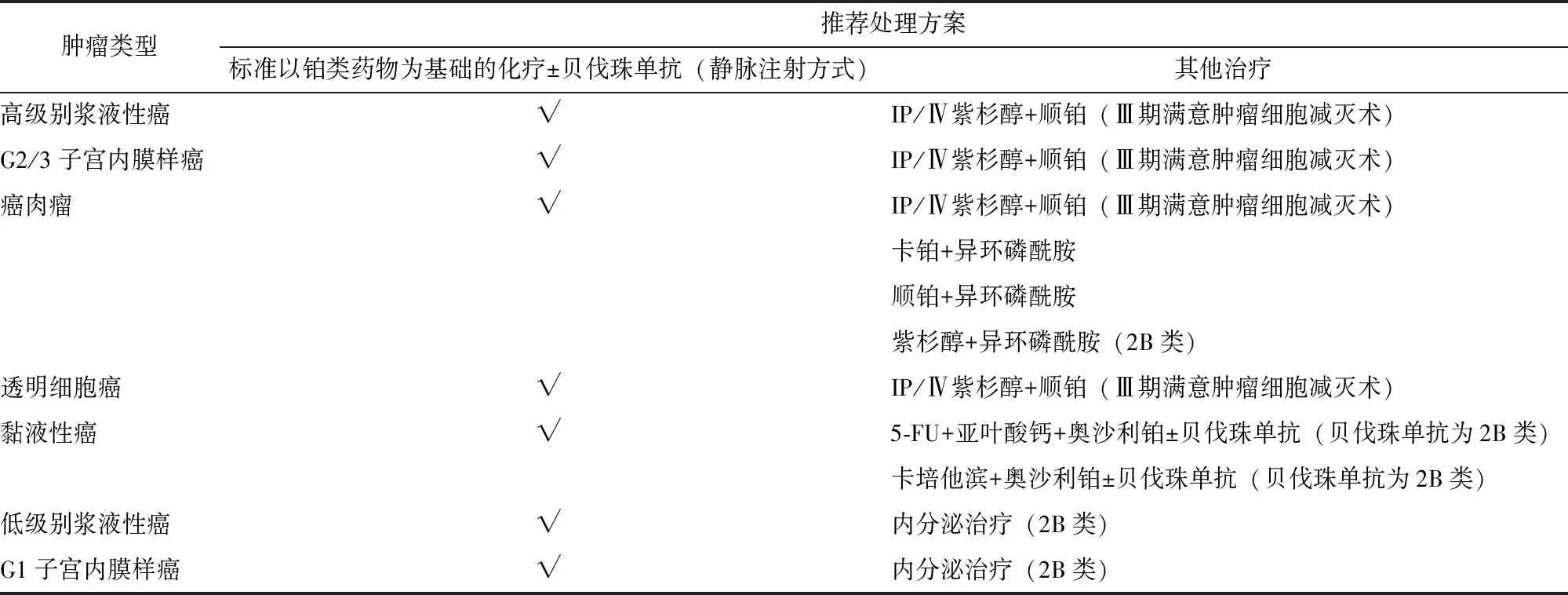
表12 Ⅱ~Ⅳ期上皮性卵巢癌术后管理推荐
2.2.1.3.1 卵巢癌肉瘤的化疗
癌肉瘤表现为多形性上皮细胞与间叶分化区域混杂,实际上是由上皮来源单细胞克隆发展而来,属于上皮性癌,恶性程度高,预后较差。GOG261研究显示,在子宫/卵巢癌肉瘤患者中,TC方案疗效不劣于紫杉醇+异环磷酰胺;卵巢癌肉瘤队列的治疗效果趋势与子宫癌肉瘤主队列相似,TC方案患者的PFS(15个月比10个月)和OS(30个月比25个月)均延长[83]。回顾性研究显示顺铂+异环磷酰胺、卡铂+异环磷酰胺对卵巢癌肉瘤也有一定疗效[78,84]。
2.2.1.3.2 卵巢透明细胞癌的化疗
JGOG3017/GCIG研究显示,顺铂+伊立替康与TC方案疗效相比差异无统计学意义,但不良反应有所不同[79]。
2.2.1.3.3 卵巢黏液性癌的化疗
卵巢黏液性癌与胃肠道肿瘤有相似之处。GOG0241研究旨在比较TC方案±贝伐珠单抗和卡培他滨+奥沙利铂±贝伐珠单抗的疗效,该研究因入组缓慢提前终止,对已入组患者进行PFS和不良反应分析,结果显示两种治疗方案比较差异无统计学意义[82]。另有4项针对铂耐药及复发的上皮性卵巢癌的研究[80,85-87],证明FOLFOX方案对卵巢黏液性癌有一定疗效。具体方案用法见表13。

表13 上皮性卵巢癌化疗方案
2.2.1.3.4 复发性卵巢少见上皮性肿瘤的化疗
复发后的化疗方案基本同卵巢高级别浆液性癌,黏液性癌亦可应用5-氟尿嘧啶+亚叶酸钙+奥沙利铂±贝伐珠单抗(贝伐珠单抗为2B类)、卡培他滨+奥沙利铂±贝伐珠单抗(贝伐珠单抗为2B类);透明细胞癌亦可应用顺铂+伊立替康。
2.2.2 卵巢生殖细胞肿瘤的化疗
卵巢恶性生殖细胞肿瘤包括无性细胞瘤、未成熟畸胎瘤、胚胎瘤和卵黄囊瘤(内胚窦瘤),除Ⅰ期无性细胞瘤和Ⅰ期G1未成熟畸胎瘤外,术后均需要接受辅助化疗。
2.2.2.1 初始化疗
卵巢恶性生殖细胞肿瘤的化疗方案从VAC方案(长春新碱+放线菌素D+环磷酰胺)到PVB方案(顺铂+长春新碱+博来霉素或平阳霉素)和BEP方案(顺铂+博来霉素+依托泊苷)的演变,其生存率也得到了较大提高[88-90]。与PVB方案相比,BEP方案疗效相似但毒性较低;4个周期的BEP方案治疗是卵巢恶性生殖细胞肿瘤的标准治疗方案。虽然数据有限,但3个周期的BEP方案治疗也可有效减少低危患者的复发[91]。
基于以上证据,卵巢恶性生殖细胞肿瘤化疗首选BEP方案,高危患者4个疗程,低危患者3个疗程(2B类)。为减少毒性作用(尤其是神经毒性),ⅠB~Ⅲ期无性细胞瘤患者可采用卡铂+依托泊苷方案化疗3个疗程[92]。针对博来霉素的肺毒性,儿童(0~14岁)患者应减少博来霉素的用量[93],具体方案见表14。

表14 卵巢生殖细胞肿瘤初始化疗方案
2.2.2.2 复发后的化疗
Kondagunta等[94]研究显示,PIT方案(顺铂+异环磷酰胺+紫杉醇)对复发或转移的生殖细胞肿瘤疗效较好。推荐首选PIT方案。若初次治疗未使用BEP方案,BEP方案仍为首选。其他可选择方案包括EP方案、多西他赛+卡铂、VIP方案(依托泊苷+异环磷酰胺+顺铂)、TC方案、VeIP方案(长春碱+异环磷酰胺+顺铂)等[88,95-99](表15)。

表15 卵巢生殖细胞肿瘤复发后化疗方案
2.2.3 卵巢性索间质肿瘤的化疗
卵巢性索间质肿瘤包括颗粒细胞瘤、颗粒卵泡膜细胞瘤和支持-间质细胞瘤。由于发病率低,患者数量少,缺乏高质量证据,一般建议以铂类药物为基础的联合化疗方案[100]。
2.2.3.1 初始化疗
推荐首选TC方案。Gurumurthy等[101]分析了5项回顾性研究,共计535例颗粒细胞瘤患者,多种含铂治疗方案中,TC方案患者不良反应和复发率更低。其他可选择的方案有EP方案、BEP方案(2B类)[102-105]。
2.2.3.2 复发后的化疗
同初始治疗方案,推荐选择与初始治疗不同的含铂类药物方案。
2.2.4 卵巢转移性肿瘤的化疗
参考原发部位肿瘤的化疗方案。
2.3 子宫内膜癌
早期子宫内膜样腺癌患者预后好,5年总生存率在80%以上,特殊类型、晚期和复发子宫内膜癌患者5年总生存率仅为55%和17%。初始治疗一般为手术治疗,术后根据手术病理分期、组织学类型、分化程度、有无脉管内癌栓、年龄等因素进行复发风险分层。早期具有中危和中高危因素的子宫内膜样腺癌患者需术后辅助放疗,而有高危因素(ⅠB期G3和Ⅱ期)的患者则需在术后辅助放疗的基础上±化疗,晚期、转移和特殊类型的子宫内膜癌患者需化疗±放疗。铂类药物是主要的化疗药物。
2.3.1 辅助化疗
2.3.1.1 早期子宫内膜癌
病灶局限于子宫但伴深肌层浸润患者预后较差。尽管辅助治疗采取盆腔外照射,仍有相当一部分患者发生远处转移。有研究显示序贯化疗/放疗可改善患者的PFS,但OS则无显著获益[106]。推荐ⅠB期G3和Ⅱ期子宫内膜癌患者在放疗基础上加用化疗(2B类),化疗方案选择TC方案。
2.3.1.2 晚期子宫内膜癌
病灶累及子宫外的患者复发风险升高,全身治疗是辅助治疗的基础。GOG122研究显示,与放疗组相比,化疗组患者预后显著改善,明确了辅助化疗的重要性,但两组患者的复发率均较高[107]。PORTEC-3研究显示,与放疗组相比,放化疗组(同步放化疗序贯化疗)患者的预后显著改善[108]。GOG258研究显示,与化疗组相比,放化疗组(同步放化疗序贯化疗)患者的PFS无显著改善[109]。推荐晚期子宫内膜癌患者应用化疗±放疗,化疗方案选择TC方案。
2.3.2 复发或转移性子宫内膜癌的化疗
铂类药物联合化疗方案在子宫内膜癌治疗中经历了AP方案(多柔比星+顺铂)、TAP方案(紫杉醇+多柔比星+顺铂)、TC方案的演变。
GOG107研究显示,与多柔比星单药比较,复发转移性子宫内膜癌患者接受AP方案可明显提高反应率和延长中位PFS,该研究奠定了铂类药物在复发转移性子宫内膜癌化疗中的地位[110]。GOG177研究显示,接受TAP方案治疗患者的反应率、中位PFS和OS均优于AP方案[111]。GOG209研究对TAP方案与TC方案进行了非劣效对比,结果显示TC方案的中位PFS与OS均不劣于TAP方案,且不良反应较少[112]。一项 Ⅱ 期临床研究分析了在TC方案基础上加用贝伐珠单抗的疗效,结果显示患者中位PFS为20个月,中位OS为56个月,反应率为82.8%,即使既往接受过TC方案化疗的二线患者,反应率也可达87.5%[113]。
基于以上证据,对于复发或转移性子宫内膜癌患者,若可耐受,推荐联合方案化疗。单药治疗亦可应用。联合方案优先选择TC方案,替代方案包括:AP方案、TAP方案、卡铂+多西他赛、卡铂+紫杉醇+贝伐珠单抗。若联合方案无法耐受,单药治疗可选择顺铂、卡铂。
第二代和第三代铂类药物如奥沙利铂、奈达铂和洛铂等应用于子宫内膜癌的研究较少。一项小样本单臂研究显示,奈达铂+伊立替康在复发难治性子宫内膜癌患者中的ORR为14.3%,安全性可接受[114]。奥沙利铂单药在含铂化疗后复发患者二线治疗的ORR为13.5%[115]。尚待进一步研究证实其有效性。
2.3.3 少见子宫内膜癌的化疗
2.3.3.1 子宫浆液性癌
一项Ⅱ期随机研究显示,在TC方案基础上联合应用曲妥珠单抗可延长人表皮生长因子受体-2(human epidermal growth factor receptor 2,HER2)阳性的晚期或复发性子宫浆液性癌患者的PFS、OS[116]。基于以上证据,对HER-2阳性的Ⅲ/Ⅳ期或复发性子宫浆液性癌,推荐曲妥珠单抗联合TC方案治疗。
2.3.3.2 子宫癌肉瘤
GOG108研究显示,与异环磷酰胺单药相比,顺铂+异环磷酰胺可显著改善子宫癌肉瘤患者的反应率和PFS,但OS比较差异无统计学意义[117]。GOG161研究显示,与异环磷酰胺单药相比,紫杉醇+异环磷酰胺的反应率、PFS和OS均显著改善[118]。GOG261研究显示,在子宫癌肉瘤患者中,TC方案的疗效不劣于紫杉醇+异环磷酰胺,接受TC方案的患者PFS(16个月比12个月,HR=0.73,P=0.01)和OS均显著延长(37个月比29个月,HR=0.87,P<0.01)[83]。基于以上证据,推荐子宫癌肉瘤患者采用TC方案化疗(1类),也可应用顺铂+异环磷酰胺。
子宫内膜癌含铂化疗方案见表16。

表16 子宫内膜癌含铂化疗方案
2.4 外阴癌/阴道癌
外阴癌和阴道癌是两种罕见的妇科恶性肿瘤,相关临床研究有限,多借鉴子宫颈癌、肛门癌或头颈癌的治疗经验。目前对其治疗多采用个体化和综合治疗手段。
2.4.1 局部晚期外阴癌
GOG101研究和GOG205研究显示术前行同步放化疗可提高手术切除率并减少盆腔廓清术可能[121-122]。推荐局部晚期外阴癌患者行同步放化疗,化疗方案为优先选用顺铂,也可应用顺铂+5-氟尿嘧啶。
2.4.2 晚期/复发性外阴癌
尚缺乏高级别证据支持标准化疗方案。推荐优先应用TP方案、TC方案、顺铂+紫杉醇+贝伐珠单抗,也可应用顺铂+长春新碱、顺铂+吉西他滨、卡铂+紫杉醇+贝伐珠单抗(2B类)。可应用单药包括顺铂、卡铂(2B类)。
2.4.3 阴道癌
阴道癌的相关研究更加有限。治疗推荐参照外阴癌和子宫颈癌。
2.5 妊娠滋养细胞肿瘤
妊娠滋养细胞肿瘤(gestational trophoblastic neoplasm,GTN)患者的治疗原则以化疗为主,辅以手术和放疗等综合治疗。化疗方案根据FIGO分期与预后评分实施分层和个体化选择[123]。含铂类药物的联合化疗方案在以下情况下推荐应用。
2.5.1 初始化疗方案中铂类药物的选择
在初治患者中,含铂化疗方案仅为超高危患者的一线治疗选择。超高危患者是指FIGO评分≥13分以及伴肝脑转移的患者。对17项回顾性数据进行总集分析的结果显示[124],对超高危患者初治应用EMA/EP方案、EMA/CO方案和FAVE方案的缓解率分别为60.0%、55.2%、63.1%,比较差异无统计学意义。对于超高危GTN患者,本指南推荐除EMA/CO方案外,可选择EMA/EP、EP/EMA、TP/TE、VIP、ICE、BEP等含铂方案。
对于超高危患者,若直接应用EMA/CO方案,可引起肿瘤坏死导致的出血、代谢性酸中毒、败血症和/或多器官衰竭,早期死亡风险升高(4周内)。给予超高危GTN患者EMA/CO方案前,应用EP方案诱导化疗可改善患者结局[125]。因此,推荐在EMA/CO方案前应用低剂量EP方案1~3个周期(2B类)。
胎盘部位滋养细胞肿瘤(placental site tropho-blastic tumor,PSTT)和上皮样滋养细胞肿瘤(epithelioid trophoblastic tumor,ETT)以手术为主要治疗方法。对于有子宫外转移或病理高危因素者,建议行辅助化疗。可选择的含铂化疗方案包括EP/EMA方案和TP/TE方案(2B类)。
2.5.2 耐药及复发GTN患者含铂化疗方案的选择
耐药及复发GTN患者化疗方案的选择应综合考虑患者既往的治疗方案和疾病程度。EMA/CO方案耐药患者应用EMA/EP方案时,完全缓解率为66.6%~84.9%[125-128]。在应用EMA/EP方案的患者中,40%的患者会经受3级及以上不良反应。对EMA/CO方案耐药的患者,采用TP/TE方案治疗后的完全缓解率可达70%~75%[129],且不良反应小于EMA/EP方案。对氟尿苷为主的联合方案和EMA/CO方案均发生耐药者,推荐的三线化疗方案均是以铂类药物为主的联合化疗,包括EMA/EP方案、TP/TE方案、VIP方案、BEP方案等(2B类)。
因GTN属罕见肿瘤,标准的含铂化疗方案缺少高级别循证医学证据。对于多种化疗耐药或复发的患者,也可考虑大剂量含铂化疗(如大剂量ICE方案)联合骨髓干细胞移植。GTN常用含铂化疗方案见表17。

表17 妊娠滋养细胞肿瘤含铂化疗方案
3 不良反应及其管理
铂类药物是非周期特异性细胞毒药物,可引起全身各系统不良反应,主要是血液学毒性、胃肠道毒性、肾毒性、神经毒性,其他还包括血管刺激、电解质紊乱等。此外,一些患者也可出现药物反应,特别是过敏反应,应予积极预防和处理[131]。
3.1 血液学毒性
血液学毒性是铂类药物最常见的不良反应,化疗后可导致不同程度的骨髓抑制,包括粒细胞减少、血小板减少、贫血,呈中-高风险。与顺铂和奥沙利铂相比,卡铂、奈达铂和洛铂对骨髓的抑制作用较强,特别是血小板减少,属剂量限制性毒性,需根据患者骨髓抑制程度、化疗方案、患者年龄、是否具有高危因素及治疗目的等因素进行综合判断,进而分层处理和预防。
3.1.1 粒细胞减少
粒细胞减少是铂类药物最常见的不良反应,其中卡铂引起粒细胞减少的发生率最高(85%,3级及以上15%~26%),其次为奈达铂(69%,3级及以上48%)、洛铂(50%,3级及以上11%),顺铂最低(25%~30%)[132]。单次口腔温度≥38.3 ℃,或≥38.0 ℃持续超过1 h,外周血中性粒细胞绝对值(absolute neutrophil count,ANC)<0.5×109/L,或预计48 h后ANC<0.5×109/L,称为粒细胞减少伴发热,是化疗最严重的不良反应。
预防和处理:3级及以上骨髓抑制,可使用长效或短效粒细胞集落刺激因子(granulocyte colony stimulating factor,G-CSF)或粒细胞-巨噬细胞集落刺激因子预防或治疗化疗引起的粒细胞减少[133]。粒细胞减少伴发热患者的治疗措施包括输血、广谱抗生素和G-CSF等。必要时可考虑下一疗程调整铂类药物的给药剂量或延长化疗间隔[133-135]。有研究显示,应用细胞保护剂如氨磷汀可降低3、4级中性粒细胞减少的发生率[136]。
3.1.2 贫血
20%~90%的铂类药物化疗患者可发生化疗相关性贫血(chemotherapy-related anemia,CRA),发生率分别为:顺铂≤45%、卡铂(71%~90%,3级及以上为21%)、奈达铂为57%、奥沙利铂(64%,3级及以上为1%)、洛铂(20%,3级及以上为5%)[132]。铂类药物可促进红细胞凋亡,同时造成肾小管细胞损伤使内源性促红细胞生成素(erythropoietin,EPO)减少而导致贫血[137]。
预防和处理:临床处理需根据贫血严重程度、治疗目的、伴随症状、患者对既往治疗的反应等因素进行综合评估。根据个体贫血风险评估,考虑EPO和/或补充铁剂和叶酸等治疗。CRA 3级(血红蛋白<60 g/L)有症状如持续心动过速、呼吸急促、胸痛、劳力性呼吸困难、轻度头晕、晕厥、重度乏力妨碍工作和日常活动等,应进行红细胞输注。
3.1.3 血小板减少
铂类药物可引起血小板减少,其发生率分别为:卡铂62%、奈达铂59%、奥沙利铂25%~30%和洛铂70%[132]。
预防和处理:对高出血风险的血小板减少患者,应根据其血小板计数和出血情况,给予治疗性或出血前预防性血小板输注;同时采用重组人促血小板生长因子、重组人白介素-11,对于血小板的恢复有一定帮助;必要时可考虑下一疗程调整铂类药物的给药剂量。二级预防主要适用于上一个化疗周期发生过3级及以上血小板减少的患者,以及上一个化疗周期发生2级血小板减少,同时伴有以下任一项出血高风险因素的患者:如出血史,化疗前血小板计数<75×109/L,既往接受过含铂类、吉西他滨及蒽环类药物等化疗方案,接受过放疗等。3级血小板减少伴有出血倾向时建议输注单采血小板,如果患者为4级血小板减少,无论有无出血倾向,均应输注血小板。
3.2 非血液学毒性
3.2.1 胃肠道毒性
恶心呕吐是铂类药物常见的不良反应。根据化疗药物致吐风险分为4类:高风险(呕吐频率>90%)、中风险(>30%~90%)、低风险(10%~30%)、极低风险(<10%)。顺铂是高致吐风险的细胞毒药物,卡铂根据曲线下面积(area under the curve,AUC)不同其致吐级别不同,AUC≥4为高风险,AUC<4为中风险。奈达铂、奥沙利铂和洛铂属于中致吐风险的细胞毒药物[132,134]。
预防和处理:使用高致吐风险铂类药物的化疗方案,需应用肾上腺皮质激素(地塞米松)、5-羟色胺3(5-hydroxytryptamine 3,5-HT3)受体拮抗剂和神经激肽-1(neurokinin-1,NK-1)受体拮抗剂三联止吐方案预防和处理。
3.2.2 肾毒性
肾脏是铂类药物的主要排泄器官,肾脏毒性常见。铂类药物肾毒性反应主要由铂元素沉积于肾脏导致,可直接或间接引起肾小管细胞的急性坏死。顺铂引起的肾毒性发生率为28%~36%,卡铂为27%、奈达铂为10%~15%,奥沙利铂、洛铂引起的肾毒性少见[132]。顺铂肾毒性为剂量限制性毒性,可发生急、慢性肾功能不全,与顺铂对肾小管损害程度有关。当顺铂用药剂量达90 mg/m2以上,是肾毒性发生的高危因素,常于用药后3~7 d发生,表现为血尿,血尿素氮和血肌酐水平升高,低镁血症,蛋白尿,肌酐清除率降低等。
预防和处理:顺铂剂量>50 mg/m2时,化疗前后需水化,以预防和减少顺铂引起的急性肾衰竭,否则可能引起不可逆的肾损害。在晚期卵巢癌患者中,重复使用顺铂时可使用氨磷汀减轻肾毒性。3级及以上肾毒性需停药。
3.2.3 神经毒性
不同铂类药物引起神经损伤的发生率和类型不同,其中奥沙利铂、顺铂的末梢神经毒性较常见,卡铂、奈达铂、洛铂引起神经损害的报道较少。铂类药物神经毒性多为剂量限制性毒性,当顺铂累积剂量达500~600 mg/m2时出现,表现为神经末梢障碍,以肢体麻木、感觉迟钝、头晕、耳鸣等为主。顺铂引起的耳毒性发生率与药物剂量和年龄相关,剂量越大,听力损害越严重。
奥沙利铂引起的神经毒性多为慢性神经毒性。多表现为一过性的手足感觉异常、麻木或口周感觉迟钝,往往在接触冷感物体时触发或加重,结束治疗后数小时或数日很快恢复。其神经毒性与奥沙利铂的累积给药剂量相关,当累积剂量为780~850 mg/m2时,3级以上神经毒性的发生率为15%;当累积剂量达1170 mg/m2时,慢性神经毒性的发生率增加至50%。神经损害大多可恢复,恢复时间为停药后12~13周或更长[132]。
预防和处理:临床上常用于预防和治疗神经毒性的药物有钙镁合剂、还原型谷胱甘肽、B族维生素、氨磷汀、神经生长因子等,有一定的缓解作用,但缺少高级别循证医学证据。推荐度洛西汀用于治疗奥沙利铂引起的神经性疼痛。
3.3 药物反应
所有药物输注时均可能发生不良反应,为输注反应或过敏反应,可发生于输注过程中或输注完成后(甚至是数天之后)。大多数药物反应为较轻的输注反应,但也可发生更严重的超敏(过敏)反应甚至是致命的过敏性休克,具体症状见表18。

表18 药物反应症状
3.3.1 药物反应症状
卡铂、顺铂、奥沙利铂常引发药物反应。铂类药物(卡铂、顺铂)相关的不良反应实为过敏反应,常发生于再次应用同类药物时,在完成初始治疗时发生率较低。应用铂类药物可出现发生率极低的严重过敏反应——休克,可引起致命的心脏循环衰竭。药物反应可能发生于静脉注射或腹腔注射用药过程中。
3.3.2 药物反应的管理
处理措施取决于反应的严重程度和引发反应的药物,基于既往发生反应的次数和严重程度推荐再次用药和脱敏。铂类药物引发的轻度、严重以及致命药物反应的处理流程见图1。
4 结语
铂类药物是作用机制独特的广谱抗肿瘤药物,以铂类药物为基础的联合化疗是妇科肿瘤最常用的化疗方案。铂类药物广泛用于各种妇科肿瘤,TC方案是上皮性卵巢癌的首选标准方案,顺铂是子宫颈癌的首选铂类药物。铂类药物多以静脉给药,亦可腹腔内用药。铂类药物的不良反应以血液学毒性、胃肠道毒性、肾毒性和神经毒性为主,部分患者可出现药物反应,特别是过敏反应,应予以高度重视,积极预防和处理。铂类药物可有原发耐药,更多属于继发耐药,顺铂与卡铂交叉耐药,第三代铂类药物交叉耐药显著减少。铂类药物耐药后一般选择非铂化疗,但可选用奥沙利铂用于铂耐药患者。耐药是铂类药物临床应用中面临的最大挑战。
利益冲突:共识制订工作组所有参与人员均声明不存在利益冲突
执笔专家组:
孔北华,刘继红,向阳,张国楠,陈刚,尹如铁,李秀琴,姜洁,沈源明,刘红,蒋芳,邓婷,李小平,鹿欣,谢幸,马丁
编审专家组(以姓氏笔画为序):
万小平(上海市第一妇婴保健院),马丁(华中科技大学同济医学院附属同济医院),王丹波(辽宁省肿瘤医院),王世宣(华中科技大学同济医学院附属同济医院),王建六(北京大学人民医院),王新宇(浙江大学医学院附属妇产科医院),尹如铁(四川大学华西第二医院),孔北华(山东大学齐鲁医院),邓婷(中山大学肿瘤防治中心),曲芃芃(天津市中心妇产科医院),吕卫国(浙江大学医学院附属妇产科医院),向阳(中国医学科学院北京协和医院),刘红(四川省肿瘤医院/四川省第二人民医院),刘继红(中山大学肿瘤防治中心),李小平(北京大学人民医院),李秀琴(中国医科大学附属盛京医院),杨兴升(山东大学齐鲁医院),杨佳欣(中国医学科学院北京协和医院),吴小华(复旦大学附属肿瘤医院),吴令英(中国医学科学院肿瘤医院),汪辉(浙江大学医学院附属妇产科医院),沈铿(中国医学科学院北京协和医院),沈源明(浙江大学医学院附属妇产科医院),宋坤(山东大学齐鲁医院),张国楠(四川省肿瘤医院/四川省第二人民医院),陈刚(华中科技大学同济医学院附属同济医院),赵霞(四川大学华西第二医院),哈春芳(宁夏医科大学/宁夏医科大学总医院),姜洁(山东大学齐鲁医院),徐丛剑(复旦大学附属妇产科医院),高雨农(北京大学肿瘤医院),郭瑞霞(郑州大学第一附属医院),崔恒(北京大学人民医院),康山(河北医科大学第四医院),鹿欣(复旦大学附属妇产科医院),梁志清(陆军军医大学第一附属医院),蒋芳(中国医学科学院北京协和医院),程文俊(南京医科大学第一附属医院/江苏省人民医院),谢幸(浙江大学医学院附属妇产科医院)

