乳蛋白重组表达与人造奶生物合成:全球专利分析与技术发展趋势
周正富,庞雨,张维,王劲,燕永亮,郑迎迎,陈敏,廖志华,林敏,
(1 中国农业科学院生物技术研究所,农业部农业基因组学重点实验室,北京 100081; 2 中国科学院天津工业生物技术研究所,工业酶国家工程实验室,天津 300308; 3 国家合成生物技术创新中心,天津 300308; 4 西南大学,西南大学-西藏农牧学院药用植物联合研发中心,重庆 400715)
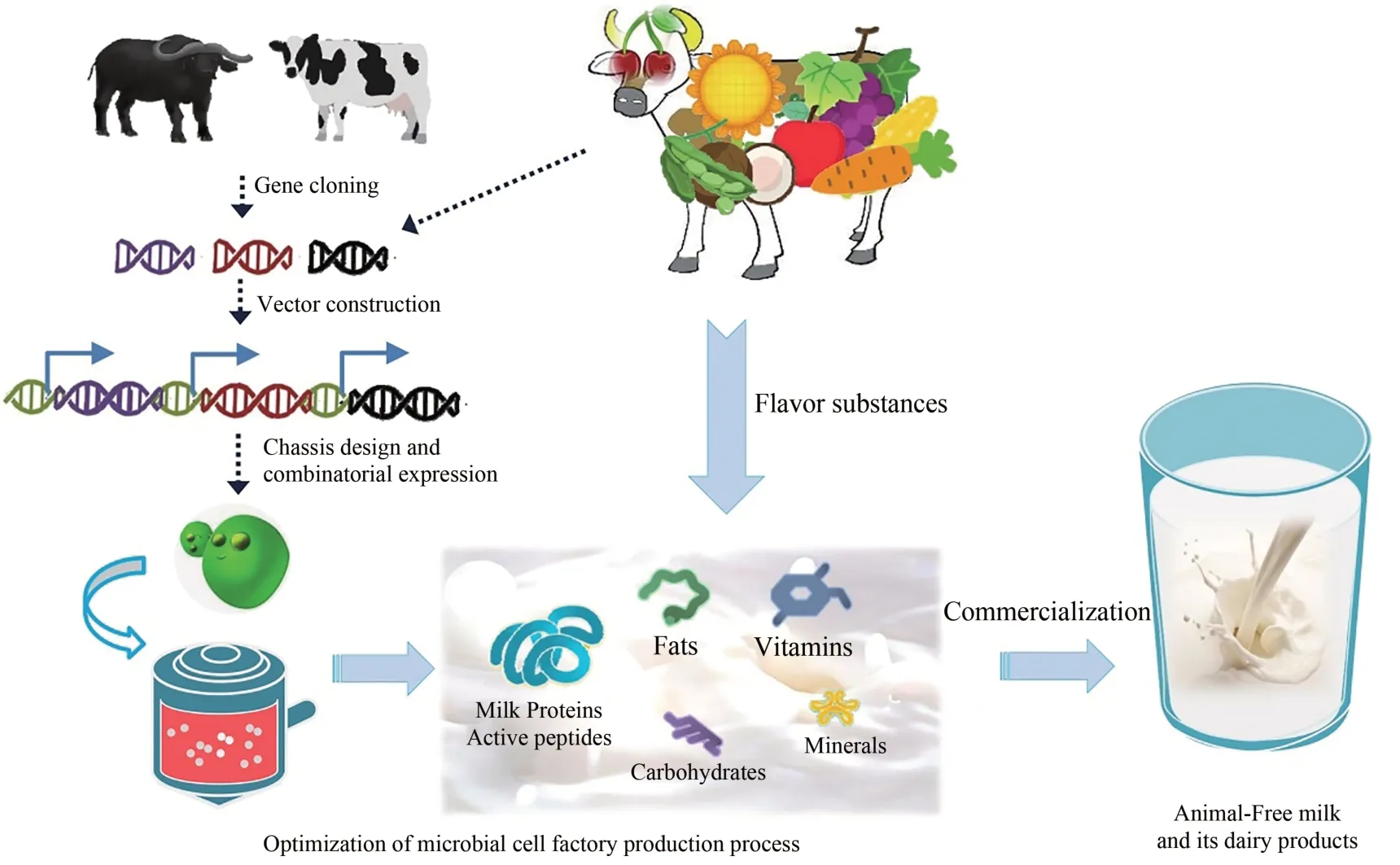
目前,全球对乳制品的需求量不断增加。随着全球人口和发展中国家经济增长,全球奶类供需年均增长率达2.3%。未来十年内,中国将持续保持乳制品进口势头,预计到2028 年鲜奶进口量将达90 万吨[1]。天然动物奶及其乳制品是最理想的蛋白营养来源,其营养成分主要是乳蛋白,同时还含有生物活性肽、脂肪、乳糖、维生素和矿物质等[2-3]。但另一方面,因含有各种致敏原,天然动物奶是婴幼儿群体中排在首位的致敏食物[4]。此外,牛奶含有4.6%左右的乳糖,导致乳糖不耐受人群食用后出现腹胀及腹泻等不良症状。特别是近年来,动物奶生产还普遍存在养殖成本高、饲料资源短缺、抗生素滥用、环境污染严重、疫病防控形势严峻等问题,亟待产业升级换代[5-6]。
面对乳制品生产的可持续性、公共卫生以及动物福利等问题,植物源或动物源的乳蛋白替代技术的研发逐步受到广泛关注,并已取得了实质性的进展,但在风味、口感和功能特性等方面还存在许多亟待解决的问题[7-8]。近年来,信息科学、生命科学和工程科学等学科交叉融合,驱动基因编辑、合成生物学、全基因组选择等前沿生物技术快速发展,为全球食品生产提供变革性的生产方式,培育孵化未来食品和细胞农业等战略性新兴产业。利用合成生物技术等颠覆性创新技术手段,构建具有特定合成能力的细胞工厂,生产人类所需的淀粉、蛋白质、油脂、糖、奶、肉等各类农产品,近年来已取得重要进展[9-10]。2014 年,美国一家基于“细胞农业”(cellular agriculture)概念的生物科技初创公司完美日(Perfect Day)公司提出人造奶(animal-free milk)概念,设计改造酵母细胞工业化发酵牛乳蛋白(如乳清蛋白和酪蛋白)以及相应营养成分,实现人造乳制品的精准营养和绿色制造[11]。随着越来越多的食品企业开始尝试合成生物技术,在实验室中制作的动植物基人造肉、人造蛋和人造母乳等产品不断涌现,美国Perfect Day 公司和以色列人造奶(Remilk)公司相继在2019 年开发出牛乳蛋白微生物合成新工艺,引领人造合成食品领域成为新的投资风口。
乳蛋白主要由酪蛋白和乳清蛋白组成,分别约占蛋白总量的80%和20%[12]。乳清中主要含有β-乳球蛋白、α-乳白蛋白、乳铁蛋白、脂肪球膜蛋白以及免疫球蛋白等[13-15]。乳蛋白表达是人造奶生物合成的核心,主要是指采用基因工程和细胞工厂等技术手段,高效表达动物奶中的各种蛋白质组分。当前,人造奶研究正处于生产工艺突破和产品商业化的初创阶段,在重要乳蛋白组分的高效合成以及人造奶制品生产工艺等方面存在亟待突破的技术瓶颈。智慧芽数据库是一款全球专利检索数据库,深度整合了从1790 年至今的全球116 个国家地区的1.5 亿专利数据,提供精准、及时的研发情报。本文通过对智慧芽数据库进行全面检索(截止到2020 年12 月),共获得362 条与乳蛋白重组表达和人造奶生物合成相关的专利文献,经过人工筛选降噪,最终明确175 项专利申请。在此基础上,对乳蛋白重组表达和人造奶生物合成相关技术的发展历程、研发现状、未来发展趋势及生物安全和伦理问题进行了系统分析。
1 国内外研发概况
1.1 发展历程
乳蛋白表达研究始于20 世纪90 年代,随后以乳腺生物反应器为核心的生物技术公司相继出现,包括美国基因药物国际有限公司、美国威斯康星乳制品营销管理局、瑞典斯比克姆股份有限公司、美国雅培公司和苏格兰医药蛋白有限公司等,其核心技术是通过转基因动物家畜的乳汁来获取乳蛋白。该过程获得的乳蛋白经修饰加工,具有稳定的生物活性,可直接用于食品加工[16]。2000—2010 年的10 年间,利用植物组织细胞和叶绿体构建植物表达系统,打造乳蛋白生产的植物生物反应器,人造奶的研发迎来新一轮发展浪潮[17](图1)。近十年来,基于基因组和系统生物学的合成生物学掀起了第三次生物技术革命,人造奶研究也取得了突破性的进展,如利用一系列模式微生物和植物作为底盘细胞工厂,高效表达乳蛋白[18];采用精细化工技术,开展乳制品人工组合物、风味物质研究与应用[19-20]。我国人造奶技术起步较晚,第一个发明专利由复旦大学于2003 年申请,涉及利用植物反应器生产乳铁蛋白技术(CN1544641A)[21]。

图1 人造奶相关专利申请量年度变化Fig.1 Annual statistic for the number of patents related to animal-free milk
1.2 竞争态势
在全球范围内,水产动物产品、谷类和牛奶是人类食用蛋白质的三大来源,其中牛奶蛋白占全球食物蛋白供应量的10%。根据2021 年波士顿咨询公司(BCG)和Blue Horizon 联合发布的研究报告(Food for thought:the protein transformation),由于动物蛋白资源短缺和生物技术创新推动,未来十五年内动植物或微生物基的替代蛋白产品将占据22%的全球食用蛋白市场份额,产业规模达到2900 亿美元。预示着以人造奶为代表的未来食品将逐步占据传统餐桌,在相关技术知识产权保护上引发激烈的国际竞争[22]。
为研究人造奶相关技术全球专利申请的主要来源地分布,本研究对每项专利申请的最先申请国等数据进行分析。由于专利申请人一般会优先选择自己所在国家申请专利,相关分析数据可以反映各个国家和地区在人造奶及相关乳蛋白重组表达领域的技术实力。从图2可以看出,美国申请人提交的专利申请最多,共72 项,占比41%。其次是欧洲,申请专利为29 项,二者占全部专利申请的一半以上,表明欧美国家在人造奶研发领域占主导地位。中国的专利申请数量为16 项,位居第3 位,表明我国在相关领域已有一定研发基础,但需要进一步加强技术工艺创新。
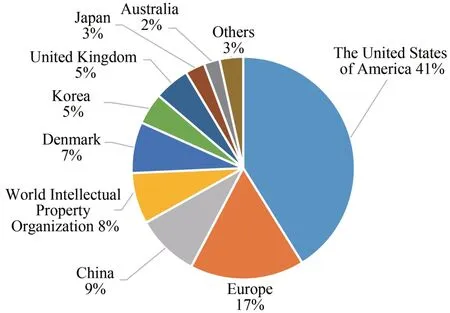
图2 人造奶相关全球专利申请人区域分布Fig.2 Geographic distribution of the applicants of patents related to animal-free milk
图3显示了人造奶相关全球专利申请的目的地分布。在人造奶相关全球专利申请中,欧洲是主要的申请地区,排名第1位。中国、日本、澳大利亚和美国位居2~5 位,表明这些国家将是未来人造奶产品生产、加工、销售的主要目的国,需要特别关注其产业化的相关法规和监管政策动向。
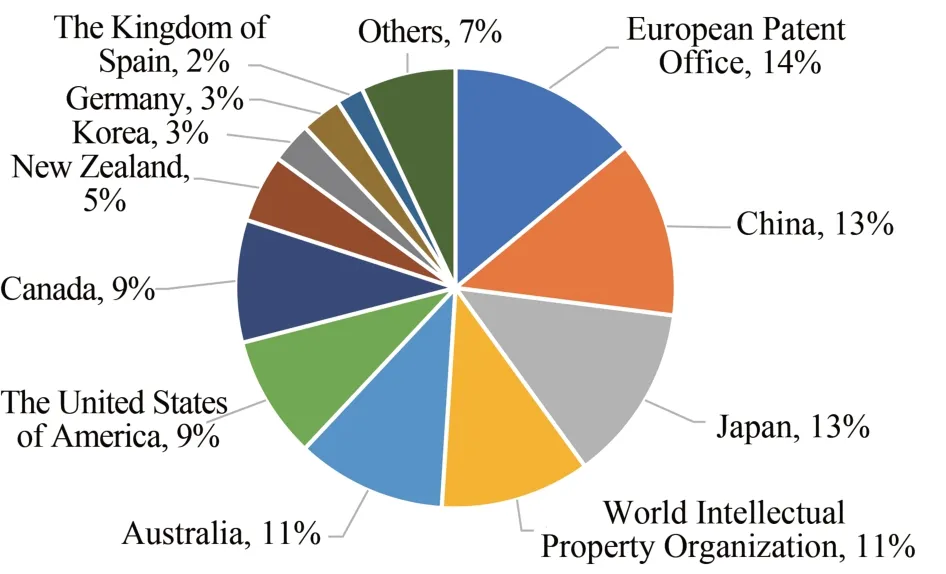
图3 人造奶相关全球专利申请的目的地分布Fig.3 Geographic distribution of patents related to animalfree milk
人造奶生产技术相关专利全球主要申请人排名显示(图4),全球排名前10 的专利申请人中,有9个是企业,在这一领域中申请量占比为95.9%,是人造奶领域技术研发的主力军。排名第一的是美国Perfect Day公司,其申请的34项专利在全球11个国家或地区进行了布局,是人造奶研发行业的技术领跑者。该公司通过酵母细胞表达重组乳蛋白,之后将分离纯化得到的重组乳蛋白与其他成分混合制成人造奶。排名第二的是美国文特里亚生物科学公司,其专利申请主要涉及转基因植物生产人乳蛋白及相关食品和食品添加剂组合物,用于婴儿配方食品的优化改良。排名第三的是荷兰帝斯曼知识产权资产管理有限公司,其专利申请主要涉及改变乳制品风味及重组表达生产乳糖酶等,其中乳糖酶制剂可用于食品和饲料产品中乳糖水解,且不产生异味化合物。瑞典斯比克姆股份有限公司排名第四,其专利申请主要涉及动物乳腺生物反应器表达重组酪蛋白,并用于婴儿配方食品。
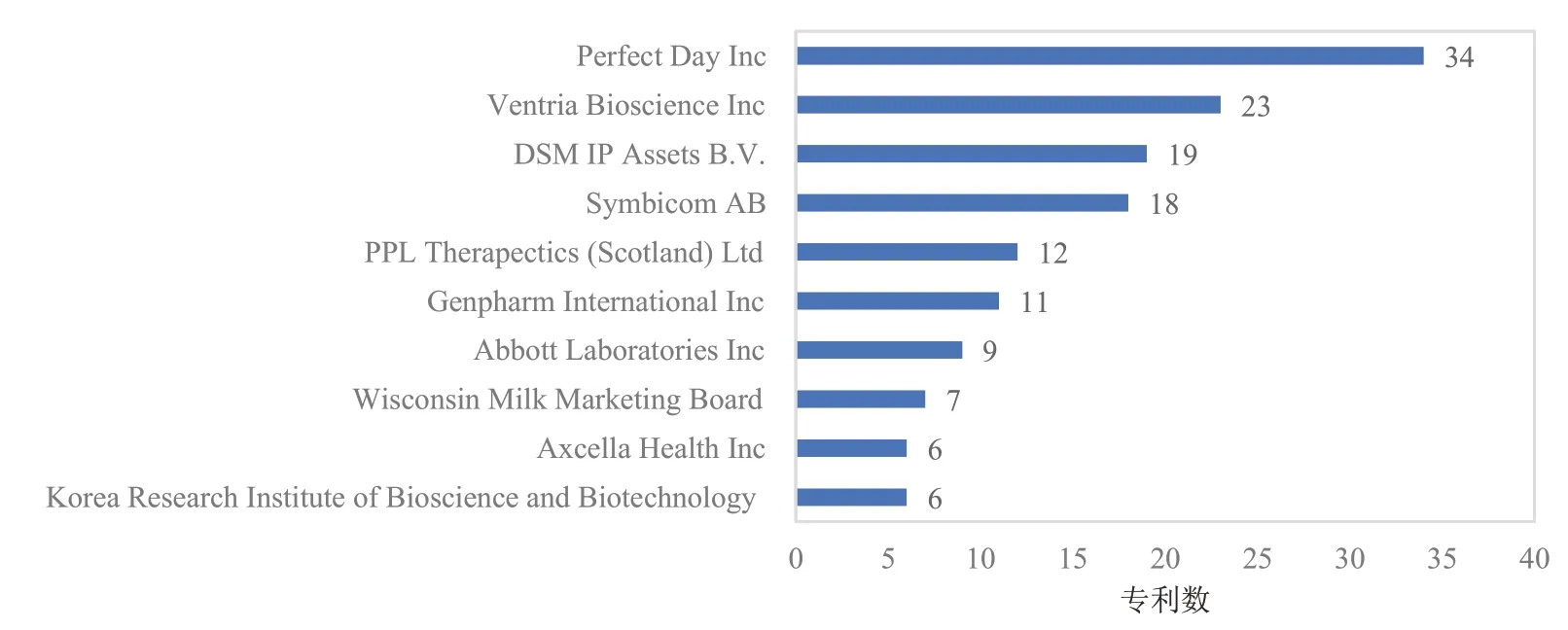
图4 人造奶相关专利申请人排名Fig.4 Ranking of the applicants of patents related to animal-free milk
1.3 我国研发现状
从1990 年到2020 年的30 年间,全球蛋白质消费量增长96%。根据中国农业展望报告(2021—2030),我国奶制品消费持续增长,2030 年奶制品消费量将达6933 万吨;同时市场缺口巨大,预计2030 年奶制品进口为 2563 万吨[23]。为满足上述消费需求和应对国际蛋白替代市场的激烈竞争,我国在乳蛋白重组表达与人造奶生物合成等技术领域已开始进行研发布局,并取得重要进展。
我国乳蛋白重组表达与人造奶相关专利共有16项,企业与科研院校的申请量占比相当(图5)。科研院校包括中国农业科学院生物技术研究所、东北农业大学、浙江工业大学、山东大学、复旦大学、泉州师范学院等,申请量为9项,主要涉及乳铁蛋白的重组表达,用于饲料的添加,作为养殖用抗生素替代品具有良好前景。企业申请相关专利共7 项,涉及乳铁蛋白的专利2 项,利用真核表达系统的毕赤酵母菌株生产乳铁蛋白,并应用于饲料的辅助添加。乳球蛋白相关专利1项,通过家畜乳腺生物反应器生产乳球蛋白,用于抗菌、抗病毒、提高免疫力等功能性开发。其他的专利5 项,涉及相关酶的重组表达,其中中国农业科学院生物技术研究所创建了一种将角蛋白(羽毛)高效转化为人工血红蛋白(肌浆蛋白)的生物合成体系(PCT/CN/2020/111685)[24],中国科学院先进技术研究院研究团队通过大肠杆菌分别完成7种牛乳蛋白的异源表达[25]。常规异源表达中,靶标蛋白表达量偏低甚至难以表达,已成为蛋白质替代产品研发上的关键技术瓶颈。中国农业科学院生物技术研究所发现来自丝氨酸蛋白酶的一段分子伴侣多肽PEP,具有帮助乳蛋白的正确折叠和促进重组蛋白体外高效表达的功能。为提高乳蛋白表达效率,通过基因重组将前肽PEP 与目标蛋白融合,实现了多种难表达乳蛋白的高效合成,且为有活性的可溶蛋白[26]。
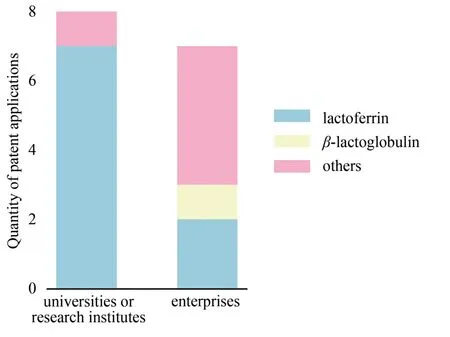
图5 国内人造奶相关专利类型分布Fig.5 Domestic patents for animal-free milk applied by universities/research institutes and companies
中国科技政策对于人造合成食品的研发持积极支持态度。2010—2019 年间,我国国家自然科学基金针对合成生物食品的应用基础研发方面给予一定的经费投入。根据国家重点研发计划“合成生物学”和“绿色生物智造”等重点专项2019—2020 年项目申报指南,我国拟投入国拨经费十几亿人民币,支持合成生物学在食品、医药和能源等领域的研究创新。近年来,我国在深圳、天津等地建立国家合成生物学创新中心,并通过国家、地方政府和企业投资,培育具有国际竞争力的合成生物科技初创企业。同时,人造合成食品领域也为我国资本市场提供了巨大商机。我国第1家食品科技风投集团——食芯资本公司专注于投资农业食品科技领域拥有颠覆性技术的初创企业,如中国合成生物科技初创企业摩珈生物、以色列细胞培养肉公司Future Meat Technologies 和英国生物科技公司Tropic Biosciences 等的创新项目。但相比人造肉等未来食品研发,目前我国乳蛋白重组表达与人造奶生物合成技术研发力量相对薄弱,国家层面的科技项目立项和企业层面的风险资金投入不足,相关知识产权保护乏力。因此,为应对日趋激烈的国际竞争,在“十四五”期间应尽快设立国家重点研发项目,加大研发投入,着力突破乳蛋白组合表达关键技术瓶颈和人造奶生产新工艺,同时食品安全监管方面应加快制定人造奶等未来食品管理法规和产业化政策。
2 技术研发进展
2.1 乳蛋白重组表达
采用基因工程和细胞工厂等技术手段,高效表达动物奶中的各种蛋白质组分,是人造奶生物合成的核心技术环节。人造奶研发技术相关专利文献分析发现,重组表达乳铁蛋白的专利申请量最高,有41 项。组合表达多种乳蛋白位居第二,有36 项;表达乳白蛋白和酪蛋白分别有21 和20项;表达乳球蛋白的最少,仅有2项。其他的申请涉及牛奶中酶蛋白,改变乳制品风味以及干酪、酸奶生产等技术内容。乳蛋白表达类型申请量对比分析表明(图6),组合表达乳蛋白是获取人造奶的主要技术。其中,美国基因药物国际有限公司通过转基因牛乳腺重组表达多种乳蛋白,生产含有多种重组肽的食物配方(AU1991069608A1)。美国文特里亚生物科学公司通过在转基因植物种子表达多种人乳蛋白,生产的乳蛋白食品以及食品添加剂组合物来改进婴儿食品配方(AU2007216827A1)。美国Perfect Day公司利用微生物细胞工厂重组表达乳蛋白,生成具有哺乳动物产生的牛乳类似风味、外观、营养价值、香气和类似口感的组合物(US20170273328A1)。其他专利涉及乳铁蛋白表达,用于饲料中抗生素的添加;或通过转基因动物家畜乳腺生物反应器表达酪蛋白和乳白蛋白,用于婴儿食品配方成分。

图6 重组表达乳蛋白类型专利申请量比对Fig.6 Patents applied for different recombinant milk proteins
2.2 人造奶生物合成
目前,美国Perfect Day 公司和以色列Remilk公司均已开发出人造奶生物合成新工艺。特别是Perfect Day 公司研发技术雄厚,2019 年12 月实现融资2亿美元,成为乳制品替代新兴行业中产业化发展势头最强劲的高科技初创企业。
美国Perfect Day 公司原名“Muufri”,创立于2014 年,总部位于美国伯克利市,是一家基于“细胞农业”概念的生物科技初创公司。该公司利用微生物的发酵作用来制造乳制品蛋白,并首创了人造奶(cow free milk)概念。该公司通过人工合成牛奶乳蛋白DNA 序列,转化到食品级酵母中表达酪蛋白和乳清蛋白,并与植物性成分混合生产出纯素食、无乳糖、无胆固醇的人造奶,可用于制作冰淇淋、奶酪、酸奶和其他一系列乳制品,已取得的重要进展包括:①酪蛋白的组合物及其生产方法(US10595545),其主要发明点在于提供了不包括动物来源组分的组合物,其含有κ-酪蛋白、β-酪蛋白、脂质、风味化合物、甜味剂和灰分[27];②乳蛋白和非动物蛋白的食物产品及其生产方法(US20190216106A1),提供了椰子油、β-乳球蛋白和豌豆蛋白等混合的人造奶,以及该人造奶发酵制备得到的酸奶[28];③用于生产包含重组成分和组合物食品的方法(WO2020081789A9),提供了在通过基于电荷来分离重组β-乳球蛋白的方法,从而用于生产具有特殊风味乳制品[29]。目前,这类人造奶乳制品已通过美国食品和药物管理局的GRAS(Generally Recognized as Safe)审查。同时,该公司与美国阿彻丹尼尔斯米德兰公司等农业巨头合作,计划到2022 年将人造蛋白产量从目前的数十吨增加到数千吨。
Perfect Day公司专利布局随研发过程同步展开(图7)。2015年首先在美国、加拿大、澳大利亚和欧洲等国家和地区针对酪蛋白组合物及其制作方法申请了8件发明专利,进行布局。2017年为拓展亚洲和南美洲市场,先后在印度尼西亚、中国、巴西和墨西哥等国家和地区,针对酪蛋白组合物及其制作方法优化改良与非动物源蛋白食品及其生产方法,申请专利14 件。随着技术逐渐成熟,2019 年,其专利申请内容涉及包括非动物源蛋白食品和生产方法、重组牛奶蛋白聚合物、产生同核的丝状真菌细胞的方法、用于生产包含重组成分和组合物食品的方法以及酪蛋白组合物和制造方法。2015 年至今,Perfect Day 公司先后申请同族专利34 件,布局11 个发达和发展中国家和地区,力图通过迅速扩张,抢占未来人造奶产品国际市场。
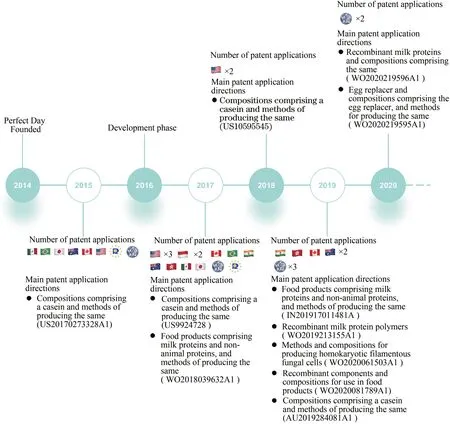
图7 Perfect Day公司人造奶相关专利申请及全球布局Fig.7 Perfect Day's patent applications for animal-free milk
下面重点介绍Perfect Day 公司于2015 年获得的美国发明专利US10595545。该专利涉及人造奶生物合成的关键核心技术,包括:①人工合成牛乳蛋白编码基因的DNA 序列,包括牛αs1-酪蛋白、牛αs2-酪蛋白、牛β-酪蛋白、牛κ-酪蛋白、牛α-乳白蛋白和牛β-乳球蛋白[16,30];②构建重组质粒,在酿酒酵母和毕赤酵母中分别表达上述6种牛乳蛋白,利用不同蛋白的亲疏水性、等电点等理化性质将其分离纯化;③通过酯交换将短链脂肪酸甘油三酯与高油酸葵花籽油结合,制备乳脂肪酸甘油三酯;④人造奶的配方组分为酪蛋白、乳清蛋白、甘油三酯、糖类、微量元素、维生素等,配方比例为每1 L 人造奶中含26 g酪蛋白、3.5 g乳清蛋白、24 g 半乳糖和5 g 灰分组合;⑤添加多种脂肪和风味化合物,包括向日葵油、椰子油、三丁酸甘油酯、甘油一酯和甘油二酯、游离脂肪酸和磷脂、δ-癸内酯、丁酸乙酯、2-呋喃基甲基酮、2,3-戊二酮、γ-十一内酯和δ-十一内酯等,用以模仿动物源奶类的口感和风味。
3 展望
3.1 乳蛋白组合表达细胞工厂创建
通过对人造奶相关专利文献的分析发现,早期的专利技术是利用动植物生物反应器来表达乳蛋白及其组合物,这样可以直接获得可食用的乳蛋白,但是对于乳蛋白的提取、分离纯化较困难,且生产成本较高。利用合成生物学等前沿技术改造天然乳蛋白及其微生物表达底盘,组合表达乳蛋白是当前一个重要技术发展趋势。目前,实现乳蛋白的生物制造替代,亟待突破的瓶颈问题是创建乳蛋白高效表达与正确组装的微生物底盘细胞[31]。
酵母菌是应用最广泛的重组蛋白高效表达平台,也是合成生物学和现代发酵工业中最常用的真核底盘细胞,在工农业及医药等行业均有广泛应用。目前,工程酵母菌底盘改造已逐渐由基因水平的酶蛋白高表达1.0 版、组学水平的代谢通路调控2.0 版,进入智能化人工设计3.0 版的新阶段。通过开发表达系统的模块、基因元件重构、基因的大规模重组和重排等关键技术,突破蛋白高效合成与表达路径各环节的技术与理论瓶颈,来实现蛋白合成路径和代谢调控网络的优化与全新合成、底盘细胞全局性改造,创建低能耗、高产出、易加工、抗逆性强蛋白高效表达体系生产重组牛乳蛋白。中国农业科学院生物技术研究所通过人工设计组装多基因串联表达模块,构建αs1-酪蛋白、αs2-酪蛋白、β-酪蛋白、κ-酪蛋白4种酪蛋白的共表达-共纯化体系,实现了酪蛋白的高效表达与组合合成,同时正在开展人、山羊、骆驼、青藏高原牦牛等不同物种乳蛋白的资源挖掘与人工优化,筛选获得优质的乳蛋白组合。2020 年Nature Communications杂志发表了题为“Synthetic biology 2020—2030: six commercially-available products that are changing our world”的文章,列举了6个在2000—2020 年间已商业化面向市场并正在改变世界的6个生物合成产品,其中包括利用重组毕赤酵表达大豆血红蛋白,作为未来人造食品配料并改善其口感和风味[32]。
丝状真菌是一类更适合于生产重组哺乳动物蛋白的底盘微生物。相比酵母菌,丝状真菌具有更强的工业化生产重组蛋白表达能力,同时其产生的含哺乳动物信号序列的重组蛋白在分泌特性及其糖基化等翻译后修饰方面与哺乳动物细胞合成的蛋白更相似[33]。我国在丝状真菌蛋白分泌表达系统及其遗传操作系统方面开展了系统研究,如中国科学院天津工业生物技术研究所通过改造获得丝状真菌如黑曲霉和米曲霉等高效蛋白表达宿主,挖掘表达元件如强启动子、信号肽、终止子、锚定蛋白以及蛋白分泌调控相关转录因子,构建了具有自主知识产权的丝状真菌蛋白分泌表达系统及重组外源蛋白工业化规模高效表达的核心平台,获得核心技术专利如一种调控sgRNA 转录的启动子、表达载体及其基因组编辑系统和应用(CN110331146B)和一种改善丝状真菌蛋白分泌能力的方法(CN106119137B)等。此外,华南理工大学申报发明专利“丝状真菌蛋白分泌压力反馈调控元件与抗反馈抑制的启动子、质粒及制备方法和转化细胞”(CN103275981A)和“一种提取丝状真菌基因组DNA 的方法及试剂盒和遗传转化子的快速筛选方法”(CN103361339A)也获得授权。2020 年,Perfect Day 公司优化了丝状真菌大量培养与筛选的实用方案,将应用于未来高效的丝状真菌底盘细胞工厂的创建中(WO202006 1503A1)。
3.2 新一代人造奶生物智造
2014 年,美国Perfect Day 公司提出人造牛奶概念,设计改造酵母细胞工业化分别发酵牛乳蛋白(乳清蛋白和酪蛋白)以及相应营养成分,模仿动物源奶类的成分、功能、质地和风味,经过精细化加工,实现人造乳制品的精准营养和绿色制造。经过生产工艺优化,该公司的人造牛奶蛋白初创产品含6种牛奶蛋白、8种脂肪酸、矿物质、维生素和糖类,具有与牛奶相似的营养成分和风味,同时还突破产业化的成本障碍,其生产成本较普通牛奶蛋白低40%左右。2019 年,该公司以每品脱(1品脱≈473毫升)20美元的价格限量销售1000 品脱含香草盐软糖、牛奶巧克力、香草黑莓太妃糖3种口味的人造奶冰淇淋,其售价与目前国内市场同规格哈根达斯冰淇淋的价格相当。与传统的牛奶生产方式相比,人造奶的生物合成工艺还具备显著的环保优势,将减少98%的用水量,91%的土地需求,84%温室气体排放,并节约65%的能源[8],将颠覆传统养殖模式,有助于世界农业碳达峰和碳中和目标实现。
与天然动物奶比较,人造奶制品还有一个显著优势就是不含乳糖、胆固醇和致敏原等不良因子。牛奶及其乳制品是FAO和WHO认定的导致人类食物过敏的八大类食品之一,牛乳蛋白过敏是婴幼儿最普遍的一类食物过敏[4,34],因此,美国及欧盟新食品标签法规定牛奶必须标示的致敏原成分。目前,牛奶中已知的主要致敏原包括αS1-酪蛋白、αS2-酪蛋白、β-蛋酪蛋白、κ-蛋酪蛋白、β-蛋乳球蛋白和α-球乳白蛋白等。通过致敏原数据库比对分析,可以针对不同来源的乳蛋白序列进行人工设计,提高其生物活性同时删除其致敏原,可望获得更加营养和健康的人造奶制品[35-36]。
但是,从口感、风味和营养而言,目前人造奶产品还无法与动物天然乳制品抗衡。在天然牛奶中,蛋白质的含量仅为3%左右,主要由酪蛋白和乳清蛋白两大部分组成,但其风味和活性成分非常复杂。牛奶特有的风味物质包括游离脂肪酸、醇、酯、内酯、醛、酮、酚、醚、含硫化合物及萜类等多种有机物,主要是由牛奶中蛋白质、脂肪、乳糖三大类物质降解或各类衍生物之间反应生成。其中,脂肪作为一种重要食物成分对未来人造乳制品的风味、口感和营养品质等改良至关重要[30]。此外,天然牛奶还含有各种生物活性物质,现已检测到50 多种,包括免疫球蛋白、乳过氧化物酶、溶菌酶、酪蛋白源和乳清蛋白源的生物活性肽、不饱和脂肪酸、激素(如褪黑素)及细胞因子(如白细胞介素)等,其来源包括从血液转入奶中,或经蛋白质水解作用形成以及乳腺本身合成等,具有多种生理功能和免疫保护作用[37]。因此,利用合成生物学技术改造微生物底盘,组合合成多种脂肪类风味物质以及多肽类生物活性物质,实现新一代人造奶的生物智造(图8),应用前景更加广阔[38-39]。
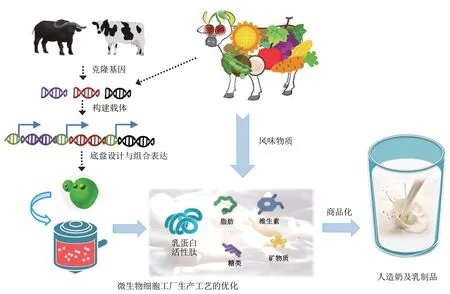
图8 乳蛋白组合表达细胞工厂创建与人造奶生物合成的技术流程Fig.8 Process diagram for the combinatorial expression of milk proteins to produce synthetic milk
3.3 生物安全与生物伦理思考
由于合成生物学具有颠覆性、交叉性和不确定性等技术特征,其相关产品如人造食品的商业化在生物安全和生物伦理方面存在较大争议。如何运用法律来平衡此类人造食品商业化带来的风险与收益,是当前国际社会普遍关注的问题。2018 年召开的联合国生物多样性会议暨《生物多样性公约》第十四次缔约方大会提出,需要注重合成生物学领域的风险评估模式、国际合作和法律考量,以应对合成生物产品商业化可能带来的安全风险。
合成生物学及其产品的安全风险评价涉及以下内容:①新遗传信息意外暴露于人类和环境;②新遗传物质在批准使用范围以外的环境中扩散;③在人工遗传物质可能改变或影响人类、动物或环境的遗传信息的情况下,发生水平基因转移的可能性;④食品营养品质改变、产生潜在过敏原和未知成分。此外,具有颠覆性特征的合成生物技术能设计全新的人工元器件,创制全新的人工基因线路(如高效固氮基因回路、表观遗传回路等)、人工生物细胞(如最小基因组、细胞工厂等)、人工生物装置(如人造叶片,生物纳米机器等)、非天然化合物(如非天然氨基酸、非天然药物等)以及人造食品(如人造肉、人造奶等),在食用安全或环境安全方面可能产生新的潜在风险。目前,世界各国在针对合成生物食品商业化问题上并未建立专门且具体的法律规范和管理措施,但普遍采用现有的法律框架进行生物安全评价和监管(表1)[40-42]。美国《联邦法典》中关于食品与药品的规定(Code of Federal Regulations,Title 21 Food and Drug)要求新型生物产品的研发和投入市场需要向生物产品评价与研究中心(Center for Biologics Evaluation and Research)进行申报,以保证生物产品的安全性和有效性。欧盟科学委员会在其发布的《适用于合成生物学的评价方法是否存在风险》(Synthetic Biology ⅡRisk Assessment Methodologies and Safety Aspects)草案意见书中明确表示,目前用于生物和遗传修饰物质的已有法规可以应用于合成生物产品。2020年,欧洲食品安全局发布关于现有指南对合成微生物进行微生物表征和环境风险评估适用性的评估报告,明确指出现有的欧洲食品安全局指南可作为对当前和未来十年内合成微生物特性描述和环境风险评估的基础,待评估产品的用途范围应涵盖所有农业食品用途,并考虑到所有类型的微生物及其相关接触途径和环境[43]。以人造肉产品为例,美国农业部和食品药物管理局等在现有法规框架下,正着手制定相关的安全标准和监管框架。人造肉产品能否可以贴上“肉”的标签已引发争议,密西西比等13 个州出台了植物蛋白肉、培养肉等不能再用“肉”字宣传的立法提案。目前,我国人造肉和人造奶等合成食品研究还处于实验室阶段,尚未有商业化产品进入市场。对于这一新型科技食品,我国还没有制定专门的立法来规范其入市前审批和入市后监管事项,因此需要加快其立法研究,确保我国合成生物学及其相关产品产业化在法定框架下健康发展[41,44]。
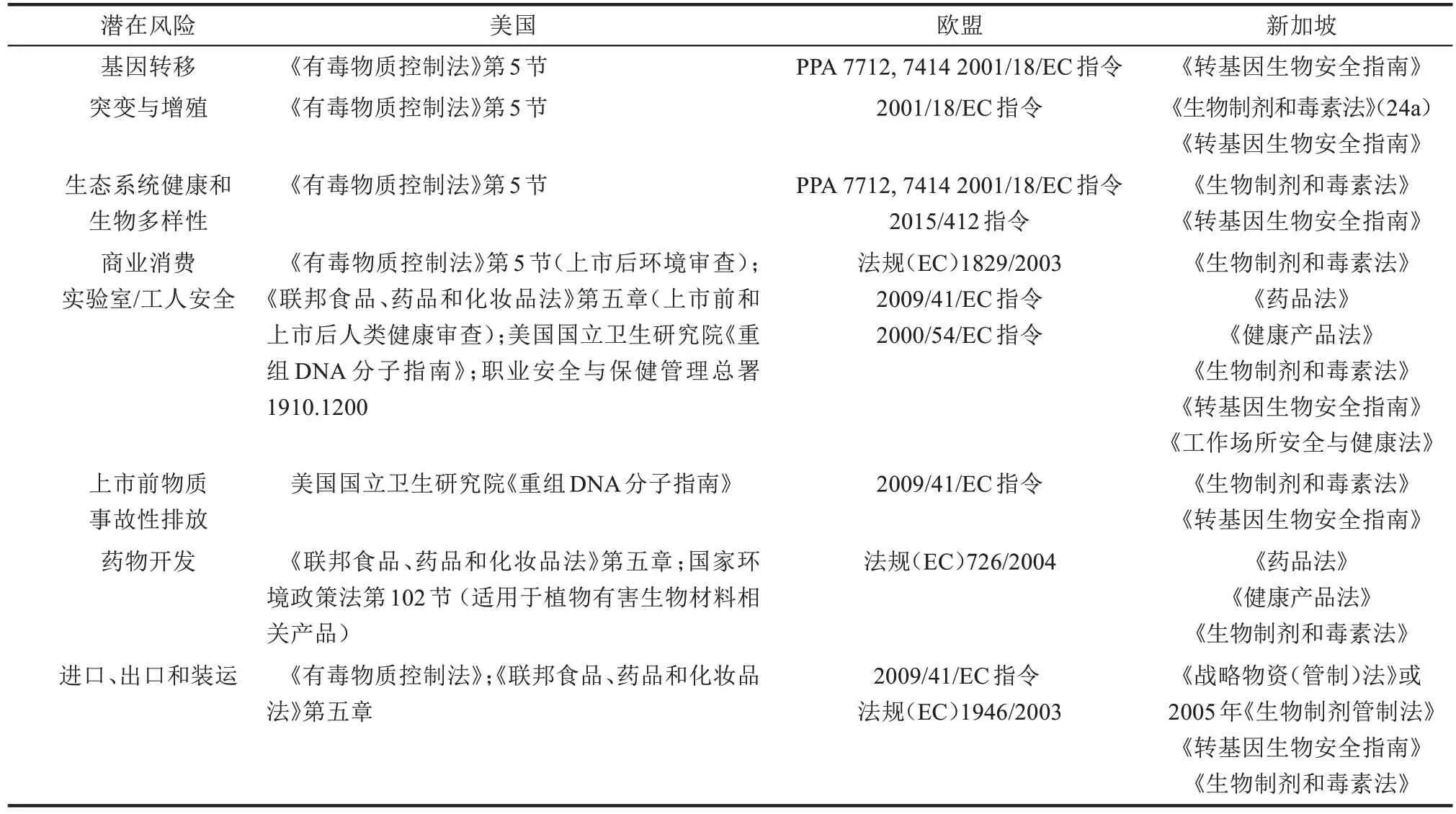
表1 美国、欧盟和新加坡合成生物技术监管相关法规[40]Tab.1 Synthetic biology regulation and governance in United States,European Union and Singapore
任何一项新兴生物科技的兴起与应用均存在生物安全风险和生命伦理争议,也伴生了一系列新兴生物科技伦理学的出现,如gen-ethics(遗传伦理学或基因伦理学)、synbio-ethics(合成生物伦理学)、nano-ethics(纳米技术伦理学)以及ⅠT-ethics(信息技术伦理学)等。合成生物学在21世纪初兴起并迅猛发展,其研究目标是创造或设计非天然的全新生命形式,由此引发了对生命概念及生命尊严的挑战和伦理争议[45-46]。合成生物食品的商业化也存在伦理风险,譬如合成生物食品的法律定义以及对自然环境和人类社会的伦理影响[47-48]。
2005 年,联合国教科文组织发布《世界生物伦理和人权宣言》,重申设立伦理委员会以评估涉及生物的研究是否违背伦理的必要性,强调生物科学研究必须符合伦理道德的基本准则。2017 年,美国农业部和食品药品监督管理局正式就细胞培育肉类产品的商业化制定了规则框架,为人造食品行业的健康发展提供法律指导。欧盟各国对于合成生物食品的商业化发展普遍持谨慎态度,其新食品法规明确规定,由细胞培养物或源自动物的组织培养物产生的食物都将被视作一种新型食品,因此需要建立与之相适应的法律监管体系和生物伦理规范。我国已审议通过的《生物安全法》规定,包括基因编辑、合成生物等前沿生物技术相关的研究、开发与应用活动必须在符合伦理原则的框架下进行。
进入新世纪以来,合成生物学、生物信息学、仿生学以及人工智能等新兴科学迅猛发展,正推动农业生产方式从传统的驯化蓄养农业、工业化农业向细胞农业转变[49-51]。细胞农业是以基因工程和细胞工程为技术核心,将革命性改变农产品生产与供应链,为不断增长的人口提供可持续和更健康的食品[52-54],为世界农业碳达峰和碳中和目标实现提供不可替代的科技支撑。此外,细胞农业可以根据要求对产品进行个性化的设计和调整,这将是绿色安全高品质食品的未来发展趋势[38,55-56]。毫无疑问,人造奶的营养与风味与天然牛奶相当,但不含乳糖、胆固醇、抗生素和致敏原等不良因子,其生产过程无需养殖动物,可以有效节约资源与能源,是一种颠覆传统养殖业的未来乳制品生产新模式,将引领未来食品产业和细胞农业发展方向[57]。

