体重管理对超重及肥胖PCOS患者代谢及妊娠结局影响
黄 芳 赵 花 彭顺英
广东省肇庆市第一人民医院 (526060)
多囊卵巢综合征(PCOS)在青春期、适龄女性发生率较高,是一种内分泌代谢紊乱病症[1]。患者多伴随有糖脂代谢异常、胰岛素抵抗、肥胖等,对生殖功能产生影响。不及时治疗会增加肿瘤、心血管疾病、糖尿病发生风险[2]。PCOS患者妊娠后会增加胎儿宫内发育迟缓、妊娠期高血压、妊娠期糖尿病发生风险,故对超重及肥胖PCOS患者进行体重管理非常重要[3]。本研究分析体重管理对超重及肥胖PCOS患者代谢指标及妊娠结局的影响,为临床治疗PCOS提供参考。
1 资料与方法
1.1 一般资料
选取2018年1月-2019年12月本院收治的超重及肥胖PCOS患者80例,随机数字表法分为两组。纳入标准:①符合PCOS相关诊断标准;②有正常子宫且至少有一侧输卵管畅通;③配偶精液正常;④体质指数(BMI)>24kg/m2;⑤均知情研究并签署知情同意书。排除标准:①存在生殖器官器质性疾病;②男方原因导致不孕;③存在各种糖尿病;④心肝肾功能严重不全;⑤近期服用过抗抑郁、减肥药物。本研究经本院伦理委员会审批。
1.2 治疗方法
1.2.1药物治疗两组患者入组后均接受基础药物治疗,治疗前存在闭经患者给予地屈孕酮片口服治疗,10mg/次,2次/d,连续10d;若闭经时间长,体内雌激素过低患者可给予芬吗通(雌二醇片/雌二醇地屈孕酮片复合包装2/10mg),1片/次,1次/d,连续28d。在月经来潮后第5d,给予优思明口服(屈螺酮炔雌醇),1次/d,1次1片,连续治疗21d,后停药1周,连续治疗3个月经周期。
1.2.2体重管理对照组行常规管理,给予患者饮食指导、运动干预,主要有告知患者戒烟戒酒、少喝咖啡,少吃高热量等食物,告知患者避免久坐,规律运动,1次30min。观察组在对照组基础上进行体重管理,管理前判断患者饮食习惯、心理情况,告知体重管理的意义、目的和重要性,患者知情同意后进行体重管理。确保患者在饮食期间蛋白质摄入量为20.0%~27.0%,碳水化合物摄入量为3.0%~5.0%,脂肪摄入量为70.0%~75.0%,在目标摄入量的基础上每日降低2090KJ,每日三餐由专门营养师根据患者喜好安排与调整,自行在家烹煮,连续管理10周,停止前先进行2周退酮,后期转变为均衡饮食。管理期间密切观察患者各项情况,一旦出现腹痛、变比、低血糖等及时处理,确保体重管理顺利。
1.3 观察指标
①比较两组卵巢体积、腰臀比、体质指数,测量治疗前后患者身高与体重计算BMI和腰臀比,阴道超声检测卵巢体积[4]。②治疗前后采集两组空腹静脉血,全自动免疫化学发光法检测性激素指标[5],化学发光法检测空腹胰岛素(FINS),使用葡萄糖氧化酶法检测空腹血糖(FBG)及餐后2h血糖(2hPBG),计算胰岛素抵抗指数(HOMA-IR)[6],酶联免疫吸附法检测白细胞介素-6(IL-6)、肿瘤坏死因子-α(TNF-α),免疫比浊法检测C反应蛋白(CRP)[7]。③治疗前后两组排卵、月经恢复,连续随访1年观察妊娠情况[8]。
1.4 统计学方法

2 结果
2.1 两组基本临床指标比较
对照组40例,年龄(30.2±1.2)岁(21~35岁),入组BMI (28.8±1.9)kg/m2;观察组40例,年龄(30.4±1.2)岁(21~36岁),入组BMI(28.4±2.1)kg/m2。两组无差异(P>0.05)。治疗后观察组卵巢体积、腰臀比、BMI均低于对照组(P<0.05)。见表1。
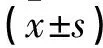
表1 两组治疗前后观察指标比较
2.2 两组性激素水平比较
观察组睾酮(T)、卵泡刺激素(FSH)、黄体生成素(LH)、雌二醇(E2)小于对照组(P<0.05)。见表2。
2.3 两组血糖、胰岛素指标比较
观察组FINS、2hPBG、FBG、HOMA-IR水平均小于对照组(P<0.05)。见表3。
2.4 两组炎症因素指标比较
观察组IL-6、TNF-α、CRP水平均小于对照组(P<0.05)。见表4。
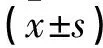
表2 两组治疗前后性激素指标对比
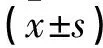
表3 两组治疗前后血糖、胰岛素指标对比
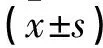
表4 两组治疗前后各炎症因子指标对比
2.5 两组临床效果指标比较
观察组排卵、月经恢复、妊娠率均高于对照组(P<0.05)。见表5。
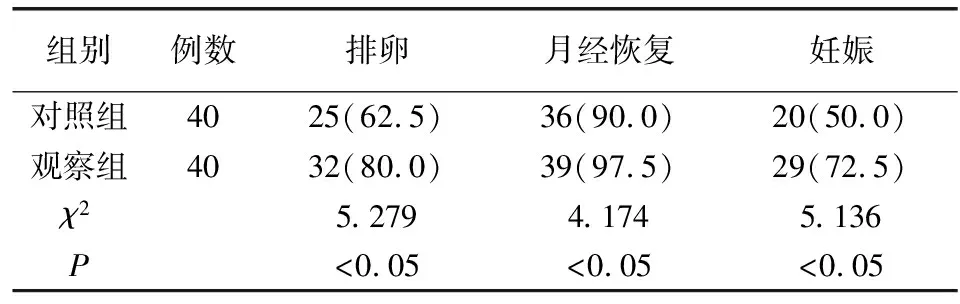
表5 两组治疗后临床效果指标对比[例(%)]
3 讨论
PCOS是临床多发疾病,症状较多,对女性身心健康、生殖健康、生活质量产生严重影响。当前临床对PCOS的发生机制还不很明确,多认为与生活方式、营养、遗传因素有关,没有特效治疗方案,多行对症治疗、健康管理,治疗目标为缓解患者症状、改善机体代谢、提高妊娠率、改善患者生活质量[9]。当前很多临床研究认为能量摄入过多、饮食结构异常在PCOS发生中发挥着重要作用,故对患者进行饮食干预非常重要,尤其是超重/肥胖PCOS患者会出现严重的胰岛素抵抗现象,导致机体代谢紊乱,激素水平异常,加重病情,体重管理非常重要[10]。以往临床也有对超重/肥胖PCOS患者进行体重管理,但是没有直接参与到饮食干预中,患者的饮食情况、依从性均无从知道,故最终的体重管理效果不理想,寻找更有效的体重管理非常重要[11]。
本研究结果显示,观察组体重管理治疗后卵巢体积、腰臀比、体质指数均低于对照组,说明在超重/肥胖PCOS患者中开展有效的体重管理可显著控制患者体质量。这是因为体重管理中,通过合理分配患者脂肪、蛋白质摄入量以提高患者饱腹感,进而减少食物摄入;同时患者处于饥饿状态可增强脂肪代谢,发挥减脂效果,体重管理效果较好[12]。
本研究结果显示,观察组体重管理治疗后性激素水平、血糖控制指标均低于对照组。说明对超重/肥胖PCOS患者有效体重管理可显著改善患者代谢及胰岛素抵抗情况。这是因为体重管理有效控制了患者碳水化合物摄入,减少了单糖吸收,降低了机体血糖水平进而降低胰岛素水平,抑制脂肪合成,调节脂代谢,改善内分泌情况[13]。因此,在超重/肥胖PCOS患者体重管理非常关键。
炎症反应在PCOS发生中起了重要作用。有报道[14]显示,PCOS患者的IL-6、TNF-α、CRP水平均高于正常人群,且超重/肥胖会加重炎症反应,长期处于炎症反应下会对生理、生殖产生不良影响。对超重/肥胖PCOS患者有效体重管理可减轻炎症反应,提高患者生育能力。本研究结果,观察组治疗后IL-6、TNF-α、CRP均小于对照组,说明超重/肥胖PCOS患者进行体重管理可改善炎症反应。这是因为体重管理可以减少患者碳水化合物摄入,减轻体重,改善胰岛素抵抗、身体代谢,进而降低炎症反应。
本研究观察组治疗后排卵、月经恢复、妊娠率大于对照组,说明有效体重管理可显著改善患者妊娠结局。这是因为体重管理可改善患者各项身体情况,使机体健康程度提高。体重管理在超重/肥胖PCOS患者中不仅可以改善患者体质量、机体代谢,还可以改善患者妊娠情况[15]。
综上所述,超重及肥胖PCOS患者在治疗期间进行体重管理效果较好,临床应予以重视并加强。

