反相HPLC法同时测定黄芩标准汤剂中黄芩苷、汉黄芩苷和黄芩素的含量
朱 琳,孙 红,陈素娥,刘亮亮
(山西卫生健康职业学院药学院,山西 晋中 030619)
黄芩为唇形科植物黄芩Scutellaria baicalensisGeorgi的干燥根[1],最早记载于《神农本草经》,是在我国临床上应用最广泛的中药材之一[2]。黄芩具有清热燥湿、泻火解毒、止血、安胎的功效。临床上常用于湿温、暑湿,胸闷呕恶,湿热痞满,泻痢,黄疸,肺热咳嗽,痈肿疮毒,胎动不安[1]。黄芩中含有多种活性成分,包括黄酮及黄酮苷类、多糖类、挥发油类等。其中,黄酮及黄酮苷为其主要成分[3-8]。黄芩的药理作用主要有抗菌、抗肿瘤、抑制心脑血管疾病、抗过敏、抗氧化、增强机体免疫、抗炎、抗癫痫等[9-14]。
中药标准汤剂是以中医学理论为指导、临床应用为基础,参照现代提取方法,经过标准化工艺制备而成的单味中药饮片水煎剂。中药饮片标准汤剂有助于保证临床用药的准确和剂量的统一,保障疗效的一致性[15-18]。目前,黄芩标准汤剂的相关研究较少,李琦等[19]制备了黄芩饮片标准汤剂,但仅以黄芩苷为指标进行质量评价,并未发现有多指标同时含量测定的相关报道。因此本研究收集了10批不同产地的黄芩药材,以《医疗机构中药煎药室管理规范》为依据,将其制备成标准汤剂,建立了黄芩标准汤剂中3种成分的含量测定方法,以期为黄芩标准汤剂的质量控制和规范其临床用药提供参考。
1 仪器与试药
1.1 试药10批黄芩药材由山西某药企提供(批号分别为TA190092001,TA190082001,TA190088001,TA190090001,TA190083001,TA190085001,TA190084001,TA190089001,TA190087001,TA190086001),并经山西卫生健康职业学院生药教研室杨翠玲副教授鉴定为黄芩Scutellaria baicalensis Georgi的干燥根。
1.2 试剂 黄芩苷(纯度为97.9%,批号:110715-201821)、汉黄芩苷(纯度97.9%,批号:112002-201702)、黄芩素(纯度为97.9%,批号:111595-201808)(中国食品药品检定研究院);甲醇和乙腈为色谱纯(天津市康科德科技有限公司);其他试剂为分析纯[利安隆博华(天津)医药化学有限公司]。
1.3 主要仪器Agilent 1200液相色谱仪(美国安捷伦科技有限公司);KQ-250DB数控超声波清洗器(昆山市超声仪器有限公司);SQP电子天平(十万分之一,德国赛多利斯公司)。
2 方法与结果
2.1 色谱条件Agilent ZORBAX XDB-C18色谱柱(4.6 mm×150 mm,5 μm);流动相为甲醇(A)-0.1%磷酸水(B),梯度洗脱程序如下:0~5min,17%~50%A;5~15min,50%A;15~20min,50%~84%A;流速为1 mL/min;检测波长为270 nm;柱温为30℃;进样量为10 μL。
2.2 混合对照品溶液的制备 取黄芩苷、汉黄芩苷、黄芩素各5 mg,精密称定,分别置5、10、5 mL量瓶中,甲醇定容,制成浓度分别为1.012、0.503 1、0.998 mg/mL的对照品储备液。精密量取黄芩苷1.00 mL、汉黄芩苷0.67 mL、黄芩素0.25 mL,置于5 mL量瓶中,甲醇定容,得到黄芩苷、汉黄芩苷、黄芩素浓度分别为202.40、67.40、49.90 μg/mL的混合对照品溶液。
2.3 供试品溶液的制备 称取黄芩标准汤剂的粉末(过40目筛)约0.3 g,置100 mL具塞锥形瓶中,加70%甲醇40 mL,称定质量,超声处理(250 W,50 kHz)30 min,放冷,再称定质量,用70%甲醇补足质量,取1mL上清液至10 mL量瓶,甲醇定容至刻度,0.22 μm微孔滤膜过滤,即得。
2.4 方法学考察
2.4.1 专属性 分别吸取空白溶剂、混合对照品溶液和供试品溶液各10 μL注于高效液相色谱仪,结果供试品溶液色谱图中的积分峰与混合对照品溶液色谱图中的积分峰一一对应,空白溶剂色谱图中没有出现相应保留时间的峰,表明该方法的专属性良好。(见图1)
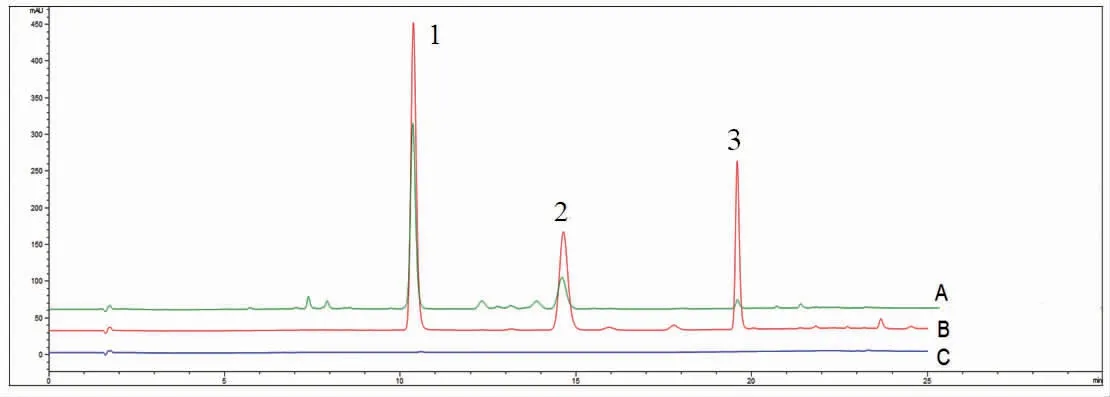
图1 HPLC色谱图
2.4.2 线性关系考察 精密吸取“2.2”项下的混合对照品溶液0.25、2、4、6、8 mL至10 mL量瓶中,甲醇稀释,得到一系列浓度的混标溶液(黄芩苷浓度为5.06、40.50、81.00、121.40、161.90 μg/mL;汉黄芩苷浓度为1.685、13.480、26.960、40.440、53.920 μg/mL;黄芩素浓度为1.248、10.000、19.960、29.940、39.920 μg/mL)。分别精密吸取以上6个浓度的混合对照品溶液各10 μL,注入高效液相色谱仪,以各色谱峰峰面积积分值(y)对浓度(x,μg/mL)进行线性回归,黄芩苷、汉黄芩苷、黄芩素的标准曲线方程、线性范围、相关系数(r)见表1。由表中数据可以看出,各指标成分线性关系良好。

表1 指标成分的回归方程、线性范围、检测限和定量限
2.4.3 定量限与检测限 把黄芩苷、汉黄芩苷、黄芩素标准溶液均先稀释到1 μg/mL,再分别按照“2.1”项下色谱条件进样,计算信噪比,再按照信噪比来进一步计算稀释倍数,直到找到信噪比约为3和10的两个浓度,即可确定检测限和定量限。(见表1)
2.4.4 精密度试验
2.4.4.1 仪器精密度 精密吸取上述黄芩苷浓度为40.50 μg/mL混合对照品溶液10 μL,按“2.1”项下色谱条件,分别连续进样6次,检测各指标成分所对应的色谱峰峰面积,黄芩苷、汉黄芩苷、黄芩素对应色谱峰峰面积RSD分别为0.6%、0.4%、0.4%,表明仪器精密度良好。
2.4.4.2 日间精密度 精密吸取混合对照品溶液10 μL,按“2.1”项下色谱条件,连续进样3 d,每天进样3针,检测各指标成分所对应的色谱峰峰面积,黄芩苷、汉黄芩苷、黄芩素对应色谱峰峰面积RSD分别为4.6%、3.9%、3.9%,均<5%,表明方法日间精密度良好。
2.4.5 稳定性试验 取同一批次的黄芩标准汤剂,按照“2.3”项下操作制备供试品溶液,按“2.1”项下色谱条件下分别在0、2、4、8、12、24 h进样测定,测得黄芩苷、汉黄芩苷、黄芩素的峰面积RSD分别为1.9%、2.1%、2.3%。表明供试品溶液在24 h内稳定性良好。
2.4.6 重复性试验 取同一批黄芩标准汤剂,按“2.3”项下供试品溶液制备方法平行制备6份,按“2.1”项下色谱条件下进样分析,测得黄芩苷、汉黄芩苷、黄芩素的峰面积RSD分别为2.2%、2.1%、4.8%,表明本方法重复性较好。
2.4.7 加样回收率试验 按“2.3”项下的供试品溶液制备方法制得供试品溶液,分别准确加入低、中、高浓度的黄芩苷、黄芩素、汉黄芩素对照品适量,每一浓度平行操作3份,计算平均回收率,结果表明该方法准确度良好。(见表2)
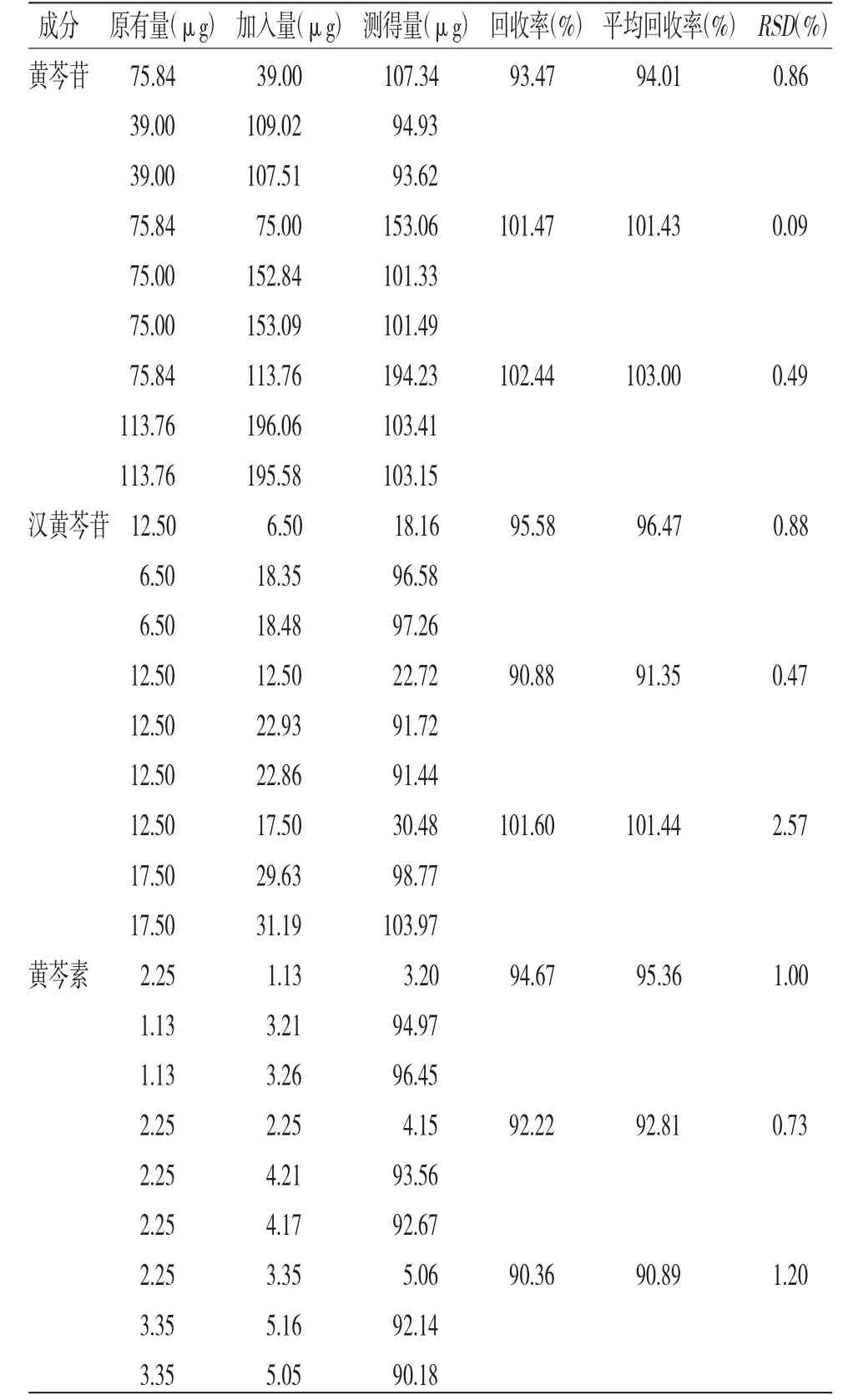
表2 黄芩苷、汉黄芩苷和黄芩素的回收率
2.5 含量测定 按“2.3”项下的供试品溶液制备方法提取黄芩标准汤剂,按“2.1”项下的色谱条件进样,各指标成分的含量见表3。

表3 10批黄芩标准汤剂的含量(%)
3 结果与讨论
3.1 检测波长的选择 供试品溶液在紫外范围(210~380 nm扫描来确定λmax。结果表明,黄芩苷的最大吸收波长为280 nm,汉黄芩苷和黄芩素的最大吸收波长为270 nm,考虑到汉黄芩苷和黄芩素的含量相对较低,黄芩苷在270 nm下响应也较高,因此把270 nm作为最佳检测波长。(见图2)
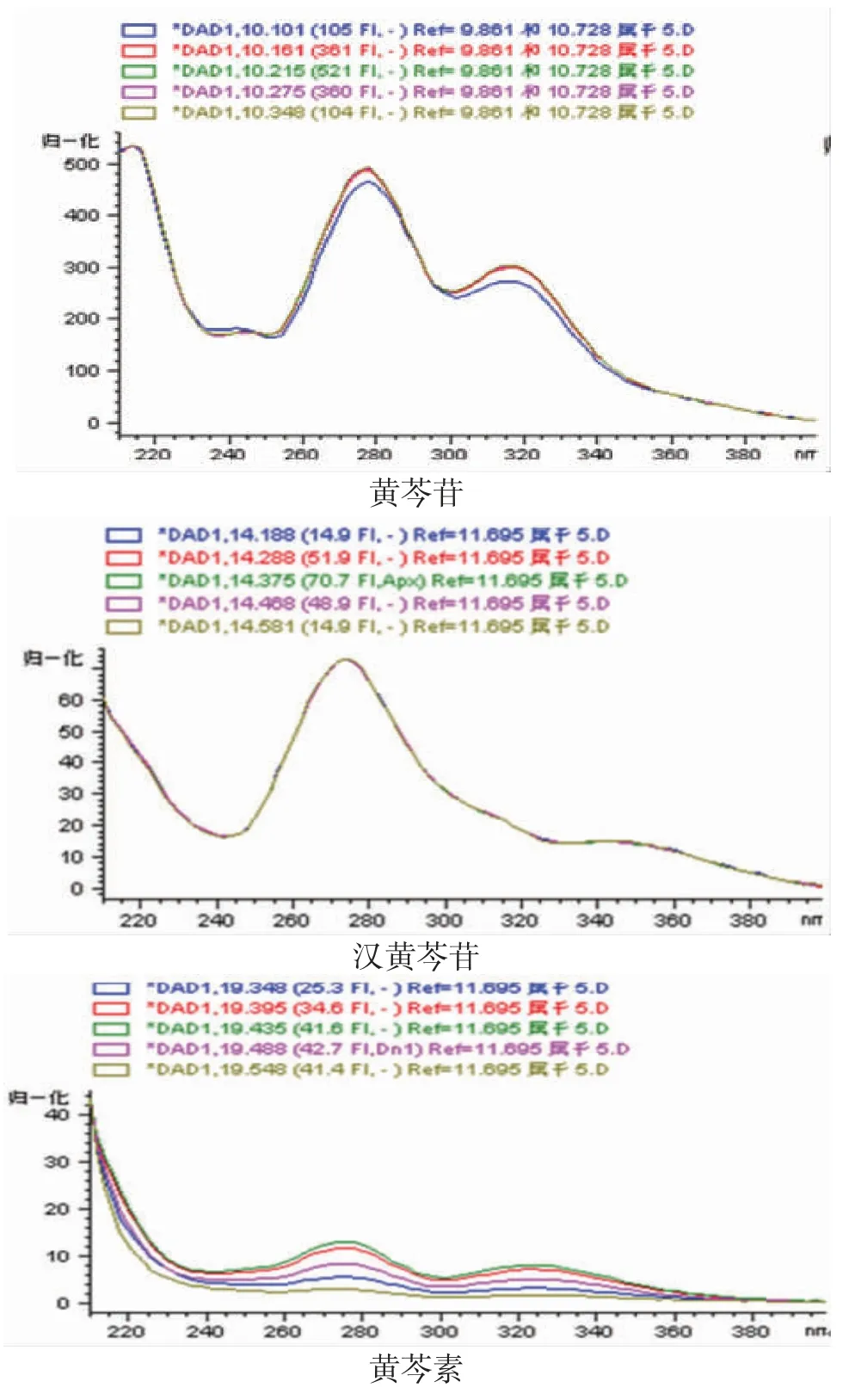
图2 各指标成分的最大吸收波长光谱图
3.2 流动相的选择 在流动相考察中发现,以乙腈-水体系作为流动相时基线漂移严重,而甲醇-水作为流动相时基线平稳。为改善峰形,减少拖尾,分别考察了水相中磷酸浓度0.05%、0.1%、0.2%时,流动相pH值对色谱参数的影响。结果表明,水相中磷酸浓度为0.1%时色谱基线较好,指标成分的对称因子接近1,峰形较好,分离度较高,理论塔板数较高,因此选择磷酸的浓度为0.1%。
此外,分别对流速、进样量和柱温进行了单因素考察,结果发现,当流速为1 mL/min,进样量为10 μL,柱温为30℃时,分离度最大,峰形最好。
3.3 提取溶剂的选择 本研究分别采用90%甲醇、80%甲醇、70%甲醇、70%乙醇、60%甲醇5种不同的溶剂对黄芩标准汤剂进行提取,通过比较指标成分的含量,发现70%甲醇提取时提取效率最高。然后进一步测定了70%甲醇提取的样品的残渣,发现残渣中黄芩苷的含量为0.17%,汉黄芩苷的含量为0.036%,黄芩素的含量为0.004 4%,因此可视为70%甲醇提取时提取比较完全。
3.4 提取体积的选择 按“2.2”项下供试品制备方法,以70%甲醇为提取溶剂,分别考察在30、40、50 mL 3种不同体积下黄芩苷、汉黄芩苷、黄芩素的提取效果。通过比较指标成分的含量,发现溶剂体积为40、50 mL时指标成分含量较大,但相差不多,因此从节约溶剂的角度考虑,选择溶剂体积为40 mL。
3.5 提取方法的考察 按“2.2”项下供试品制备方法,以70%甲醇为提取溶剂,分别考察超声提取和回流提取时黄芩苷、汉黄芩苷、黄芩素的提取效果,结果表明,超声的提取效率与回流提取差别不大,由于回流提取比较复杂、耗费时间长,因此选择超声提取。
4 结 论
本研究建立了同时测定黄芩标准汤剂中3种指标成分(黄芩苷、汉黄芩苷、黄芩素)含量的HPLC方法,该方法简单、高效,为黄芩标准汤剂的质量控制提供了一定的参考。由含量测定结果分析可知,10批标准汤剂中3种成分的RSD分别为7.20%、5.85%、28.82%,含量存在一定差异,这可能与药材本身含量的差异有关。不同产地的地质、水源及气候条件可能导致黄芩药材的含量不同,从而导致标准汤剂中指标成分的含量有所差异。因此,在实际生产中,应当注意固定饮片的来源,以保证标准汤剂含量的均一性。

