牛肉中凝固酶阳性葡萄球菌定量检测FAPAS的能力验证结果与分析
杨丹婷 陈丹霞 苏妙贞 刘单单 周露
(广东省食品检验所 广东广州 510435)
1 前言
葡萄球菌属(Staphylococcusspp.)在自然界中分布广泛,是类触媒试验阳性的革兰氏阳性球菌,包括金黄色葡萄球菌(S.aureus)、金黄色葡萄球菌金黄色亚种(subsp.aureus)、金黄色葡萄球菌厌氧亚种(subsp.anaerobius)、表皮葡萄球菌(S.epidermidis)、施氏葡萄球菌(subsp.schleiferi)、松鼠葡萄球菌(S.sciuri)、松鼠葡萄球菌松鼠亚种(subsp.sciuri)、松鼠葡萄球菌肉亚种(subsp.carnaticus)、松鼠葡萄球菌啮齿亚种 (subsp.rodentium)、中间葡萄球菌(S.intermedius)海豚葡萄球菌(S.delphini)、腐生葡萄球菌(S.saprophyticus)、里昂葡萄球菌(S.lugdunensis)等66个种和亚种[1]。
对公众健康有重要潜在威胁的微生物群是凝固酶阳性的耐药葡萄球菌菌株,特别是耐甲氧西林的金黄色葡萄球菌(MRSA)和假中间菌(MRSP),其通常是动物源性的。其中,金黄色葡萄球菌一直被认为是全世界食物中毒的最重要因素之一,也是最重要的致病葡萄球菌,作为第二大凝固酶阳性分离菌群(12%),尽管其对人体有特殊的适应性(如其有1个对人血红蛋白有高亲和力的受体),但也能在家畜和野生动物中定居或引起感染,主要会引起局部组织的化脓性感染、菌血症等[2-3]。
为确保检验检测实验室的能力,CNAS-CL01《检测和校准实验室能力认可准则》中提出实验室可通过能力验证的手段来确认人员能力及确保实验结果的有效性[4]。能力验证是利用实验室间比对,按照预先制定的准则评价参加者的能力[5]。通过开展能力验证,能够发现实验室存在的问题,监控实验室的运行状态,提高实验室检测能力和检测水平,确保检测出证的质量。
英国FAPAS分析实验室能力验证(Food Analysis Performance Assessment Scheme)是目前具备组织能力验证项目资格的机构之一,专门从事食品检测分析方面的能力评估体系,通过实验室间测试结果的比对来判定实验室能力的合格评定活动。FAPAS可以开展包括理化检测、微生物检测、转基因检测以及水检测等项目,是目前国际食品领域权威的能力验证提供者,也是全球食品领域最大、最全面的分析化学水平测试评估计划[6]。通过参加国际能力验证,与国际检测同行交流检测结果,有助于提升检测能力自信,且对于持续提高实验室检测水平和质量控制具有重要意义。
本实验室参加了2019年7月FAPAS组织的凝固酶阳性葡萄球菌定量检测实验,以FAPAS提供的作业指导书制备样品[7],检验过程参考GB 4789.10-2016《食品安全国家标准 食品微生物学检验 金黄色葡萄球菌检验》[8]。本文对实验结果进行分析与讨论,以期为相关人员提供参考。
2 材料与方法
2.1 试剂与仪器
生物安全柜(新加坡ESCO公司);生化培养箱(上海一恒科学仪器有限公司);显微镜(卡尔蔡司);VITEK 2 COMPACT自动微生物快速检测分析系统(法国梅里埃);VITEK MS全自动快速微生物质谱鉴定系统(法国梅里埃)。
磷酸缓冲盐溶液(PBS);缓冲蛋白胨水(BPW);Baird-Parker琼脂平板(BP板);金黄色葡萄球菌显色培养基(金显板);金黄色葡萄球菌测试片(3M测试片);金黄色葡萄球菌反应确认片(3M确认片);脑心浸液肉汤(BHI);冻干血浆;营养琼脂(NA板);革兰氏染色液;VITEK革兰氏阳性细菌鉴定卡(GP卡)。
质控菌:表皮葡萄球菌FSCC 223011;金黄色葡萄球菌ATCC 6538。
2.2 试验方法
2.2.1 样品处理
水化过程:向样品管中加入10 mL缓冲蛋白胨水,将样品管轻轻倒转几次,并确保彻底冲洗样品管,之后在室温下放置30 min,相当于一个10 g的原始样品。
2.2.2 样品稀释
将水化后的10 g样品全部转移至匀质袋中,之后用90 mL PBS冲洗样品管,并转移至同个匀质袋中,充分混匀制成10-1,依次进行10倍稀释至10-6。
2.2.3 样品接种
平板法:每个稀释度分别吸取0.3 mL、0.3 mL、0.4 mL至BP板和金显板,涂布均匀;纸片法:每个稀释度吸取1 mL样品匀液于3M测试片中央处,使用压板将样品匀液均匀覆盖于培养面积上,每个稀释度做2个平行,等样品吸收完毕后培养。
2.2.4 培养观察
BP板于36℃培养48 h;金显板和3M测试片于36℃培养24 h。
(1)若BP板观察到可疑菌落,则计数并进行下一步确证实验,即革兰氏染色及血浆凝固酶实验。挑取可疑菌落数在20~200 CFU间的稀释度平板进行确证。共挑取5个以上可疑菌落,接种至BHI,36℃培养24 h后,进行血浆凝固酶实验。同时用表皮葡萄球菌作阴性对照,金黄色葡萄球菌6538作阳性对照。计算过程参考GB 4789.10-2016。
(2)金显板根据说明书判断可疑菌落形态,计数。
(3)若3M测试片观察到可疑菌,则需使用反应确认片确定,即掀开测试片上层膜,将确认片置入,小心压紧,注意不能残留气泡,36℃继续培养1~3 h后观察,计数。
2.2.5 仪器鉴定
在BP板和金显板中各挑取5个可疑菌落分纯于NA板,36℃培养24h,取新鲜培养的菌落于VITEK 2 COMPACT和VITEK MS进行鉴定。
2.2.6 z值的计算
该样品的测试结果采用“z-比分数”评价,z-比分数计算如下:
根据能力验证结果报告书:

式中:x—测试人所提交的测试结果的log10值;
x∂—指定值;根据能力验证结果报告书为3.73;
σp—标准差;根据能力验证结果报告书为0.25。
当|z|≤2,测试结果满意;当2<|z|≤3,测试结果可疑;当|z|>3,测试结果不满意[9]。
3 结果与分析
BP板中所有菌落形态相同:圆形,表面光滑、凸起、湿润,菌落直径为2~3 mm,黑色,有光泽,周围绕以不透明圈,其外有清晰带,见图1;金显板中所有菌落形态相同:圆形紫红色菌落,见图2;3M测试片中菌落均为紫红色,贴确认纸片后菌落周围出现粉红环,见图3;将BP板和金显板计数的平板中各挑取5个菌落进行革兰氏染色,镜检结果均为革兰氏阳性葡萄球菌,见图4;10个验证菌凝固酶实验,结果均为阳性,同时阳性对照金黄色葡萄球菌ATCC 6538:凝固酶实验阳性,阴性对照FSCC 223011:凝固酶实验阴性,见图5。说明实验结果可靠。其VITEK 2 COMPACT和VITEK MS结果均为金黄色葡萄球菌。说明用以上方法进行凝固酶阳性葡萄球菌实验计数结果可靠,计数结果见表1。

图1 BP板上菌落的形态

图2 金显板上菌落的形态

图3 3M测试片上菌落的形态(贴确认片前后)

图4 革兰氏染色镜检结果

图5 血浆凝固酶实验及阴阳性对照
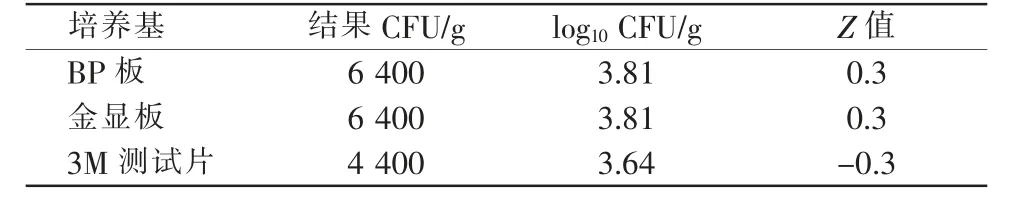
表1 3种培养基的计数结果
本次能力验证最终通报的结果为3.73 log10CFU/g,本实验室最终上报结果为6 400 CFU/g,log106400=3.81 CFU/g,Z=0.3<2,验证结果为满意。
4 讨论
本次FAPAS能力验证取得满意结果。通过参加本次能力验证,提高了本实验室人员对凝固酶阳性菌的认识水平及检测能力,对实验室的发展有促进作用,同时满意的能力验证结果可作为本实验室持续保持技术能力的证明。
本实验需要注意的是:实验前应严格按照FAPAS作业指导书对样品进行处理和活化,活化时间应为30 min;平板法所需的培养基应在实验前提前烘干,方便涂布过程中菌液的快速吸收。
本实验过程用不同培养基比对及阴阳性对照进行质量控制,确保检测结果的准确性,但仍有可以改进的部分:本次能力验证要求做凝固酶阳性葡萄球菌计数,根据GB4789.10—2016用BP平板、金显板及3M测试片都是检验金黄色葡萄球菌的的培养基,有可能存在漏检其他凝固酶阳性葡萄球菌的情况。由于这次能力验证样品分别在上述3种培养基中只有1种菌落形态,且计数结果平行,后经仪器鉴定为金黄色葡萄球菌,故认为样品中只添加了金黄色葡萄球菌,所以直接上报BP平板的结果,最终结果满
意。BP板是食品安全国家标准、FDA、OSO等常用培养基,金黄色葡萄球菌或其他葡萄球菌会在BP板产生相近特征[10]。GB/T 23743-2009《饲料中凝固酶阳性葡萄球菌的微生物学检验Baird-parker琼脂培养基计数法》中也采用BP平板对凝固酶阳性葡萄球菌进行选择培养[11]。除了本实验所用的3种培养基外,用于血浆凝固酶阳性葡萄球菌的分离的培养基还有兔血浆纤维蛋白原琼脂培养基(RPF),阳性菌落在RPF中为灰黑色菌落,外围有浑浊沉淀环[12],故可用RPF进行凝固酶阳性实验。另外也可以用分子生物学手段LAMP法检测食品中凝固酶阳性葡萄球菌,该方法具有灵敏度高、可操作性强的优点[13]。

