干扰TP53INP2抑制牛成肌细胞分化
杜嘉伟,杜鑫泽,杨昕冉,宋贵兵,赵慧,昝林森,2,王洪宝,2
干扰抑制牛成肌细胞分化
杜嘉伟1,杜鑫泽1,杨昕冉1,宋贵兵1,赵慧1,昝林森1,2,王洪宝1,2
1西北农林科技大学动物科技学院,陕西杨凌 712100;2国家肉牛改良中心,陕西杨凌 712100
肌肉可以维持哺乳动物运动功能并调节机体代谢,它的数量和分布对肉质有重要影响,骨骼肌的生长发育及其遗传特性在很大程度上影响甚至决定家畜的产肉量和肉品质,研究骨骼肌的生长发育具有重要意义。对自噬的调控作用以及对前体脂肪细胞分化的调控机制已有研究,而对于牛成肌细胞分化的影响尚未报道。【】探究TP53INP2对秦川牛成肌细胞分化的影响,为肉牛肉用性状分子育种工作提供理论依据。利用实时荧光定量PCR(real-time fluorescence quantitative PCR,RT-qPCR)技术检测了在24月龄秦川牛不同组织中的表达特性,同时分析了其在体外培养的牛骨骼肌成肌细胞不同分化时期的表达规律;合成基因siRNA并转染秦川牛成肌细胞,转染后12h进行诱导分化,观察成肌细胞表型变化,并利用RT-qPCR技术和Western Blot技术分别检测其在诱导分化第四天时分化标志基因和蛋白的表达情况。1.RT-qPCR结果显示,在成年秦川牛背最长肌组织中表达量最高,在小肠组织中表达量最低。在成年牛心脏、肝脏、肾脏、网胃、瘤胃中表达量较高,在其余组织中表达量较低(与背最长肌相比)。2.随着成肌细胞的分化,该基因在第0—4天表达量呈上升趋势且在第4天达到峰值,随后表达量呈下降趋势。3.在成肌细胞中干扰后,试验组肌管的数量和长度均显著低于对照组。4.干扰并提取细胞总RNA,RT-qPCR结果显示,成肌细胞分化标志基因肌细胞生成素()和肌球重链蛋白3()相对于对照组表达量显著降低。5.干扰并提取细胞总蛋白,Western Blot结果显示,试验组MYOG、MYH3、MYOD的蛋白表达量均降低且与对照组相比差异极显著。干扰对牛成肌细胞的分化具有抑制作用,提示该基因可能对秦川牛肌肉组织的生长发育具有重要的调控作用,可对其进行深入的功能研究以期用于肉牛的分子育种实践中。
;分化成肌细胞;秦川牛
0 引言
【研究意义】骨骼肌是人类最丰富的组织,约占总体重的50%,参与许多重要功能[1]。随着人们生活质量的提高,牛肉作为重要的肉食品,优质、高档牛肉供不应求[2-3]。肌肉的数量和分布对肉质有重要影响[4-5],因此研究肌肉再生和分化的调控机制对畜牧业具有重要意义。另外,研究骨骼肌的生长发育对于提高家畜的产肉性能和改善肉质品质也具有重要意义。【前人研究进展】肿瘤蛋白p53诱导核蛋白(TP53INP)家族包括TP53INP1和TP53INP2两个蛋白[6]。目前研究的较多且较为清楚,是在19世纪90年代末由3个不同的独立实验室发现的,作为p53靶基因在癌症研究领域成为了研究热点[7]。是的重要旁系同源物,又称为DOR或PINH[8]。该基因编码的蛋白质可直接作用于一个重要的自噬相关蛋白LC3,该蛋白的主要功能为促进自噬体的形成,主要在细胞质中起作用[9],但XU等研究发现促进核仁的rRNA的合成,协助核仁的合成代谢并刺激核仁的分解代谢[10]。TP53INP2在细胞核内可作为核受体,如哺乳动物的糖皮质激素受体(glucocorticoid receptor,GR)、维生素D受体(vitaminDreceptor,VDR)和过氧化物酶体增殖物激活受体γ(peroxisome proliferator- activatedreceptorγ,PPARγ)等的转录辅激活因子,表明TP53INP2在细胞核内主要发挥转录辅激活因子的作用[11-12]。用饥饿培养基或雷帕霉素( rapamycin)诱导细胞自噬,TP53INP2会迅速从细胞核移位至细胞质中,与自噬标志蛋白相互作用[11,13-15]。许多研究证实,自噬参与脂肪细胞的分化,并在分化早期起着至关重要的作用[16-17]。ROMERO等通过在3T3-L1前体脂肪细胞上的研究表明对于前体脂肪细胞分化是负向调控的[16]。最近的一些研究表明TP53INP2在细胞凋亡信号通路上发挥作用,它可以正向调控细胞凋亡[15,18-19]。【本研究切入点】对自噬的调控作用以及对前体脂肪细胞分化的调控机制已有研究,而对于牛成肌细胞分化的影响尚未报道。同时本研究通过对24月龄秦川牛不同组织进行qRT-PCR,发现基因在背最长肌组织中的表达量最高,因此决定研究干扰对秦川牛成肌细胞分化的作用。【拟解决的关键问题】本研究通过siRNA转染秦川牛成肌细胞,确定干扰对秦川牛成肌细胞分化的作用,为秦川牛的肉质性状改良及良种选育提供一定的理论基础。
1 材料与方法
本试验于2020年上半年在陕西杨凌西北农林科技大学国家肉牛改良中心完成。
1.1 试验动物采样
样本均来自西北农林科技大学国家肉牛改良中心的肉牛良种繁育场,将3头成年秦川牛(24月龄)作为研究对象,屠宰后取心脏、肝脏、脾脏、肺脏、肾脏、大肠、小肠、瘤胃、网胃、皱胃、肾周脂肪、皮下脂肪、背最长肌等组织,液氮冷冻后转存-80℃冰箱长期保存。新生牛背最长肌组织用于后续成肌细胞的分离培养。
1.2 主要试验耗材与仪器设备
TB GreenTMPremix EX TaqTMⅡ(TaKaRa),DEPC水,电泳液(Solarbio),电解液(Solarbio),10X TBST Buffer(Sangon Biotech),PBS缓冲液(HyClone),QuickBlock Western一抗稀释液(Beyotime),QuickBlock Western二抗稀释液(Beyotime),QuickBlock Western封闭液(Beyotime),无水乙醇(西陇化工),三氯甲烷(西陇化工),异丙醇(范德生物),RIPA(Solarbio),PMSF(Solarbio),反转录试剂盒(TaKaRa),Trizol(TaKaRa),胎牛血清(PAN),F-12/DMEM(Hyclone),马血清(Hyclone),Lipofectamine 3000(ThermoFisher),opti(Hyclone),蛋白上样缓冲液(Solarbio)。
转膜仪(BIO-RAD),电泳槽(BIO-RAD),4℃离心机(Eppendorf),实时荧光定量仪(BIO-RAD),QL-901漩涡震荡仪,37℃恒温培养箱(Thermo Fisher),荧光倒置显微镜(Olympics),酶标仪(Tecan Austria GmbH 5082)。
1.3 试验方法
1.3.1 秦川牛各组织总RNA的提取和cDNA的合成 采用传统的Trizol法提取各组织的总RNA。提取过程为:取少量组织样于研钵中,加入液氮反复研磨;加入500 μL Trizol,继续研磨混匀后转移至1.5 mL离心管中,室温放置15 min后4℃、12 000 r/min离心15 min;取上清,按Tizol总体积1/5的量加入氯仿,剧烈振荡15 s后室温静置5 min;4℃、12 000 r/min离心15 min;取上清加入等体积的异丙醇充分混匀后室温静置10 min,4℃、12 000 r/min离心10 min;弃上清,加入1 mL 4℃预冷的体积分数75%乙醇,4℃、8 000 r/min离心5 min;室温干燥2—5 min;用适量RNase-free水溶解RNA,测定浓度后于-80℃保存备用。使用酶标仪检测所提取总RNA的纯度及浓度,并使用1%琼脂糖凝胶电泳检测RNA的完整性。以提取的RNA为模板,按照PrimeScript RT Reagent Kit with gDNA Eraser试剂盒操作步骤进行cDNA的合成。
1.3.2 秦川牛成肌细胞培养,siRNA的合成及转染 秦川牛成肌细胞的分离培养参见文献[20]。将秦川牛成肌细胞复苏后采用生长培养基(含体积分数20%胎牛血清和体积分数1%双抗的F-12/DMEM)培养。针对TP53INP2 mRNA序列,由广州锐博生物有限公司合设计成siRNA及阴性对照。待细胞生长密度达到80%时进行转染,具体操作步骤参照Lipofectamine 3000试剂盒说明书,复合物1:125 μl opti+5 μl(si- TP53INP2/si-NC)孵育5 min,复合物2:125 μl opti+ 3.75 μl lip3000孵育5 min,之后将复合物2加入复合物1中充分混匀后室温孵育5 min。用PBS清洗细胞两遍后,加入含有复合物1、2混合物的生长培养基,培养12 h后,更换为分化培养基(含体积分数2%马血清和体积分数1%双抗的F-12/DMEM)培养,每2 d更换一次培养基,于分化第0、2、4、6、8、10天取细胞样品,采用Trizol法提取RNA[21]。
1.3.3 cDNA样品准备和RT-qPCR 已提取的RNA根据试剂盒反转录为cDNA。根据GenBank已公布的牛序列,利用Primer Premier 5.0软件设计特异实时荧光定量引物,送交西安擎科有限公司合成。以作为内参,利用TB GreenTMPremix EX TaqTMⅡ进行实时荧光定量PCR反应。PCR反应体系15 μL:TB Rreen Ⅱ 7.5 μL,cDNA 1.2 μL,上下游引物各0.3 μL,加RNase free H2O补足体系,技术重复3次。于Bio-Rad荧光定量PCR仪上进行反应,反应条件:95℃30 s,95℃5 s,60℃30 s,72℃30 s,40个循环;采集熔解曲线荧光信号和达到峰值循环数Ct值。采用2-△△Ct法对数据进行分析,具体公式为△Ct1=待测组目标基因Ctmean-待测组Ctmean;△Ct2=基测组目标基因Ctmean-基准组Ctmean;RQ= 2-(△Ct1-△Ct2)=2-△△Ct[22]。另外,本研究中所有实时荧光定量PCR结果均以作为内参基因,所有实时荧光定量PCR引物序列见表1。
1.3.4 提取细胞总蛋白 吸出细胞培养板中所有培养基,并用PBS轻柔的清洗细胞2—3次;6孔板每孔按RIPA(蛋白裂解液)﹕PMSF(蛋白酶抑制剂)=100﹕1的比例加入150 μL混合液;冰上裂解30 min,于冰上用细胞刮刮细胞培养板底部,使细胞充分裂解;将裂解液转移至1.5 mL离心管中,4℃,12 000×离心10 min,离心后将上清液转移至另一新的离心管中,按照上清液﹕上样缓冲液(5X)=4﹕1的比例加入蛋白上样缓冲液;煮沸10 min,保存于-80℃。
1.3.5 Western Blot 配制 12% 的分离胶,用乙醇压平液面,室温静置至少 30 min;待分离胶凝固后,弃去上层的乙醇,配制浓度为 5% 的浓缩胶,混合后加入两玻璃板中间,迅速插入梳子;将胶板装入垂直板电泳槽,拔掉梳子灌入1×Tris-Gly电泳缓冲液,淹没中间室,并漫过点样孔;上样(通常上样蛋白量为 10—20 μg),80 V 电压电泳,待样品进入分离胶后,调电压至 120 V,待样品中溴酚蓝迁移至凝胶最下端时,电泳完毕;将胶板从电泳槽中拆下,小心取出凝胶,装配转移装置,提前用甲醛浸泡1—2 min 激活PVDF膜并浸泡厚滤纸;使用Bio-Rad公司的转膜装置进行转膜;转膜结束后,放入TBST溶液洗10 min;将膜置于封闭液中,摇床上室温封闭2 h,封闭结束后TBST 溶液漂洗膜 3 次,10 min/次;将一抗用一抗稀释剂稀释至相应比例:GAPDH(1﹕5000),MYOD(1﹕1000),MYOG(1﹕200),MYH3(1﹕500)之后在 4℃条件下用一抗过夜孵育PVDF 膜;回收抗体,TBST 溶液漂洗膜 3 次,10 min/次;将二抗用二抗稀释剂稀释至相应比例,室温下摇床上避光孵育膜2 h;TBST 溶液漂洗膜 3 次,10 min/次;化学发光显影。
1.3.6 统计分析在不同组织中以及肌细胞不同分化时期的表达差异采用单因素方差分析进行计算,多重比较以表达量最低组织或诱导分化第0天为对照,使用LSD方法进行。在成年牛特定组织中的表达差异分析用t检验进行计算,以<0.05表示差异显著性判断标准。本研究数据采用GraphPad Prism6软件进行统计分析并作图。
2 结果
2.1 成年牛不同组织TP53INP2相对表达量的检测
由图1可知,在各组织中广泛表达,但表达量不尽相同。其中在小肠中表达最低,在小肠、脾脏、肾周脂肪、大肠、肺脏、皱胃、皮下脂肪等组织中的整体表达水平较低(与背最长肌相比);在网胃、肾脏、瘤胃、肝脏、心脏等组织中整体表达水平较高;另外,该基因在背最长肌中表达量最高且极显著地高于其他组织。
2.2 TP53INP2在成肌细胞不同分化天数的表达规律的测定
在成肌细胞诱导分化不同天数的相对表达量是以第0天作为标准计算得出的结果。由图2可知,从整体趋势来看,的表达量先上升后下降,其表达量在第4天达到最高。
2.3 TP53INP2 siRNA干扰效率的检测
如图3所示,在siRNA转染牛成肌细胞后的第4天,通过qRT-PCR检测其干扰效率,测得干扰效率约为84%,可用于后续试验研究。
2.4 干扰TP53INP2基因后对成肌细胞分化的影响
如图4所示,在干扰后处理组和对照组的分化表型差异极显著,处理组肌管明显少于且短于对照组;图5显示当干扰后,处理组和的相对表达量极显著低于对照组,而处理组的相对表达量低于对照组,但差异不显著;图6、图7所示处理组中的蛋白表达量均极显著低于对照组。
3 讨论
3.1 TP53INP2在成年牛不同组织的相对表达量
肌肉的发育离不开肌细胞的增殖分化,而增殖分化的过程是极其复杂的[23]。成肌细胞具有增殖和分化的能力,但融合成肌管之后便失去增殖能力,转而进行分化[24]。近些年来,已有的研究报道表明,TP53INP2可以作为骨骼肌基底自噬的激活因子,它被认为是骨骼肌质量的负调控因子,其蛋白可以通过自噬调节肌肉质量其负调控肌肉质量的这一功能主要是由于能激活成肌细胞中自噬这一过程[1,12]。本试验采用qRT-PCR技术检测并获得了在成年秦川牛不同组织中的表达模式及该基因在成肌细胞诱导分化不同天数的表达规律,研究结果初步揭示了的表达特性及规律。在成年秦川牛各组织中,在背最长肌中的表达量极显著高于其他组织,这说明其对牛肌肉组织的生长发育可能会具有重要的调控作用。
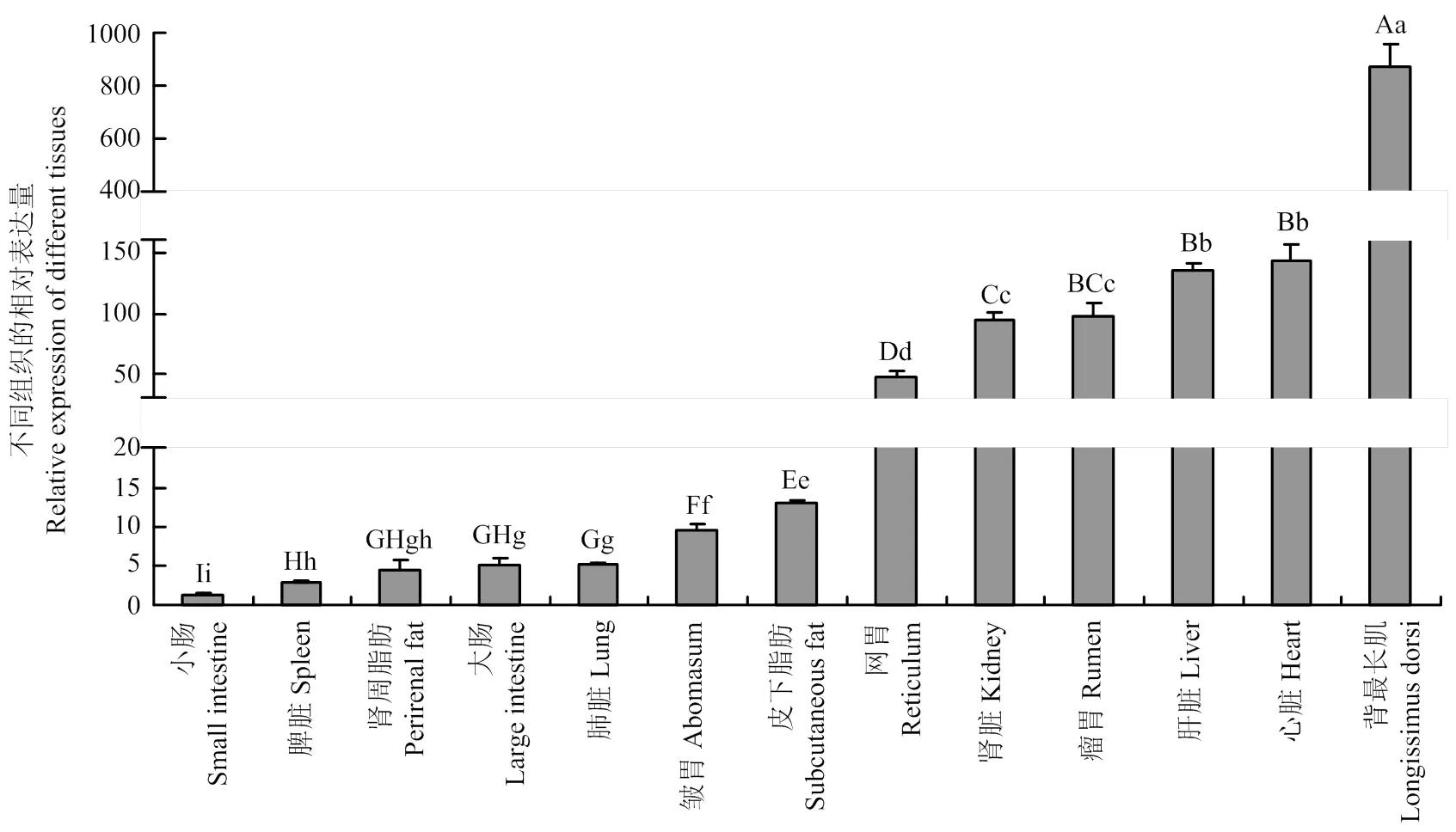
标不同小写字母表示差异显著(P<0.05),标不同大写字母表示差异极显著(P<0.01),标相同字母表示差异不显著
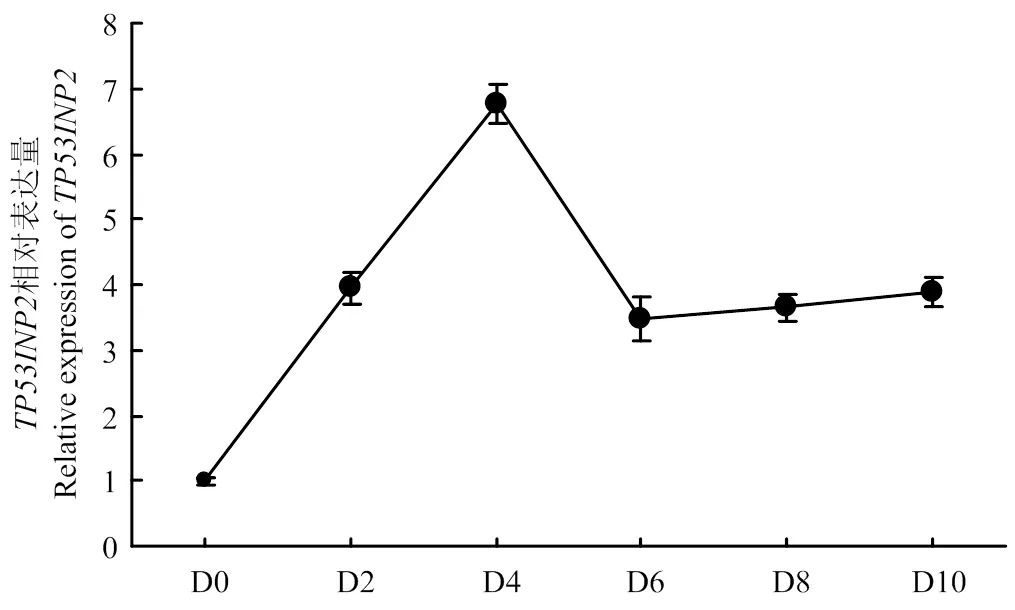
D0:成肌细胞诱导分化第0天;D2:成肌细胞诱导分化第2天;D4:成肌细胞诱导分化第4天;D6:成肌细胞诱导分化第6天;D8:成肌细胞诱导分化第8天;D10:成肌细胞诱导分化第10天
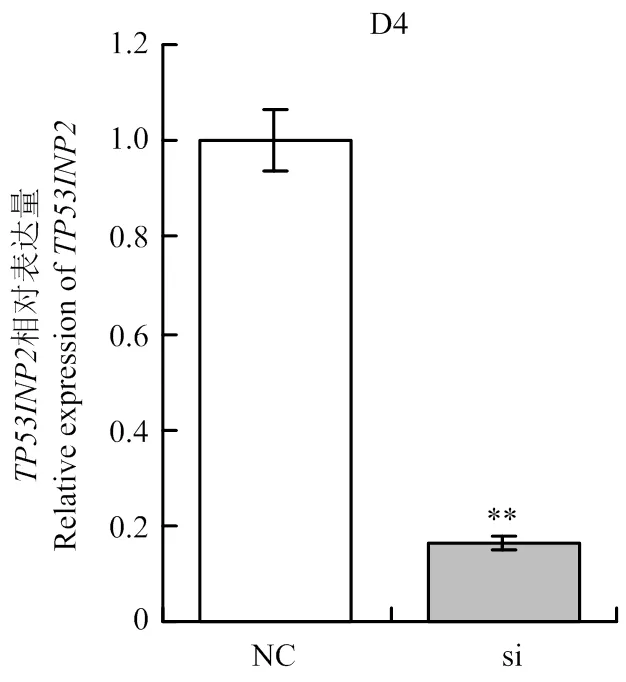
**代表差异极显著。下同
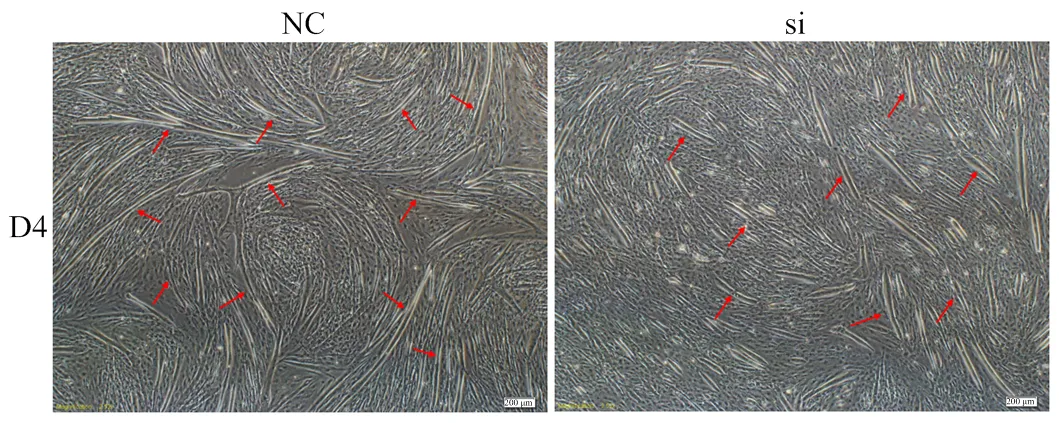
红色箭头表示肌细胞融合所形成的肌管
3.2 TP53INP2对肌肉分化的影响
目前已有的在不同组织的表达模式分析也仅限于小鼠和人上,研究报道证明在人和小鼠的骨骼肌、心脏及脑等组织的表达量非常高[25],这与本研究的结果是一致的。根据在成肌细胞不同分化天数的表达规律可以知道其整体表达趋势是先上升后下降且在诱导分化的第4天表达量达到最高,提示该基因可能对肌细胞的分化有一定的调控作用,因此研究者在成肌细胞中利用siRNA干扰该基因进行后续功能试验。结果显示,在诱导分化的第4天,处理组中成肌细胞分化较慢,肌管较少、较短,而对照组中肌细胞融合得更好,肌管更多更长,处理组与对照组差异极显著,因此初步判定干扰后抑制成肌细胞的分化。qRT-PCR和Western Blot结果显示,处理组肌细胞分化标志基因、和的表达水平均被下调,同样提示干扰后抑制了成肌细胞的分化。肌细胞生成素(MYOG)是骨骼肌细胞中特异性表达的转录因子,其可促进一些肌肉相关基因的表达并对于成肌细胞的终末分化有至关重要的调控作用,在本研究中当干扰的表达后,MYOG的RNA及蛋白水平都极显著下调,这更加肯定了TP53INP2对于成肌细胞分化的功能[26]。肌球重链蛋白3(MYH3)属于MYH家族,其编码的蛋白含有IQ结构域及肌球蛋白头样结构域,有研究报道证明该基因对于胎儿肌肉发育有至关重要的作用,若引起该基因突变将引发疾病,在本研究中干扰后,的表达被抑制,因此证实能影响骨骼肌肌肉的发育[27]。肌源性分化蛋白1(MYOD),其可通过诱导细胞增殖周期停滞以促进成肌细胞分化,另外其与及一同占据一些成肌过程中肌肉形成特异性基因的启动子核心区域,以促进成肌[28-29]。本研究中,抑制的表达后,的表达也被抑制,再次证实了牛成肌细胞的分化受到了抑制。目前,尚未见到调控肌细胞分化的文献报道,不过已有研究证实够激活肌细胞自噬,而肌细胞自噬激活则会促进肌细胞的分化[30],据此推测干扰可能通过抑制牛肌细胞自噬以起到抑制成肌细胞分化的作用,但其具体作用机制还有待深入研究。
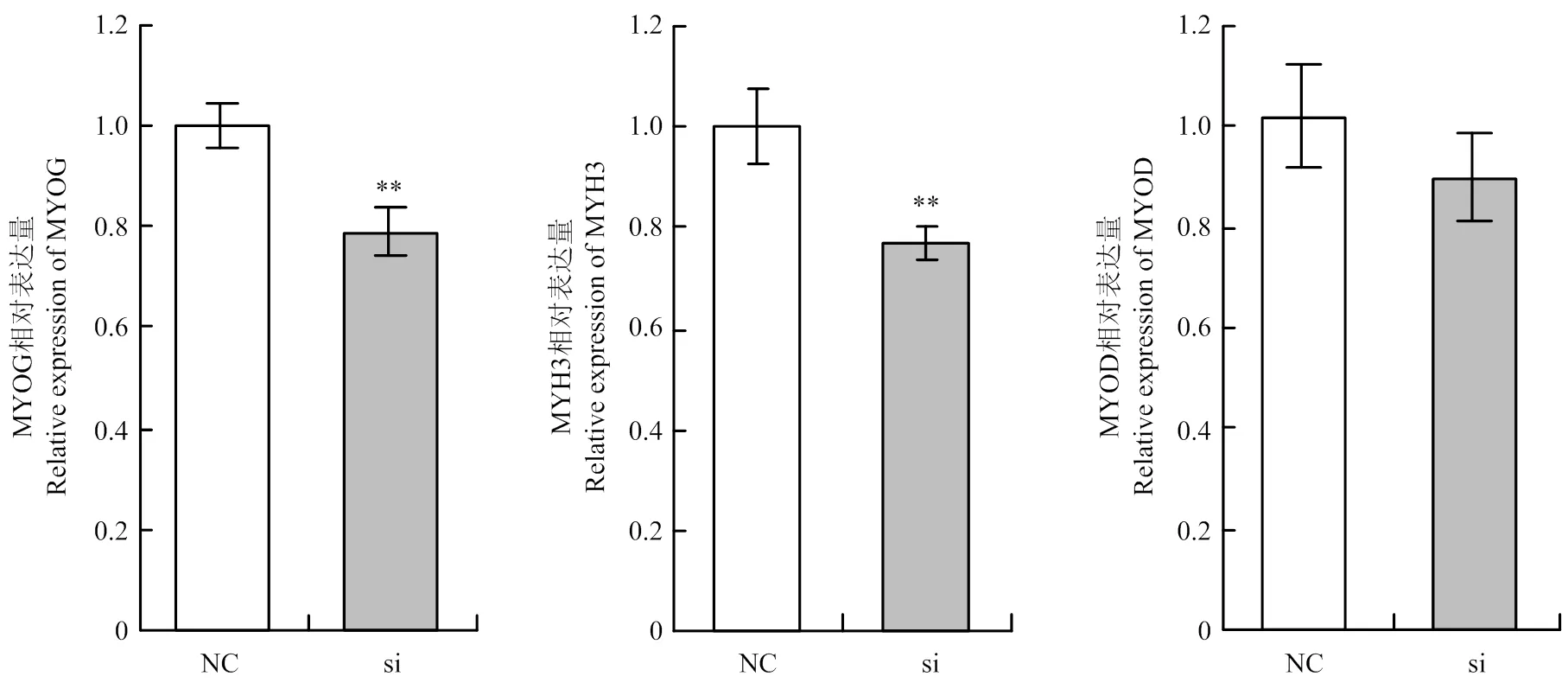
图5 成肌细胞分化标志基因mRNA水平检测
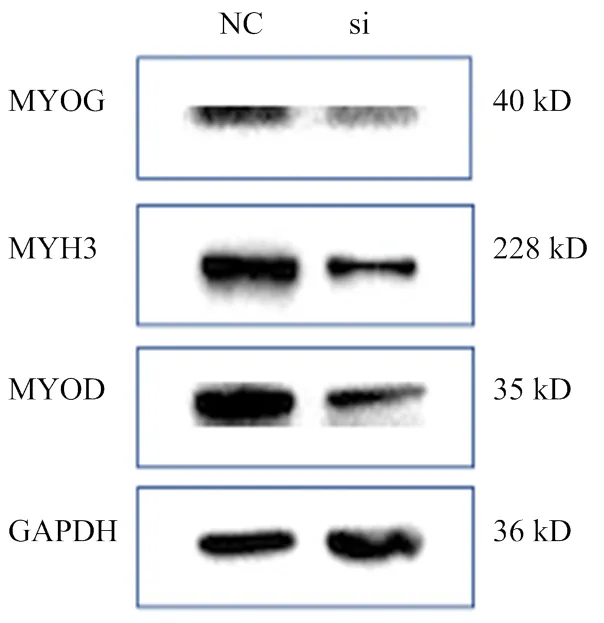
图6 Western Blot检测成肌细胞分化标志基因
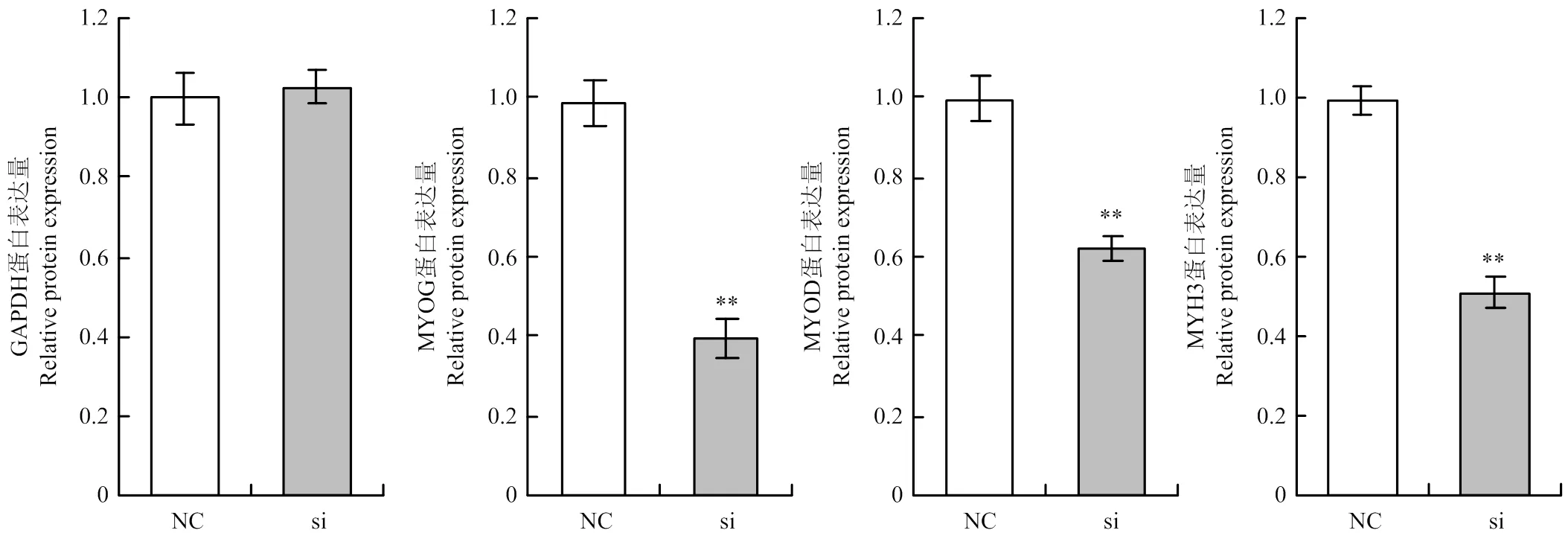
图7 不同标志蛋白相对表达量
4 结论
在成年秦川牛背最长肌中表达量最高且极显著高于其他组织;在秦川牛成肌细胞不同分化天数,的mRNA表达量总体趋势为先上升后下降,且在第4天表达量最高;干扰的表达后,抑制了秦川牛成肌细胞的分化。
[1] SALA D, ZORZANO A. Is TP53INP2 a critical regulator of muscle mass. Current opinion in clinical nutrition and metabolic care, 2015, 18(3): 234-239. doi: 10. 1097/MCO. 0000000000000163.
[2] 陈俐静, 陈卓, 李娜, 孙亚伟, 李红波, 宋雯雯, 张杨, 姚刚. 新疆褐牛与安格斯牛胴体及肉质性状及脂代谢相关基因表达差异比较. 中国农业科学, 2020(22): 4700-4709.
CHEN L J, CHEN Z, LI N, SUN Y W, LI H B, SONG W W, ZHANG Y, YAO G. Comparison of the carcass and beef quality traits with the expression of the lipid metabolism related genes between Xinjiang brown cattle and Angus beef cattle. Scientia Agricultura Sinica, 2020(22): 4700-4709. (in Chinese)
[3] 宁越, 米雪, 陈星伊, 邵建航, 昝林森. SMAD1基因的沉默和过表达及对秦川牛原代成肌细胞生肌的影响. 中国农业科学, 2019, 52(10): 1818-1829. doi:10.3864/j.issn.0578-1752.2019.10.014.
NING Y, MI X, CHEN X Y, SHAO J H, ZAN L S. Silencing and overexpressing SMAD family member 1(SMAD1) gene and its effect on myogenesis in primary myoblast of Qinchuan cattle(). Scientia Agricultura Sinica, 2019, 52(10): 1818-1829. doi:10.3864/ j.issn.0578-1752.2019.10.014. (in Chinese)
[4] 吴垚群, 陈少康, 盛熙晖, 齐晓龙, 王相国, 倪和民, 郭勇, 王楚端, 邢凯. 用高通量测序技术研究松辽黑猪与长白猪背最长肌mRNA和lncRNA的差异表达. 中国农业科学, 2020(4): 836-847.
WU Y Q, CHEN S K, SHENG X H, QI X L, WANG X G, NI H M, GUO Y, WANG C D, XING K. Differential expression of mRNA and lncRNA in longissimus dorsi muscle of Songliao black pig and Landrace pig based on high-throughput sequencing technique. Scientia Agricultura Sinica, 2020(4): 836-847. (in Chinese)
[5] SUN Y J, LIU K P, HUANG Y Z, LAN X Y, CHEN H. Differential expression of FOXO1 during development and myoblast differentiation of Qinchuan cattle and its association analysis with growth traits. Science China Life Sciences, 2018, 61(7): 826-835. doi:10.1007/s11427-017-9205-1.
[6] HE M Z, ZHAO Y L, YI H Q, SUN H, LIU X D, MA S M. The combination of TP53INP1, TP53INP2and AXIN2: potential biomarkers in papillary thyroid carcinoma. Endocrine, 2015, 48(2): 712-717. doi:10.1007/s12020-014-0341-8.
[7] OKAMURA S, ARAKAWA H, TANAKA T, NAKANISHI H, NG C C, TAYA Y, MONDEN M, NAKAMURA Y. p53DINP1, a p53-inducible gene, regulates p53-dependent apoptosis. Molecular Cell, 2001, 8(1): 85-94. doi:10.1016/s1097-2765(01)00284-2.
[8] ZHANG W Y, LI P W, WANG S J, GONG C, W LI, M XUE, SU X T, WANG Y N, ZAN L S. TP53INP2 promotes bovine adipocytes differentiation through autophagy activation. Animals, 2019, 9(12): 1060. doi: 10. 3390/ani9121060.
[9] HUANG R, LIU W. Identifying an essential role of nuclear LC3 for autophagy. Autophagy, 2015, 11(5): 852-853. doi:10.1080/15548627. 2015.1038016.
[10] XU Y F, WAN W, SHOU X, HUANG R, YOU Z Y, SHOU Y H, WANG L L, ZHOU T H, LIU W. TP53INP2/DOR, a mediator of cell autophagy, promotes rDNA transcription via facilitating the assembly of the POLR1/RNA polymerase I preinitiation complex at rDNA promoters. Autophagy, 2016, 12(7): 1118-1128. doi: 10. 1080/15548627. 2016. 1175693.
[11] SANCHO A, DURAN J, GARCÍA-ESPAÑA A, C MAUVEZIN, ALEMU E A, LAMARK T, MACIAS M J, DESALLE R, ROYO M, SALA D. DOR/Tp53inp2 and Tp53inp1 constitute a Metazoan gene family encoding dual regulators of autophagy and transcription. PLoS One, 2012. doi: 10. 1371/journal. pone. 0034034.
[12] DAVID S, SAŠKA I, NATÀLIA P, VICENT R, JORDI D, DANIEL B, SAADET T, MARTINE L, HUBERT V, MONIKA K K. Autophagy- regulating TP53INP2 mediates muscle wasting and is repressed in diabetes. The Journal of Clinical Investigation, 2014, 124(5): 1914-1927. doi: 10. 1172/JCI72327.
[13] LEE Y K, JUN Y W, CHOI H E, HUH Y H, KAANG B K, JANG D J, LEE J A. Development of LC3/GABARAP sensors containing a LIR and a hydrophobic domain to monitor autophagy. EMBO Journal, 2017, 36(8): 1100-1116. doi: 10. 15252/embj. 201696315.
[14] NOWAK J, IOVANNA J L. TP53INP2is the new guest at the table of self-eating. Autophagy, 2009, 5(3): 383-384. doi:10.4161/auto.5.3. 7698.
[15] JONATHAN N, CENDRINE A, JOËL T L, PIERRE P, MARIE- JOSÈPHE P, INÉS V M, GUILLERMO V, JEAN-CHARLES D, LUCIO I J. The TP53INP2 protein is required for autophagy in mammalian cells. Molecular Biology of the Cell, 2009, 20(3): 870-881. doi: 10. 1091/mbc. e08-07-0671.
[16] GOLDMAN S, ZHANG Y, JIN S. Autophagy and adipogenesis: implications in obesity and type II diabetes. Autophagy, 2010, 6(1): 179-181. doi:10.4161/auto.6.1.10814.
[17] KOVSAN J, BLÜHER M, TARNOVSCKI T, KLÖTING N, KIRSHTEIN B, MADAR L, SHAI I, GOLAN R, HARMAN- BOEHM I, SCHÖN M R, GREENBERG A S, ELAZAR Z, BASHAN N, RUDICH A. Altered autophagy in human adipose tissues in obesity. The Journal of Clinical Endocrinology and Metabolism, 2011, 96(2): E268-E277. doi:10.1210/jc.2010-1681.
[18] FROMM-DORNIEDEN C, LYTOVCHENKO O, VON DER HEYDE S, BEHNKE N, HOGL S, BERGHOFF J, KÖPPER F, OPITZ L, RENNE U, HOEFLICH A, BEISSBARTH T, BRENIG B, BAUMGARTNER B G. Extrinsic and intrinsic regulation of DOR/TP53INP2expression in mice: effects of dietary fat content, tissue type and sex in adipose and muscle tissues. Nutrition & Metabolism, 2012, 9(1): 86. doi:10.1186/1743-7075-9-86.
[19] HU Y, LI X, XUE W, PANG J, MENG Y, SHEN Y, XU Q. TP53INP2-related basal autophagy is involved in the growth and malignant progression in human liposarcoma cells. Biomedicine & Pharmacotherapy, 2017, 88: 562-568. doi:10.1016/j.biopha.2017. 01.110.
[20] 赵艳芳. Rybp基因对秦川牛成肌细胞分化作用的研究[D]. 杨凌:西北农林科技大学. 2017.
ZHAO Y F. The effect of Rybp gene on the differentiation of Qinchuan bovine myoblasts[D]. Yangling: Northwest A & F university. 2017. (in Chinese)
[21] 赵艳芳, 张乐, 王亚宁, 宁越, 王洪宝, 昝林森. 牛Rybp基因的表达特性分析. 西北农林科技大学学报(自然科学版), 2018, 46(5): 8-15, 29. doi:10.13207/j.cnki.jnwafu.2018.05.002.
ZHAO Y F, ZHANG L, WANG Y N, NING Y, WANG H B, ZAN L S. Expression characteristics of cattle Rybp gene. Journal of Northwest A&F University(Natural Science Edition), 2018, 46(5): 8-15, 29. doi:10.13207/j.cnki.jnwafu.2018.05.002. (in Chinese)
[22] 李佩韦, 吴森, 王亚宁, 王洪宝, 昝林森. PLIN2基因在秦川肉牛皮下脂肪组织中的表达规律及基因多态性与肉质性状的关联分析. 中国畜牧兽医, 2018(6): 1580-1589.
LI P W, WU S, WANG Y N, WANG H B, ZAN L S. Expression patterns of PLIN2gene in subcutaneous adipose tissue and association analysis of single nucleotide polymorphisms with meat quality traits in Qinchuan cattle. China Animal Husbandry & Veterinary Medicine, 2018(6): 1580-1589. (in Chinese)
[23] 马懿磊. 黄牛IGF1R基因遗传变异及其对成肌细胞增殖、分化的影响[D]. 杨凌:西北农林科技大学,2019.
MA Y L. Genetic variation of cattle IGF1R gene and its effect on the proliferation and differentiation of myoblasts[D]. Yangling: Northwest A & F university. 2019. (in Chinese)
[24] HINDI S M, TAJRISHI M M, KUMAR A. Signaling mechanisms in mammalian myoblast fusion. Science Signaling, 2013, 6(272): re2. doi:10.1126/scisignal.2003832.
[25] BAUMGARTNER B G, ORPINELL M, DURAN J, RIBAS V, BURGHARDT H E, BACH D, VILLAR A V, PAZ J C, GONZÁLEZ M, CAMPS M, et al. Identification of a novel modulator of thyroid hormone receptor-mediated action. PLoS One, 2007, 2(11). doi: 10. 1371/journal. pone. 0001183.
[26] ZHANG Z T, XU F, ZHANG Y N, LI W, YIN Y H, ZHU C Y, DU L X, ELSAYED A K, LI B C. Cloning and expression of MyoG gene from Hu sheep and identification of its myogenic specificity. Molecular Biology Reports, 2014, 41(2): 1003-1013. doi:10.1007/s11033-013- 2945-0.
[27] SCALA M, ACCOGLI A, DE GRANDIS E, ALLEGRI A, BAGOWSKI C P, SHOUKIER M, MAGHNIE M, CAPRA V. A novel pathogenic MYH3mutation in a child with Sheldon-Hall syndrome and vertebral fusions. American Journal of Medical Genetics Part A, 2018, 176(3): 663-667. doi:10.1002/ajmg.a.38593.
[28] WARDLE F C. Master control: transcriptional regulation of mammalian Myod. Journal of Muscle Research and Cell Motility, 2019, 40(2): 211-226. doi:10.1007/s10974-019-09538-6.
[29] 王欣悦, 石田培, 赵志达, 胡文萍, 尚明玉, 张莉. 基于绵羊胚胎骨骼肌蛋白质组学的PI3K-AKT信号通路分析. 中国农业科学, 2020(14): 2956-2963.
WANG X Y, SHI T P, ZHAO Z D, HU W P, SHANG M Y, ZHANG L. The analysis of PI3K-AKT signal pathway based on the proteomic results of sheep embryonic skeletal muscle. Scientia Agricultura Sinica, 2020(14): 2956-2963. (in Chinese)
[30] KIM J H, CHOI T G, PARK S, YUN H R, NGUYEN N N Y, JO Y H, JANG M, KIM J, KIM J, KANG I, HA J, MURPHY M P, TANG D G, KIM S S. Mitochondrial ROS-derived PTEN oxidation activates PI3K pathway for mTOR-induced myogenic autophagy. Cell Death and Differentiation, 2018, 25(11): 1921-1937. doi:10.1038/s41418-018- 0165-9.
Interference inGene Inhibits the Differentiation of Bovine Myoblasts
DU JiaWei1, DU XinZe1, YANG XinRan1, SONG GuiBing1, ZHAO Hui1, ZAN LinSen1,2, WANG HongBao1,2
1College of Animal Science and Technology, Northwest A&F University, Yangling 712100, Shaanxi;2National Beef Cattle Improvement Center, Yangling 712100, Shaanxi
【】Muscle can maintain the motor function of mammals and regulate body metabolism. Its quantity and distribution have an important influence on meat quality. The growth and development of skeletal muscle and its genetic characteristics influence and even determine the meat production and meat quality to a large extent. It is of great significance to study the growth and development of skeletal muscle. The regulatory effect ofon autophagy and the regulation mechanism on the differentiation of preadipocytes have been studied, but whether it affects the differentiation of bovine myoblasts has not been reported. 【】This study aims to explore the effect ofon the differentiation of Qinchuan bovine myoblasts in order to provide a theoretical basis for the molecular breeding of beef cattle meat traits. 【】The real-time fluorescence quantitative PCR (RT-qPCR) technology was used to detect the expression characteristics ofat different stages of differentiation were analyzed.gene siRNA was synthesized and transfected to Qinchuan bovine myoblasts, cells were induced to differentiation 12 hours after transfection, phenotypic changes of myoblasts were observed at different time pionts, and RT-qPCR and Western Blot technologies were performed respectively to detect the expression of differentiation marker genes and proteins on the fourth day of induced differentiation. 【】1. RT-qPCR results showed that the expression level ofwas the highest in adult Qinchuan cattle Longissimus dorsi muscle tissue and the lowest in the small intestine tissue. It is higher in adult bovine heart, liver, kidney, reticulum and rumen, and lower in other tissues (compared with longissimus dorsi). 2. With the differentiation of myoblasts, the expression of this gene increased from 0 to 4 days and reached a peak on the 4th day, and then decreased. 3. After interfering withsiRNA in myoblasts, the number and length of myotubes in the test group were significantly lower than those in the control group. 4. RT-qPCR results showed that the expression of myoblast differentiation marker genes myogenin () and myosin heavy chain protein 3 () was significantly lower than that of the control group. Western Blot results showed that the protein expressions of MYOG, MYH3 and MYOD in the test group were reduced and the differences were extremely significant compared with the control group.【】Interfering ofhas an inhibitory effect on the differentiation of bovine myoblasts, suggesting that this gene may have an important regulatory effect on the growth and development of Qinchuan cattle muscle tissue, and it can be used for in-depth functional research for molecular breeding of beef cattle practice.
; differentiation; myoblasts; Qinchuan cattle

10.3864/j.issn.0578-1752.2021.21.017
2020-09-25;
2021-03-12
国家自然科学基金(31572363)、陕西省人才推进计划青年科技新星项目(2017KJXX-76)、国家重点研发计划项目(2017YFD0502002)
杜嘉伟,E-mail:614502306@qq.com。通信作者王洪宝,E-mail:wanghongbao@nwsuaf.edu.cn
(责任编辑 林鉴非)

