低剂量利伐沙班在非瓣膜性房颤患者中有效性和安全性的Meta 分析*
孙 洁,陈国梅,黄 吉
太仓市第一人民医院(苏州大学附属太仓医院)药剂科,太仓215400
心房颤动(atrial fibrillation,AF),简称房颤,是一种常见的室上性心律失常。在全球疾病负担(GBD)的一项研究估计,2010 年房颤的全球年龄调整后的患病率为0.5%左右[1]。鉴于房颤的患病率随着年龄的增长而增加,血栓栓塞是心房颤动最大的临床危害,因此目前各房颤指南已将抗凝列于房颤治疗策略中的首位[2]。较经典药物华法林,新型口服抗凝药利伐沙班(Rivaroxaban)剂量相对固定、药物食物及疾病相互作用少、严重出血(如颅内出血等)并发症少等,被越来越多患者所接受。但目前国内对其特异性拮抗剂可及性差,在发生严重出血时,存在一定安全隐患,尤其是老年及出血风险较大的患者,临床医生在用药时普遍考虑低剂量使用。囿于利伐沙班低剂量使用的疗效及安全性还需要大量的临床研究加以证实,故本文将通过Meta 分析对这一情况进行探讨,为临床用药提供参考。
2 资料与方法
2.1 检索策略
计算机检索PubMed、Cochrane Library、Web of Science、GeenMedical、中国知网(CNKI)、维普数据库、万方数据库,查找所有比较低剂量利伐沙班和华法林治疗非瓣膜性房颤的有效性和安全性的随机对照试验和队列研究,并追溯纳入文献的参考文献。英文以“Rivaroxaban”、“low-dose”或“different dosage”,”Atrial Fibrillation”,”Warfarin”为检索词,中文文献以“利伐沙班”、“低剂量”或“小剂量”、“房颤”、“华法林”为检索词,检索时间均为建库至2020 年7 月31 日。
2.2 文献质量评价
采用NOS 量表对纳入的队列研究进行质量评价。评分项目总分9 分:①队列选择情况4 分;②组间可比性2 分;③结局暴露因素的测量或结果测量3 分。NOS 量表评分≥5 分为高质量文献。以Jadad 改良后的评分量表评价纳入的随机对照试验质量,评价标准为:①由计算机产生的随机数字或类似方法记2 分,提及随机试验、但未描述随机分配的方法记1分,未随机或者采用交替分配的方法如单双号记0 分;②充分随机化隐藏记2 分,不充分随机化隐藏记1 分,交替分配或未使用随机化隐藏记0 分;③采用了完全一致的安慰剂片或类似盲法记2 分,试验陈述为盲法、但未描述方法记1 分,未采用双盲或盲的方法不恰当记0 分;④描述了撤出或退出的数目和理由记1 分,未描述撤出或退出的数目或理由记0 分。总分0~3 分视为低质量文献,4~7 分视为高质量文献。
2.3 文献纳入与排除标准
纳入标准:①研究对象为经心脏彩超、心电图证实为非瓣膜性房颤的患者;年龄≥18 周岁;CHA2DS2-VASc 评分均≥2 分(S2 和A2 分别代表既往有血栓栓塞病史和年龄≥75 岁)。这两项因素可成倍增加患者血栓栓塞的风险,是房颤患者血栓栓塞的主要危险因素,所以这两项的评分各为2分。而A、H、C、D、Sc、V 则分别代表年龄>65 岁、高血压、心衰、糖尿病、女性和血管疾病等。血管疾病是指心肌梗死、复合型主动脉斑块以及外周动脉疾病,这几项分别代表1 分。最高评分为9 分,CHA2DS2-VASc 评分≥2 者需口服抗凝药物;评分为1 分者,口服抗凝药物或不进行抗栓治疗均可;无危险因素,即评分0 分者不需抗栓治疗。HAS-BLED 评分为1~3 分(H:高血压1 分,A:异常肝肾功能各计1 分,S:卒中1分,B:出血1 分,L:INR 值不稳定1 分,E:老年>65 岁1 分,D:药物、饮酒各计1 分,最高分9 分,总分≥3 分为出血高危患者)[2]。②入选的均为低剂量利伐沙班(15 mg 或10 mg)与华法林治疗非瓣膜性房颤的有效性和安全性比较的随机对照试验或队列研究。③评价指标包括卒中、体循环栓塞、全因死亡、颅内出血、消化道出血等。
排除标准:①随访时间小于6 个月。②临床上已有明显的活动性出血史患者。③严重肾功能不全(肌酐清除率<10 mL·min-1)及接受血液透析的患者。④凝血功能异常且伴有严重出血倾向的患者。
2.4 资料提取
由两位研究者分别按照纳入、排除标准独立进行文献筛选,遇到分歧时可通过讨论或征求第三人意见的方式解决。提取内容包括第一作者的姓名、论文发表的时间、样本量、患者基本信息、给药方案、结局指标。
2.5 统计学方法
采用Cochrane 协作网出品的RevMan 5.3、Stata12 软件进行统计学分析。计量资料采用均数差(mean difference,MD)为效应指标,总发生率为二分类变量,采用危险度比(Risk Ratio,RR)为效应指标,各效应量均给出其点估计值和95%CI。采用卡方检验判断各研究结果间的异质性(检验水准为α=0.1),同时结合I2定量判断异质性的大小。对无统计学异质性的研究采用固定效应模型合并分析,存在统计学异质性的研究采用随机效应模型合并分析。明显的临床异质性采用亚组分析或敏感性分析等方法进行处理,或只进行描述性分析。Meta 分析的检验水准设为α=0.05。
3 结果
3.1 文献检索结果及质量评价
通过数据库检索获得相关英文文献198 篇,中文文献5篇,剔除重复的文献61 篇,经阅读文题和摘要后剔除不符合纳入标准的文献112 篇,然后阅读全文,进一步排除数据不全或没有对照组的文献,最终纳入6 篇合格文献[3~8]。队列研究按照NOS 量表评分,2 篇文献均>5 分。按照Jadad 改良后的评分量表评分,4 篇文献均不低于4 分,均为高质量文献。筛选流程见图1。

图1 筛选流程
本研究纳入文献6 篇,患者总数为66334 例,纳入文献基本特征主要有第一作者、研究年份、总样本量、利伐沙班剂量、华法林剂量、随访时间、年龄、男性所占比、CHA2DS2-VASc 评分、HAS-BLED 评分、INR、高血压患者所占比、糖尿病患者所占比等。利伐沙班剂量为10~15 mg。研究的CHA2D2-VASc 评分≥2 分,HAS-BLED 评分在2 分左右。适当调整华法林用量使INR 基本稳定在2.0~3.0。结果见表1。

表1 纳入文献的基本特征
3.2 低剂量利伐沙班和华法林组有效性比较
3.2.1 脑卒中6 篇文献[3-8],报道了采用低剂量利伐沙班与华法林治疗非瓣膜性房颤患者脑卒中发生率,各研究无统计学异质性(P=0.59,I2=0%),采用固定效应模型进行分析。Meta 分析结果显示,采用低剂量利伐沙班治疗非瓣膜性房颤患者脑卒中发生率低于华法林,差异有统计学意义[RR=0.80,95%CI(0.74,0.86),P<0.000 01],见图2。

图2 低剂量利伐沙班组与华法林组脑卒中发生率的比较
3.2.2 心肌梗塞4 篇文献[3-5,7],报道了采用低剂量利伐沙班与华法林治疗非瓣膜性房颤患者心肌梗塞发生率,各研究有统计学异质性(P=0.06,I2=65%),采用随机效应模型进行分析。Meta 分析结果显示,采用低剂量利伐沙班治疗非瓣膜性房颤患者心肌梗塞发生率与华法林相比差异无统计学意义[RR=0.77,95%CI(0.53,1.11),P=0.16],见图3。
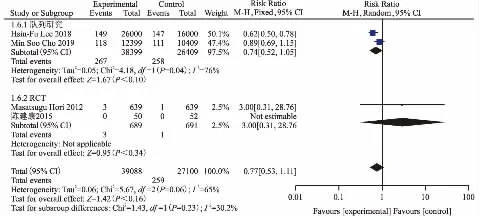
图3 低剂量利伐沙班组与华法林组心肌梗塞发生率的比较
3.2.3 全因死亡4 篇文献[3-5,7],报道了采用低剂量利伐沙班与华法林治疗非瓣膜性房颤患者全因死亡发生率,各研究有统计学异质性(P<0.000 01,I2=96%),采用随机效应模型进行分析。Meta 分析结果显示,采用低剂量利伐沙班治疗非瓣膜性房颤患者全因死亡发生率与华法林相比差异无统计学意义[RR=0.75,95%CI(0.50,1.12),P=0.16],见图4。

图4 低剂量利伐沙班组与华法林组全因死亡率的比较
3.3 低剂量利伐沙班和华法林组安全性比较
3.3.1 颅内出血6 篇文献[3-8],报道了采用低剂量利伐沙班与华法林治疗非瓣膜性房颤患者颅内出血发生率,各研究无统计学异质性(P=0.30,I2=18%),采用固定效应模型进行分析。Meta 分析结果显示,采用低剂量利伐沙班治疗非瓣膜性房颤患者颅内出血发生率低于华法林,差异有统计学意义[RR=0.55,95%CI(0.48,0.64),P<0.00001],见图5。

图5 低剂量利伐沙班组与华法林组颅内出血发生率的比较
3.3.2 消化道出血6 篇文献[3-8],报道了采用低剂量利伐沙班与华法林治疗非瓣膜性房颤患者消化道出血发生率,各研究无统计学异质性(P<0.000 01,I2=96%),采用随机效应模型进行分析。Meta 分析结果显示,采用低剂量利伐沙班治疗非瓣膜性房颤患者消化道出血发生率低于华法林,差异无统计学意义[RR=0.80,95%CI(0.56,1.16),P=0.24],见图6。

图6 低剂量利伐沙班组与华法林组消化道出血发生率的比较
3.3.3 轻微出血4 篇文献[3,6-8],报道了采用低剂量利伐沙班与华法林治疗非瓣膜性房颤患者轻微出血(包括皮下出血、黏膜出血、鼻出血等)发生率,各研究无统计学异质性(P=0.93,I2=0%),采用固定效应模型进行分析。Meta 分析结果显示,采用低剂量利伐沙班治疗非瓣膜性房颤患者轻微出血发生率低于华法林,差异无统计学意义[RR=0.85,95%CI(0.53,1.39),P=0.52],见图7。

图7 低剂量利伐沙班组与华法林组轻微出血发生率的比较
3.3.4 敏感性分析随访时间短的研究结果剔除后,与原始数据相对比,其变化差异无统计学意义,提示该研究结果比较可靠。
3.3.5 发表偏倚为考察纳入文献是否存在发表偏倚。针对不同的终点事件,绘制漏斗图,见图8。

图8 各研究的漏斗图
该图形结构对称,呈倒漏斗形式,结果为阳性,表明纳入文献无发表性偏倚。同时Begg’s 及Egger’s 检验均P>0.05,说明漏斗图是对称的,研究不存在偏倚。
4 讨论
心房颤动是临床最常见的持续性心律失常[9]。全球流行病学调查显示,2010 年房颤的全球患病率为0.5%,其中年龄>40岁的人群患房颤的终生风险分别是男性26%、女性23%[1]。房颤的患病率及发病率均随年龄增长逐步增加,且各年龄段男性均高于女性[10]。我国一项流行病学调查显示,房颤年龄校正后患病率为0.65%,在>80 岁人群中高达7.5%[11]。另一项调查结果显示,我国房颤年龄校正后患病率为0.74%,<60 岁男女患病率分别为0.43%和0.44%,>60 岁男女患病率分别增长至1.83%和1.92%[12]。房颤是脑卒中的独立危险因素[13],有研究表明,房颤患者的中风率是每年4.5%,其中一半以上可导致死亡或终身残疾[14]。因此,预防房颤引起的血栓栓塞是房颤治疗环节中重要的一节。在有血栓栓塞危险因素的房颤患者中,应用华法林抗凝可明显减少血栓栓塞事件,并改善患者的预后[15]。近年来新型口服抗凝药也被证实可明显减少脑卒中和血栓栓塞并发症,同时可显著降低颅内出血的风险[16,17]。华法林作为传统的抗凝药物,临床适应症和疗效得到较好的证实;但其容易受食物、药物的影响,而且需要通过定期监测INR 指标来调整剂量,治疗窗比较窄,个体差异大。即使在发达国家中也只有一半患者根据临床实践指南服用华法林[18]。
利伐沙班作为新型口服抗凝药的一种,选择性地阻断Xa 因子的活性位点,特异性高,且不需要辅因子(例如抗凝血酶Ⅲ)以发挥活性,独立于内源性抗凝血酶发挥作用[19]。利伐沙班吸收迅速,口服后2~4 小时内达到峰值,生物利用度高。利伐沙班经细胞色素P450(CYP)3A4、CYP 2J2 和不依赖CYP 的机制进行代谢,约三分之二的药物通过代谢降解,其余三分之一以原型药物主要经肾脏主动分泌的方式随尿液排泄,与质子泵抑制剂没有相互作用[19,20]。
在此次研究中,考虑到不同队列研究可能究存在纳入患者受到干扰因素不可控、偏倚来源多等因素的影响,但RCT设计严密,研究组间可比性强,减少了一定的选择偏倚,结论可靠,但由于严格的纳排标准,样本量不够大,所以把它们分成不同的亚组,结果显示,低剂量利伐沙班治疗非瓣膜性房颤患者脑卒中发生率低于华法林,差异有统计学意义,而在队列研究亚组中这种差异更明显。但是在心肌梗死、全因死亡方面,低剂量利伐沙班的有效性与华法林总体差异虽无统计学意义,但在队列研究亚组中,可能由于研究人数较多,事件发生数量被记录的更全面,而结果更倾向于低剂量利伐沙班。
低剂量利伐沙班和华法林组安全性比较结果显示,在颅内出血方面低剂量利伐沙班出血发生率低于华法林,差异有统计学意义,同样,在队列研究亚组中这种差异更显著。轻微出血发生率与华法林相比,差异无统计学意义。值得注意的是,低剂量利伐沙班并未体现出其常规剂量与华法林比较在消化道出血发生率上的差异,表明低剂量的利伐沙班不增加消化道出血风险。而在RCT 亚组中,Z 值的P=0.08,以本研究的检验水准α=0.05 要惋惜地拒绝无效假设,但是期待样本量更大、质量更高的多中心RCT 对这个问题继续开展研究,未来可能会有阳性结果。
综上所述,本文通过全面检索文献,纳入研究包括队列研究和RCT,对低剂量利伐沙班治疗非瓣膜性房颤患者安全性和有效性的相关文献进行Meta 分析,结果发现,与华法林治疗相比,低剂量利伐沙班能更有效地降低脑卒中的风险,不增加消化道出血风险,且有较强减少消化道出血风险的倾向。而在全因死亡、心梗及轻微出血的发生率方面虽未看到低剂量利伐沙班的更多优势,但并不增加这些事件的发生率,与华法林相比,有效性及安全性并没有下降。
最近的临床实践[21,22]显示,为了防止出血并发症,各国都倾向于使用低剂量的新型口服抗凝药(NOACs)。特别是亚洲人群,接受低剂量利伐沙班(10~15 mg·d-1)的患者数极高(约93%),这可能是与体型差异、年龄大、合并症多、害怕药物引起的医源性出血事件、经济(药物费用)问题等原因有关。值得注意的是,不适当的处方低剂量NOACs 可能导致更多血栓栓塞事件,而不能更多地减少大出血。这与心血管并发症[23]而住院的发生率增加相关。
因此,结合利伐沙班药理、药动学特点,使用低剂量利伐沙班用于长期需要抗凝治疗的非瓣膜性房颤患者是可行的。本研究没有进一步对纳入患者的年龄、性别、肝肾功能状况、合并药物、用药依从性等作分层次探讨,结果可能不全面。由于纳入研究的患者基本情况、地区种族、药物使用剂量及疗程等方面存在一定的差异性,且主要重大事件数较少,可能会影响Meta 分析结果。期待有更多的临床相关试验研究,为临床合理用药提供循证证据。

