氟氯氰菊酯残留检测与紫外降解荧光光谱研究
季仁东,韩 月,王晓燕,马士才,卞海溢,刘小红,2,3,陈 勇
(1.淮阴工学院 江苏省湖泊环境遥感技术工程实验室,江苏 淮安 223003;2.中国科学院重庆绿色智能技术研究院,重庆 400714;3.重庆青年职业技术学院 健康医学院,重庆 400712;4.淮安龙渊农业科技有限公司,江苏 淮安 223001)
氟氯氰菊酯(C23H19ClF3NO3)纯品为粘稠的、部分结晶的琥珀色油状物,特殊气味,不挥发。适用小麦、玉米、十字科蔬菜、果树和烟草等植物的杀虫,能有效防治叶螨、棉蚜、桃蚜、果蝇等多种翅目类害虫[1-3]。大量农药喷洒进入环境中,会造成食物中农药残留和土壤污染,从而影响生态环境和人体健康。研究发现氟氯氰菊酯等农药对人体造成危害主要通过作用于中枢神经的锥体外系统、小脑、脊髓和周围神经[4,5],其临床表现以神经系统为主。因此,氟氯氰菊酯的残留检测至关重要。
目前已报道的氟氯氰菊酯农药残留检测方法主要包括气相色谱[6,7]、气相色谱-串联质谱[8]、气相色谱/质谱分析[9]、QuEChERS前处理-气相色谱[10]、气相色谱-负化学源-质谱联用[11]、气相色谱-离子阱串联质谱[12]和高效液相色谱[13]等分析方法。这些方法虽然准确度高,但是操作繁琐、检测时间长。荧光光谱具有检测快速、操作简单、实验消耗成本低等优点。本文通过荧光光谱对氟氯氰菊酯进行了实验研究,简化了以往农药残留检测过程,分析了氟氯氰菊酯的荧光特性,构建了检测模型函数。
农药降解技术可以降低氟氯氰菊酯农药毒性,有效保护生态环境和人类健康。目前报道的氟氯氰菊酯生物降解方法[14],主要有环保酵素[15]、光杆菌降解[16]、战氏生物农残降解剂[17]等。而基于荧光光谱分析方法应用紫外光技术照射降解氟氯氰菊酯还未见相关文献报道。本文通过紫外光方法对氟氯氰菊酯农药进行了降解实验,其原理是紫外光照射破坏农药成分结构,主要成分双键断裂,使得与有机碳相结合的其他元素分离开,将难降解的有机物分解为小分子物质[18]。本文基于荧光光谱对氟氯氰菊酯降解进行了表征和建模,所得结果对氟氯氰菊酯农药残留检测及其降解分析具有一定参考价值。
1 实验
1.1 实验样品
氟氯氰菊酯:成都科利隆生化有限公司,有效成分含量50 g/L,剂型:乳油。
1.2 实验仪器
荧光光谱由LS55荧光分光光度计(美国Perkin Elmer)采集,激发波长设置为255 nm。
1.3 实验过程
首先在纯净水中配成浓度为0.05 mg/mL的氟氯氰菊酯药品。然后取2.5 mL纯净水放于比色皿,取不同体积浓度为0.05 mg/mL的氟氯氰菊酯标准溶液逐量加入到比色皿中,并使溶液均匀混合,在每次加入农药后将溶液进行充分搅拌;得到不同浓度的氟氯氰菊酯样本溶液后,检测氟氯氰菊酯溶液的荧光光谱。
量取一定浓度的氟氯氰菊酯溶液进行不同时间长度的紫外光照射降解,利用荧光分光光度计获取降解后的药液荧光光谱,最后分析得到同一浓度药液不同降解时间与荧光光谱特征峰强度之间的对应关系。
2 结果与分析
2.1 氟氯氰菊酯农药荧光光谱检测
对所配置的不同浓度氟氯氰菊酯样本溶液利用LS55获取荧光光谱,其结果如图1所示。图中数字1代表纯净水样本,从2到8分别对应7种不同浓度的氟氯氰菊酯样本溶液,从1到8对应氟氯氰菊酯溶液浓度值分别为:0、0.000 980、0.002 83、0.006 14、0.009 02、0.013 8、0.015 8和0.019 1 mg/mL。与纯净水荧光光谱比较发现,氟氯氰菊酯在296 nm处存在明显的荧光峰,而且随着氟氯氰菊酯农药浓度的提高,荧光强度相应提高。因此,可以把296 nm荧光峰作为氟氯氰菊酯的特征峰。

图1 不同浓度的氟氯氰菊酯荧光光谱图
针对氟氯氰菊酯溶液浓度与296 nm处特征峰荧光强度进行回归,分析氟氯氰菊酯残留浓度及其荧光强度之间的对应关系,指数拟合后结果如图2所示。结果表明:氟氯氰菊酯浓度与特征峰荧光强度具有很好的指数函数关系,相关系数为0.997 8,函数关系式为

图2 氟氯氰菊酯溶液浓度值与荧光光谱在296 nm处荧光强度之间的关系
y=-358.65232*exp(-x/0.00516)+369.45623
(1)
式中:x为氟氯氰菊酯浓度,y为296nm处荧光强度。可见所得结果符合荧光强度-浓度理论计算公式,其计算公式为[19]
If=YfI0(1-e-abc)
(2)
式中:Yf为物质的荧光量子产率,I0为激发光强度,a为吸光系数,b为样品池光径,c为样品浓度。
为验证此函数关系的准确性,在同等实验条件下分别配置浓度为0.001 92、0.003 70、0.005 36、0.006 90、0.007 63、0.008 33 mg/mL的6种氟氯氰菊酯溶液,测量其荧光光谱并获取296 nm处荧光强度值。将此特征峰荧光强度值分别代入模型函数式(1)中计算其对应的样本预测浓度,具体结果如表1所示,函数回收率在96%~104%范围内,平均回收率为98.9%,相对标准偏差2.6%。

表1 氟氯氰菊酯的测定及其回收率
2.2 紫外光降解氟氯氰菊酯实验研究
利用紫外光对所配制的氟氯氰菊酯溶液(0.015 75 mg/mL)进行不同时间降解,每次降解后获取其荧光光谱,其结果如图3所示,图中从1到8为紫外光降解时间0、1、3、5、11、21、38、80 min后的荧光光谱。其中紫外光源放射光波长为253.7 nm,功率3 W,管压9.5~13 V,管流300 mA。由图3可以看出不断增加氟氯氰菊酯的降解时间,其特征峰荧光强度则随之降低,这说明在紫外光的照射下,农药中有效成分随着时间的增加而逐渐消失。当降解超过11 min后,氟氯氰菊酯特征峰开始逐渐消失。同时随着光照时间的延长,320 nm处荧光强度相对值逐渐增强,考虑这是由于紫外光照射使得农药发生化学反应[20]。
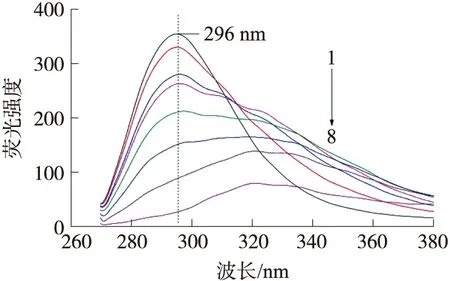
图3 经紫外光照射降解后氟氯氰菊酯溶液荧光光谱
利用Origin8.5软件分析数据,针对296 nm处的荧光特征峰,分析经过不同时间紫外光降解后的氟氯氰菊酯溶液荧光强度,并建立相应的函数关系,结果如图4所示。结果表明降解时间与荧光强度之间具有很好的指数函数关系,相关系数为0.993 2,模型函数关系式为

图4 氟氯氰菊酯296 nm处荧光强度与紫外光降解时间关系
y=309.49211*exp(-x/22.01384)+26.46234
(3)
式中:x为紫外光作用时间,y为296 nm处荧光强度。
根据图(3)中采集得到的7个不同照射时间对应的样本荧光光谱,将其296nm处的荧光强度值分别代入式(1)中可计算得到降解后对应的氟氯氰菊酯溶液预测浓度值,再结合降解率公式(4),可求得降解率参数,结果如表2所示。其中,降解率的计算公式如下

表2 紫外光照射降解氟氯氰菊酯浓度变化及其降解率
(4)
式中:D为降解率,Ct为降解时间t作用后所对应的氟氯氰菊酯溶液浓度,C0为氟氯氰菊酯降解前的初始浓度。
为验证降解模型函数的准确性,在同等实验条件下分别对氟氯氰菊酯溶液进行紫外光照射2、4、9、17、24、44 min不同时间的降解,测量每次降解后的荧光光谱并获取296 nm处对应的特征峰荧光强度。根据推导出的降解模型函数关系式(3),将上述6个不同的降解作用时间代入此模型函数,可计算得到其对应的特征峰荧光强度预测值,并可进一步计算出回收率,具体结果如表3所示,分别列出了氟氯氰菊酯296 nm处实际荧光强度、由指数模型计算出的预测荧光强度以及回收率。统计可得这6个测试样本所对应的平均回收率为98.25%,由此可知紫外降解时间与296 nm特征峰荧光强度之间的指数函数模型准确性较高。
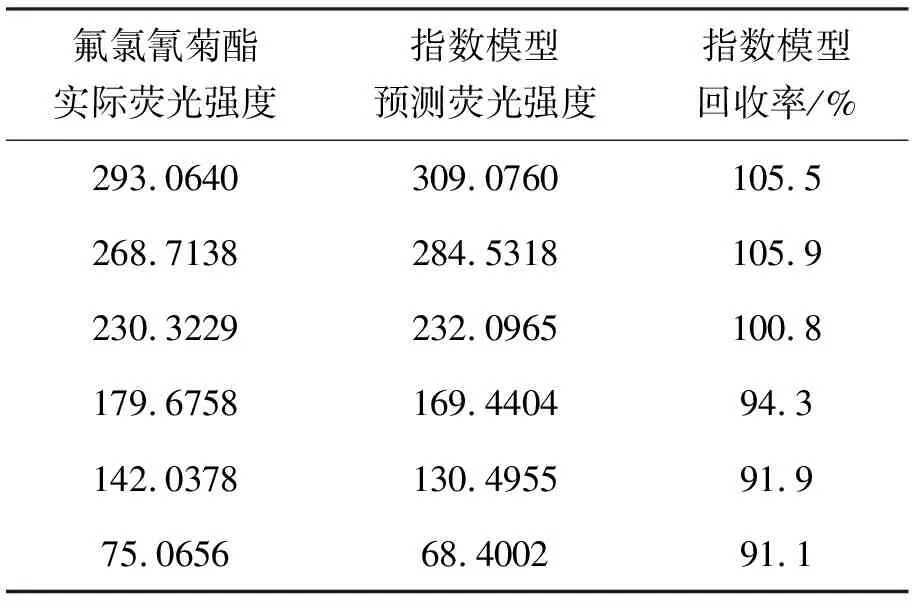
表3 紫外光降解氟氯氰菊酯指数函数模型性能参数计算
3 结束语
利用荧光分光光度计检测不同浓度氟氯氰菊酯的荧光光谱,其特征峰位置为296 nm。回归分析氟氯氰菊酯溶液的浓度值与特征峰荧光强度值并得到相应的预测模型函数。模型函数具有较好的相关系数、相对标准偏差和回收率。通过对氟氯氰菊酯溶液进行紫外光照射降解实验,得到降解时间与特征峰荧光强度之间的模型函数。实验数据表明此溶液特征峰的荧光强度随着降解时间的延长,逐渐减小,即降解率逐步提高。结果表明荧光光谱方法可以快速检测氟氯氰菊酯农药残留,且紫外光照射方法能够有效降解氟氯氰菊酯农药。研究结果对氟氯氰菊酯残留检测方法及其降解表征方法的选择具有一定的参考价值,下一步将会针对混合农药的残留检测及其同步荧光光谱法开展实验研究。
本文仅针对水源中的氟氯氰菊酯残留进行荧光光谱检测分析,基于这种方法同样可以实现在蔬菜、果汁等介质中的残留检测。

