心肺运动试验(CPET)精准预测功能状态良好的肺切除手术患者的术后并发症风险*
俞剑昀, 孙兴国, 卢 琳,包丽芳, 蒋 峻
(1. 浙江大学医学院附属第二医院心内科,杭州 310009;2. 浙江大学医学院附属金华医院电生理科,金华 321000;3. 中国医学科学院 北京协和医院国家心血管中心阜外医院 心血管疾病国家重点实验室,心血管疾病国家临床医学中心,北京 100037)
肺癌,是我国及全世界发病率和死亡率最高的恶性肿瘤之一[1,2]。胸腔镜肺切除术是早期非小细胞肺癌(non small cell lung cancer, NSCLC)的推荐优选局部治疗方式[2]。而肺切除术后并发症的发生率估计在5%到40%以上,这些并发症也影响患者的长期预后[3]。因此,所有拟行肺切除手术的患者都应该接受全面的术前评估。
症状限制性极限运动的心肺运动试验(cardiopulmonary exercise testing, CPET),作为无创、客观、定量、连续、可重复的临床检测方法[4],连续动态记录呼吸、循环、代谢及神经等多系统相互配合实现的气体交换,强调运动时外呼吸和细胞呼吸耦联,用整体整合生理学医学新理论体系对CPET 数据进行深度分析,目前已成为能够一次试验实现整体功能评估的唯一技术手段,是心肺代谢功能评估的金标准,也是评估有氧运动的最佳方法[5-12]。
CPET 是预测肺切除术及复杂高危麻醉手术风险的金标准[13-15]。但多数研究中所涉及的CPET 指标对肺切除术后并发症及死亡率的预测,都是基于肺部较大范围的手术及患者术前心肺功能较差的基础上。有学者认为用简易方式推算出峰值摄氧量(PeakO2)>15 ml/(min·kg)[13]、一氧化碳弥散量 (DLCO)和FEV1的预计术后值均大于60%[13,15]时手术风险低,不需要行CPET 检查。但是整体整合生理学医学体系认为CPET 适用于所有人[7,12]。为此我们对功能状态好的胸腔镜下肺切除手术患者,随访术后并发症,探讨术前CPET 客观定量指标能否精准预测术后并发症的风险。
1 对象与方法
1.1 研究对象
本研究选取浙江大学医学院附属金华医院2019年5 月至2019 年11 月期间,肺CT 诊断为“肺占位性病变”,入住胸外科完成CPET 后行胸腔镜下肺切除手术的患者共448 例,根据术后有、无并发症分为两个亚组。所有患者在行CPET 前均已签署知情同意书。
排除标准:资料不全者、不能配合完成检查者、入院时已明确患有除肺癌外的其它恶性肿瘤、曾行放化疗者、近3 月有脑梗塞、心肌梗死、外科手术史等。相关资料均从住院病历中获得。
1.2 随访及并发症确认
随访患者从术后至出院,记录分析并发症的发生情况。常规术后3~5 d 出院。
一般并发症:胸管持续时间≥7 d、术后感染、轻度心功能不全、肺不张;严重并发症:肺栓塞、呼吸衰竭、心力衰竭、脑部疾病及死亡[16]。
1.3 CPET 的操作与数据分析
患者检查前不停用任何日常药物[17]。采用德国耶格(Jaeger)公司MasterScreen-CPX 心肺运动系统,按照美国加州大学洛杉矶分校(Harbor-UCLA)医学中心标准完成CPET 及数据处理[11,18]。坐位完成静态肺功能检查(pulmonary function testing, PFT)后,连续监测心肺代谢指标,在功率自行车上静息3 min,以60~65 r/min 蹬车速率无负荷热身3 min,以 10~30 W/min 功率递增直至症状限制性的极限运动,继续记录≥6 min 的恢复情况[19]。无氧阈(AT)采用V-slope法[20]测得。PeakO2、Peak Work Rate 等均表示为实测值和占预计值的百分数(%pred=实测值/预计值×100%)[18-21]。
1.4 统计学处理
分类数据以百分比表示,计量资料用均数±标准差(最小值~最大值)(±s, min~max)表示,应用SPSS 软件进行数据处理。符合正态分布的计量资料,组间比较采用独立样本t检验,不符合正态分布的计量资料,组间比较使用Mann-Whitney U 检验[4]。计数资料组间比较使用卡方检验。危险系数 (OR)的计算使用Wald logistic 回归模型[22]。
2 结果
2.1 一般情况和PFT 指标比较
本研究448 例患者中高血压68(15%)例;糖尿病45(10%)例。
术后并发症随访时间(4.24±3.37,2~49) d。有并发症患者30 例,发生共9 种43 次并发症;最常见为胸管持续时间延长,共21 次;严重并发症10 次,其中死亡1 次。
无并发症亚组418 例和并发症亚组30 例比较,老龄、男性、吸烟、淋巴结转移、术后住院时间、空腹血糖和Rest SBP 组间均有统计学差异(P<0.05),并发症亚组上述指标较高呈正相关;FVC(%pred)、VC (%pred)和FEV1(%pred)也有统计学差异(P<0.05),并发症亚组上述指标较低呈负相关。而FEV1/FVC(%pred)、体重指数、静息舒张压(Rest DBP)和最大通气量(MVV)两亚组间无统计学差异(P>0.05,表1)。
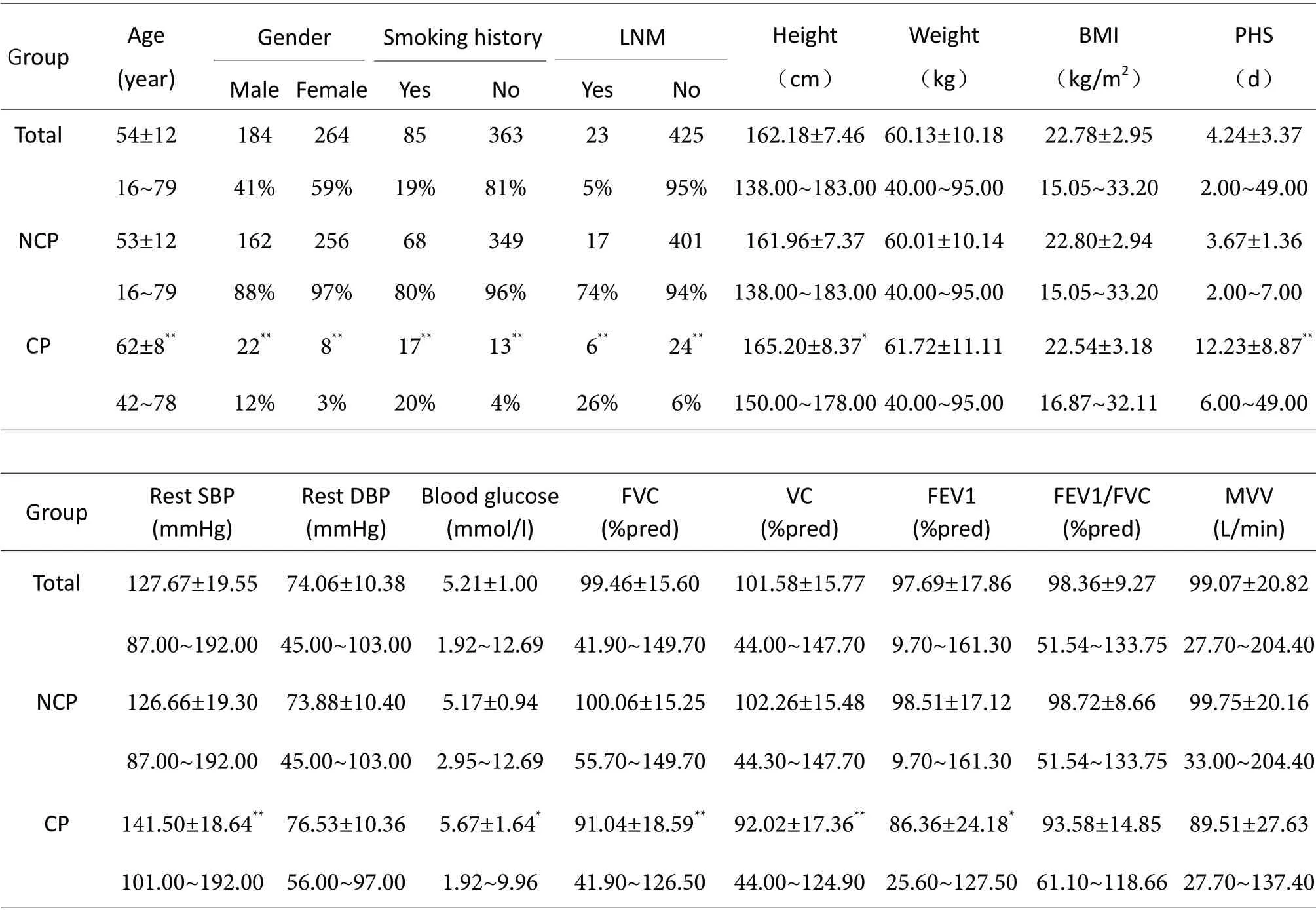
Tab 1. Comparison of general conditions and static pulmonary function test
2.2 CPET 核心指标比较
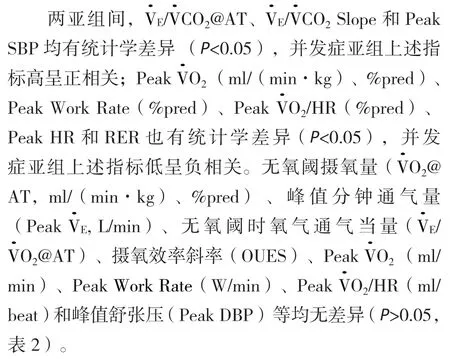

Tab. 2 Comparison of core data of CPET
2.3 CPET 主要指标的分切值及其OR

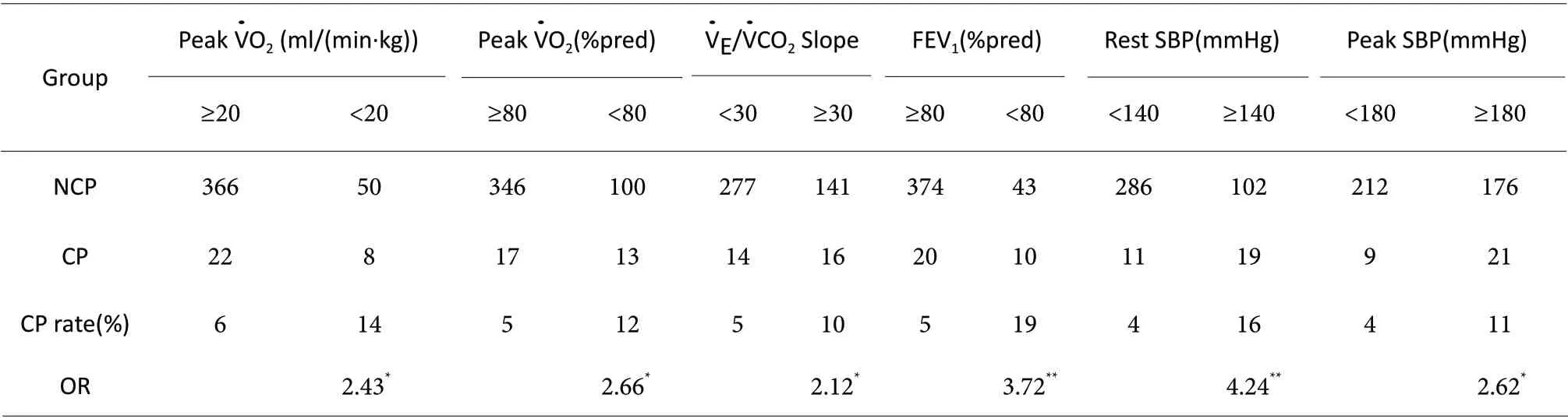
Tab 3. The best cut value and OR of the main indicators of CPET
2.4 术后死亡患者情况
患者男性67 岁,行全麻胸腔镜下左上肺叶切除+纵膈淋巴结清扫术,浸润性肺腺癌,肿块最长径2.1 cm,术后至死亡共28 d,术前有吸烟、高血压、糖尿 病 史,FEV1(25.6%pred) 、FVC(41.9%pred)、PeakO2(55%pred)和Peak Work Rate(53%pred)均低,Peak SBP(189mmHg)和Rest SBP(142mmHg)显著升高。上述指标均在本研究分切点的高风险区。
3 讨论
3.1 本研究患者心肺代谢功能状态好
并发症亚组年龄偏高,其中男性、吸烟及淋巴结转移占比偏高,此结果与一些学者的研究结果一致[3,23,24];空腹血糖及Rest SBP 也较高。根据整体整合生理学医学认为血压、血糖的升高是人体代偿反应,背后一定存在以“缺”为核心的需供不平衡和/或体内不同器官组织的局部与整体上不平衡的病理生理[6-8,25],故血压血糖高则术后并发症风险高。以Rest SBP(140 mmHg)和 Peak SBP(180 mmHg)分割的OR分别为4.24 和2.62 也证实了上述观点。且运动中过高血压虽提示心脏仍有代偿功能,但也存在显著相对需供不平衡,所以风险高。
所有患者PFT 均值基本正常,但并发症亚组的FEV1(%pred)、FVC(%pred) 和VC (%pred) 显著偏低,而换算成FEV1/FVC(%pred)后无差异,说明肺容量的降低对术后并发症有预测价值。虽然FEV1已逐渐失去了独立于其它参数单独预测部分肺切除手术风险的作用[14,26-29];但我们以FEV1(80%pred)分切所得的OR 为3.72,说明即使在前人认为肺切除手术低风险的人群中,低PFT 者依然存在较高术后并发症风险。

因此,胸腔镜肺切除手术前行CPET,若发现其指标低于正常及合并有其它能导致并发症风险增加的因素时,临床医生和护士必须引起足够的重视,干预其术前可调控因素,严格控制血压、血糖、血脂,嘱患者戒烟限酒、提高营养及整体功能状态,以更好的应对麻醉手术创伤[3];同时强调更严密的术中术后操作、监测和护理,以减少并发症发生[36]。鉴于全麻肺叶切除手术创伤大,而且肺部占位肿瘤切除后病理切片结果还可能是恶性癌变,患者的担忧可以想像必然都存在巨大精神心理负担,所以特别强调应该进行充分的心理疏导[37,38]。
3.2 本研究局限性

综上所述,在整体功能状态好的患者中,术前CPET 指标的降低可精准预测麻醉手术后并发症风险增加。高龄、男性、吸烟、高血压、高血糖和淋巴结转移等也提示并发症风险高。术前CPET 精准预测麻醉手术意外与并发症风险值得进一步深入研究,特别是严格质控、扩大病例数量和更广泛应用于整体功能状态较差患者。

