正常人和无睡眠呼吸异常慢病患者睡眠期间的呼吸源性心率变异初步报告*
王继楠,孙兴国△,谢友红,宋 雅,台文琦,周晴晴,张艳芳,石 超,徐 凡,刘 方,张 也,郝 璐,葛万刚,李 浩,徐丹丹
(1.重庆医科大学附属康复医院,重庆 400050;2.国家心血管病中心,中国医学科学院阜外医院,北京协和医学院心血管疾病国家重点实验室,心血管疾病国家临床医学研究中心,北京 100037;3.湖北省中医院,武汉 430061)
整体整合生理学医学理论认为任何生命活动的完成均需要呼吸、循环、神经体液、代谢等系统联合一体化调控才能实现,而呼吸、循环、代谢一体化调控是生命活动的核心[1-4]。动脉血液中的PaO2、PaCO2和[H+]a 等血气信号在呼吸过程中不是恒定的,而是随着呼吸呈周期性波浪式变化。使用超快反应氧电极、PCO2或pH 电极可记录到实验动物的动脉血液信号的波浪式曲线,并且在心功能正常和心力衰竭患者身上也能够证实波浪式信号的存在,这种周期性波浪式动态信号才是通过外周化学感受器进行呼吸调控的主要信号[5-9]。循环的主要目的是运输机体生命活动所必须的氧和代谢所需要的能量物质以及排出代谢产物,这个过程需要呼吸系统的协调配合;另一方面,血气信号的变化刺激化学感受器使自主神经活性变化,进而影响心率、血压、每搏输出量等循环指标的变异性[2-4]。生命活动的正常进行需要呼吸和循环的密切配合,二者相互影响、相互作用,才能维持机体能量代谢和内环境的稳态。因此,我们提出了所有循环指标变异性均为呼吸源性的吸气和呼气交替出现所致[1-9]。但是,心率是否随呼吸周期的变化而呈周期性波浪形变化尚无人体实验证据。
睡眠期间多导睡眠图(polysomnography, PSG)监测是一种有效的方法评估受试者是否患有睡眠呼吸暂停低通气综合征,此外它也能够实时动态、准确有效地监测患者夜间安静平稳状态下鼻气流、呼吸、心率、血压、血氧饱和度等指标[10,11]。而人体在入睡后至睡醒前,PSG 动态监测下呼吸和心电图R-R 间期心率变化之间的相互联系和相互作用却未见相关文献报道。循环系统和呼吸系统之间的一体化调控能否在夜间利用PSG 验证无从得知。故此研究利用PSG 监测夜间睡眠中各项指标,验证呼吸为循环指标变异的起源,进一步为整体整合生理学医学理论提供证据。
1 对象与方法
1.1 研究对象
本研究回顾性分析了在2014 年以来签署知情同意书后行心肺运动试验(cardiopulmonary exercise testing, CPET)和PSG 监测的8 例正常人和10 例无睡眠呼吸异常的慢性疾病患者。存在睡眠呼吸异常的慢病患者相关研究在本系列另一篇文章中分析报告[12]。正常人纳入标准:(1)既往和目前均无高血压、高血脂、糖尿病、冠心病、脑卒中等心脑血管疾病和其他疾病,临床无任何疾病诊断;(2)PSG 评估无睡眠呼吸暂停低通气综合征,呼吸暂停低通气指数(apnea hypopnea index, AHI)<5 次/小时。无睡眠呼吸异常的慢性疾病患者纳入标准:(1)既往明确诊断冠心病和(或)高血压和(或)糖尿病和(或)高脂血症等慢性病;(2)PSG 评估无睡眠呼吸暂停低通气综合征,AHI<5 次/小时。排除标准:心脑血管病急性期,妊娠期,认知功能障碍,下肢功能障碍等活动不便者。受试者在监测当日禁用镇静剂、咖啡、酒及茶等干扰监测结果的食物及药物。睡眠呼吸暂停低通气综合征,AHI ≥5 次/小时。
1.2 CPET 评估
1.2.1 CPET 的严格质控
使用意大利科时迈(COSMEDS.R.L.)公司Quark PFT Ergo 型全导联心电图、无创血压、血氧饱和度和气体交换为一体的心肺运动测试系统,评估心肺储备功能和运动耐力等整体功能状态。所有受试者签署知情同意书后进行检测。每天测试前进行气体容量定标、高中低三流速定标、空气校准、O2和CO2两点式系统自身定标及第三方代谢模拟器定标,以保证气体交换测定的精准度。所有定标通过方可进行检测[13]。
1.2.2 CPET 的规范化操作
受试者首先于坐位完成全套静态肺功能检查,然后采用自行车功率计进行动态心肺运动检查,检查全程记录12 导联心电图、无创血压、血氧饱和度、各项肺通气和气体交换等指标。按照Harbor-UCLA 医学中心标准连续递增功率方案,完成症状限制性最大极限CPET。静息3 min 后,以60 r/min 蹬车速率无负荷热身3 min。根据受试者年龄、性别和估计的功能状态,预设电磁自行车功率计的功率递增速率10~30 W/min,设定受试者在6~10 min 内达到症状限制性最大极限CPET,获得最大运动功率;然后继续记录≥ 5 min 恢复期数据[14]。
1.2.3 CPET 统一整体判读的数据计算分析
按照Harbor-UCLA 医学中心数据分析解读原则从生产厂家软件系统导出所有测定指标的每次呼吸(breath-by-breath) 原始数据进行每秒数据切割(second-by-second),然后进行10 s 平均数据用来制作孙氏新九图、无氧阈(AT)图和10 s 数据表格,并按照标准计算原则对峰值摄氧量(Peak V.O2, L/min,ml/(min·kg), %pred)、AT(L/min, ml/(min·kg),%pred)等核心指标进行分析[14,15]。
1.3 PSG 监测评估
1.3.1 PSG 方案
使用穿戴式SOMNOScreen 系统(SomnoMedics,德国)进行PSG 监测。受试者在病房连续监测两晚,第一晚供受试者适应设备及环境,第二晚正式记录检测数据。睡眠环境需温度适宜、光线适宜、安静、无干扰,女性受试者避开生理期。睡眠呼吸暂停的判断标准[16]:(1)睡眠呼吸暂停:睡眠过程中口鼻呼吸气流消失或明显减弱(较基线幅度下降>90%),持续时间≥10 s;(2)阻塞性睡眠呼吸暂停:口鼻气流消失,胸腹式呼吸仍然存在;(3)中枢性睡眠呼吸暂停:口鼻气流与胸腹式呼吸同时消失;(4)混合性睡眠呼吸暂停:在1 次呼吸暂停过程中,先出现中枢性呼吸暂停,后出现阻塞性呼吸暂停;(5)低通气:睡眠过程中口鼻气流较基线水平降低>30%并伴血氧饱和度下降≥4%,持续时间≥10 s;或口鼻气流较基线水平降低>50%并伴血氧饱和度下降≥3%,持续时间≥10 s;(6)AHI:平均每小时呼吸暂停与低通气的次数之和。
1.3.2 PSG 数据计算与分析
采用第二晚睡眠期间的数据进行计算。呼吸气流数据采样率为128 Hz。心电图R-R 间期的采样率为256 Hz,心率由R-R 间期计算而来,即心率(bpm)=60 000/R-R 间期(ms)。所有受试者在睡眠期间均会出现呼吸暂停或因体位改变导致短暂的鼻氧管松动甚至脱落,此期间未被记录的呼吸周期不会计算在内。同样因体位改变等原因导致的心电干扰不会计算在心率变异周期内。
1.3.2.1 呼吸相关数据计算与分析:呼吸周期、呼吸频率、平均呼吸周期时间
呼吸周期:气流流速为0 代表着呼吸切换。每一个呼吸周期气流流速从0 开始,流速小于0 时开始吸气,吸气速率逐渐加快后减慢至0,流速大于0 时开始呼气,呼气速率逐渐加快后减慢至0,一次吸气和一次呼气共同组成一个呼吸周期,详见图1a。呼吸周期数表示为B-1、B-2……B-n,B-n 为整个晚上的总呼吸周期数。
呼吸频率:每分钟呼吸次数。平均呼吸周期时间为睡眠总时间与B-n 的比值,即60/呼吸频率。
呼吸幅度:该设备能监测鼻气流流速、胸式呼吸和腹式呼吸三种方式的呼吸幅度,不能计算肺通气容量的绝对值,所以本文仅以鼻气流表示之。
1.3.2.2 心率变异性(HRV)相关数据计算与分析:心率、呼吸节律的HRV 周期时间(HRV-B-T)、和HRV 周期心率变化幅度(HRV-B-M)
整晚心率变异周期总数(HRV-n):与B-n 计算相似,我们取连续一次心率由最低点上升至最高点,再由最高点下降至最低点,为一次HRV;整个晚上的HRV 总次数为HRV-n,详见图1b。采用人工手动计算受试者在入睡后至睡醒前的心率变异周期总数。夜间心率较平稳且连续不断产生上下波动,一次HRV包括上升和下降,而上升和下降是连续成对出现的,只需计算波峰或者波谷的次数即为心率变异周期数。波峰的特征为连续三个数值中第二个数值为最大值。由于R-R 间期采样率为256 Hz,计算心率时会出现连续多个相同心率值,统计波峰个数时将连续相同数值默认为一个数值计算。心率变异周期数表示为HRV-1、HRV-2……HRV-n,HRV-n 为整个晚上总心率变异周期数。
心率:每分钟心跳次数。每个心率变异周期的心跳次数表示为心跳总数与HRV-n 的比值。HRV 率定义为每分钟HRV 次数,即60/HRV 心跳次数。
平均心率变异周期时间(HRV-B-T)和平均心率变异周期幅度(HRV-B-M):HRV-B-T=睡眠时间/HRV-n 的比值。HRV-B-M=心率出现上升下降变化时最低-最高(上升)和最高-最低(下降)2 个变化值(绝对值)取平均值,如图1b 所示。
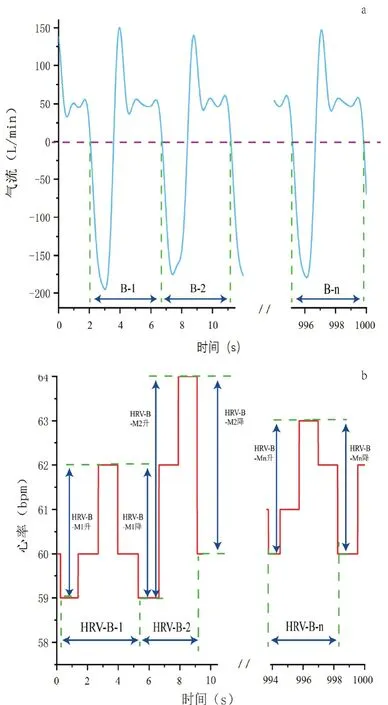
图1. 呼吸周期和心率变异周期示意图
1.4 统计学处理
本研究采用统计学软件SPSS 对相关数据进行处理和分析,连续变量以均数±标准差(±s)表示,分类变量以相对数和(或)百分比表示。组间连续变量采用独立样本t检验比较,分类变量比较采用Fisher 确切概率法。线图采用绘图软件Origin 绘制。
2 结果
2.1 所有受试者一般资料分析
本试验总共纳入18例受试者,其中8例正常人(男性4 名,女性4 名),10 例为无睡眠呼吸异常的慢性疾病患者(男性7 名,女性3 名),一般资料如表1所示。
正 常 人 年 龄(27.8±4.6 ,22~35) 岁, 身 高(171.6±7.0 ,161~182) cm, 体 重(68.8±14.7,50~103)kg,BMI 为(23.2±3.5 ,19.3~31.1),AHI为(1.7±1.3,0.1~4.3)次/小时。
无睡眠呼吸异常的慢性疾病患者年龄(52.0±15.6,26~72)岁,身高(169.5±6.1,160~180)cm,体重(74.1±15.6,54~105) kg,BMI 为(25.6±4.0,19.8~33.9),AHI 为(2.9±1.2,0.8~4.8)次/小时,其诊断信息详见表4。两组人群间比较年龄具有统计学差异(P<0.01),正常人显著年轻且均无任何临床疾病诊断;无睡眠呼吸异常的慢性疾病患者其余信息均与正常人无显著差异。
2.2 CPET 核心数据比较
2.3 正常人呼吸和R-R 心率的HRV 指标数据分析
正常人睡眠时长为(7.58±1.56,4.78~9.43)h,B-n 为(6581.63±1411.90,4804~8599)次,平均呼吸周期时间为(4.19±0.57,3.52~5.51)s,呼吸频率 为(14.56±1.74,10.89~17.04) bpm;HRV-n 为(6638.38±1459.46,4721~8784)次,睡眠期间心跳总数为(26719.00±5511.22,16592~33067)次,每个HRV 心跳数为(4.08±0.62,3.44~5.19)次,HRV率为(14.69±1.87,10.71~16.74)次/分,平均心率为(59.18±8.65,47.08~79.87) bpm,平均心率变异幅度为(5.74±3.21,2.33~10.17) bpm,平均心率变异周期时间为(4.16±0.62,3.58~5.60) s(表3)。
2.4 无睡眠呼吸异常的慢病患者呼吸和R-R 心率的HRV 指标数据分析
无睡眠呼吸异常的慢性疾病患者睡眠时长 为(8.33±0.69,6.78~9.17) h,B-n 为(7354.50±1443.50,5147~9812) 次, 平 均 呼 吸周期时间为(4.20±0.69,3.24~5.55)s, 呼吸频率为(14.68±2.33,12.48~18.51) bpm;HRV-n 为(7291.20±1399.31,5028~9455) 次,睡眠期间心跳总数为(28603.40±5249.11,20633~40133)次,每个HRV 心跳数为(3.97±0.56,3.09~4.84) 次,HRV率为(14.55±2.26,10.79~17.84)次/分,平均心率为(59.48±6.78,53.19~78.08)bpm,平均心率变异幅度(2.88±1.44,1.50~6.45)bpm,平均心率变异周期时间为(4.23±0.68,3.36~5.56) s(表4)。
2.5 无论是正常人还是慢病患者,只要没有睡眠呼吸异常则呼吸周期/心率变异比值接近1
正常人和无睡眠呼吸异常的慢性疾病患者各自的B-n 次数与HRV-n 次数、呼吸频率与HRV 率都基本相同、紧密相关,B-n/HRV-n 接近1,差异无统计学意义。无论是正常人还是无睡眠呼吸异常的慢性疾病患者,其平均呼吸周期时间和平均心率变异周期时间都基本一致,两组间均无统计学差异。同一受试者在同一晚呼吸频率较慢时心率变异周期次数少,在呼吸频率较快时心率变异周期次数相应增多,但是二者比值均接近1,如图2 所示。此外,不论是正常人还是无睡眠呼吸异常的慢性疾病患者,其心率变异的变化幅度和快慢与呼吸气流均存在相关性。当相对高通气时,平均心率较快,心率的变化幅度也相应较大;相对低通气时,平均心率较慢,心率的变化幅度也较小,此时的呼吸周期数和心率变异周期数依旧基本相同,如图3 所示。提示睡眠期间无睡眠呼吸异常时心率变异性基本上属于呼吸源性。

图2. 呼吸周期指数和心电图R-R 心率变异周期指数存在个体差异
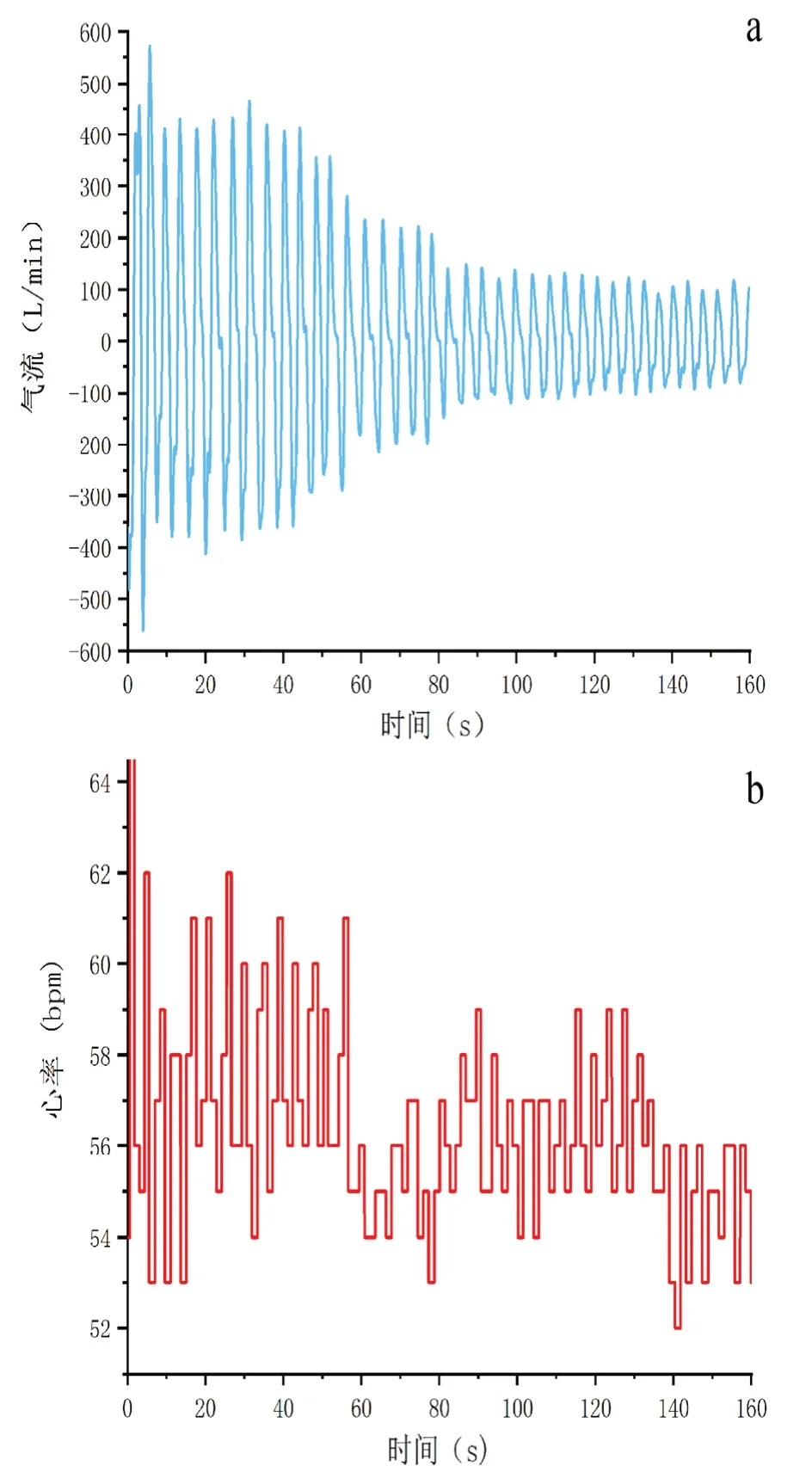
图3. 心率的变化幅度和快慢与呼吸气流均存在相关性
2.6 正常人HRV 幅度明显高于无睡眠呼吸异常的慢病患者
观察所有受试者夜间心率的变化,我们发现正常人心率变化幅度明显高于无睡眠呼吸异常的慢性疾病患者,且差异有统计学意义。并且不同受试者的心率变化幅度存在明显的个体差异,部分受试者心率变化幅度大,最高可达10.17 bpm,部分受试者心率变化幅度小,最低可至1.50 bpm。
3 讨论
3.1 本研究结果呼吸与心率变异之间密切相关,提示心率变异可能为呼吸源性
本研究发现所有受试者的B-n 次数和HRV-n 次数基本相同,B-n/HRV-n 接近1,心跳总和/ HRV-n无显著差异,平均呼吸周期时间和平均心率变异周期时间基本一致,呼吸频率和HRV 率存在个体差异。所有受试者心率的变化幅度存在个体差异。我们的研究结果显示,不论是正常人还是无睡眠呼吸异常的慢性疾病患者,心率变异均与呼吸节律呈波浪式变化,进一步为整体整合生理学医学理论/呼吸-循环一体化调控提供了临床人体实验证据。
Tab.1 正常人和无睡眠呼吸异常的慢病病人的一般资料分析(s)

Tab.1 正常人和无睡眠呼吸异常的慢病病人的一般资料分析(s)
M:男性;F:女性;BMI:体质量指数;AHI:呼吸暂停低通气指数
指标 正常人(n=8)无睡眠呼吸异常慢性疾病患者(n=10)P性别(M/F) 4/4 7/3 0.346年龄(岁) 27.8±4.6 22~35 52.0±15.6 26~72 0.000身高(cm) 171.6±7.0 161~182 169.5±6.1 160~180 0.524体重(kg) 68.8±14.7 50~103 74.1±15.6 54~105 0.494 BMI 23.2±3.5 19.3~31.1 25.6±4.0 19.8~33.9 0.214 AHI(次/小时) 1.7±1.3 0.1~4.3 2.9±1.2 0.8~4.8 0.072
3.2 正常人功能状态优于无睡眠呼吸异常的慢病患者
整体来说,本研究纳入的正常人年龄明显低于无睡眠呼吸异常的慢性疾病患者,因为参与本次试验的正常人多是于阜外医院工作或进修的年轻医生和访问学者,而无睡眠呼吸异常的慢性疾病患者多为于阜外医院就诊的年长患者,且合并多种慢性基础疾病。所有受试者进行CPET 发现,正常人PeakO2和AT 显著高于慢性疾病患者。PeakO2和AT 是反映心肺代谢整体功能的核心指标[18],证明正常人整体功能状态优于无睡眠呼吸异常的慢性疾病患者。但是,不论是何组受试者,均无睡眠呼吸暂停低通气综合征。因为合并此疾病的人群在夜间睡眠过程中频发呼吸暂停和(或)通气量降低,呼吸处于一种异常状态,呼吸和心率之间调控模式与无此疾病的人群显著不同。人体大脑皮层发出指令而做出的主动的、主观非自主神经控制的活动可以直接改变呼吸等功能状态,进而影响其他系统功能状态[19,20]。夜间睡眠过程中人体呼吸相对平稳,受自主神经(神经体液调节)和非自主神经(大脑皮层)调控作用弱,呼吸和心率不易受其影响,并且其他干扰因素少,是用来探讨呼吸与循环功能的绝佳时机。
Tab. 2 CPET 核心指标 (±s)

Tab. 2 CPET 核心指标 (±s)
Peak O:峰值摄氧量;AT:无氧阈;OUEP:摄氧通气效率峰值平2台:Lowest /CO2:二氧化碳排出通气效率最小值;/CO2 Slope:二氧化碳排出通气斜率;%pred:百分预计值=测定值/预计值×100%
指标 单位 正常人(n=8)慢性疾病患者(n=10) P Peak V.O2 L/min 2.1±0.6 1.4~3.1 1.5±0.4 1.0~2.5 0.031 ml/(min·kg) 31.3±7.8 21.6~49.1 19.9±3.3 15.0~25.0 0.000%pred 83.8±8.9 73.0~103.5 70.1±14.9 35.7~93.0 0.045 AT L/min 1.0±0.2 0.8~1.3 0.8±0.1 0.5~1.0 0.006 ml/(min·kg) 15.3±2.3 12.4~18.7 10.2±1.6 7.6~12.5 0.000%pred 77.5±9.9 68.1~101.0 60.7±8.3 52.7~76.9 0.002 OUEP ratio 44.6±4.7 36.2~49.3 35.1±6.6 26.8~46.9 0.005%pred 105.9±9.3 93.0~122.0 92.2±12.0 70.3~113.5 0.023 Lowest V.E/V.CO2 ratio 24.1±2.0 20.7~27.1 30.0±4.1 22.9~35.5 0.003%pred 96.8±7.5 86.9~109.1 109.5±10.3 94.2~129.7 0.014 V.E/V.CO2 Slope slope 22.7±2.5 19.1~27.7 27.8±4.1 20.7~33.1 0.011%pred 93.0±9.6 77.0~110.0 106.0±11.0 86.5~125.3 0.024
3.3 基于整体整合生理学医学相关的实验依据初步探讨呼吸源性心率变异发生机制
整体整合生理学医学理论认为,心肺调控是一体的,呼吸与循环功能相互影响,相互作用。现代医学多种临床实践已证实传统的“呼吸指标”在循环障碍患者病情严重程度、诊断和鉴别诊断、临床预后评估等方面均有很好的实用价值[5,17,18,21]。但是,呼吸与循环之间相互影响的具体机制却不甚清楚。我们本次的研究发现呼吸信号的周期性波浪式变化能够引起心率的上升下降变异。本研究中所有受试者夜晚睡眠期间呼吸周期数与心率变异周期数基本相同,二者比值接近于1,且平均呼吸周期时间和平均心率变异周期时间基本一致,说明心率的波浪式变化随呼吸节律出现,所以我们认为这种心率变异为呼吸源性的。此前孙兴国教授团队已成功通过连续逐搏取血的方法证实,新生儿在第一次自主呼吸前的氧气全部由脐带静脉运输,胎盘剥离后脐带动脉氧分压随时间逐渐降低,其到达触发呼吸的阈值时触发第一次吸气[22,23]。正常自主呼吸的人动脉血气PaO2、PaCO2、[H+]a 和SaO2均存在明显的波浪式信号,且高通气时血气信号的周期性波浪信号增强,憋气时变弱,但这一信号在静脉中很弱[5-7,22-24]。
Tab. 3 正常人呼吸和R-R 心率的HRV 指标数据分析 (,n=8)
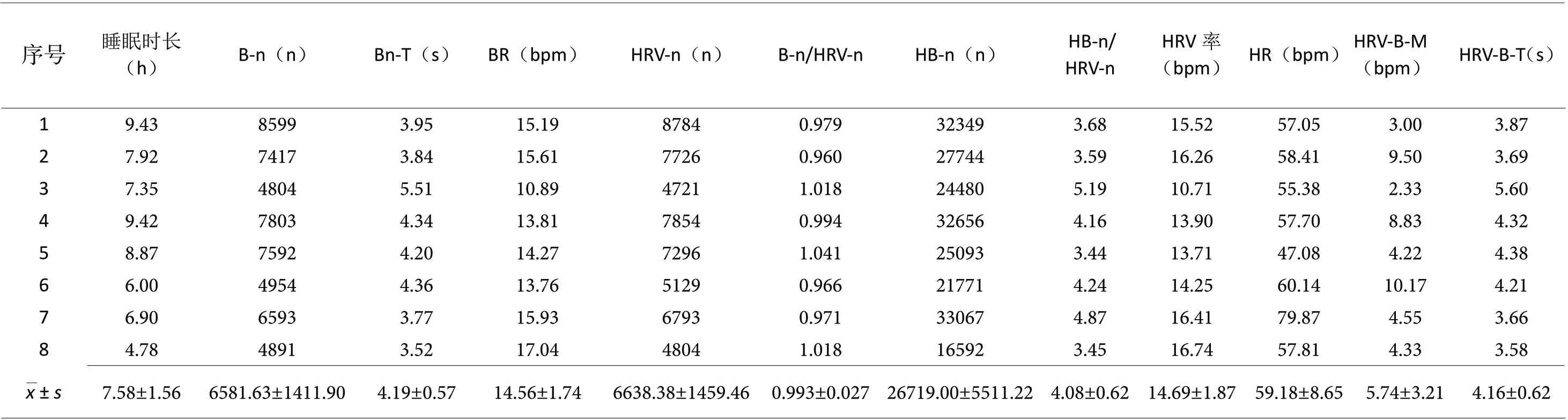
Tab. 3 正常人呼吸和R-R 心率的HRV 指标数据分析 (,n=8)
B-n:呼吸周期数;Bn-T:平均呼吸周期时间;BR:呼吸频率;HRV-n:心率变异周期数;HB-n:睡眠期间心跳总数;HB-n/HRV-n:每个心率变异周期内心跳次数;HRV 率:每分钟心率变异次数;HR:睡眠期间平均心率;HRV-B-M:平均心率变异幅度;HRV-B-T:平均心率变异周期时间
序号 睡眠时长(bpm) HRV-B-T(s)19.43 8599 3.95 15.19 8784 0.979 32349 3.6815.5257.05 3.00 3.87 27.92 7417 3.84 15.61 7726 0.960 27744 3.5916.2658.41 9.50 3.69 37.35 4804 5.51 10.89 4721 1.018 24480 5.1910.7155.38 2.33 5.60 49.42 7803 4.34 13.81 7854 0.994 32656 4.1613.9057.70 8.83 4.32 58.87 7592 4.20 14.27 7296 1.041 25093 3.4413.7147.08 4.22 4.38 66.00 4954 4.36 13.76 5129 0.966 21771 4.2414.2560.1410.17 4.21 76.90 6593 3.77 15.93 6793 0.971 33067 4.8716.4179.87 4.55 3.66 84.78 4891 3.52 17.04 4804 1.018 16592 3.4516.7457.81 4.33 3.58 ±s7.58±1.56 6581.63±1411.904.19±0.57 14.56±1.746638.38±1459.46 0.993±0.027 26719.00±5511.22 4.08±0.62 14.69±1.87 59.18±8.65 5.74±3.21 4.16±0.62(h) B-n(n) Bn-T(s) BR(bpm) HRV-n(n) B-n/HRV-n HB-n(n) HB-n/HRV-n HRV 率(bpm) HR(bpm)HRV-B-M
Tab. 4 无睡眠呼吸异常的慢性疾病患者呼吸和R-R 心率的HRV 指标数据分析 (,n=10)

Tab. 4 无睡眠呼吸异常的慢性疾病患者呼吸和R-R 心率的HRV 指标数据分析 (,n=10)
B-n:呼吸周期数;Bn-T:平均呼吸周期时间;BR:呼吸频率;HRV-n:心率变异周期数;HB-n:睡眠期间心跳总数;HB-n/HRV-n:每个心率变异周期内心跳次数;HRV 率:每分钟心率变异次数;HR:睡眠期间平均心率;HRV-B-M:平均心率变异幅度;HRV-B-T:平均心率变异周期时间*P< 0.05 与正常人比较
5249.113.97±0.56 14.55±2.2659.48±6.782.88±1.44*4.23±0.68化,冠心病7.6775503.6616.4177650.972265133.4116.8857.762.003.55 ±s左主干支架植入术后 6.785147 4.74 12.85028 1.024 21382 4.25 12.36 53.191.71 4.85 9 甲状腺结节,锁骨下淋巴结,心悸 9.178433 3.91 15.058566 0.984 32349 3.78 15.57 57.14.50 3.85 10 高血压,高血脂,糖尿病,动脉硬脑梗 8.839812 3.2418.5194551.03829208 3.09 17.8455.113.14 3.36 7室性早搏,高脂血症,高血压9.025849 5.55 16.025841 1.001 20633 3.53 10.79 56.531.50 5.56 8 高血压,高血脂,糖尿病,冠心病,高血压 8.156092 4.8212.4862750.97130345 4.84 12.8362.186.45 4.68 5高血压,高脂血症,糖尿病 8.336579 4.56 14.246392 1.029 26673 4.17 12.79 57.731.88 4.69 6 虚弱症,高血压,冠心病,腔隙性冠心病,高血压8.8284633.7515.9783551.013291413.4915.7954.982.563.8 4 HRV-B-M(bpm) HRV-B-T(s)1病毒性心肌炎,心力衰竭8.5789543.4517.4287661.021401334.5817.0578.082.573.52 2高血压,肺癌切除术后7.9366664.2813.9764691.03296574.5813.662.172.504.41 3序号 诊断 睡眠时8.33±0.697354.50±1443.504.20±0.6914.68±2.337291.20±1399.311.008±0.02428603.40±长(h) B-n(n) Bn-T(s) BR(bpm)HRV-n(n) B-n/HRV-n HB-n(n) HB-n/HRV-n HRV 率(bpm) HR(bpm)
我们认为人体呼吸活动使肺泡内PaO2和 PaCO2改变,通过肺毛细血管的PaO2、PaCO2及[H⁺]a 等血气信号产生同样的变化,在左心作用下经过约2~3 次心跳时间由外周化学感受器感受,再经上传神经上传,通过神经中枢环路刺激循环中枢从而引起心血管反射,改变交感、副交感神经张力,反馈调控窦房结和心肌的节律和兴奋性,进而使心率产生上升和下降的变异[2-4,25,26]。所以呼吸引起的血气信号波浪式变化能够产生心率变异,并且不同呼吸状态下心率快慢和心率变异幅度均有差异。高通气时,平均心率较快,心率的变化幅度也相应较大;低通气时,平均心率较慢,心率的变化幅度也较小,但是这种高通气和低通气只是相对而言,呼吸系统正常时也会出现,并未达到疾病程度。我们课题组另外一项分析夜间频发波浪式呼吸患者的初步研究提示,在波浪式呼吸期间,心率变异周期数较呼吸周期数减少,可能与患者动脉PaO₂、PaCO₂波浪式幅度降低有关[12]。
位于颈动脉体和主动脉体的外周化学感受器对低氧刺激敏感,位于延髓腹侧面和脑干的中枢化学感受器对高碳酸血症刺激敏感,低氧和高碳酸血症都可以激活化学感受器反射触发交感神经兴奋,使心率加快[27,28]。研究表明,急进高原后的低氧状态会引起心率明显增快[29,30]。这是由于缺氧导致动脉血PaO2下降,循环系统将缺氧信号经外周化学感受器上传至交感神经,从而使心率加快。我们的前期研究发现,阻塞性睡眠呼吸暂停的特征是睡眠期间有呼吸暂停发作,并伴有不同程度的低氧血症和高碳酸血症,且呼吸暂停事件发生期间和之后即刻有心率、血压异常急剧上升[31]。间歇性发作的低氧和二氧化碳水平升高可引起交感神经活动的激增和相关心血管变化,妨碍心血管系统的正常自主调控[32-35]。在正常呼吸时是否也存在这个趋势,即血气信号PaO2下降时心率上升,我们不得而知,需要进一步的试验验证。目前国内外关于心率变异性的研究集中于心电图中的R-R 间期变异性,常被用来评价自主神经功能,呼吸源性的心率变异相关临床应用需要我们进一步探索[36-38]。
3.4 正常人心率变异幅度高于无睡眠呼吸异常的慢病患者
我们的研究发现,正常人心率变异幅度显著高于无睡眠呼吸异常的慢病患者,同时心率变异幅度也存在明显个体差异,部分正常人显著高于慢性疾病患者。这些差异提示其可能与受试者性别、年龄、日常活动耐量、生活环境和疾病状态等有关,值得我们进一步深入研究。正常人心跳总和/HRV-n 高于慢性疾病患者,表示每个心率变异周期内正常人心率次数多于慢性疾病患者,差异没有统计学意义。
3.5 本研究局限性
鉴于本次研究纳入的受试者样本量相对较小,研究结果可能存在一定的偏差,今后的试验可以进一步扩大样本量进行,可能更便于发现差异。心率变异相关数据为人工计算,结果可能存在一定误差,今后将编写软件实现电脑计算。此外,因受试者在睡眠期间出现呼吸暂停或因体位改变导致短暂的鼻氧管松动甚至脱落,及心电干扰等情况使呼吸周期或心率变异的计算产生误差。并且此次研究观察到的仅是呼吸与心率变化之间存在的现象,未能深入到发生机制的探讨。
综上所述,呼吸周期数与心率变异周期数存在高度显著的一致性,平均呼吸周期时间和平均心率变异周期时间也是高度一致,实验验证了整体整合生理学医学理论所提出的正常呼吸期间心率变异起源于呼吸的假说,也是对完善整体整合生理学医学呼吸、循环、代谢等所有系统一体化调控机制的有力支撑。在未来的医学发展方向上,我们要秉承“以人为本”的观点,构建以整体论为背景的现代创新医学模式-整体整合生理学医学,实现真正的慢病与健康防治康养一体化管理。

