基于PET/CT模拟定位系统的靶区勾画对老年食管癌调强放疗心脏的剂量学研究
王璐
(九江市第一人民医院肿瘤科,江西 九江 332000)
食管癌是我国常见的恶性肿瘤,2018 年中国癌症报告显示,食管癌在全国恶性肿瘤中发病率居第6 位,死亡率居第4位,且发病中位年龄为55岁,>60岁的老年患者占比约为63%[1]。我国食管癌病理类型以鳞癌为主,食管鳞癌对放疗较敏感。RTOG8501 奠定了同期放化疗在食管癌中的治疗地位,在局部晚期的食管癌治疗中,放疗是主要治疗手段。老年患者因体质或其他基础疾病,其基础心功能较差;而食管在解剖上毗邻心脏,在食管癌放疗过程中,心脏不可避免受到一定剂量的照射,心脏受照射剂量较高将对心脏功能造成进一步的损伤[2]。老年食管癌患者因心功能受损而中断或终止放疗是临床是常见的原因,放疗后因心衰致死的发生率逐年升高。目前临床上常用的是计算机断层扫描仪(CT)定位系统,但在国内采用PET/CT模拟定位系统治疗食管癌的研究较少。基于此,本研究开展基于PET/CT模拟定位系统的靶区勾画对老年食管癌调强放疗心脏的剂量学研究,现报道如下。
1 资料与方法
1.1 临床资料 选取2019年1月至2020年6月本院收治的30 例老年食管癌患者,均进行靶区勾画,将实施PET/CT 模拟定位系统16例患者纳入A组,将实施CT模拟定位14例患者纳入B组。A组男8例,女8例;年龄61~78岁,平均年龄(68.71±2.12)岁;病程1~3年,平均病程(2.13±0.05)年;病灶分布:食管上段5 例,食管中段6 例,食管下段5 例;根据AJCC 第八版癌症分期系统[3]进行分期,cTNM 分期:T4N0M0 8例,T4N1M0 5例,T4N2M0 3例。B组男7例,女7例;年龄61~79 岁,平均年龄(68.16±2.19)岁;病程1.50~3.50 年,平均病程(2.15±0.03)年;病灶分布:食管上段4 例,食管中段6 例,食管下段4 例;cTNM 分期:T4N0M0 7 例,T4N1M0 4例,T4N2M0 3例。两组性别、年龄、病程、病灶分布、TNM分期等临床资料比较差异无统计学意义,具有可比性。本研究均经过医学伦理委员会批准。
1.2 诊断标准 符合《内科学》[4]中的诊断标准:X线检查表现为食管黏膜皱襞紊乱、中断、局部管腔狭窄,充盈缺损,管壁僵直,蠕动消失或见软组织阴影等病变;且经临床病理检查确诊为鳞癌。
1.3 纳入及排除标准 纳入标准:符合上述诊断标准;美国东部肿瘤协作组(ECOG)评分0~1 分;年龄>60 岁;治疗前心功能分级(NYHA分级)≤1级;治疗前完善心电图、心脏超声等检查;患者及家属均知情并签署知情同意书;卡氏评分(KPS)≥70 分;无穿孔,无瘘,无破溃至纵隔的深溃疡。排除标准:腺癌、小细胞癌者;不能接受根治性放疗/放化疗者;合并其他恶性肿瘤者;患精神以及意识障碍疾病者;合并免疫功能异常者;心脏、肝脏、肾脏、脊髓等功能异常者;传染性疾病者。
1.4 方法 两组定位前患者均空腹>6 h,遵医嘱排空膀胱。1.4.1 B组 采用CT定位:定位过程中患者保持仰卧姿势,伸直双臂放于体侧或交叉双肘放于额前。采用头颈肩罩固定颈段和上段者,采用癌体膜固定中下段和食管胃交界。食管下段和食管胃交界处,会被呼吸和心脏等器官运动影响,可使用四维模拟CT(4D-CT)实施定位,定位过程中观测肿瘤实际运动偏移情况,提升放疗精度。除造影剂过敏者外在静脉造影增强扫描时,层厚0.5 cm,扫描完整的肿瘤病灶、锁骨上、双侧颈部和双肺等范围,结束后将图像输送到TPS。
1.4.2 A 组 采用本院PET/CT 模拟机定位:使用同一热塑体膜进行体位固定,使用GAMMEX 放疗定位灯进行定位,注入18F-FDG,医嘱患者静卧休息60 min,排空小便后仰卧检查床上,先行CT 扫描,使用上海联影uMi510,再行PETCT扫描,扫描后直接传送TPS系统进行靶区勾画。
1.4.3 靶区勾画 两组均由某一固定的放疗科医师分别勾画患者CT 及PET-CT 模拟机定位图像。阳性淋巴结靶区(GTV)为肿瘤区和阳性淋巴结靶区,在食管造影片的影像学及食管镜或腔内超声内窥镜下明确肿瘤情况。纵膈窗及肺窗CT片全面呈现原发肿瘤的大小为GTV,CT片显示肿大淋巴结[如肿大淋巴结远离原发病灶或/和触诊可确定的转移淋巴结部位如锁骨上淋巴结、气管旁淋巴结确诊转移或不能除外转移的淋巴结(GTVnd)],放置银夹标记后,GTV以银夹标记的上下界为准;CTV为高危靶区,包括GTV和GTVnd+预防照射的淋巴引流区(隔断食管癌靶区勾画的标准和CTV2相同)。GTV外放到CTV的标准是食管纵轴上下3~5 cm,前后左右l cm。上下外放更多的原因为食管黏膜下常见肿瘤漫润,甚至可能存在多原发病灶。阳性淋巴结GTV外放到CTV的边界为0.5~1.0 cm。由主治医生根据病灶的浸润和运动情况决定具体范围[5]。使用ELEKTA Synergy VMAT 肿瘤放疗设备,应用飞利浦Pinnacle3 TPS逆向调强方式,布野方式采用7 野方式,处方剂量:PTV 61.4 Gy/34 Fx,限量器官脊髓Dmax<40 Gy,双肺V20<30%,V30<20%,心脏心脏受照30 Gy 的体积(V30)<40%,心脏受照30 Gy 的体积(V30)<30%。对勾画靶区和危及器官进行优化剂量计算,比较CT图像和PET/CT 图像心脏平均剂量Dmean 及V30、V40 照射剂量。两组均于治疗结束后完善心电图、心超检查,评估心功能分级。
1.5 观察指标 心脏平均剂量:对勾画靶区和危及器官进行优化剂量计算,比较CT图像和PET/CT图像下GTV、PTV的心脏Dmean、V30、V40照射剂量。
1.6 统计学方法 采用SPSS 20.0统计软件进行数据分析,计量资料以“±s”表示,比较采用t检验,以P<0.05为差异有统计学意义。
2 结果
计算后,A组GTV Dmean、PTV Dmean及V30、V40照射剂量均低于B组,差异有统计学意义(P<0.05),见表1。
表1 两组心脏平均剂量比较(±s)
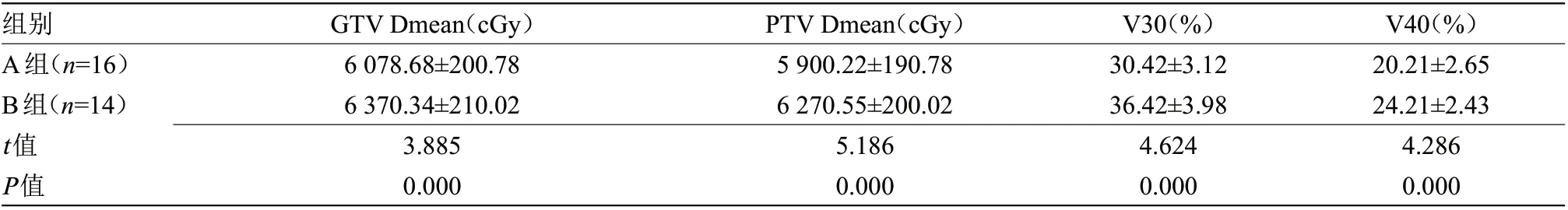
表1 两组心脏平均剂量比较(±s)
注:GTV Dmean,心脏平均剂量;PTV Dmean,计划靶区心脏平均剂量
组别A组(n=16)B组(n=14)t值P值GTV Dmean(cGy)6 078.68±200.78 6 370.34±210.02 3.885 0.000 PTV Dmean(cGy)5 900.22±190.78 6 270.55±200.02 5.186 0.000 V30(%)30.42±3.12 36.42±3.98 4.624 0.000 V40(%)20.21±2.65 24.21±2.43 4.286 0.000
3 讨论
处于早期食管癌阶段的患者不存在较显著的症状表现,患者多出现胸骨后不适感、灼烧感、针刺或牵拉样痛感,且会存在食物缓慢通过、滞留或轻度哽噎感,不同患者症状和持续时间存在差异。食管癌中晚期表现为进行性吞咽困难、食物反流、腋下疼痛等症状。放化疗是高龄食管癌患者的主要治疗手段,但会对正常心脏组织造成一定的损害,且影响患者肺功能[6]。
孙利平等[7]研究表明,放疗在减少乳腺癌局部复发的同时会引起心脏放射损伤。损伤一旦出现通常是不可逆的,放射性心脏病(RIHD)已成为长期生存患者的主要非乳腺癌死亡原因。降低心脏受照剂量和体积能预防RIHD 的发生。李安华[8]研究指出,经受肿瘤放疗后引起的心脏毒性损伤是导致肿瘤生存患者死亡的主要原因,主要包括左心功能不全、心力衰竭、系统性高血压等。目前,随着放疗技术的发展,靶区的精确勾画能作为药物精确投放的前提,因此,高剂量区及靶区于三维方向上满足形态一致性,靶区药物使用剂量为最优选择,靶区外缘剂量骤减,才可达到增强治疗效果,且减弱损害正常心脏组织程度的目的[9]。目前,勾画食管癌靶区的范围暂无统一的金标准,常规的靶区勾画采取的手段主要有食管内镜超声(EUS)、钡餐、CT。其中CT 定位系统临床应用范围较广泛,能获得正常组织和病变组织间的三维图像和解剖关系,是食管癌诊断和分期的重要手段。但单纯用形态学特征进行食管癌诊断误差较大,如在淋巴结炎性增大时假阳性出现率较大,且正常体积的转移淋巴结也会表现为假阴性;同时,在实施CT定位勾画靶区时,不同的放疗科医生间存在明显的差异。目前CT勾画靶区出现较大差异的原因如下:①靶区过大,其中肿瘤受照面积及剂量过大,周围的正常组织受照面积及剂量剂过大;②过小靶区,因靶区小造成肿瘤漏照或受照剂量不足。故使用CT明确勾画靶区时还需参考相关影像资料。
目前,核磁共振血流量扫描(MRS)、单光子发射计算机断层成像术(SPECT)、正电子发射型计算机断层扫描仪(PET)等功能影像学检查与融合CT下对靶区进行勾画能反映肿瘤代谢功能和解剖功能的高效结合,称为生物靶区。在靶区勾画中,GTV 的靶区勾画最重要,GTV 不仅对CTV 以及PTV的勾画形态起决定作用,还可利用GTV的合理剂量,明确肿瘤分期及疗效。其中正电子发射型计算机断层扫描仪/计算机断层扫描仪(PET/CT)模拟定位系统受限于融合图像误差和经济成本尚未在临床普及。勾画靶区中另一个重要的内容是确定淋巴结转移范围。当前诊断淋巴结转移的标准是受累淋巴结伴随体积增大,且CT横断面图像表现为直径≥10 mm 或15 mm,即按照受累淋巴结直径范围判断淋巴结是否出现转移,存在一定的误差。而PET能有效探测正常体积大小或体积增大的淋巴结,其大小的变化也不会影响探测转移淋巴结的结果,其淋巴结转移探测的特异性和敏感性均高于CT探测。因此,PET/CT在二者联合下进行转移淋巴结的探测,可更有效提升探测敏感性,且能准确显现淋巴结大小、结构、代谢改变情况,提高转移淋巴结诊断的准确性。于洋[10]研究表明,PET/CT显像用于膀胱肿瘤显像中,能较好的诊断出阳性淋巴结病灶转移情况,且显示邻近组织的浸润效果较好,在指导临床诊断和了解肿瘤病变具有重要参考价值。
本研究结果显示,计算后,A 组GTV Dmean、PTV Dmean及V30、V40照射剂量均低于B组,与张璋等[11]研究结果一致,表明应用PET/CT 融合图像相比单纯CT 勾画的靶区可提高靶区的精确性,并改善靶体积和危及心脏器官的照射剂量,降低对放疗对心脏产生的毒性。分析原因为,基于PET/CT模拟定位系统的靶区勾画实现了解剖成像与功能成像的融合,当前的PET/CT 已具备5~7 mm 的系统分辨率,明显弥补了单纯PET图像模糊的不足,且融合图像下所明确的靶区能清晰且准确地区分肿瘤组织和非肿瘤组织,PET/CT模拟定位系统下能更准确的提供肿瘤大小、位置信息,尤其是对转移淋巴结的判断具有显著的提示作用,提高了放疗靶区的准确性,为应用PET/CT制订放疗计划做好充分的前期准备。既往有研究[12]表明,PET/CT 模拟定位系统在区分肿瘤组织与炎症、判断局部复发与残留、发现潜在转移病灶等方面有显著的优势,能减少不同医师间靶区勾画的差异。因此,基于PET/CT模拟定位系统的三维治疗计划可勾画更精准的靶区;给予靶区更高剂量分布同时更好的保护危及器官;放射科医生在实施治疗计划的过程中可依据靶区调整射野分布,最大可能给予靶区高剂量、正常器官低剂量。蒋亚齐等[13]研究表明,CT 下勾画靶区GTV 明显高于PET/CT GTV;CT下肺、心脏、食管、脊髓的受量均高于PET/CT;而两者勾画GTV PET/CT比较差异无统计学意义。表明PET/CT可更好地降低肺、心脏、食管、脊髓的受量,保护周围正常组织和器官,并能明显减少不同放疗科医师勾画靶区的差异,降低放疗毒性程度,利于改善预后。
综上所述,在食管癌患者中应用基于PET/CT模拟定位系统的靶区勾画,能有效降低危及心脏器官的照射剂量,减少对心脏功能的损伤。

