铁钼法甲醇制甲醛催化动力学研究及反应器模拟
邵青楠,迟子怡,李学刚,肖文德
(上海交通大学 化学化工学院,上海 200240)
甲醛(HCHO)是一种重要的化工原料,也是C1化学的基石。 其主要用于生产“三醛”树脂、1,4-丁二醇、聚甲醛、乌洛托品、二苯甲烷二异氰酸酯(MDI)等化学品。 目前,我国已成为世界最大的甲醛生产与消费国,预计到2022年,国内需求量将超过2800× 104吨[1]。 工业上,甲醛由甲醇催化氧化制得,有银法和铁钼法两种工艺,分别采用银和钼酸铁催化剂。 相比于银法,铁钼法的反应温度低,甲醛浓度高,具有成本低、产量大等优势[2]。 而国内现有甲醛装置大多采用银法工艺,铁钼法技术及催化剂则依靠进口,制约了该法在我国的发展[3]。 为适应近年来大规模生产高浓度甲醛的需求,开展铁钼法甲醛生产工艺研究意义重大。 甲醇氧化为强放热反应,对操作条件非常敏感。 工业上采用列管式反应器控制温度,同时确保进料低于甲醇空气混合物的爆炸极限,但在实际操作中仍易引发局部过热而使催化剂失活,工艺条件的限制也导致甲醛生产率较低亟待提高。 为进一步提升铁钼法工艺水平,需要进行准确的反应器动力学模拟和工艺条件研究。
目前,国外已对该反应的动力学和反应器建模进行了报道。Soares等[4]综述了甲醇氧化反应的机理和动力学,该反应遵循氧化还原(Redox)机理,催化剂中的晶格氧参与反应,气相氧再补充表面耗尽的晶格氧。Santacesaria等[5]在低于250 °C的无梯度反应器中进行实验, 根据该机理拟合了动力学方程。Windes等[6]也采用该机理建立了动力学模型,并由此建立了一维非均相和二维拟均相固定床模型。Diakov等[7]以幂级数模型研究了甲醇氧化反应动力学,认为甲醇与氧气的级数分别为0.5与0。 Deshmukh等[8]在微分反应器中,测定了230~260 °C温度下HCHO、CO、二甲醚(DME)、二甲氧基甲烷(DMM)的生成速率,假设存在两种活性位点,建立了基于L-H机理的动力学模型。 Partopour等[9]采用该动力学模型,对空气进料下装填不同形状催化剂的固定床进行了CFD模拟,结果表明圆环形颗粒具有最佳的反应转化率和选择性。 然而前人的研究大多是在低甲醇浓度与空气进料条件下进行的,且考察的温度也低于实际生产的反应温度,难以指导工业条件下的甲醛生产。
本文基于铁钼商用催化剂, 在250~350 °C温度范围与循环尾气进料组成下,研究了甲醇氧化制甲醛的反应动力学,建立了反应管的二维轴对称模型,并研究了各工艺条件对反应器性能特别是热点温度的影响。
1 催化动力学研究
1.1 实验部分
1.1.1 主要试剂及催化剂
甲醇(99.5%),上海凌峰化学试剂有限公司;氮气(99.9995%),液化空气(上海)有限公司;氧气(99.5%),液化空气(上海)有限公司;催化剂为某10× 104吨/年甲醛生产商提供的Fe-Mo圆环形催化剂,尺寸为4.5 mm × 4.5 mm × 1.3 mm (直径 × 高度 ×壁厚)。 对催化剂进行了XRD与ICP表征,其组成为Fe2(MoO4)3与MoO3,铁和钼质量分数分别为13.4%和56.9%,n(Mo)/n(Fe)比为2.48。
1.1.2 实验装置及方法
实验装置如图1所示,反应器为盐浴U型管固定床反应器。 催化剂经研磨后筛选出0.3 g的粉末(80~100 目),与适量石英砂混合均匀后装填。 由平流泵计量的甲醇和流经质量流量计的氮气、氧气混合后进入预热器加热,而后进入U型管内反应。反应器出口气体由针阀控制, 部分流入色谱做定量分析,其余经尾气处理后排空,装置出口为常压。 在实验条件下气流的线速度很大且催化剂粒径较小,已消除了内外扩散的影响。
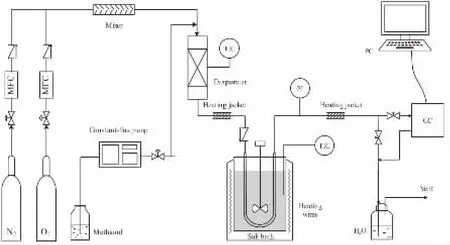
图1 甲醇制甲醛实验装置
气体组成由配有热导池检测器(TCD)的GC9560气相色谱仪测定, 分别由MolSieve 5A柱分离N2、O2与CO,Porapak Q柱分离甲醛、甲醇、二甲醚与水。 氩气作载气, 压力为0.3 MPa,5A分子筛柱温为50 °C,Porapak Q柱以10 °C/min从110 °C程序升温至150 °C。
1.2 实验结果与讨论
1.2.1 甲醇氧化反应特征
在铁钼法工艺中,甲醛仅通过甲醇的部分氧化产生,反应式为:
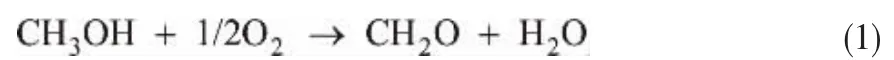
副产物主要有CO和DME,且在不同条件下还可能产生少量CO2、DMM、甲酸和甲酸甲酯[4],在实验条件下以上物质浓度极低难以被检出,因此仅考虑浓度较高的CO和DME。甲醇和水在反应中会占据甲醛的吸附位点从而抑制甲醛进一步氧化,故CO主要由甲醇的直接氧化生成[10,11],见反应式(2)。 同时,该过程还会发生甲醇的可逆脱水反应生成DME,如反应式(3)所示。
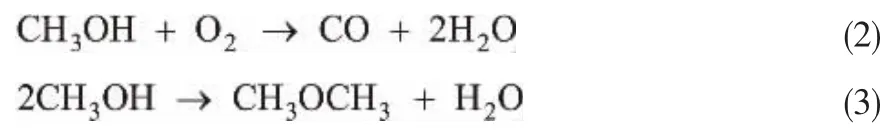
甲醇在空气中的爆炸下限为6.7%,目前工业上使用循环尾气代替空气进料,将氧含量(物质的量分数,下同)由21%降低至10%,从而允许更高含量的甲醇进料,国外先进的技术设计值已达到11%[12]。图2和3所示分别为甲醇和氧气含量的影响。 提高甲醇与氧气含量,甲醇转化率和甲醛收率都增加,但当氧含量不足时,甲醇转化率和甲醛收率均迅速下降,副产物增多。 此时,甲醇将消耗催化剂中的晶格氧使其活性下降,故该反应需确保氧气相对过量,但不超过13%的安全限值[12]。
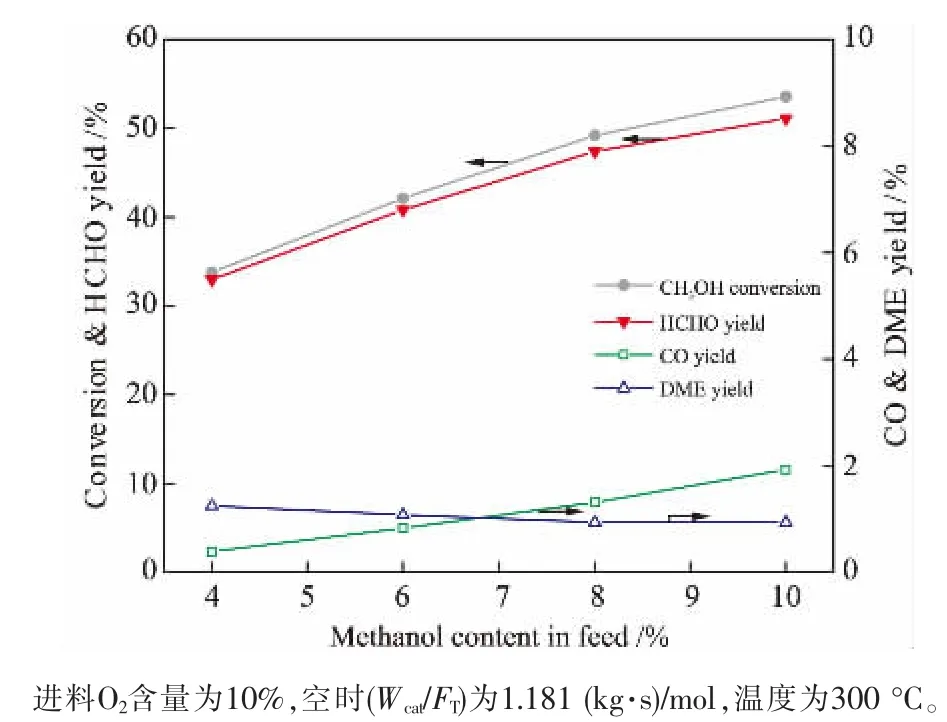
图2 甲醇含量对转化率及产率的影响

图3 氧气含量对转化率及产率的影响
1.2.2 动力学模型
甲醇制甲醛反应遵从Mars-van Krevelen机理[13],其中催化剂的表面晶格氧为反应活性位点,可将吸附的甲醇氧化为甲醛并生成氧空位,该步为反应的控速步骤。 之后气相氧又将其重新氧化至初始状态,使晶格氧得以循环。 这两步反应可表示为:
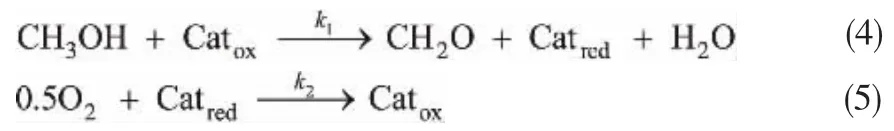
式中,Catox与Catred分别表示氧化态与还原态的催化剂,对应的反应速率为:

当反应达到稳态时,二者速率相等,即:
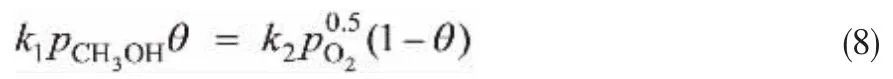
由此可求出氧化态的分率θ,代入式(6)即可得到该机理的动力学方程:
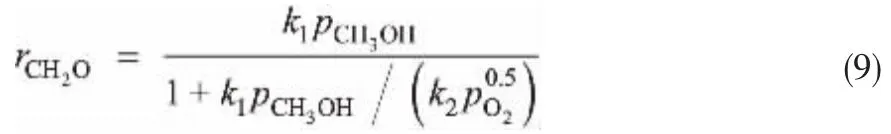
副反应可采用类似形式的速率方程,即反应速率正比于催化剂表面晶格氧分率θ[14]。 Cheng[10]的研究表明,甲醇氧化为CO对甲醇为0.5级,对氧气为0.1级。 本文实验发现,在氧气过量条件下,该反应对氧含量变化不敏感,且甲醇的反应级数为0.5,故将该反应动力学表示为:
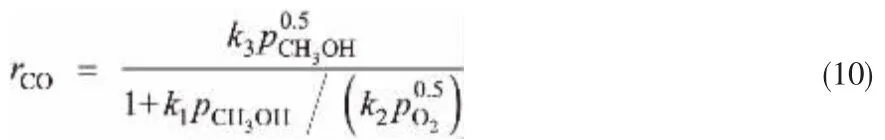
Soares[11]和Moustafa[14]报道了铁钼催化剂上甲醇脱水反应的速率方程,认为该反应对甲醇为2级,且遵循SN2机理。 此外甲醇生成DME是一个可逆反应,可将其动力学方程表示为:
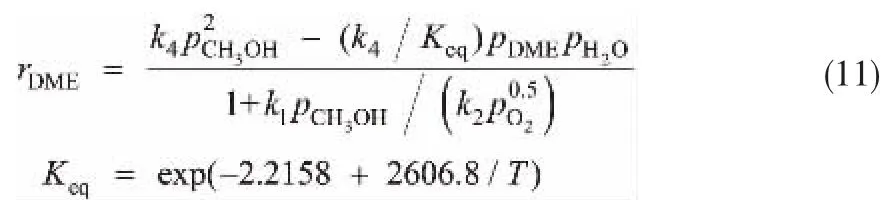
所需拟合的动力学参数为式(9)~式(11)中各ki的指前因子ki,0与活化能Ei。 为降低模型强非线性所带来的计算复杂性, 将Arrhenius方程改写为如式(12)所示形式,式中,T0为参考温度,其值为573.15 K。
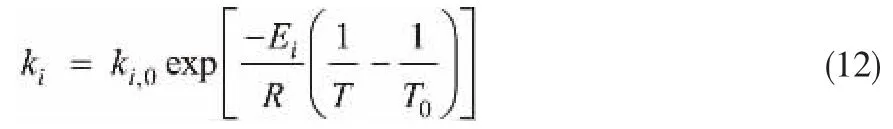
1.2.3 模型参数拟合
对于小管径U型管反应器, 搅拌的盐浴可使反应热被及时移走,最大限度地消除温度梯度,故可认为床层温度均匀且等于盐浴温度。 反应气流在管内的流动视作平推流,床层压降很小可忽略不计。 基于以上假设,对于任意组分i,其反应速率Ri可表示为:

式(13)中初始条件为反应器入口组分的物质的量分数,如式(14)所示:

本文通过Matlab对动力学参数进行求解。 采用ode45函数对式(13)积分,再由非线性最小二乘法拟合得到各参数。 参数估计的目标函数为各组分物质的量分数的残差平方和,如式(15)所示。式中,wi为组分i的权重,由于CO和DME浓度较低,计算时取w为10。

参数的拟合结果如表1所示,实验测定值与模型计算值的对比如图4和图5所示。 可以看出,在各温度条件下,各实验测定值与模型计算值之间吻合良好。 对动力学模型进行统计检验,分别计算决定性指标ρ2及回归均方和与模型残差均方和之比F。经计算,ρ2= 0.992 > 0.99,F远大于10F0.05,这进一步说明回归的动力学模型是可靠的。 关于活化能,已有文献报道, 生成HCHO、CO和DME的反应活化能分别在75~92 kJ/mol、44~72 kJ/mol和63~77 kJ/mol范围内[14,15],可见本文研究结果与已有研究相吻合。
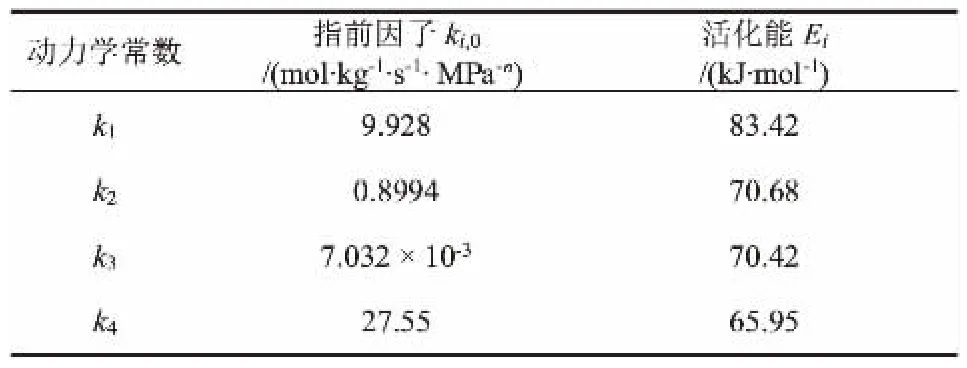
表1 动力学模型参数回归结果
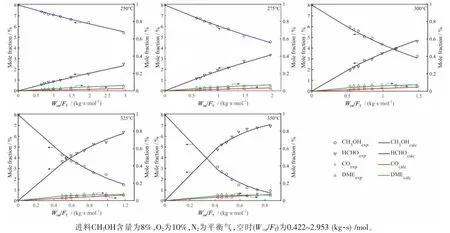
图4 实验值与模型计算值对比
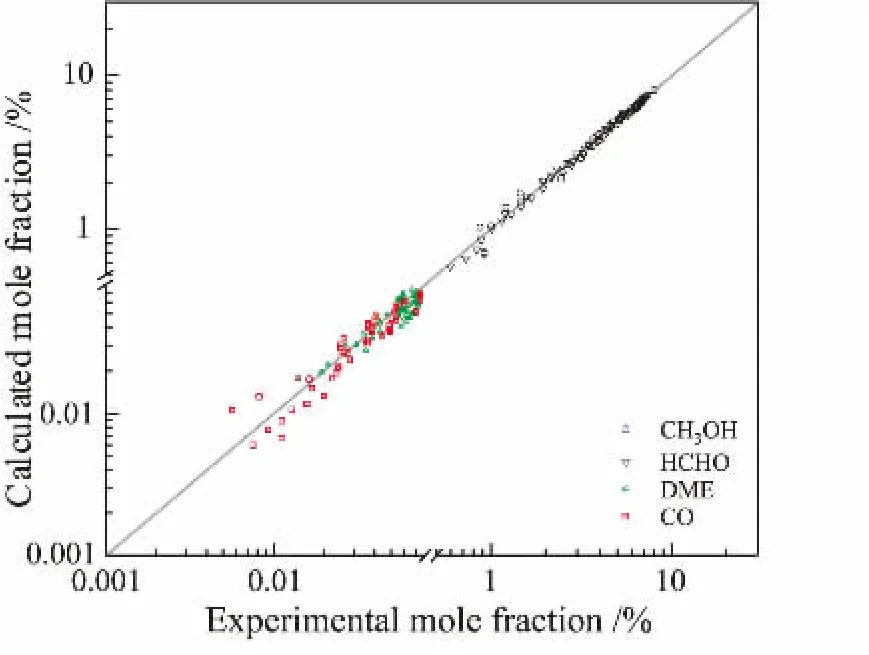
图5 各组分物质的量分数实验与计算值对角线图
2 反应器模拟
2.1 模型的建立与求解
2.1.1 反应器数学模型
对列管式固定床反应器,构建了r轴与z轴方向上的圆柱体几何结构。 在工业装置中,反应管内的气速足够高,流体与催化剂之间的传递阻力较小。经压汞法测定,铁钼催化剂的平均孔径为414.79 nm,主要为大孔结构,内扩散阻力小,可忽略颗粒内的温度差与浓度差。 故可将催化剂床层视作连续的多孔介质,采用二维轴对称拟均相模型。
通过对流扩散方程描述气体在多孔介质中的质量传递。 由于反应组分浓度远低于N2, 可用Fickian定律描述物质传递中的扩散项:
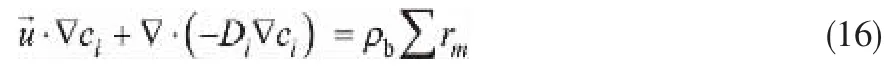
考虑气流与催化剂之间的温度差,采用局域非热平衡的双能量方程描述耦合化学反应的气固相传热。 气相与固相的能量方程分别为式(17)与式(18):
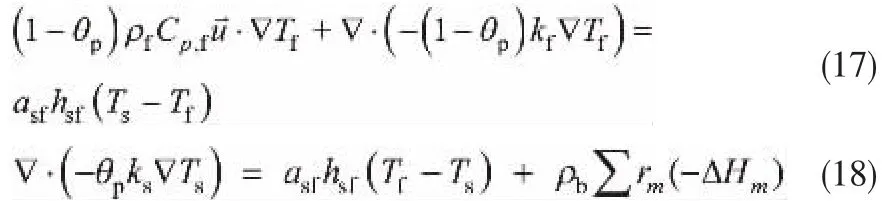
气体连续性方程为:

在多孔介质区域, 气体流动的动量守恒由Brinkman方程描述:

采用Ergun方程计算式中的渗透率κ与参数β:

在反应器入口处(z = 0)规定了进料的组分、温度、速度与压力:
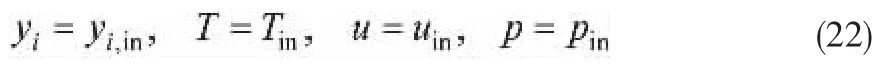
在出口处(z = L)抑制回流,假设对流控制质量与热量传递,忽略浓度扩散作用与热辐射。 在对称轴处(r = 0)采用对称边界条件:
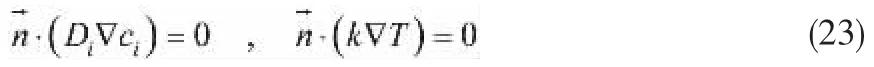
壁面边界(r = R)无滑移且无物质通量,并定义热通量条件描述床层与管壁间的换热:

2.1.2 模型设置与求解
为研究各参数对反应器性能的影响,首先确定一组基准工况条件进行模拟。 选择气相进口温度为200 °C,压力为0.152 MPa,空速为17000 h-1,进口甲醇含量为8%,氧气含量为10%,其余为氮气,反应管壁温在管外熔盐换热下保持250°C。 反应器结构参数为:反应管长为0.8 m,内径为0.021 m,床层空隙率为0.5,催化剂堆积密度为900 kg/m3。 其他求解所需物性参数的表达式如表2所示。

表2 物性参数
反应管模型是一个二阶非线性偏微分方程组,在COMSOL软件中采用有限元方法对其离散, 并由全耦合求解器进行计算。
对基准工况条件下的模型进行求解,得到甲醇浓度与床层温度分布如图6所示。 甲醇刚进入反应管时浓度较高,但此时床层温度低,氧化速率较慢。在壁面加热与反应放热下, 温度沿轴向加速上升,在管中部床层达到热点温度374 °C。 之后随着甲醇逐渐耗尽,反应速率下降,在壁面移热下温度也随之降低。
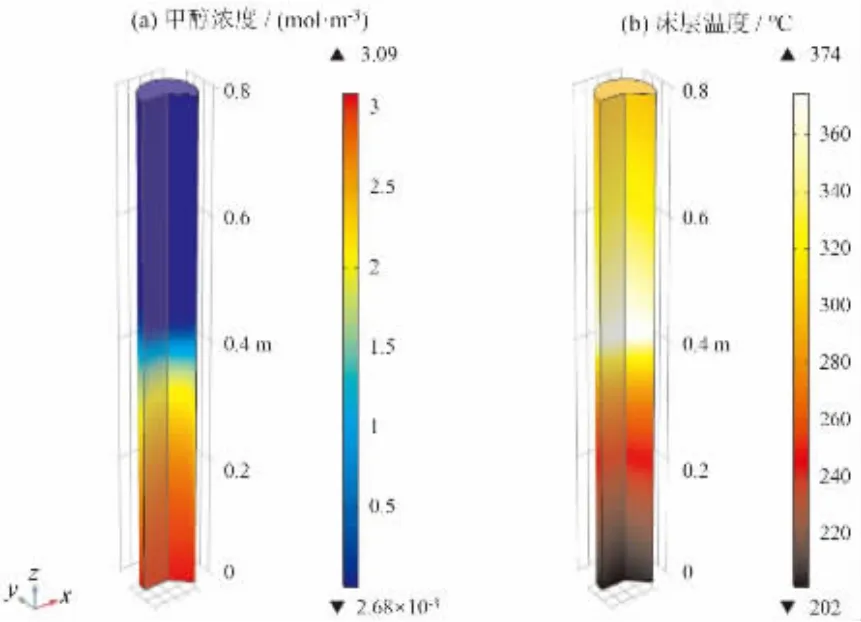
图6 基准工况下(a)甲醇浓度和(b)床层温度分布云图
管内各组分浓度的轴向分布如图7所示。 甲醇浓度沿轴向降低直至完全转化。 甲醛浓度不断升高,至出口处产率达到91.7%,与工业实际值相符。同时甲醇生成的副产物CO和DME浓度也逐渐升高,在甲醇接近完全转化后, 由于甲醇脱水为可逆反应,在管后段DME浓度有所降低,甲醛和CO产率则进一步增加。
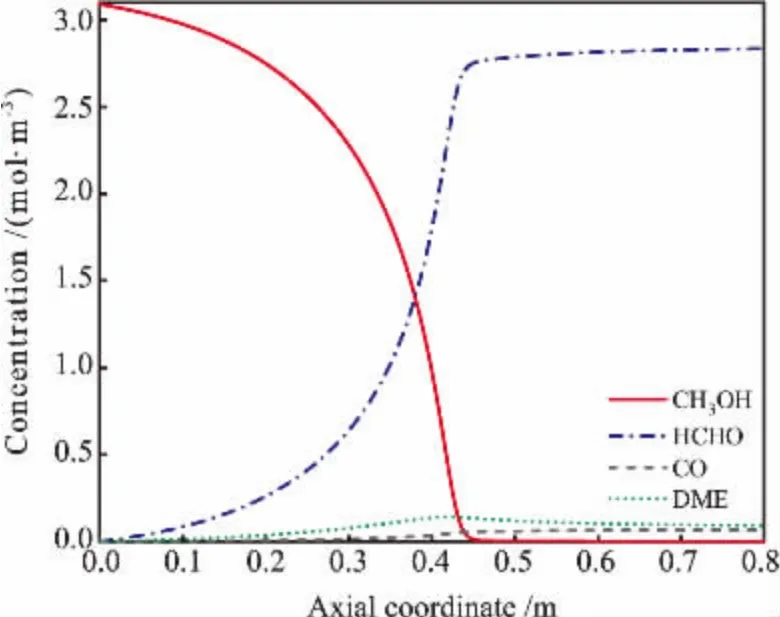
图7 基准工况下反应管内各组分浓度的轴向分布
2.2 模拟结果与讨论
2.2.1 进料甲醇含量的影响
甲醇含量对反应管内温度与组成的影响较大。图8和图9分别为进料甲醇含量对管内温度和出口产物分布的影响。 进料甲醇含量提高,氧化速率明显加快,热点温度上升且热点位置前移,同时DME产率增加,甲醛产率下降。而当甲醇含量增加至10%时,管内高温使甲醇脱水反应的平衡逆向移动,DME产率下降,甲醛产率升高,此时的热点温度已超出安全操作范围,极易产生飞温。 故提高甲醇含量有利于增加甲醛产量,而限制其含量提高的关键因素为床层温度,一般还需调节反应管壁温与采用稀释催化剂,来保证高含量甲醇进料下的反应管具有可靠传热,防止局部过热的发生。
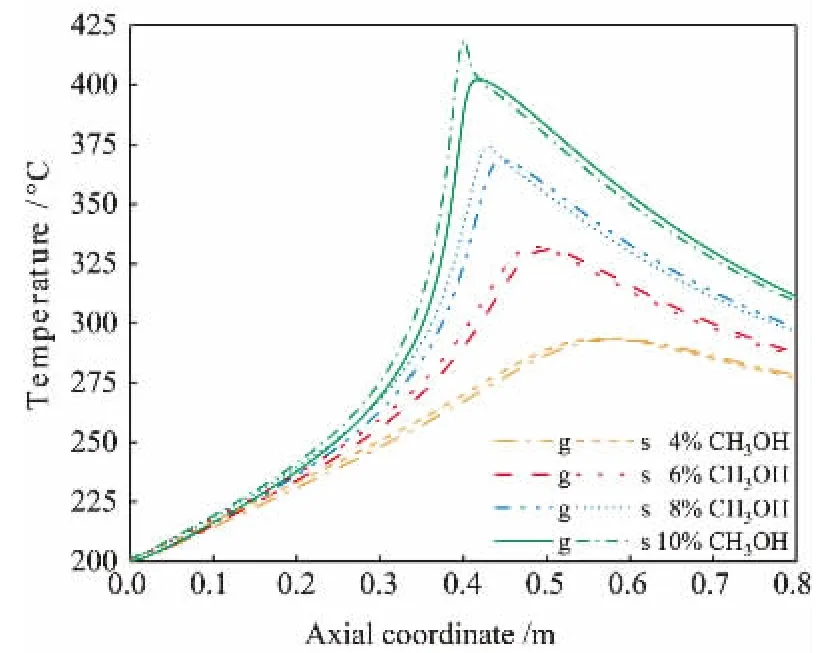
图8 进料甲醇含量对气相(g)与固相(s)温度分布的影响
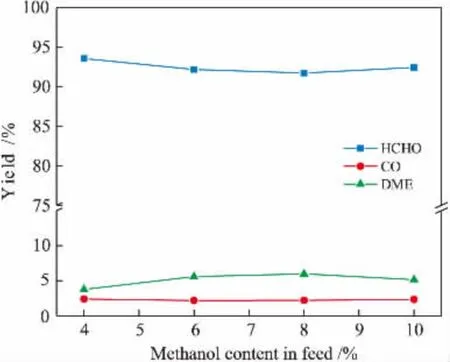
图9 进料甲醇含量对出口产物分布的影响
2.2.2 温度的影响
在高温下,催化剂会因熔结与钼升华而失活,床层最高温度不应超过400 °C[4]。图10和图11所示分别为进料温度与反应管壁温对温度分布的影响。 当提高进料和壁面温度时,管内温度升高,热点位置前移。 且相比进料温度,该反应对壁温更加敏感,其变化使床层温度产生了更大波动。 这是由于提高进料温度主要起到增加反应管前段“预热层”温度的作用,使反应更快进入高温区域,而反应管壁温则直接影响了热点区域的撤热速率,在该区域产热和撤热平衡较为脆弱易引发飞温。 故操作时应严格控制管外热载体温度。
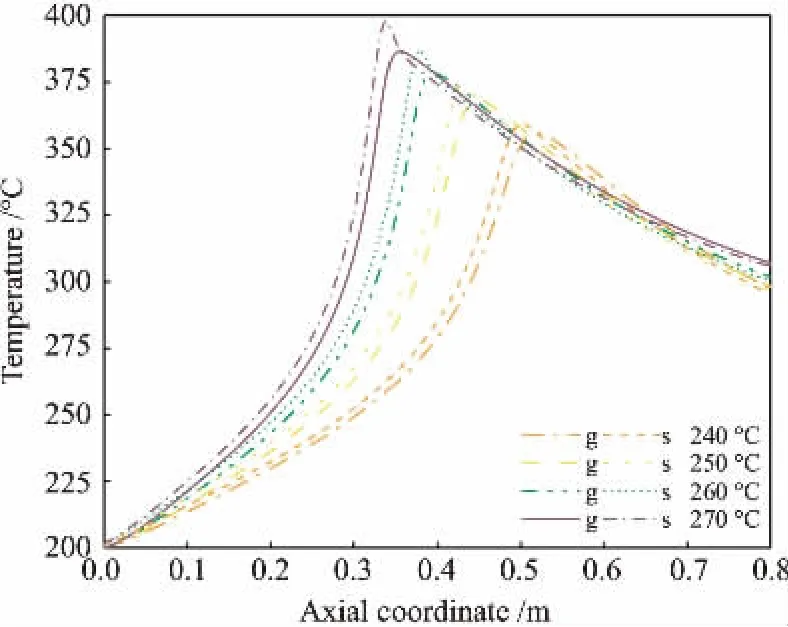
图10 反应管壁温对气相(g)与固相(s)温度分布的影响
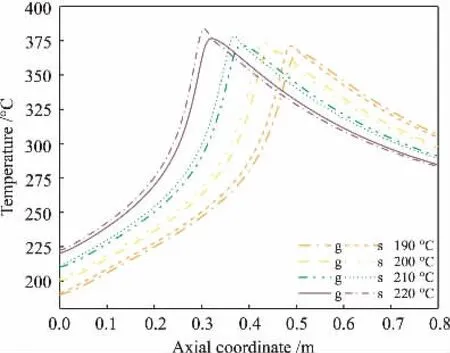
图11 进料温度对气相(g)与固相(s)温度分布的影响
由于高温不利于可逆放热的甲醇脱水反应正向进行, 且主反应在高温下的平衡常数仍很大,故温度升高,DME产率下降, 甲醇转化率与甲醛产率皆有所增加。 在工业生产中,综合考虑操作的安全与稳定性,可采用甲醇预热方法使床层处于较高温度范围内。
2.2.3 空速的影响
空速虽未出现于动力学表达式中,但其确是影响反应进程的重要工艺条件。 图12和图13所示分别为空速对管内温度和甲醛产率的影响。 随着空速的增大,热点温度变化不大仅略有下降,同时热点位置后移,热幅变宽。 这是由于增大空速使单位管长的停留时间缩短,反应在更后端位置达到热点。 反应管内的放热量取决于反应物总消耗量,而大部分甲醇是在反应管热带区域被消耗的,故热点温度变化不大。 同时,气流与催化剂的接触时间缩短也使甲醛产率略有下降,而空速对各组分的选择性影响不大。 可见空速并非该反应的灵敏操作参数,适合用于提高甲醛生产率。
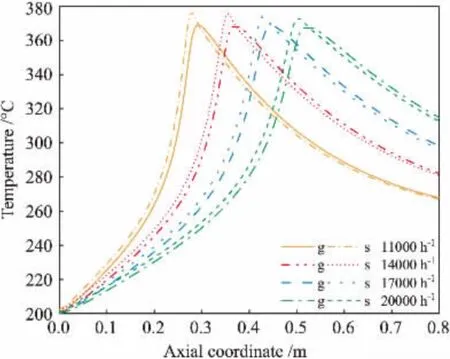
图12 空速对气相(g)与固相(s)温度分布的影响
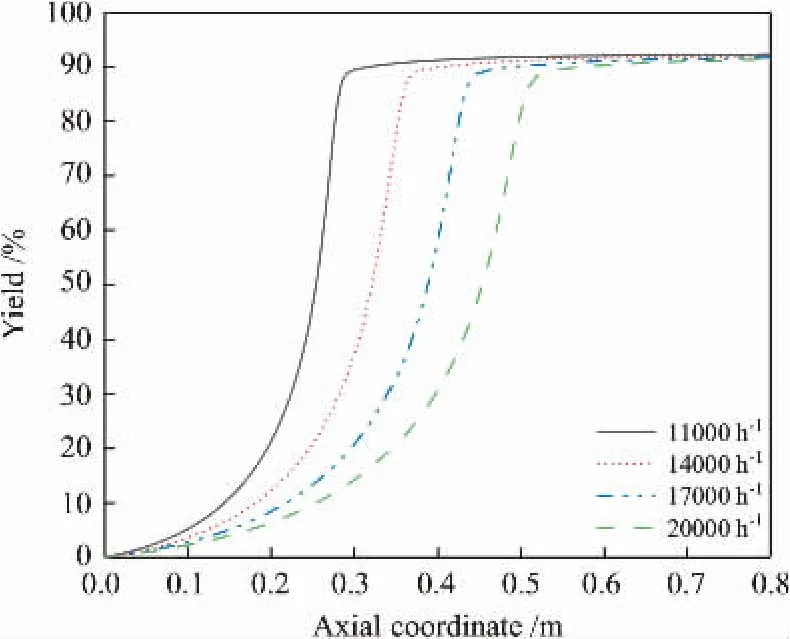
图13 空速对甲醛产率轴向分布的影响
此外,提高空速还可使气流具有足够的线速度消除催化剂表面的外部扩散阻力,但这也伴随着床层压降增大、动力消耗增加。 因此在工业生产中,空速的选择还应综合考虑其他操作条件。
2.2.4 入口压力的影响
甲醇氧化生成甲醛是分子数增加的气体反应,压力升高对其正反应不利。 图14为入口压力对出口产物分布的影响。

图14 入口压力对出口产物分布的影响
由图14可以看出,入口压力升高,甲醛产率下降,DME产率增加。 压力对反应管内温度分布的影响类似于空速。 压力升高,管内流速增大,热点位置略有后移且热点温度变化不大。 相比于增加进料甲醇含量引起的温升,提高入口压力和反应空速不易导致飞温,操作弹性更大。
3 结论
本文采用铁钼商用催化剂, 在工业操作条件下,围绕反应动力学及反应器模拟对甲醇制甲醛工艺进行了研究,得出结论如下:
(1)在管式固定床反应器中测定了甲醇氧化反应的本征动力学数据, 选取HCHO、CO和DME为关键组分,根据Mars-van Krevelen机理建立了动力学模型。 统计检验结果表明,所回归的模型是可靠的。
(2)针对列管式固定床反应器,建立了多孔介质二维拟均相反应管模型,并考察了工艺条件对反应器性能的影响。 适当提高甲醇含量、反应空速与进料压力皆有助于增大甲醛生产率。 其中甲醇含量与反应管壁温是床层温度的敏感操作参数,易引发局部过热,故操作中应严格控制进料含量与管外热载体温度。


