咪喹莫特联合干扰素-α诱导大鼠银屑病模型的建立
王楠楠,蔡婷婷,刘霞,朱婉萍
(浙江省中医药研究院,浙江 杭州 310007)
银屑病是一种免疫介导的慢性炎症性皮肤病。目前银屑病的发病机制尚未明确,有研究表明辅助性T细胞(Th)17相关的细胞因子能诱导皮肤内黏附分子的表达和淋巴细胞的浸润,促进角质形成细胞的增殖、分化,释放炎性介质,在银屑病的发生发展中起到重要作用[1]。
银屑病动物模型有助于探究其潜在发病机制,是药物疗效评价的重要工具。目前尚未有与人类银屑病发病机制完全相同的动物模型,各种银屑病模型均基于不同的致病机制,有其各自的特点和局限性,使用较多的有咪喹莫特诱导小鼠模型[2-4],普萘洛尔诱导豚鼠模型等[5-6],但缺乏标准的操作规范,受干扰因素较多,模型维持时间较短,不适宜长期研究。
本实验室前期研究发现单用咪喹莫特诱导的银屑病大鼠模型不够稳定。有研究发现咪喹莫特加用干扰素(IFN)刺激,可诱导更为稳定、典型的银屑病小鼠模型[7]。与小鼠相比,大鼠是更接近人类的实验动物,其背部皮肤面积较大,皮损特征易于观察,病理生理特征易于研究,可较好的进行银屑病发病机制的研究及银屑病动物模型的补充。故本实验采用咪喹莫特单用、咪喹莫特联合IFN-α诱导大鼠银屑病模型,从皮肤形态、病理及细胞因子的表达等方面阐释模型的临床和病理特点,建立稳定、可复制的银屑病动物模型。
1 材料与方法
1.1 实验材料
1.1.1 实验动物 SPF级Wistar大鼠35只,雄性,体质量(200±20)g,购于北京维通利华实验动物技术有限公司,许可证号:SCXK(京)2016-0006,由浙江省中医药研究院实验动物中心饲养。
1.1.2 药品与试剂 5%咪喹莫特乳膏(0.25g/袋×4袋,四川明欣药业有限责任公司,19030239);300万U重组人干扰素-α-2a注射液(1.0 mL/瓶,沈阳三生制药有限责任公司,201807031);PA-J化合物,Kv1.3钾离子通道抑制剂,由实验室合成;白细胞介素(IL)-17 抗体,BOSTER,0001712Da472158。
1.1.3 主要设备 Nikon eclipse 80i显微镜(Nikon公司);CCD:DS-Fi1 500万象素(Nikon公司);图象分析软件Carl Zeiss Imaging Systems(Carl Zeiss公司);电子分析天平[勒-托利多仪器(上海)有限公司];超低温冰箱(Thermo公司)。
1.2 方法
1.2.1 动物分组 SPF级雄性Wistar大鼠35只,按体质量随机分为4组,分别为空白对照组、咪喹莫特单用组、咪喹莫特联用组、PA-J组,其中单用组5只,其余每组10只。
1.2.2 造模及给药 大鼠适应性喂养数日后,将各大鼠背部中央区域(2 cm×2 cm)的毛剃去后,用温和型脱毛膏脱去表面短毛,洗净擦干,备用。若实验过程中背毛再次长出,则用剃毛刀剔除毛发。
每日上午,咪喹莫特单用组大鼠背部按照20 mg/cm2均匀涂抹5%咪喹莫特乳膏(每袋0.25 g,涂抹3只);咪喹莫特联用组及PA-J组大鼠背部涂抹5%咪喹莫特乳膏,10 min后将重组人干扰素-α-2a注射液按照1万U/500 g腹腔注射;空白对照组大鼠背部涂以等量凡士林,1次/d。下午,PA-J组大鼠背部按0.5 mg/只滴涂药物,连续10 d。
1.2.3 银屑病皮损面积和严重程度指数(PASI)评分 第11 d,依据PASI评分标准,给予大鼠皮损处红斑、鳞屑及表皮浸润增厚程度0~4的积分。评分标准如下:0,无;1,轻度;2,中度;3,重度;4,极重度,见表1。对各组大鼠积分取平均值,观察各组大鼠皮损的变化情况。
1.2.4 HE染色 将大鼠背部皮损组织取材,4%中性甲醛固定、石蜡包埋、切片,经HE染色,显微镜下观察皮肤组织形态学变化,进行Baker评分。
Baker评分具体标准如下:表皮层中发现Munro小脓肿2.0分;角化过度0.5分;角化不全1.0分;颗粒层变薄或消失1.0分;棘层增厚1.0分;皮突延长、起伏根据轻中重度分别计0.5分、1.0分、1.5分。真皮层中单一核或多核细胞浸润根据轻中重度分别计0.5分、1.0分、1.5分;乳突上顶0.5分;毛细血管扩张0.5分。
1.2.5 免疫组化 按照产品说明书上的免疫组化两步法操作规程染色。即将石蜡包埋后的皮损组织,切片置60℃烤箱烘烤2 h;切片脱蜡至水;蒸馏水洗2 min;高压热修复;3%H2O2溶液阻断过氧化物酶,10 min;磷酸盐缓冲液(PBS)洗 5 min×3 次;滴加一抗,37℃孵育1 h;PBS洗5 min×3次;滴加二抗,37℃孵育 60 min;PBS洗 5 min×3次;DAB 显色2 min;复染、透明后封片。将每张切片所要分析的部位显微镜下拍摄照片,进行图象分析。
总光密度(IOD):阳性表达部位(∑Area)×该部位的平均光密度(Density);阳性指数:即IOD/照片总像素(IOD面积以象素单位计算),用DAB显色的免疫组化切片阳性区域为棕黄色,阳性指数表示总光密度均分到该照片的值。
2 结果
2.1 对银屑病大鼠皮损PASI评分的影响 空白对照组皮肤光滑完整,未见红斑、鳞屑;咪喹莫特单用组皮肤仅见少量鳞屑;咪喹莫特联用组皮肤可见大块鳞屑、红斑;PA-J组皮肤可见部分鳞屑,未见红斑,见图1。与空白对照组比较,单用组与联用组PASI评分明显增高(P<0.01),且联用组优于单用组(P<0.05);与联用组比较,PA-J组PASI评分明显降低(P<0.05),见表2。
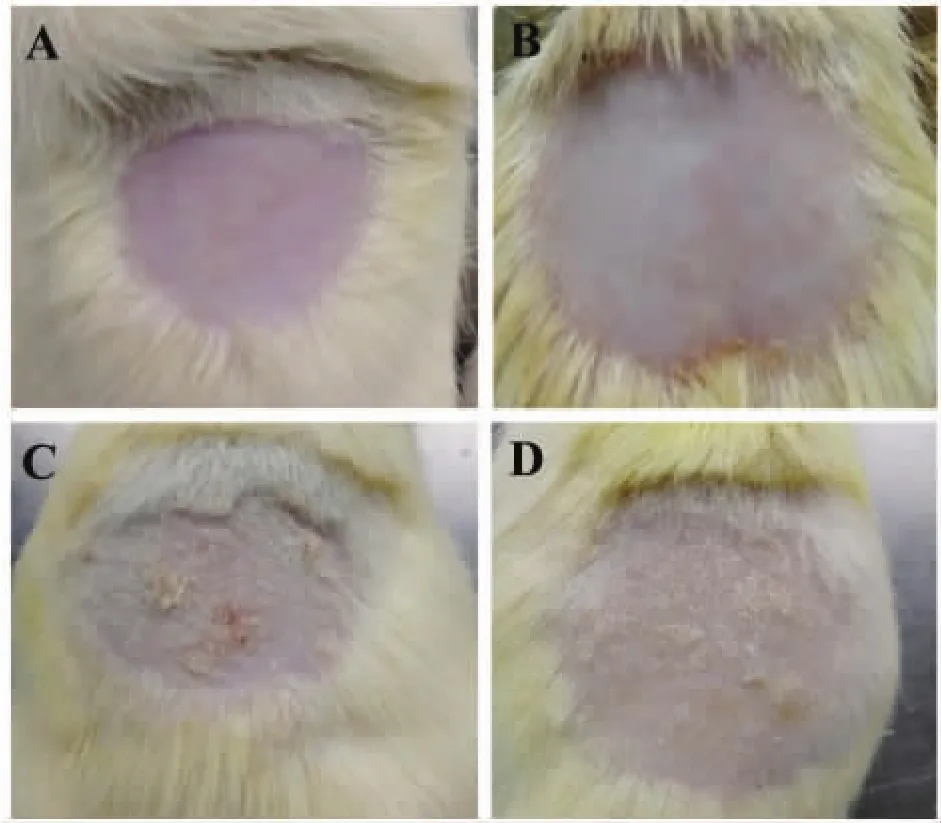
图1 银屑病大鼠背部皮损严重程度
表2 对银屑病大鼠皮损PASI评分的影响 (±s)
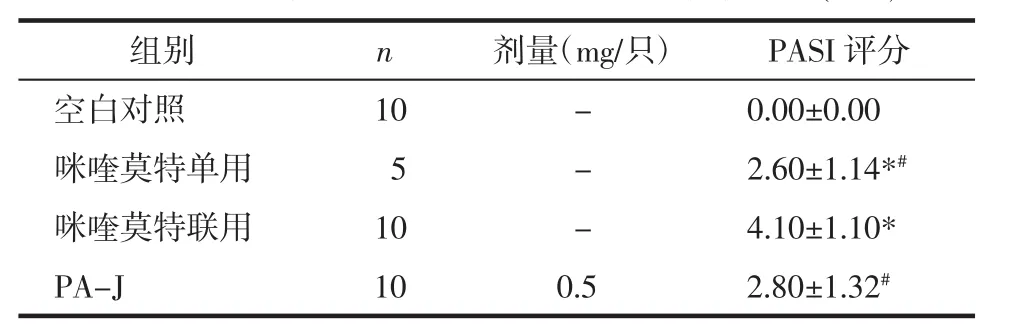
表2 对银屑病大鼠皮损PASI评分的影响 (±s)
注:与空白对照组比较,*P<0.01;与咪喹莫特联用组比较,#P<0.05。
组别 n 剂量(m g/只) P A S I评分空白对照 1 0 - 0.0 0±0.0 0咪喹莫特单用 5 - 2.6 0±1.1 4*#咪喹莫特联用 1 0 - 4.1 0±1.1 0*P A-J 1 0 0.5 2.8 0±1.3 2#
2.2 对银屑病大鼠皮损病理改变的影响 空白对照组皮肤结构完整清晰,未见过度角化、棘层肥厚、毛细管扩张,真皮层有少量炎性细胞浸润;咪喹莫特单用组皮肤可见角化不全,棘层轻度肥厚,皮突延长起伏明显,真皮层炎性细胞浸润;咪喹莫特联用组皮肤可见明显角化过度、角化不全、棘层肥厚、乳突上顶,真皮层大量炎性细胞浸润;PA-J组皮肤结构完整,颗粒层可见、部分皮肤延长起伏、未见棘层肥厚,真皮层可见炎性细胞浸润,见图2。
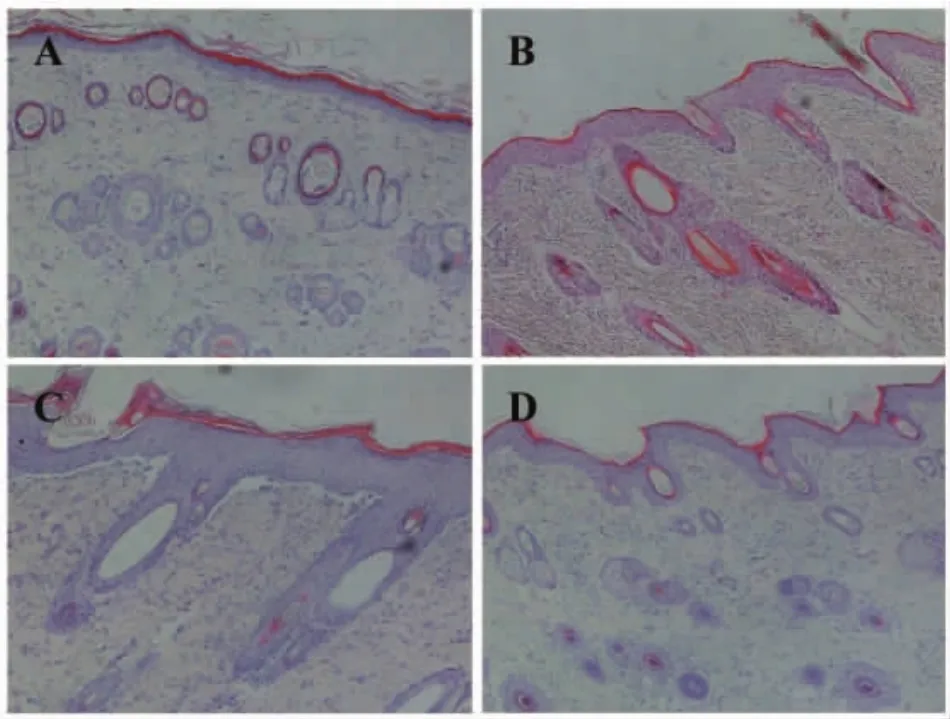
图2 大鼠背部皮损病理改变(HE染色×100)
与空白对照组比较,单用组与联用组Baker评分明显增高(P<0.01),且联用组优于单用组(P<0.01);与联用组比较,PA-J组Baker评分明显降低(P<0.01),见表3。
表3 对银屑病大鼠皮损Baker评分的影响 (±s)

表3 对银屑病大鼠皮损Baker评分的影响 (±s)
注:与空白对照组比较,*P<0.01;与咪喹莫特联用组比较,#P<0.01。
组别 n 剂量(mg/只) Baker评分空白对照 10 - 2.15±0.53咪喹莫特单用 5 - 4.60±0.55*#咪喹莫特联用 10 - 6.30±1.21*PA-J 10 0.5 3.60±0.94#
2.3 对银屑病大鼠皮损组织IL-17表达的影响 通过前面临床皮肤形态及皮损病理改变,可以判定咪喹莫特联用组明显优于单用组。因此,没有检测单用组大鼠皮损组织IL-17表达。
空白对照组大鼠皮肤组织中真皮层可见少量棕黄色区域,IL-17表达较少;咪喹莫特联用组皮肤组织中表皮层及真皮层可见大量棕黄色区域,IL-17高表达;PA-J组皮肤组织中IL-17表达较低,见图3。
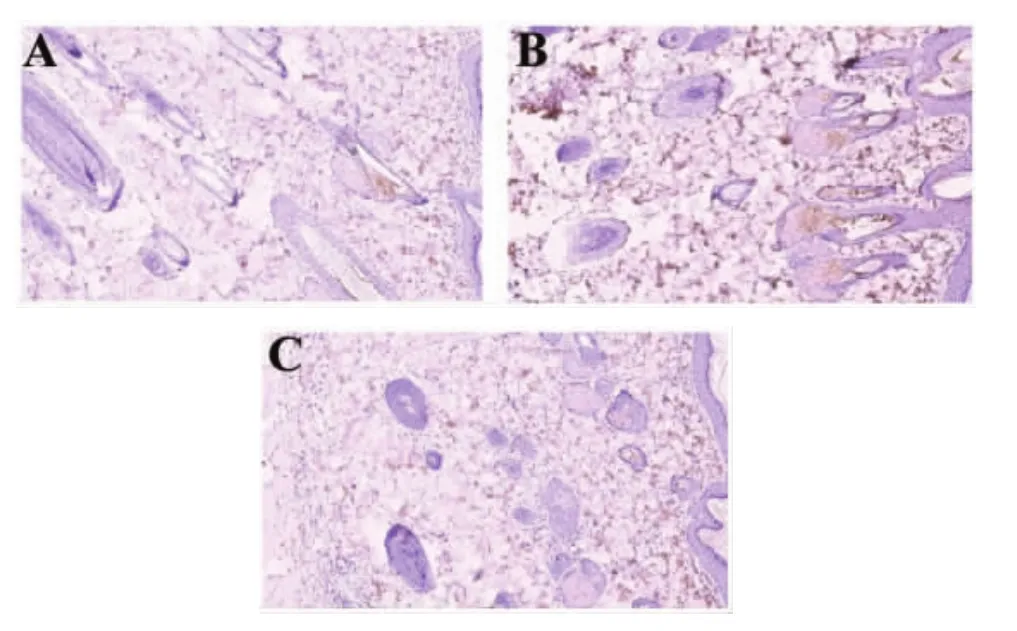
图3 大鼠背部皮损组织免疫组化(DAB染色×100)
与空白对照组比较,咪喹莫特联用组IL-17总光密度值及阳性指数均明显增高(P<0.01);与联用组比较,PA-J组IL-17总光密度值及阳性指数均明显降低(P<0.01),见表4。
表4 对银屑病大鼠皮损IL-17的影响 (±s)
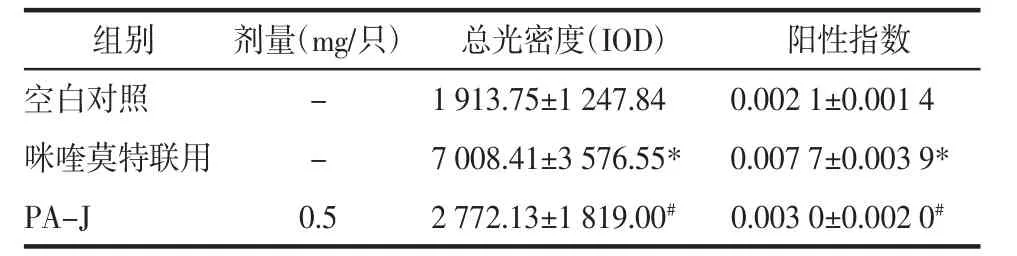
表4 对银屑病大鼠皮损IL-17的影响 (±s)
注:与空白对照组比较,*P<0.01;与咪喹莫特联用组比较,#P<0.01。
组别 剂量(m g/只) 总光密度(I O D) 阳性指数空白对照 - 1 9 1 3.7 5±1 2 4 7.8 4 0.0 0 2 1±0.0 0 1 4咪喹莫特联用 - 7 0 0 8.4 1±3 5 7 6.5 5* 0.0 0 7 7±0.0 0 3 9*P A-J 0.5 2 7 7 2.1 3±1 8 1 9.0 0# 0.0 0 3 0±0.0 0 2 0#
3 讨论
动物模型在药物的研发中起着重要作用,目前银屑病模型主要有基因工程、自发性、异种移植及药物诱发等动物模型[8-9],其中基因工程价格昂贵、建模较长;自发性突变鼠模型在治疗上使用抗银屑病药物无法减轻其炎性细胞浸润和缺乏T淋巴细胞表达等症状,极少使用[10];异种移植比较接近人类银屑病遗传、表型和免疫变化,但对实验技术要求高,限制其应用[11]。药物诱发模型,其操作简单,经济易得,有重现性,在普通实验室广泛应用。但其也存在着局限性,该模型为急性非特异性炎性反应,除引起皮肤改变外,还引起全身性炎性反应,与人类银屑病的慢性炎症性皮肤病存在一定的差异[12-13]。各种银屑病模型均基于不同的致病机制,有其各自的特点和局限性,因此了解并建立不同类型的动物模型,有助于更合理的选择,促进银屑病发病机制的研究及治疗药物的研发。
IL-17是Th17细胞分泌的细胞因子,通过促炎性细胞因子及趋化因子的释放,诱导炎性基因的表达,抑制角质形成细胞表达黏附因子,破坏皮肤屏障,在银屑病发病机制中起着重要作用[14]。大量研究表明银屑病患者中IL-17水平明显升高[15-16]。目前针对IL-17相关的生物制剂已经开始应用于临床银屑病的治疗,并有良好的疗效[17]。
实验中发现单用咪喹莫特诱导大鼠银屑病模型时,大鼠颈部及四肢处毛发出现脱落现象,而联合IFN-α使用时,症状消失。可能原因为咪喹莫特诱导激活毛囊周围的Toll样受体(TLR)7,致使生长期毛囊丢失免疫赦免而产生退化及萎缩[18]。而重组人干扰素-α-2a能够调节机体免疫功能,改善脱毛症状,同时通过Th1和Th17介导的免疫应答促进或加重银屑病的发生[19]。本实验采用咪喹莫特联合IFN-α成功诱导银屑病大鼠模型。在临床方面,大鼠背部皮肤出现鳞屑、红斑等临床症状;在组织学方面,皮损病理观察可见颗粒层变薄甚至消失、棘层肥厚、乳突上顶,真皮层大量炎性细胞浸润等银屑病样特点;在发病机制方面,皮损组织中IL-17表达明显升高。因此,该模型符合银屑病的临床及病理特点,是可靠、稳定的银屑病动物模型,可用于药物的研发及病因机制的探索。

