经口机器人手术在头颈肿瘤外科中的应用*
袁舜棋,张萌,张勤修
610041 成都,成都中医药大学医学与生命科学学院/附属生殖妇幼医院 耳鼻咽喉头颈外科 (袁舜棋、张勤修);618000四川 德阳,德阳市人民医院/成都中医药大学附属德阳医院 耳鼻咽喉头颈外科(张萌)
一直以来,头颈肿瘤的外科治疗意味着运用各种开放式手术切除肿瘤。随着技术的进步,手术范围不断扩大,术后出现的功能障碍和外观畸形等并发症也越来越严重,严重影响了患者的生活质量。近年来手术机器人系统的出现,其对深在部位所具备的良好视野和操作优势,为克服开放式手术的缺点带来了曙光。经口机器人手术(transoral robotic surgery,TORS)于2005年被Weinstein等[1]首次提出可应用于头颈外科。他运用TORS为一只犬实施了声门上喉切除术,发现TORS具有视野良好和容易止血的优点。随后,一些学者也证明了TORS可应用于头颈外科,且具有良好的可行性和安全性[2-4]。从那以后,TORS就被认为是一种在头颈肿瘤外科领域可替代部分传统开放式手术的新技术。此后,美国食品药品监督管理局在2009年12月批准了达芬奇手术系统用于头颈部良恶性肿瘤切除的TORS。至此,手术机器人系统的发展和微创技术的革命使得TORS在头颈外科中得到了迅速发展。本文对手术机器人的发展历史、TORS的起源、以及近年来TORS用于头颈各部位肿瘤治疗的现状进行了综合叙述,并对TORS的发展作出了展望。
1 手术机器人
“Robot”源于1920年捷克作家Karel Chapek写的剧本《罗萨姆的全能机器人》,它是一种具有人类外观、特征和功能的机器[5]。20世纪70年代,随着航天事业的发展,为解决宇宙航行中对宇航员进行远程手术的问题,美国国家航空航天局开始着手研发可远程操控的手术机器人[6]。世界上第一台被用于医疗的机器人PUMA 560是1978年Victor Scheinman研发的,严格意义上讲它只是一个机械臂,该设备1985年被 Kwoh用于神经外科组织活检术[7]。1995年,一家名为“Intuitive Surgical”的新兴公司取得了相关知识产权,于1999年推出第一个手术机器人并将其命名为“达芬奇”,以纪念人类历史上第一个机器人的设计者、文艺复兴时期科学与艺术巨匠“列奥纳多·达·芬奇”。
达芬奇手术机器人系统由3部分组成(图1):1)主控制台;2)床旁机械臂系统(核心部件为具有互动功能的内置式腕状机械臂);3)成像系统(包括高清内窥镜和一个带有3D图像处理器的视觉系统)。医生通过主控制台内屏幕和操控手柄远程操纵腕状机械臂进行手术。因为具有三维可视化、运动缩放、震颤过滤、灵活的操作界面和舒适的人体工程学等优点,达芬奇机器人系统已经在外科机器人领域占据主导地位[6]。达芬奇机器人的机械臂采用多关节设计,使其在深在部位操作中非常灵活,因而最初被用于一些心脏手术,随后在泌尿外科的前列腺切除术和妇科的各种手术中被广泛采用,这也是头颈肿瘤外科中TORS发展的技术基础。需要注意的是,目前在医疗行业中被大众所接受的“手术机器人”,严格意义上来说只是一种机器,因为它没有自己的“思维”,不能自行完成手术。它只是医生眼和手的延伸,需要在外科医生的操控下完成手术。
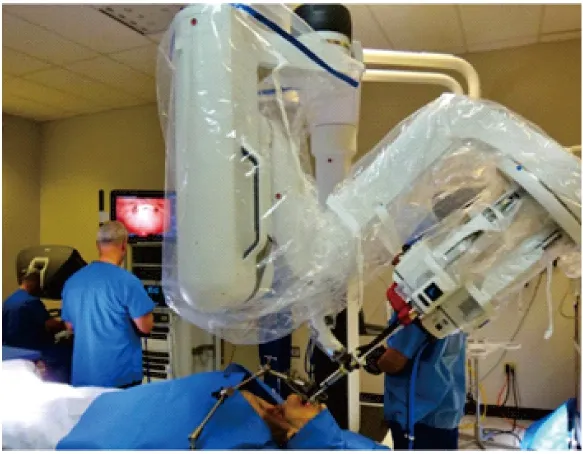
图1 经口机器人手术[2]
2 TORS在头颈肿瘤外科应用
2.1 咽部肿瘤
2.1.1 口咽癌 口咽癌手术几十年来的经典入路是下颌骨裂开,但一直被吞咽困难、咬合错位、颞下颌关节疼痛和外观畸形等并发症所困扰。由于放化疗技术的进步,非手术治疗一度成为口咽癌最常用的治疗方法[8]。随着TORS技术的引入及发展,使得手术在口咽癌患者的治疗中重新崭露头角。
进行TORS手术时,患者经鼻气管插管全身麻醉,使用开口器暴露口咽部,置入内镜臂及器械臂,助手在床旁辅助,主刀医生坐在控制台前进行手术[9]。与传统开放手术相比,对于适应证选择合适的病例,TORS术后除了有良好的吞咽功能外,还显示了良好的肿瘤治疗效果,减少了胃造瘘率和气管切开率,与单纯放疗相比还具有更好的卫生经济学效益[10-11]。与经口激光显微手术相比, TORS具有四手(两只器械臂及助手双手)、放大3D视觉和腕式器械的优势,并且学习曲线要短得多[12]。另外,咽后淋巴结因其解剖位置深在,传统术式很难进入进行清扫,在口咽癌咽后淋巴结的转移一般采用放射治疗,随着TORS的出现,可以很容易地进入和切除咽后淋巴结,术后复发率也明显降低[13]。
基于目前文献[9,12,14-16],扁桃体癌TORS切除的适应证为:1)T1-2期;2)部分经过选择的T3或T4期。舌根癌适应证:单侧T1-2期舌根癌。TORS治疗口咽癌主要禁忌证有:1)需切除舌根、咽后壁50%以上或会厌全切除;2)肿瘤位于会厌谷中线或舌根,靠近双侧舌动脉;3)肿瘤侵犯舌根、下颌骨、颈动脉鞘、颈内动脉、椎前筋膜或颅底;4)肿瘤有远处转移;5)患有影响设备放置和定位的疾病的患者,如闭合的牙齿(开口小于1.5 cm)、巨舌症、上颌骨缺损和颈椎相关疾病。
目前TORS是许多临床试验的基础,这些临床试验可能会改变口咽癌的治疗规范[17]。一篇荟萃分析显示TORS与开放式手术相比,在提高无瘤生存率、降低饲管依赖和平均住院天数以及降低游离皮瓣重建的风险方面具有优势[18]。但是,也有研究显示TORS对肿瘤或功能结局没有显著影响[19]。因此需要通过长期随访比较研究来验证口咽癌的肿瘤、功能、预后(包括手术并发症)之间的关系。
2.1.2 鼻咽癌 放疗或同步放化疗是鼻咽癌最常见的治疗方法,但是放疗后复发仍是治疗的难题[20],近年来手术切除放疗后复发的鼻咽癌取得了重大进展。TORS的优势在于对深在部位具有良好的视野和可弯曲操作的机械臂,能经口越过软腭向上达到鼻咽部,为复发鼻咽癌的切除提供了一个新的操作方便的入路[14,20-21]。目前,TORS仅适用于切除鼻咽腔内的肿瘤。对于向前侵犯翼腭窝、鼻窦和向上侵犯颈内动脉的肿瘤则为禁忌证。TORS治疗早期复发鼻咽癌的效果也较为满意。Tsang等[21]报告了他们利用TORS治疗复发鼻咽癌的早期结果:术后随访2年,总生存率和无瘤生存率分别为83%和61%。总之,TORS为治疗复发鼻咽癌提供了一个新的手段,其前景值得期待[22]。
2.2 喉癌
经口激光显微手术(transoral laser microsurgery,TLM)是早期喉癌微创手术的标准治疗手段[23]。然而,尽管经验丰富的团队对TLM进行了多次改进,但因喉部解剖结构的复杂性、手术器械到达远端的困难,在少数肿瘤患者的TLM中,充分暴露声门进行操作仍严重受限[24]。由于TORS可克服前述缺点,因此已被应用于早期喉癌的手术治疗,且已被证明在选定的患者中无论是声门上或声门癌,部分喉切除术以及全喉切除术都是可行的[25-28]。
目前,TORS主要用于声门上喉部分切除术。适应证包括:喉癌,声门上型,Tis、T1、T2期,以及少数选择性的T3期肿瘤。另外,TORS全喉切除术也被证明是可行的。适应证为局限于喉腔内较大范围的肿瘤。禁忌证为肿瘤侵犯喉外组织[14,29-30]。
TORS在喉癌的治疗中显示了较好的疗效。Kayhan等[25]报道了48例声门型喉癌患者接受TORS治疗。平均随访时间为(65.6 ±16.6)个月,总生存率为97.9%,无病生存率为89.6%,保留喉率97.9%。Hussain等[23]对84例声门上喉癌患者行手术治疗,其中 19名患者行TORS声门上喉切除术 (其中T1期 8例,T2期9例,T3期2例),65名患者行TLM(其中T1期26例,T2期27例,T3期9例 ,T4期3例)。随访24个月,经TORS治疗后无瘤生存率为71.4%(n=5/7),TLM治疗后为64.9%(n=24/37),肿瘤切除术的局部复发率TORS为0,TLM为11%。Asik等[31]对832例患者进行TORS和TLM声门上喉癌切除术的荟萃分析显示:总生存率(分别为82.4%和77.0%)和肿瘤特异性生存率(分别为87.0%和75.8%),得出TLM组和TORS组之间没有统计学上的显著差异。TLM组中有164例(19.7%)复发,而TORS组66例患者中只有6例(9%)复发。基于目前荟萃分析表明[28,30],TORS声门上喉切除术的肿瘤预后与开放声门上喉切除术非常相似。
但以上研究均为回顾性分析,证据水平较低,文章数量较少,因此TORS是否能提供与TLM相媲美的肿瘤和功能结果仍有待证明,但确实为喉癌的治疗提供了一种新的手段,且已经显示其优越性。
2.3 颌下腺肿瘤
传统的颌下腺切除术是经颌下入路进行的,但术后颌下的瘢痕影响美观,因此从口底切除颌下腺的方法正在逐步发展中。Capaccio等[32]应用TORS行下颌下腺切除术,手术时间为110分钟,术后超声未见腺体残留且无重大并发症,仅在3个月后患者描述舌尖有轻微刺痛。Lin等[33]证明了在保留舌下腺和沃顿氏管的情况下,采用TORS切除下颌下腺的可行性,这种方法的优点是颌下无疤痕,但是缺点是舌神经的短暂性麻痹和手术时间的延长。因此,对于拒绝颈部瘢痕和面神经麻痹风险的患者,经口机器人下颌下涎腺切除术是一种可行且安全的替代传统的治疗方法[34]。
2.4 甲状腺肿瘤
由于传统甲状腺切除术后瘢痕严重影响美观,甚至导致社会心理负担[35]。因此,近年来经口腔前庭入路行甲状腺切除术备受关注[36-37]。理想的微创手术是将组织损伤降低到最小,避免术后产生广泛的组织损伤和瘢痕。TORS口腔前庭入路通过在下唇系带以及两侧作切口插入外套管后置入内窥镜及腕式器械,或外加腋下机械臂辅助进行手术[38],这种方法被证明是安全、可行的[39-40]。
目前TORS口腔前庭入路甲状腺切除术的适应证是:1)结节性甲状腺肿或甲状腺腺瘤直径<6 cm;2)甲状腺乳头状癌或甲状腺滤泡状癌最大直径<2 cm;3)甲状腺直径<10 cm。禁忌证是:1)巨大甲状腺肿和甲状腺癌伴甲状腺外扩张;2)广泛颈淋巴结转移;3)远处转移;4)颈部放疗史或颈部手术史[38,41-43]。
TORS口腔前庭入路与传统口腔前庭入路甲状腺切除术相比,有几个优点:1)多关节的机械臂和额外的腋下机械臂反牵引带状肌使处理上极变得容易;2)对喉返神经周围组织的反向牵拉使甲状腺悬韧带易于剥离,甲状腺组织不易残留,从而降低了对喉返神经损伤的风险[42];3)与其他机器人辅助入路相比,因其切口到达术区更近,需要剥离的组织较少,造成的损伤及术后疼痛更轻[41,44]。TORS行甲状腺切除术的同时也可行中央区淋巴清扫术,因为它可以反向牵拉气管、带状肌和喉返神经周围组织,视野自上而下且对称,使得清扫变得较为简单易行[42]。Tunca等[41]和Kim等[45]证实TORS无腋下辅助口腔前庭入路甲状腺切除术安全可行,在手术时间及住院时间方面展现出优势,并且其术后并发症、钙水平、甲状旁腺激素和疼痛程度与腋下辅助入路无显著差异,这种入路将“真正无疤痕”理念变为现实。此外,机器人技术的进步已经具备了通过单个操作孔进行操作的能力[46],这比传统的机器人平台具有优势。
2.5 运用游离组织瓣进行功能重建
头颈部恶性肿瘤切除后软组织缺损会造成功能损害及容貌改变,因此运用游离组织瓣修复缺损显得格外重要。因头颈部特殊的解剖结构,传统开放修补显微镜血管吻合法在视野、操作灵活性方面较局限[47]。随着TORS的出现,一些学者正在探索运用机器人辅助行游离皮瓣修补术来弥补传统方法的不足[48-51]。Lai等[50]运用游离前臂桡侧皮瓣修复口咽部缺损的研究中证明使用TORS吻合的供体血管直径明显小于标准手术显微镜和手工缝合技术,机器人辅助游离组织瓣微血管吻合术是一种先进、安全的手术技术。
3 TORS的不足与未来展望
综上所述,TORS在进入头颈肿瘤外科领域以来,在短短的10余年取得了惊人的成就,机器人手术系统的技术进步和外科医生观念及手术技巧的进步是两个主要的因素。目前,TORS最大的不足是在使用游离组织瓣进行修复方面具有很大的局限性,这也大大限制了TORS技术适应证的进一步拓展。尽管少数医生运用手术机器人在开放式手术中吻合微血管进行游离组织瓣功能重建方面做了一些有益的探索,但由于微血管吻合技术本身具有很高的难度导致了只有少数医生才能掌握,故这项技术只能在很小范围内开展。所以,在将来的工作中,我们应该充分发挥手术机器人的视觉放大和操控精准的优点并用于微血管吻合,在TORS中直接在狭窄的空间中进行游离皮瓣重建微血管吻合。这将极大地拓展TORS技术的应用范围,有力地促进TORS技术的发展。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。

