二维液相色谱法同时测定人血浆中伊马替尼及其代谢产物浓度的方法学研究*
董馨蔚,蒋刚,马松涛,陈燕
610500 成都,成都医学院 药学院(董馨蔚、马松涛);610041 成都,四川省肿瘤医院·研究所,四川省癌症防治中心,电子科技大学医学院 临床药学部(蒋刚、陈燕)
甲磺酸伊马替尼(imatinib mesylate,IM)是一种小分子蛋白酪氨酸激酶抑制剂,分子式为C29H31N7O·CH4SO3,可有效抑制BCR-ABL酪氨酸激酶及c-Kit等的活性,其作为靶向药物,临床用于治疗慢性粒细胞白血病、不可切除/或发生转移的胃肠间质瘤(gastrointestinal stromal tumors,GIST)、急性淋巴细胞白血病等。IM在人体内主要循环代谢产物是N-{4-甲基-3-[(4-吡啶-3-嘧啶-2-基)氨基]苯基}-4-(哌嗪-1-甲基)-苯甲酰胺(N-去甲基伊马替尼,N-Desmethyl imatinib,NDI),其药效与原型药相似,且IM作为口服小分子靶向药物,存在巨大的个体内差异及个体间差异[1],而多项研究表明IM血药浓度与患者临床反应及获益存在相关性[2-4],故IM及其代谢产物的血药浓度监测在临床科学制定合理用药方案及精准个体化治疗中具有重要意义。
二维液相色谱(two-dimensional liquid chromatography with ultraviolet detection,2D-LC-UV)系统由全自动2D-LC-UV耦合仪与岛津高效液相色谱(high-performance liquid chromatography,HPLC)仪组成进行药物浓度测定。所有部件由耦合仪连接,包括自动进样器,一维色谱泵,中间转移系统,二维色谱泵,紫外检测器等模块;血液样品经自动化处理后,传递至后级HPLC进行定量分析。具体结构见图1。本文采用其二级单工模式建立一种同时测定人血浆中IM和NDI浓度的方法,主要经过一维液相色谱系统(以下简称LC1)进样、目标物转移、二维液相色谱系统(以下简称LC2)进样三个步骤;LC1进样:样品从自动进样器进入流路系统中,首先经过一维萃取柱进行第一次分离(图1A);目标物转移:样品经过萃取柱的一级分离后,含有目标物的物质或成分被捕获之后转移至中间柱(图1B);LC2进样:中间柱捕获到一级分离目标物后与分析柱相连,目标物最后进入二维分析柱再次分离并到达检测器进行测定(图1C),该方法分离能力强[5],已有研究者采用2D-LC-UV建立了测定伏立康唑、氯氮平、丙戊酸、氨磺必利等药物血药浓度的方法[6-9],但基于2D-LC-UV建立的IM及其代谢产物人血药浓度的检测方法国内未见报道。
1 材料与方法
1.1 仪器
2D-LC-UV检测系统:由全自动多级2D-LC-UV耦合仪MLC2420(湖南德米特仪器有限公司)与HPLC仪LC-20AT(日本岛津公司)组成;GH-202型电子天平(上海右一仪器有限公司);TG-16高速离心机(四川蜀科仪器有限公司);XW-80A漩涡混合器(上海琪特分析仪器有限公司);Mini-15K微型高速离心机(杭州奥盛仪器有限公司);四川优普超纯水机(四川优普超纯科技有限公司)。
1.2 药品与试剂耗材
IM标准品(纯度>99%,北京中科质检生物技术有限公司,420020);NDI标准品(纯度>99%,中国食品药品检定研究院,批号:A8029);IM(格列卫,瑞士诺华制药公司,WMY83);空白马血浆(美国Gibco公司,批号:16050-122);乙腈(色谱纯,天津市科密欧化学试剂有限公司);磷酸(色谱纯,天津市科密欧化学试剂有限公司);氨水(色谱纯,上海阿拉丁生化科技股份有限公司,批号:F2026012);磷酸铵三水(含量>98%,大连美仑生物技术有限公司,MB0216);ORG-1A去蛋白剂(湖南德米特仪器有限公司)。

图1 二维液相色谱仪二级单工模式工作流程图
1.3 色谱条件
一维萃取柱:型号为Aston SX1(3.5 mm×25 mm,5 μm),流动相为V(甲醇)∶V(乙腈)∶V(磷酸铵水溶液)=25∶20∶55,流速=0.8 mL/min;中间柱型号为Aston SCB(4.6 mm×10 mm,3.5 μm),辅助流动相为纯水;二维分析柱:型号为Aston SCB(4.6 mm×125 mm,5 μm),流动相为V(乙腈)∶V(磷酸铵盐溶液)=38∶62,流速=1.2 mL/min;柱温:40 ℃,检测波长:264 nm;进样量:500 μL。
1.4 溶液配制
1.4.1 标准曲线工作溶液的配制 IM标准曲线工作液的配制:精确称取IM标准品1.40 mg,用50%甲醇的水溶液溶解并定容于10 mL容量瓶中,得到0.14 mg/mL的IM标准储备液。精密吸取IM储备液,并用50%的甲醇进行稀释,得到IM六个浓度校准品溶液,分别为:134.4、448.0、1 120.0、2 800.0、7 000.0和14 000.0 ng/mL,并在-20℃条件下保存,作为标准曲线工作液。
NDI标准曲线工作液的配制:精确称取NDI标准品6.86 mg,用50%甲醇的水溶液溶解并定容于5 mL容量瓶中,得到1.372 mg/mL的NDI标准储备液。精密吸取NDI储备液,并用50%的甲醇进行稀释,得到NDI六个浓度校准品溶液,分别为:131.7、439.0、1 097.6、2 744.0、6 860.0和13 720.0 ng/mL,并在-20℃条件下保存,作为标准曲线工作液。
1.4.2 质控品溶液的配制 IM质控品溶液的配制:精密吸取1.4.1中IM储备液,并用50%的甲醇进行稀释,得到IM低、中、高三种质控品溶液,分别为:336.0、8 400.0、11 200.0 ng/mL,以备质控品配制。
NDI质控品溶液的配制:精密吸取1.4.1中NDI储备液,并用50%的甲醇进行稀释,得到NDI低、中、高三种质控品溶液,分别为:329.3、8 232.0、10 976.0 ng/mL,以备质控品配制。
1.5 血浆样品制备
标准曲线血浆样品制备:用移液枪分别移取1.4.1配制的若干种不同浓度的IM及NDI标准曲线工作溶液100 μL,加入900 μL空白血浆混合制成不同浓度IM及NDI的标准曲线血浆样品,(IM:13.44、44.80、112.00、280.00、700.00和1 400.00 ng/mL;NDI:13.17、43.90、109.76、274.40、686.00和1 372.00 ng/mL)。
质控品制备:用移液枪分别移取1.4.2配制的低、中、高浓度IM及NDI质控品溶液100 μL,加入900 μL空白血浆混合,分别得到IM及NDI低、中、高3个浓度质控品样品,(IM:33.60、840.00、1 120.00 ng/mL;NDI:32.93、823.20、1 097.60 ng/mL)。
1.6 样品处理
取1 000 μL有机处理剂(ORG-1A去蛋白剂)于2 mL无菌Ep管中,加入400 μL待测血浆样品,涡旋仪涡旋60 s后,高速离心(145 000 rpm,8 min),用移液枪取上清液至进样瓶中,待进样分析。若为人血液样品,则先进行离心(5 000 rpm,5 min),取其上清液再进行上述操作,将上清液置于-20℃的条件下进行保存。
1.7 方法学考察
1.7.1 专属性 分别对空白血浆、空白血浆加入IM+NDI标准品以及患者口服IM后血浆样品,在1.3的色谱条件下进样检测。
1.7.2 标准曲线与定量下线 取1.5所制备的IM及NDI标准曲线血浆样品,在1.3色谱条件下进行检测分析,以质量浓度为横坐标X,峰面积为纵坐标Y进行线性回归,拟合得到相应的IM和NDI标准曲线方程。并取1.5所制备的IM及NDI标准曲线最低点浓度的血浆样品各6组平行组,在1.3的色谱条件下同日进样,计算其定量下限的变异系数。
1.7.3 回收率与精密度 取1.5所制备的IM及NDI定量下限、低、中、高质控品样品,每个浓度设置5组平行组,在1.3的色谱条件下同日进样,并计算回收率及日内精密度;每个浓度再设置5组平行组,连续进样3天,计算方法日间精密度。
1.7.4 稳定性 取1.5制备的IM及NDI低、中、高质控品样品,每个浓度设置3组平行组,分别考察样品在4°C条件下12 h、反复冻融3次以及-80℃环境放置20 d的稳定性。
1.8 统计学方法

1.9 血药浓度检测的临床应用
根据上述所建立的同时测定人血浆中IM及其代谢产物浓度的方法,选择口服IM的GIST患者血样进行验证与应用。患者选择条件为长期、稳定服用IM超过一个月,并在患者第二日服药前2~3 h进行采血。本论文课题已获得四川省肿瘤医院伦理委员会的批准(批件号:SCCHE-02-2020-044),涉及的血样采集患者均签署了《知情同意书》。
2 结 果
2.1方法学考察结果
2.1.1 专属性 按照上述条件测定,其专属性结果见图2,血浆样品分离测定不受内源性物质等杂质干扰;IM和NDI保留时间分别为10.8 min、7.5 min左右。

图2 伊马替尼与N-去甲伊马替尼2D-LC-UV色谱图
2.1.2 标准曲线与定量下限 拟合得到相应的IM和NDI标准曲线方程分别为:Y=1 011.48X-3 526.20(R2=0.9999),定量下限:13.44ng/mL;Y=670.901X-914.774(R2=0.9999),定量下限:13.17 ng/mL;IM与NDI定量下限的变异系数测定结果分别为5.79%和2.77%,均小于6%(表1)。

表1 最低定量限(N=6)
2.1.3 回收率与精密度 结果表明,IM和NDI的日内、日间精密度相对标准偏差均小于6%,回收率均在90%~110%之间,回收率与精密度良好,具体结果见表2。

表2 方法回收率与精密度结果(N=5)
2.1.4 稳定性 结果显示,所有稳定性实验考察结果相对标准偏差均小于5%,表明该方法稳定性良好,短期、长期、反复冻融的储存条件并不影响本方法对样品的准确测定(表3)。
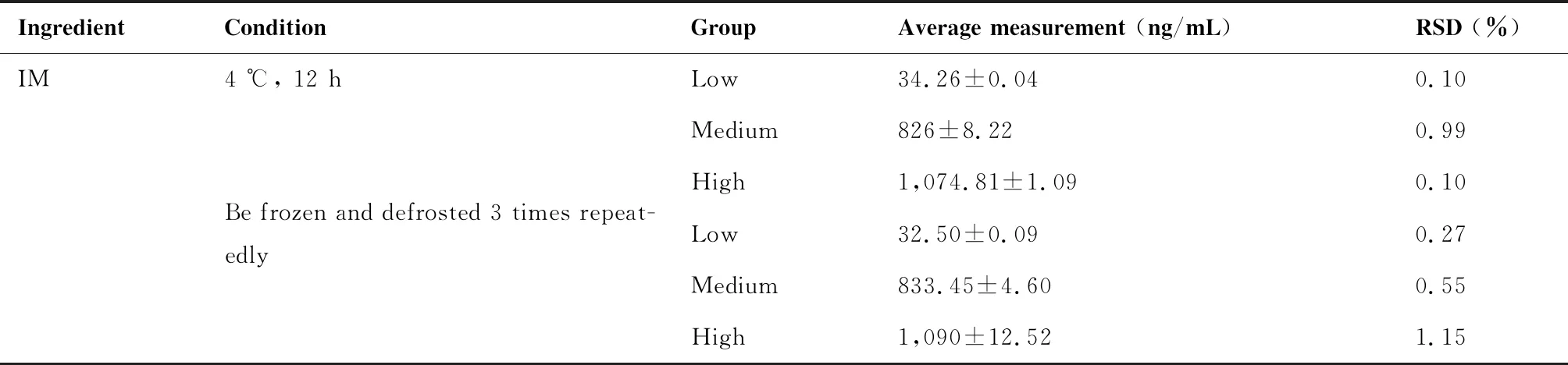
表3 样品稳定性结果(N=3)

(Table 3 continues on next page)
2.2 血药浓度检测临床应用
本研究选择了10位口服IM的GIST患者进行验证与应用。样品测定随行一个中浓度质控品,结果其变异系数均<5%(IM变异系数小于3.11%,NDI变异系数小于0.78%),患者血药浓度结果见表4。

表4 以2D-LC-UV法检测临床GIST患者血药浓度
3 讨 论
目前,关于IM血药浓度的检测方法主要有HPLC法[10]、反相高效液相色谱(reversed phase high-performance liquid chromatography,RP-HPLC)[11]、液相色谱-串联质谱法(liquid chromato-graphy-tandem mass spectrometry,LC-MS/MS)[12]、超高效液相色谱-质谱(ultra-performance liquid chromatography-tandem mass spectrometry,UPLC-MS/MS)法[13]等;其中HPLC法虽操作要求不高,价格较为低廉,但分析时间较长、重现性较差,血液样品前处理过程复杂;LC-MS/MS法在上述方法中较为成熟、专属性好且准确度高,常作为首选方法[14],但其成本昂贵,“基质效应”影响大且对操作人员要求较高。本研究所采用的2D-LC-UV可综合HPLC法与LC-MS/MS法的优点,较HPLC法精准度高、重现性好,较质谱法及LC-MS/MS法无“基质效应”等,具体特点如下:1)本方法进样体积为500 μL,是HPLC和LC-MS/MS等方法进样量的25倍左右,可有效提高灵敏度与准确度;2)待测血浆样品处理步骤简单、操作简便,有机处理剂沉淀蛋白离心后上清液可直接进样,无需氮吹、复溶、萃取等操作;3)通过文献查阅,暂未发现使用HPLC法和RP-HPLC法建立同时测定IM及NDI血药浓度的方法,UPLC-MS/MS法可同时检测IM及其代谢物浓度,但仅限于大鼠血浆[15]。本研究应用的是全自动2D-LC-UV系统,其中间柱所具有的拦截与透过作用可实现不同化学结构药品或成分的共同测定[6],故本方法可同时测定IM及NDI的血药浓度,且成功应用于临床患者的血药浓度检测;4)其他:本研究方法无“基质效应”,进样前色谱柱平衡仅需15~20 min,样品定量分析完成过后也无需冲洗色谱柱,且操作简单,成本低廉。这些特点可在保证检测精准度的情况下大大提升临床应用的简便度,并降低成本。
IM血药浓度与患者药物反应密切相关。B2222回顾性研究中,有关IM患者血药浓度与药效关系的分析结果显示,获得完全缓解、部分缓解或者疾病无进展患者的血药浓度比未起上述疗效患者的血药浓度高,且IM血浆药物谷浓度C0>1 100 μg/L的患者可获得更明显的临床获益,其无进展生存期要明显长于C0<1 100 μg/L的患者[16]。而NDI作为IM的活性代谢产物,具有与IM相似的药理活性[17]。研究表明,患者服用IM后,其血药浓度、疗效及毒副反应表现存在较大的个体差异[18],不同国家与地区患者人群的血药浓度及对IM的临床效应也有所不同[19-21];本研究根据所建立的2D-LC-UV进行了临床应用,结果显示服用相同剂量IM的GIST患者,其IM血药浓度结果却300.34~1 392.07 ng/mL不等。IM血药浓度的高低受多种因素影响,有研究结果表明白细胞数、体表面积、粒细胞数、酸性糖蛋白、肌酐清除率、白蛋白以及血红蛋白水平均有可能是改变IM药动学参数的重要协变量[14];除此之外,肝肾功能等患者自身病理状况也是导致IM血药浓度产生个体化差异的关键因素之一:挪威专家进行回顾性研究[22]发现,IM稳态血药谷浓度随疾病进展而降低;一项评估不同肝功能水平的口服IM晚期肿瘤患者的药动学研究[23]结果显示,不同程度的肝功能不全患者在使用平均剂量时,其稳态血药浓度比肝功能正常患者有所增加;赵曼等[18]研究显示,轻中度肾功能异常的患者较肾功能正常的患者调整药物剂量后的Cmax和AUC均明显增加。近几年,愈来愈多研究发现,CYP家族代谢酶、多药耐药蛋白、乳腺癌耐药蛋白、有机阳离子转运体1和有机阴离子转运蛋白等药代动力学相关基因多态性可导致IM在体内的药代动力学参数发生改变,故而引起个体间临床效应的差异[24-27],如CYP3A5*5(6986A>G)基因多态性研究中,携带GG基因型的个体与AA基因型相比,CYP3A5酶的表达降低至少0.1%,患者具有相对更高的IM血药浓度水平[28]。故而IM血药浓度检测可体现个体药物治疗反应特点,为临床科学合理制定用药方案及实现个体化治疗、提高疗效以及降低不良反应风险起到重要作用。
关于IM有效血药浓度范围还未有明确指定,但现阶段较为公认的是慢性粒细胞白血病患者IM血药浓度大于1 000 ng/mL、GIST患者血药浓度大于1 100 ng/mL可作为最低有效治疗参考[28-29],由于每个国家和地区患者人群的血药浓度存在差异,故关于中国患者有效血药浓度范围有待进一步研究。本研究主要建立了一种同时检测人血浆中IM及其代谢产物浓度的2D-LC-UV,并于临床进行验证与应用。方法学研究结果显示专属性,灵敏度,日内、日间精密度(相对标准偏差<6%)及稳定性(相对标准偏差<5%)良好;回收率>90%;IM线性范围13.44~1 400.00 ng/mL(R2=0.9999),NDI:13.17~1 372.00 ng/mL(R2=0.9999),线性关系良好。该方法较传统HPLC法准确度高、重现性好,较LC-MS/MS法操作简便、无“基质效应”,2D-LC-UV样品前处理简单,检测时间短且成本较为低廉,可用于临床IM血药浓度检测。
作者声明:本文全部作者对于研究和撰写的论文出现的不端行为承担相应责任;并承诺论文中涉及的原始图片、数据资料等已按照有关规定保存,可接受核查。
学术不端:本文在初审、返修及出版前均通过中国知网(CNKI)科技期刊学术不端文献检测系统的学术不端检测。
同行评议:经同行专家双盲外审,达到刊发要求。
利益冲突:所有作者均声明不存在利益冲突。
文章版权:本文出版前已与全体作者签署了论文授权书等协议。

