硫酸头孢喹肟纳米凝胶的制备及疗效初步评价
董 贵,孟凡艳,鲁壮壮,贺建忠,陶大勇,陈 伟,,罗万和* (1.塔里木大学 动物科学学院/新疆生产建设兵团 塔里木动物疫病诊断与防控工程实验室,新疆 阿拉尔 8400;2.新疆生产建设兵团 塔里木畜牧科技重点实验室,新疆 阿拉尔 8400;.新疆生产建设兵团 塔里木盆地生物资源保护利用重点实验室,新疆 阿拉尔 8400)
由金黄色葡萄球菌(Staphylococcusaureus,S.aureus)引起的奶牛乳腺炎对奶牛生产的危害性很大[1-4]。更重要的是,S.aureus可逃避机体免疫系统和抗菌药物的清除作用,以小菌落变异株(Staphylococcusaureussmall colony variants,SASCVs)的方式在宿主细胞内持续存在,引起奶牛持续性和反复性感染奶牛乳腺炎[5]。硫酸头孢喹肟因对S.aureus具有较强的抗菌活性,且经乳房灌注后可迅速分布整个乳房并维持较高的药物浓度,故常用于治疗由S.aureus引起的奶牛乳腺炎。其中魏占勇等[6]用硫酸硫酸头孢喹肟乳房注入剂治疗干乳期奶牛乳房炎,其治愈率为66.7%。但兽医临床上不合理使用硫酸头孢喹肟治疗奶牛乳腺炎,导致硫酸头孢喹肟难以清除SASCVs菌株,特别是胞内SASCVs菌株,已引起细菌耐药性等问题[7]。
在离子交联剂作用下,通过凝胶材料之间静电作用自组装所形成的纳米凝胶药物递送系统可用于包裹各种药物分子[8]。纳米凝胶具有优良的载药能力、结构稳定性和生物相容性等特点,可增强抗菌药物对细菌的抗菌活性,并提高药物的生物利用度[9]。为提高硫酸头孢喹肟对由SASCVs菌株引起的奶牛乳腺炎的治愈率,本研究以SASCVs菌株为研究对象,以纳米凝胶为药物递送系统,在离子交联剂作用下,通过凝胶材料之间静电作用自组装形成硫酸头孢喹肟纳米凝胶,以外观性状、微观形态、沉降体积比、再分散性、包封率(EE)、载药量(LC)、粒径和Zeta电位为指标,筛选最优配方;通过临床症状和PCR确定是否成功构建SASCVs菌株感染小鼠模型;通过对比最优硫酸头孢喹肟纳米凝胶和其商品化注射剂治疗小鼠感染模型的结果,评价硫酸头孢喹肟纳米凝胶的优势。本研究旨在为治疗由SASCVs菌株引起的奶牛乳腺炎提供依据。
1 材料与方法
1.1 药品与试剂硫酸头孢喹肟注射液(四川正牧生物药业有限公司,批号:221362299,含量:2.5 g/L);三聚磷酸钠(TPP,国药集团化学试剂有限公司,批号:20131105,含量:98%);海藻酸钠(SA,化学纯,国药集团化学试剂有限公司);硫酸头孢喹肟标准品(上海源叶生物科技有限公司,批号:B34157,纯度≥98%);硫酸头孢喹肟原料药(国药集团化学试剂有限公司,批号 20110601,纯度99%);明胶(国药集团化学试剂有限公司,批号:20231010);引物、dNTP、Easy Taq酶和Easy Taq buffer(生工生物工程(上海)股份有限公司);细菌基因组DNA提取试剂盒(天根生化科技北京有限公司)。
1.2 主要仪器激光纳米粒度仪ZS3600(丹东百特仪器有限公司);集热式恒温磁力搅拌器DF-101S(上海力辰邦西仪器科技有限公司);加热磁力搅拌器IT-07A3型(上海沪西股份有限公司);PCR仪、凝胶成像系统、电泳仪(Bio-Rad公司)。
1.3 试验菌株金黄色葡萄球菌ATCC 29213、SASCVs菌株由本实验室保存。
1.4 实验动物120只清洁级昆明小鼠(18~22 g)由塔里木大学动物实验站提供。
1.5 硫酸头孢喹肟纳米凝胶的制备分别以不同质量浓度(0.20,0.25,0.30 g/L)的TPP、明胶(10,15,20,25 g/L)和SA(10,15,20,25 g/L)为离子交联剂、阳离子药物载体和阴离子药物载体,通过静电作用自组装形成硫酸头孢喹肟纳米凝胶。具体制备方法为:称取一定量的TPP、明胶和SA分别溶于一定体积的蒸馏水中,同时称取一定量硫酸头孢喹肟溶于一定体积的无水乙醇中,涡旋使其完全溶解。先后分别将硫酸头孢喹肟溶液和TPP溶液在1 500 r/min 转速下,缓慢滴加至明胶溶液中。再将明胶混合溶液在1 500 r/min转速下,缓慢滴加至SA溶液中,通过静电作用自组装形成硫酸头孢喹肟纳米凝胶。
1.6 配方筛选以制备纳米凝胶的外观性状、微观形态、沉降体积比、再分散性、EE、LC、粒径和Zeta电位为指标,筛选硫酸头孢喹肟纳米凝胶最优配方。
1.6.1外观性状 根据中国兽药典中对于液体制剂的要求,观察硫酸头孢喹肟纳米凝胶系统的外观性状,包括气味、颜色、状态等,判断有无变色、发霉、产生气体、异物或其他变质现象。
1.6.2微观形态 精密量取制得的硫酸头孢喹肟纳米凝胶1 mL,用蒸馏水稀释100倍摇匀,经过负染后吸取2 μL样品滴在带有薄膜的铜网上,待干燥后通过扫描电镜观察其微观形态。
1.6.3沉降体积比 准确量取30 mL纳米凝胶置于量筒中并摇匀,静置3 h,将沉降前悬浮物液面初始高度记录为H0,静置3 h后观察沉降物部分高度不再改变时为H,则沉降体积比为H/H0。
1.6.4再分散性 准确量取30 mL纳米凝胶放于量筒中,以60 r/min旋转3 min,根据是否重新均匀分散评价纳米凝胶的再分散性。
1.6.5含量测定 通过紫外分光光度计绘制硫酸头孢喹肟的标准曲线。精确吸取制备的硫酸头孢喹肟纳米凝胶1 mL,经离心后,吸取上清液,并过滤。通过细胞超声破碎仪使凝胶体系破坏后,用紫外分光光度计测定其中硫酸头孢喹肟的含量,即未被包封的硫酸头孢喹肟的含量。根据下式计算出EE和LC。
EE=(纳米凝胶中替米考星含量/替米考星总量)×100%;
LC=(纳米凝胶中替米考星含量/纳米凝胶总量)×100%。
1.6.6Zeta电位和粒径 从硫酸头孢喹肟纳米凝胶中量取200 μL样品,用蒸馏水稀释 10倍,保存于5 mL 离心管中备用,使用马尔文纳米激光粒度仪测定Zeta电位和粒径,每次试验重复测定3次,取平均值。
1.7 PCR检测方法采用50 μL PCR扩增体系:ddH2O 40.7 μL,Easy Taq酶0.3 μL,Easy Taq buffer 5 μL,dNTP 1 μL,上、下游引物各1 μL,模板DNA 1 μL。nuc基因扩增程序:94℃ 5 min;94℃ 1 min,55℃ 30 s,72℃延伸1.5 min,34个循环,72℃总延伸3.5 min。以金黄色葡萄球菌ATCC 29213为阳性对照,以灭菌去离子水为阴性对照。

表1 引物信息
1.8 SASCVs菌株感染小鼠模型的建立将SASCVs菌株复苏、传代后,取100 μL处于对数生长期菌株接种于2 mL LB肉汤培养基中,37℃孵育24 h,即为试验原液,并用生理盐水稀释至1×109CFU/mL,作为备用菌液。将120只18~22 g小鼠随机分成4组(硫酸头孢喹肟纳米凝胶治疗组、商品化硫酸头孢喹肟注射剂治疗组、阳性对照组、阴性对照组),每组30只。其中硫酸头孢喹肟纳米凝胶和注射剂治疗组、阳性对照组每只小鼠各接种0.4 mL备用菌液,连续感染3 d,构建SASCVs菌株感染小鼠模型。第4组小鼠不进行感染(阴性对照组)。确认感染后,每3 h观察1次,期间观察被感染小鼠的精神状态,并记录小鼠的外观变化、临床症状和死亡情况,以临床症状角度判定是否构建SASCVs菌株感染小鼠模型。同时采集被感染小鼠的病变组织,经细菌基因组DNA提取试剂盒提取其DNA后,进行PCR扩增,以分子生物学角度判定是否构建SASCVs菌株感染小鼠模型。
1.9 治疗试验将硫酸头孢喹肟纳米凝胶(2.5 mg/kg)和商品化硫酸头孢喹肟注射剂(2.5 mg/kg)通过肌肉注射治疗感染小鼠模型。具体如下:硫酸头孢喹肟纳米凝胶治疗组采用硫酸头孢喹肟纳米凝胶治疗被感染小鼠;商品化硫酸头孢喹肟注射剂治疗组采用商品化硫酸头孢喹肟注射剂治疗被感染小鼠;阳性对照组将SASCVs菌株感染小鼠后,不做任何处理;阴性对照组的小鼠不感染SASCVs菌株。连续治疗3 d,观察并记录5 d内小鼠治疗情况。
2 结果
2.1 硫酸头孢喹肟纳米凝胶配方的筛选
2.1.1外观性状 当TPP为 0.25 g/L、明胶为 25 g/L、SA为 15 g/L时,所制备的硫酸头孢喹肟纳米凝胶为最佳配比,无沉淀和絮状物,颜色清亮、无异常气味、无发霉、无变色、无沉淀等异物、不产生气体及其他变质现象(图1)。

图1 硫酸头孢喹肟纳米凝胶的外观性状
2.1.2微观形态 扫描电镜下头孢喹肟纳米凝胶的形态表征如图2所示,头孢喹肟呈不规则块状,体积较小,表面较为光滑平整,被明胶和海藻酸钠所形成的网络结构所包裹。
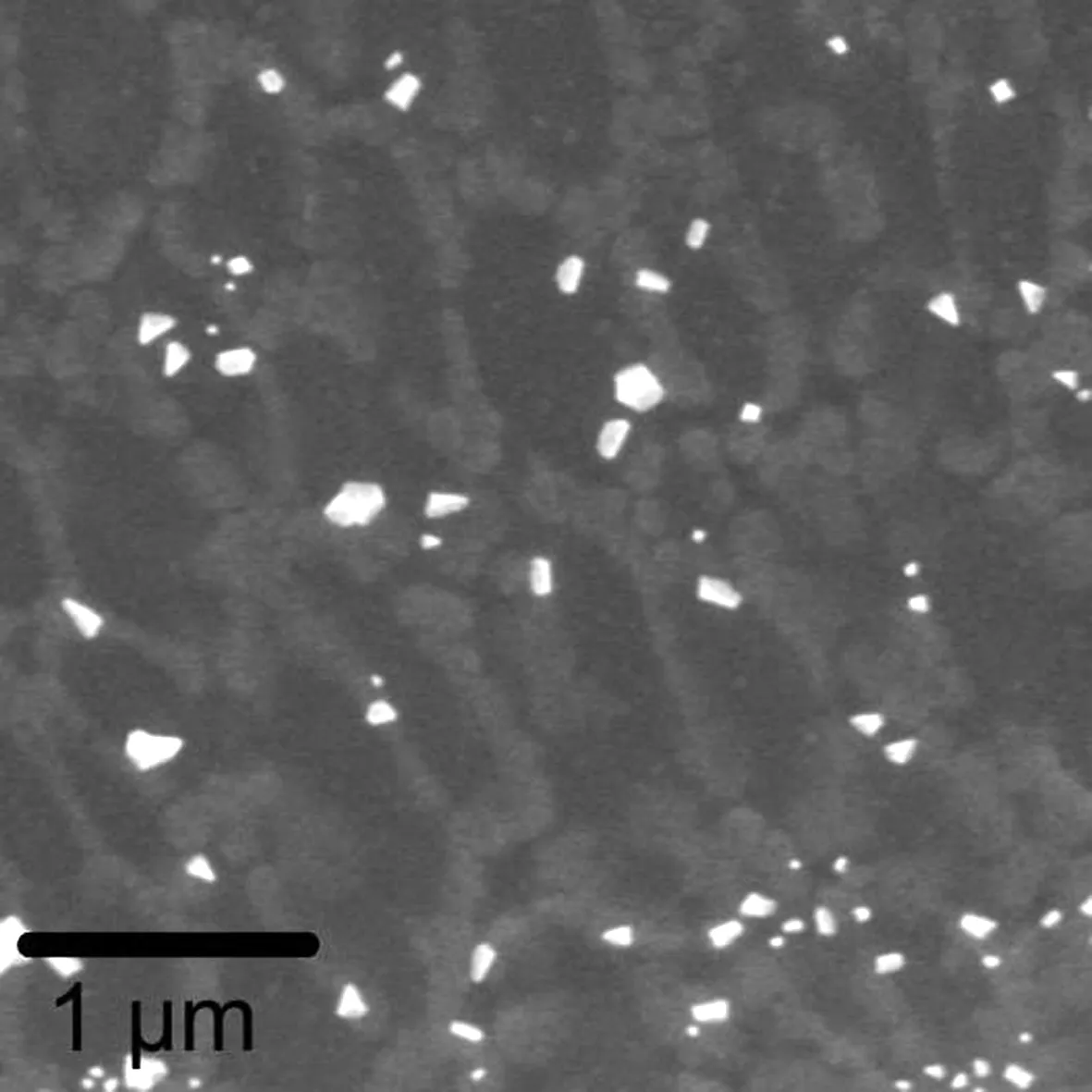
图2 硫酸头孢喹肟纳米凝胶的微观形态(× 10 000)
2.1.3沉降体积比和再分散性 根据药典规定H/H0值不得低于0.9。H/H0值越大,即代表沉降物的高度与纳米凝胶的原始高度越接近,相应的纳米凝胶也就越稳定。所制备的硫酸头孢喹肟纳米凝胶H/H0值为1,表明该纳米凝胶制剂稳定性高。量筒下部的沉降部分能很快的重新均匀分散,表明该纳米凝胶不易凝集,再分散性良好。
2.1.4EE和LC 测定了在 291 nm 处硫酸头孢喹肟浓度与D值的标准曲线,由图3可见,在0.5~100 mg/L的质量浓度范围内线性关系良好,标准曲线回归方程为y=0.512 9x+0.148 6,相关系数r=0.999 4,线形关系良好。根据标准曲线回归方程,计算出其EE和LC分别为(71.2%±1.32)%,(16.3±0.45)%。
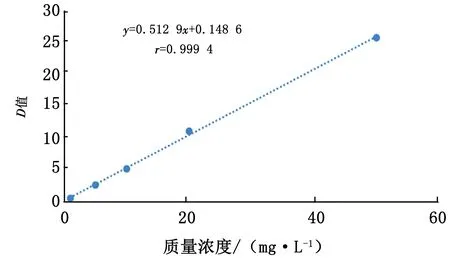
图3 硫酸头孢喹肟的标准曲线
2.1.5Zeta电位和粒径 最优配方的硫酸头孢喹肟纳米凝胶的粒径为(23.01±1.14) nm,Zeta电位为(-25.4±0.91) mA,如图4,5所示。
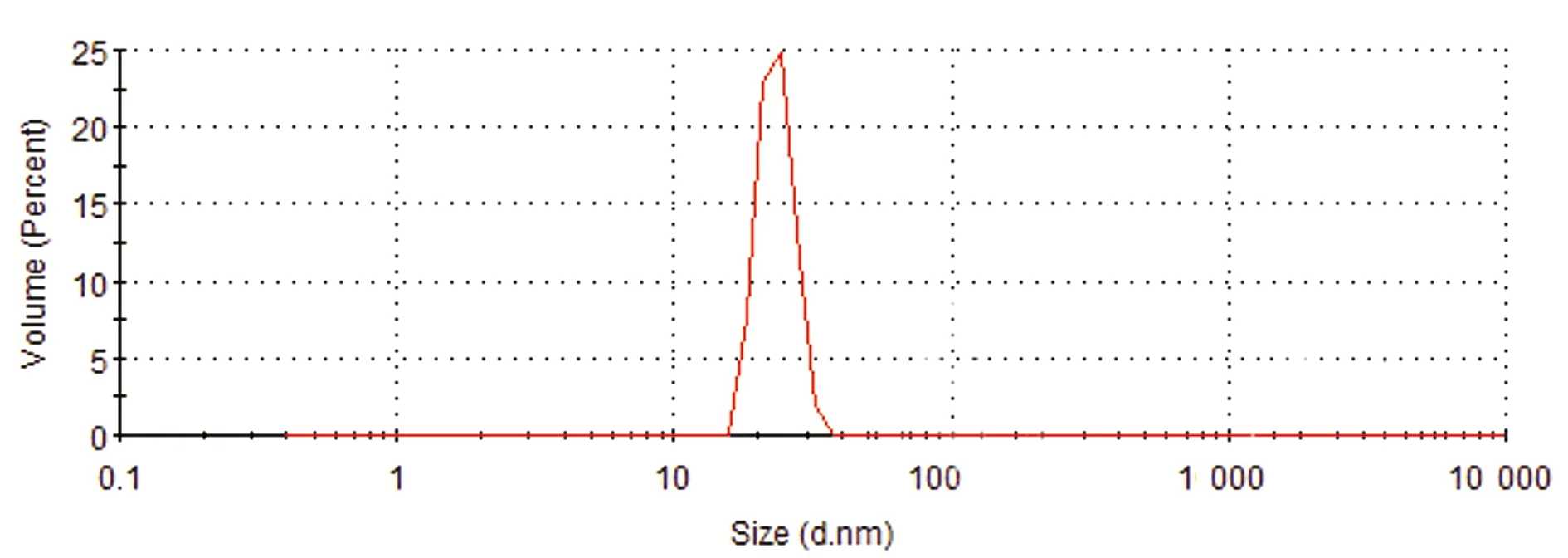
图4 硫酸头孢喹肟纳米凝胶的粒径
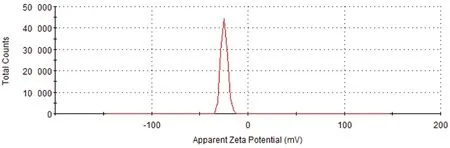
图5 硫酸头孢喹肟纳米凝胶的Zeta电位
2.2 感染小鼠模型的判定
2.2.1临床症状 感染SASCVs菌株小鼠在1 d后出现精神状态较差,活动、饮食、饮水较少,背毛耸立,肛门周围的污秽物较多且黏性较大,眼为干酪样物封闭。后期出现蜷缩和肛门周围红肿等现象,阴性对照组小鼠饮食和饮水均正常,未出现任何临床发病症状。即从临床症状角度判定已构建SASCVs菌株感染小鼠模型。
2.2.2PCR检测 将感染小鼠病变组织经细菌基因组DNA提取试剂盒提取DNA后,进行PCR扩增。结果显示,其DNA扩增产物大小为279 bp且为单一明亮的目的条带,如图6所示。即从分子生物学角度判定已成功构建SASCVs菌株感染小鼠模型。
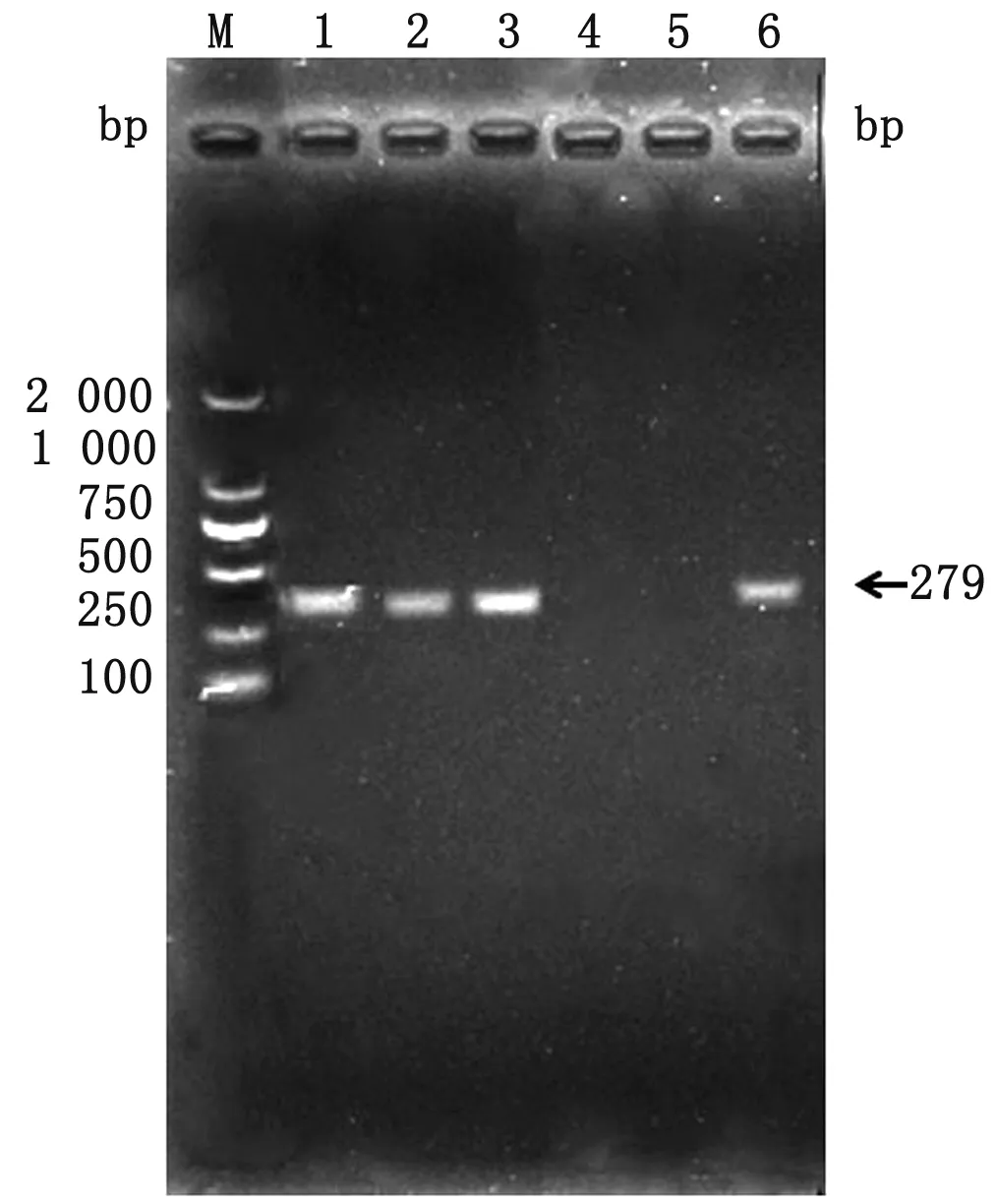
M.DL2000 DNA Marker;1.硫酸头孢喹肟纳米凝胶治疗组小鼠DNA;2.商品化硫酸头孢喹肟注射剂治疗组小鼠DNA;3.阳性对照组小鼠DNA;4.阴性对照组小鼠DNA;5.阴性对照;6.阳性对照图6 SASCVs菌株感染小鼠模型的PCR扩增结果
2.3 治疗结果被感染小鼠经硫酸头孢喹肟纳米凝胶及其商品化注射剂治疗后,肛门周围干净,无污秽物,眼周干酪样封闭症状消失,饮食饮水及精神状态恢复正常。将治愈后小鼠组织经细菌基因组DNA提取试剂盒提取DNA后,进行PCR扩增。扩增结果显示,治疗组未出现目的条带,如图7所示。即从分子生物学角度判定已成功治愈SASCVs菌株感染的小鼠。
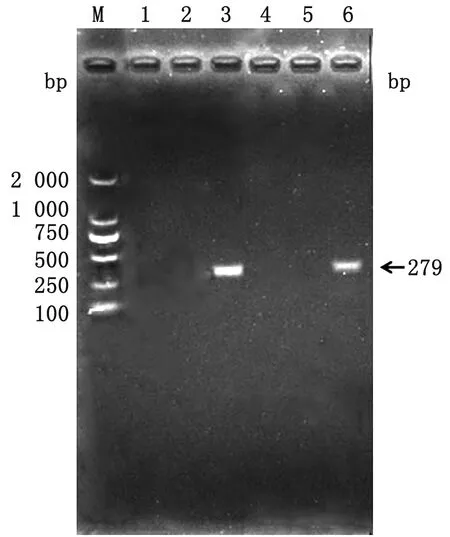
M.DL2000 DNA Marker;1.硫酸头孢喹肟纳米凝胶治疗组小鼠DNA;2.商品化硫酸头孢喹肟注射剂治疗组小鼠DNA;3.阳性对照组小鼠DNA;4.阴性对照组小鼠DNA;5.阴性对照;6.阳性对照图7 治疗SASCVs菌株感染小鼠模型的PCR扩增结果
3 讨论
由S.aureus引起的奶牛乳腺炎给奶牛养殖业带来巨大损失,其SASCVs在宿主细胞内持续存在,引起奶牛持续性和反复性感染奶牛乳腺炎。由于SASCVs菌株可寄生于细胞中,常规抗菌药物剂型难以有效治疗胞内SASCVs菌株感染,会引起治疗失败和细菌耐药性等问题[5]。纳米凝胶可通过凝胶材料(如SA、壳聚糖、明胶、羧甲基壳聚糖等)长时间黏附于奶牛乳腺表面,并渗入乳腺上皮细胞内,将包裹的抗菌药物送达到感染部位,有助于靶向治疗由SASCVs引起的奶牛乳腺炎[10-11]。而凝胶材料的选择对于纳米凝胶的制备至关重要。明胶具有优异的阳离子药物载体功能、一定的抗菌活性、抗炎和抗氧化作用,可提高动物机体免疫力,对于治疗SASCVs感染具有重要意义[12]。SA的水溶液表现出聚阴离子行为,因其具有无毒性、pH值敏感性、生物黏附性和生物相容性,且所形成的凝胶反应条件温和、可避免敏感性药物、蛋白质、细胞和酶等活性物质的失活,常用于阴离子药物载体[13]。ZHOU等[14]通过将固体脂质纳米技术与水凝胶技术相结合,以壳聚糖为阳离子药物载体,以SA为阴离子药物载体,通过静电作用自组装成替米考星复合纳米凝胶,大大改善了替米考星对S.aureus感染的治疗效果。MUKHOPADHYAY等[15]通过离子凝胶技术,以明胶为阳离子药物载体,以羧甲基壳聚糖为阴离子药物载体,制备了恩诺沙星纳米凝胶,提高了恩诺沙星的生物效应。由此可见,以明胶、壳聚糖、羧甲基壳聚糖和SA等为凝胶材料所制备的纳米凝胶可提高抗菌药物对细菌的抗菌活性,改善其生物效应[16]。
本试验以TPP为离子交联剂,以明胶为阳离子药物载体,以SA为阴离子药物载体,通过阴阳离子之间的静电作用自组装形成硫酸头孢喹肟纳米凝胶。其制备工艺简单,操作方便。经过对TPP、明胶和SA配方比例筛选后,发现当TPP为 0.25 g/L、明胶为 25 g/L、SA为 15 g/L时,所制备的硫酸头孢喹肟纳米凝胶为最佳配比。最优配方的硫酸头孢喹肟纳米凝胶外观性状显示无沉淀和絮状物,颜色清亮、无异常气味、无发霉、无变色、不产生气体及其他变质现象,符合兽药典中对于液体制剂的要求;通过扫描电镜,头孢喹肟纳米凝胶的微观形态显示头孢喹肟呈不规则块状,体积较小,表面较为光滑平整,并且被明胶和海藻酸钠所形成的网络结构所包裹,这与ZHOU等[14]所绘制的纳米凝胶模式图相符合;最优配方的硫酸头孢喹肟纳米凝胶沉降体积比为1,表明该纳米凝胶制剂稳定性高;可快速重新均匀分散,表明该纳米凝胶不易凝集,再分散性良好;EE和LC分别为(71.2±1.32)%,(16.3±0.45)%,与FENG等[17]所制备纳米凝胶的EE和LC相接近,表明硫酸头孢喹肟纳米凝胶具有较优的EE和LC;且最优配方的硫酸头孢喹肟纳米凝胶的平均粒径为(23.01±1.14) nm,具有较小的药物尺寸,有助于该纳米凝胶制剂进入宿主细胞内,进而靶向治疗胞内SASCVs感染;Zeta电位为(-25.4±0.91) mV,有利于该纳米凝胶制剂通过静电作用与宿主细胞膜表面正电荷相作用,并吸附于细胞表面,从而更有利于该纳米凝胶制剂进入宿主细胞内。因此,通过表征该纳米凝胶制剂的外观性状、微观形态、沉降体积比、再分散性、EE、LC粒径和Zeta电位等,本试验所研制的硫酸头孢喹肟纳米凝胶符合纳米凝胶的制备要求。
本试验将SASCVs菌株感染小鼠后,出现一系列临床发病现象,如活动、饮食、饮水较少,背毛耸立,肛门周围的污秽物较多且黏性较大,眼为干酪样物封闭,蜷缩和肛门周围红肿等现象;将感染小鼠病变组织经细菌基因组DNA提取试剂盒提取DNA后,其DNA扩增产物大小在279 bp且为单一明亮的目的条带。故通过临床症状和PCR判断已成功构建SASCVs菌株感染小鼠模型。将硫酸头孢喹肟纳米凝胶和其商品化注射液对于SASCVs感染小鼠模型的治愈率分别为90.0%和86.7%,表明本试验所研制的硫酸头孢喹肟纳米凝胶治疗SASCVs感染小鼠的效果略优于硫酸头孢喹肟注射液。综上所述,本研究已初步制备出硫酸头孢喹肟纳米凝胶,具有较好的疗效,为治疗由SASCVs菌株引起的奶牛乳腺炎提供了依据。

