以精神分裂症患者为受试者的生物等效性试验的实践与思考
王夏子,方平飞,朱荣华,杨玲凤,阳喜定,燕强勇,李亚敏(1. 中南大学湘雅护理学院,长沙 410013;. 中南大学湘雅二医院一期临床研究室,长沙 410011)
精神分裂症是一种临床常见的重性精神病,给患者本人及社会带来深远的负面影响。氯氮平对难治性精神分裂症疗效突出[1],但进口原研氯氮平片价格高昂,国产仿制氯氮平片与原研药在治疗效果上是否具有等效性,需通过生物等效性试验来确定。生物等效性试验中的受试者大部分为健康志愿者,由于氯氮平存在首剂效应,健康人服用氯氮平发生严重不良反应的风险远大于患者。出于对受试者的安全考虑,氯氮平片生物等效性试验应选择已经接受过一种批准的氯氮平产品的确定维持剂量治疗的精神分裂症患者[2]。
与健康受试者相比,精神障碍者属于受试者中的弱势人群,其权益更容易在临床试验中受到损害。与其他疾病患者相比,精神分裂症患者发病时行为失控导致的伤人、自伤等行为,使研究者和受试者人身安全受损的风险更高,而其行为能力的不稳定导致其依从性也处于动态变化状态。同时,试验药物氯氮平不良反应较多,即便受试者为长期规律服用氯氮平的患者,也应在试验过程中设置并落实全面的安全性观察。
本院研究机构围绕国家精神卫生临床医学研究中心、国家代谢性疾病临床医学研究中心两个国家中心,建设以精神性疾病和糖尿病为重点的重大疾病防治药物研发的临床评价技术平台。2018年7月至2019年10月期间,采取由药物Ⅰ期临床研究室为主导与精神科合作的形式,先后完成4家制药企业生产的氯氮平片人体生物等效性试验。试验过程中,基于精神疾病患者及精神类药物的特点,在试验的各个阶段实施针对性措施,可保护受试者权益,提高试验质量。
1 试验设计
采用随机、开放、双治疗、两周期交叉设计,10 d为一个周期,两周期间无清洗期,在整个试验周期内受试者均住院。
1.1 药品[2-3]
氯氮平片(受试制剂,规格:每片25 mg,分别由万邦德制药集团股份有限公司、江苏云阳集团药业有限公司、常州制药厂有限公司、上海上药信谊药厂有限公司生产);氯氮平片[参比制剂,商品名:CLOZARIL,规格:每片25 mg,HLS Therapeutics(USA)Inc.]。
1.2 受试者的选择[4-5]
试验均通过了中南大学湘雅二医院伦理委员会批准[(2018)伦审【药】第(K088)号、(2018)伦审【药】第(K064)号、(2018)伦审【药】第(K079)号、(2019)伦审【药】第(K220)号]。所有受试者均为精神分裂症患者,签署知情同意书之后开始筛选体检。
1.2.1 入组标准 ①年龄18~65周岁(包含两端),男女不限;②根据ICD-10诊断为精神分裂症者;③试验前已连续服用稳定剂量的氯氮平片至少3个月,且日服剂量为150~350 mg,在研究期间能够耐受每隔12 h服用100 mg。
1.2.2 排除标准 ①有并发的精神或神经疾病;②有癫痫发作或癫痫病史或有严重疾病病史;③试验前1个月内发生急性胃肠道疾病、急性肝肾疾病、急性代谢疾病、急性内分泌疾病者;④试验前1年内日吸烟超过20支或每周饮酒超过14单位酒精;⑤试验前3个月内参加过其他药物或医疗器械试验者;⑥试验前3个月内献血或大量失血(≥200 mL);⑦ 实验室检查白细胞总数低于4×109·L-1,或中性粒细胞绝对数低于2×109·L-1。
1.3 给药方案与血样采集[2]
入选的受试者随机分为两组,每12 h分别用240 mL水送服100 mg的氯氮平片受试制剂和参比制剂。其中,首次服用参比制剂和受试制剂后尽量保持仰卧位至少6 h,同时,应限制运动至少12 h。第10日早晨给药前10 h至给药后4 h内,要求受试者保持空腹状态,并于早晨给药前1 h至给药后1 h内,禁止饮水。
药物代谢动力学(PK)采血时间点为:第7~10日早晨给药前1 h内,以及第10早晨给药后0.25、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、5.0、6.0、8.0、10.0、12.0 h处采集血浆样品。第11日交叉给药进行第二周期试验,第二周期操作同第一周期。
2 试验运行管理
2.1 科室合作管理模式
由于精神分裂症患者的特殊性,受试者同批次入组管理困难,其他机构氯氮平生物等效性试验一般采用分批入组的方式[6]。本院研究机构采取由药物Ⅰ期临床研究室为主导与精神科合作的形式,Ⅰ期临床试验研究者团队通过以往生物等效性试验操作过程的积累,具有丰富的研究经验,负责提供符合试验要求的设施设备,规范标准操作,规范研究药品、样本、记录、文档的管理;精神科医护人员与精神分裂症患者相处及沟通经验丰富,主要负责受试者观察,及时评估受试者的状态,必要时提供心理疏导。两科室合作运行管理试验,受试者可同批入组入住Ⅰ期临床试验研究病房,并得到与精神科病房同质化的诊疗护理。
2.2 保护受试者权益
2.2.1 筛选期 严格入排标准,筛选时尽量选择病情较稳定、沟通理解能力较强患者;知情同意是重要的一环,也是对于精神障碍受试者比较特殊的过程。本研究的知情同意过程由受试者与其法定监护人共同参与并签字,根据受试者表达意愿的能力程度,在征得其法定监护人代理同意的同时,也询问受试者本人是否愿意参加临床研究,并尊重受试者本人的意愿。
2.2.2 住院期 针对性的临床观察:以阴性症状为主的慢性精神分裂症患者思维形式障碍、言语贫乏,不能及时、准确地向研究者描述躯体不适,精神科医护应耐心询问受试者主观感受,观察并详细记录受试者情绪变化;而幻听、妄想等阳性症状容易导致暴力攻击行为,一旦发现受试者出现指令性语言的幻听、被害妄想症状,需对其进行密切观察,必要时专人监护,预防伤人、自伤、毁物行为,并由研究医师评估受试者是否退出试验。
针对药物的不良反应实施全面的安全性监护:
①受试者服药后避免剧烈运动,注意观察有无头晕、体位性低血压。
②粒细胞缺乏症为氯氮平严重不良反应,试验期间需监测受试者粒细胞水平,在第一周期PK采血结束后对受试者进行血常规检查。同时,注意预防粒细胞降低导致的继发性感染,生活上做好必要协助,使受试者作息规律,协助患者洗澡等其他日常清洁避免口腔、尿路感染等。
③交感神经亢奋引起心动过速为氯氮平另一严重不良反应,受试者在服用研究药物期间每日定时监测其生命体征,当测得心率大于100次·min-1时,由研究医师评估是否使用普萘洛尔缓解症状,并记录合并用药情况。
④便秘也是常见的不良反应,未经缓解可能引起患者的拒药不合作、情绪波动、甚至加重精神症状。每日查房时询问受试者大便情况,连续3 d未解大便、大便困难或合并由便秘引起的恶心、腹痛的受试者,遵医嘱使用开塞露,记录不良事件并追踪转归情况。
2.2.3 随访期 精神分裂症受试者的治疗是长期的,出组后随访应该重点关注合理用药。由于试验期间所有受试者氯氮平给药方案均为每12 h口服100 mg的氯氮平片,试验期结束后研究医师应开具针对性用药方案,并随访了解停用试验用药换药后反应,维持患者病情稳定,防止病情复发。
2.3 质量控制要点
2.3.1 加强科室沟通协调 试验前详细的授权分工和分工确认培训会是减少实施过程中风险提高试验质量的必要前提[7],Ⅰ期临床研究室负责组织两科室多次协调会议及培训。两个科室履行各自职责同时建立畅通的沟通渠道,及时发现问题并高效解决,也是提高药物临床试验质量的重要保障[8]。
2.3.2 重视试验安全管理 在生物等效性试验中,病房环境是影响不良事件发生的重要因素[9]。在整个试验周期内受试者均住院,为确保环境安全,试验开始前由精神医护对所有区域进行反复检查,避免患者可接触锐器等危险物品。入住前寄存所有随身携带物品及衣物,试验期间及时清点受试者生活用品及餐具,避免牙刷、筷子等被患者制作成利器。准备约束性措施器具,严格掌握保护性约束适应证。设置单独隔离室进行约束,避免约束失控患者影响其他受试者情绪。除常规急救药物,应针对氯氮平可能出现的不良事件及严重不良事件准备对症处理药物。
2.3.3 关键节点合理排班 研究表明,精神分裂患者服药依从性差,易出现藏药行为[10]。而生物等效性试验血标本采集时间窗窄,这种频繁的有创操作,可能会导致精神障碍患者的应激反应。在给药、密集采样等时间交叠阶段的关键节点做好风险预估,保证人力充足,合理搭配,预备机动人员。由Ⅰ期临床研究室护士进行操作,精神科护士和安保人员依次引导每位受试者配合操作,注意态度温和动作轻柔,适时安抚。排班表上注明如分药、采血核对、机动采血等详细内容,做到详尽分工、责任到人。
3 结果
3.1 高效率完成临床试验
4项氯氮平试验受试者均同批入组,历时(24±1.22)d完成临床评价部分。共筛选入组104例,脱落5例(其中女性2例),无增补,完成两周期试验99例。4项试验脱落率分别为7.14%(2/28)、4.17%(1/24)、7.69%(2/26)、0(0/26),脱落原因见表1。
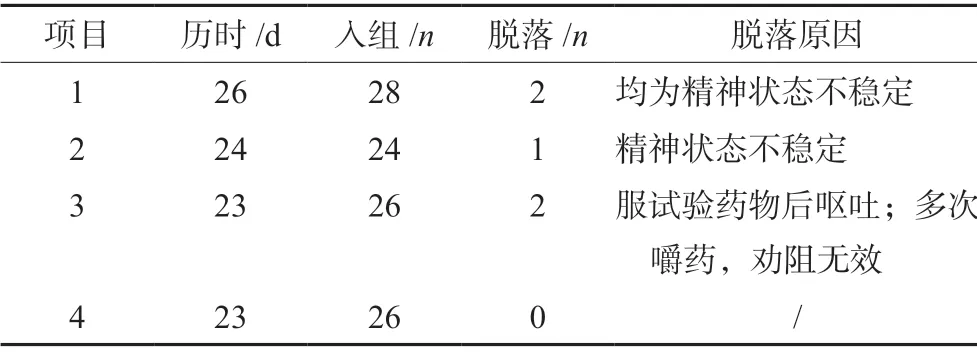
表1 受试者脱落原因Tab 1 Subjects’ dropout
3.2 高质量实施临床试验
目前,4项试验结果均表明氯氮平片受试制剂和参比制剂具有生物等效性,安全性良好。Ⅰ期临床试验研究护士在血样采集、生命体征测量等操作时进行质量检查,PK血样采集共出现2例次采血超窗,其原因均为血管条件较差导致的采血困难,其他均在时间窗允许范围内。生命体征测量,无超窗现象。共有88例受试者发生338例次不良事件,发生率为84.62%。受试制剂和参比制剂均有1例次重度不良事件,其余均为轻度或中度不良事件。4项试验过程中均未发生暴力事件,无任何人员受伤。
3.3 受试者依从性良好
除退出的受试者外,其余完成试验受试者均在两周期按方案要求服用了规定剂量的药物,未发现有药品藏匿或者吐出的情况,整体服药依从性良好。在研究者引导下,主动配合采样、生命体征测量、体格检查、心电图检查等操作。在精神科护士协助下,试验期间所有受试者作息规律,饮食饮水和活动均符合方案要求。
4 小结
在药品审评标准不断提高的新形势下,招募精神分裂症患者作为受试者开展精神类药品生物等效性试验,需要临床研究机构全面合理地进行管理,以降低试验风险,在保护受试者权益的同时保证试验质量。专业的Ⅰ期临床研究室团队能够在整个试验过程针对不良事件发生可能的风险要素构成,认真落实试验进展的每个阶段和细节,采取相应的质量控制措施,降低可能存在的风险[11],但欠缺对患者诊疗经验。临床科室医护虽然临床经验丰富,但可能存在对临床试验不够重视,认为与普通临床操作相同即可等错误认识[12]。本研究根据研究室经验,通过药物Ⅰ期临床研究室与精神科协调合作模式,发挥各自专科领域特长,优势互补,并基于精神分裂受试者及研究药物特点进行管理,取得了较好的试验结果,可供以其他种类疾病患者作为研究对象的药物临床试验参考。

