并流沉淀法降低铜电解液中砷锑铋杂质离子的研究
王军辉,姚夏妍,焦晓斌,牛永胜,汪友元,鲁兴武,余江鸿,席利丽
(1.白银有色集团股份有限公司,甘肃白银 730900;2.西北矿冶研究院,甘肃白银 730900;3.甘肃省有色金属冶炼新工艺及伴生稀散金属高效综合利用重点实验室,甘肃白银 730900)
0 引言
铜电解精炼过程中电解液的清晰度是保证阴极铜质量的必要条件,尤其是在高电流密度下,电解液必须经过净化,以减轻杂质离子对阴极铜质量的影响[1]。在所有的杂质离子中,As、Sb 及Bi 离子的电位与Cu2+接近,既能和阳极铜一起溶解,同时又可与Cu2+一起在阴极上析出,还能以其他形式进入阴极,成为铜电解过程最有害的杂质。正常情况下,电解液中的As、Sb 离子在电解液中主要以或以形式存在,此时会形成沉淀阳极泥,有助于改善阴极铜质量;其他情况会以漂浮阳极泥形态存在,漂浮阳极泥产生的原因相对较复杂[2-4],但其比重轻、溶解度小、表面活性大,极易附着在阴极铜表面上,影响铜的电极结晶成核过程[5]。因此,铜电解液砷锑铋的净化一直是湿法冶金领域的研究热点。
现有的主流净化方法大致可以分为两类:一种是电解沉积法,砷锑铋离子与Cu2+浓度一同被降低,存在电耗高、铜损失量大的问题;第二种是采用萃取剂或树脂通过萃取方法或离子交换法降低砷锑铋离子浓度,但实际生产中存在液量大的缺陷。最近,有研究人员采用吸附法及膜分离法使砷锑铋离子从铜电解液中分离[6],此方法虽有大量研究,但尚未实现工业化应用。
一般而言,铜电解过程中不同价态的As、Sb、Bi会形成SbAsO4、BiAsO4等化合物,如As5+和Sb3+结合形成SbAsO4沉淀,As3+和Sb5+结合形成AsSbO4沉淀,因此,可以通过SO2还原As5+和Sb5+、H2O2氧化As3+和Sb3+来调整化合价,促使砷锑铋形成沉淀阳极泥。为了减少氧化剂与还原剂的接触几率而造成试剂浪费,本文利用分流手段,以铜电解液中Cu2+及砷锑铋离子为研究对象,开展并流沉淀法降低铜电解液中砷锑铋杂质离子的实验,研究SO2和H2O2的加入量和温度对铜和砷锑铋离子浓度的影响,并分析对流沉淀法降低铜电解液中砷锑铋杂质离子的机理。
1 实验介绍
1.1 实验装置
图1 是实验装置示意图,整个循环系统由管道、阀门、SO2储气瓶、双氧水滴加装置、反应罐、砷化氢(AsH3)检测仪、加热装置以及搅拌装置组成。其中,SO2储气瓶自带流量调节装置,实验过程中AsH3检测仪用于检测AsH3的逸出浓度,并以此确定SO2的进气量。H2O2通过滴加方式进入到反应罐中,温度通过加热装置调节,实验过程中所用设备的详细信息如表1所示。
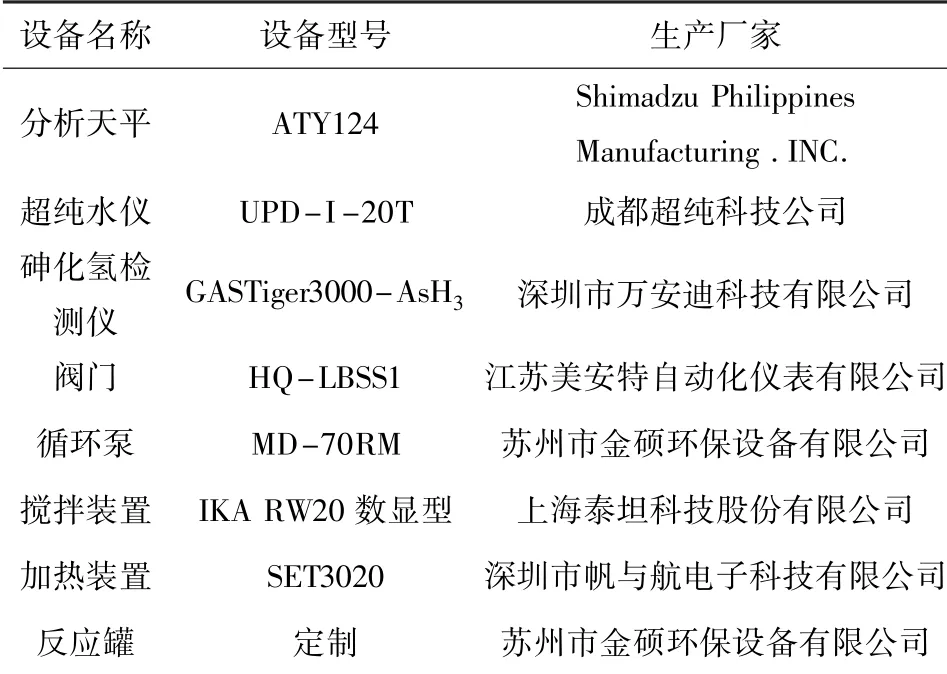
表1 主要实验设备
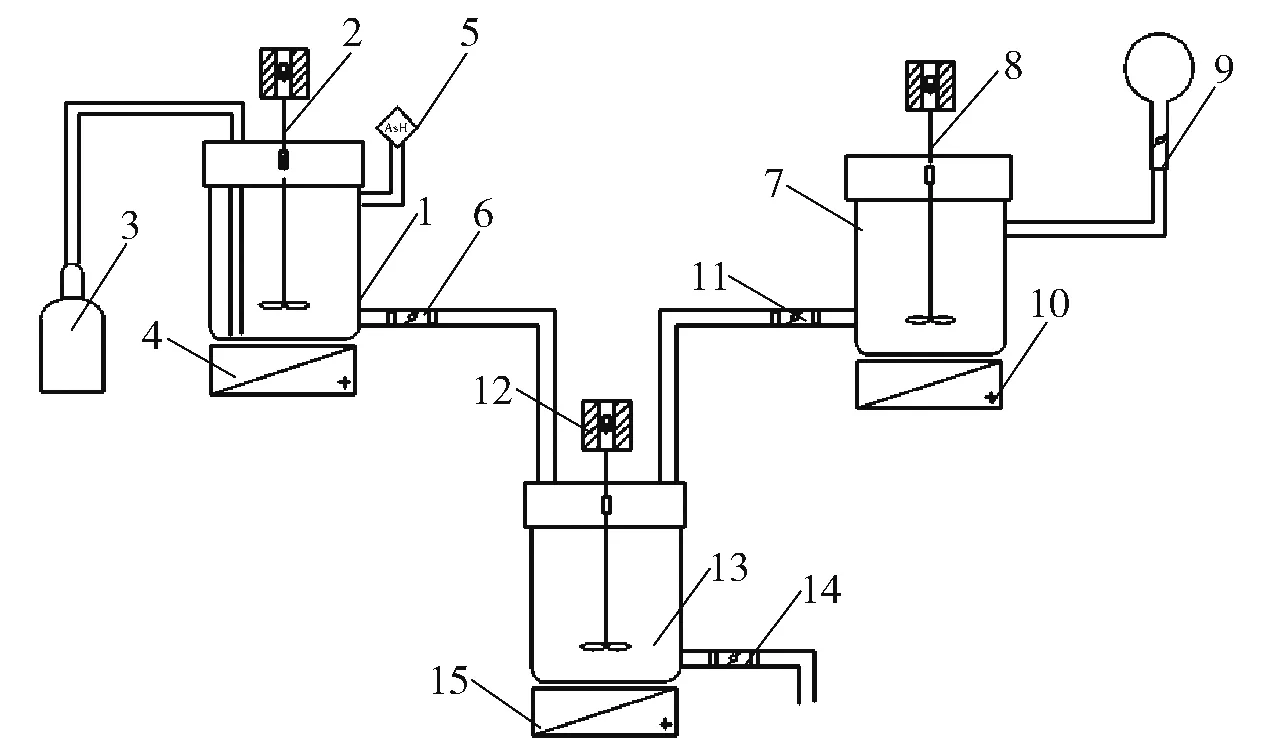
图1 实验装置示意图
1.2 实验原料
实验所用的铜电解液由白银有色集团股份有限公司铜业公司提供,主要成分及含量见表2。

表2 铜电解液的化学成分 g/L
实验所用的SO2纯度达到99.96%,由白银有色集团股份有限公司铜业公司提供。
实验所用的氧化剂为浓度30% H2O2,由国药集团化学试剂有限公司提供。
1.3 实验方法
实验分三部分,第一部分确定通入SO2浓度,并考察温度对SO2还原铜电解液的影响;第二部分确定H2O2的加入量,并考察温度对H2O2氧化铜电解液的影响;第三部分考察温度对并流法沉淀铜电解液杂质的影响。
1)取一定量的铜电解液加入SO2反应罐和H2O2反应罐,向SO2反应罐通入SO2,时刻观察砷化氢检测仪的显示器,当逸出AsH3浓度达到0.03 mg/m3时,即为SO2的最佳通入量,根据反应时间可计算出SO2最佳浓度,其中,反应时间设置为10 min。
2)开启加热装置将两罐的铜电解液加热至实验设置的温度,同时开启砷化氢检测仪,通过阀门调节SO2和H2O2的加入量,结合砷化氢检测仪,根据电解液中砷锑铋离子浓度最适合生成沉淀的条件得到H2O2加入量、反应时间、温度与搅拌速度的最佳值,各实验反应60 min 后检测电解液离子浓度。
3)量取一定量的铜电解液分别置于SO2反应罐和H2O2反应罐中,同时开启两反应罐的加热装置、搅拌装置,开启阀门6 和11,将SO2反应罐和H2O2反应罐中的铜电解液并流至并流混合反应罐中,按照已确定的H2O2加入量、SO2进气浓度、搅拌速度、反应时间等实验条件,研究温度对并流法沉淀铜电解液中砷锑铋杂质的影响,并确定最佳温度。
1.4 实验原则
1)尽可能按照化学反应配比As5+与Sb3+、As3+与Sb5+的比例,尽量使铜电解液中的砷、锑、铋离子生成沉淀,减少杂质含量。
2)尽可能保持Cu2+浓度稳定,不对铜电解工序造成影响。铜电解过程中阳极铜中的砷锑铋在电解过程中首先以三价离子形式进入电解液,并流沉淀法通入SO2会促进少量As3+转变为As3-,Cu2+转变为Cu+,导致Cu3As 与AsH3形成,引起Cu2+浓度降低以及AsH3气体的逸出。同时,向电解液中滴加H2O2会促使Cu+和As3+不断被氧化,导致Cu3As的形成量减少,从而影响Cu2+浓度的变化趋势,并且这种变化趋势又会受到温度的影响。因此,在一定条件下向电解液同时加入双氧水和二氧化硫可维持Cu2+浓度不变。
1.5 检测分析
实验过程中需要测量铜电解液中Cu2+与砷锑铋的离子浓度,采用火焰原子吸收分光光度法测量,为了保证实验数据的准确性,每个样品重复实验3次,取其平均值作为实验结果。
2 实验原理
正常环境条件下,铜电解液中的大部分砷以As5+存在、锑以Sb3+存在、铋以Bi3+存在,有少量的砷以As3+存在、锑以Sb5+存在。此时,由于离子浓度有限,会形成少量沉淀阳极泥,但电解液中的As5+与Sb5+、As3+与Sb3+也会形成漂浮阳极泥,这对生产非常不利。
分析实际生产产生的漂浮阳极泥成分,发现锑是形成漂浮阳极泥的核心元素,所以降低电解液中锑离子浓度可降低铜电解过程中形成漂浮阳极泥的概率,达到提高电解液清晰度和改善阴极铜表观质量的目的。
一定条件下向铜电解液中通入SO2时,发生式(1)反应式。此时,部分As5+被还原为As3+,部分Sb5+被还原为Sb3+,由于铜、砷、锑、铋离子浓度存在差异,只有少量Sb5+被还原成与可形成SbAsO4沉淀;同时,SO2将Cu2+还原为Cu+,影响正常的铜电解反应。
向电解液中通入H2O2时,发生式(3)反应式。此时,电解液中部分As3+被氧化为As5+,Sb3+被氧化为Sb5+,Sb5+形成HSb(OH)6,但由于As3+存在的量很少,所以只能形成少量AsSbO4沉淀;另外,加入双氧水会在电解液中促进CuO 的形成,导致阳极钝化。
并流沉淀技术就是通过向电解液中通入SO2和H2O2来调整As5+与Sb3+、As3+与Sb5+的比例,双氧水的氧化作用将As3+氧化为As5+,SO2的还原作用将Sb5+还原为Sb3+,在一定条件下,可维持Cu2+不受损耗,提高SbAsO4、BiAsO4以及AsSbO4等沉淀的形成量,减少电解液中砷、锑、铋杂质含量。具体反应原理见图2,化学反应见式(1)~(3)[7]。
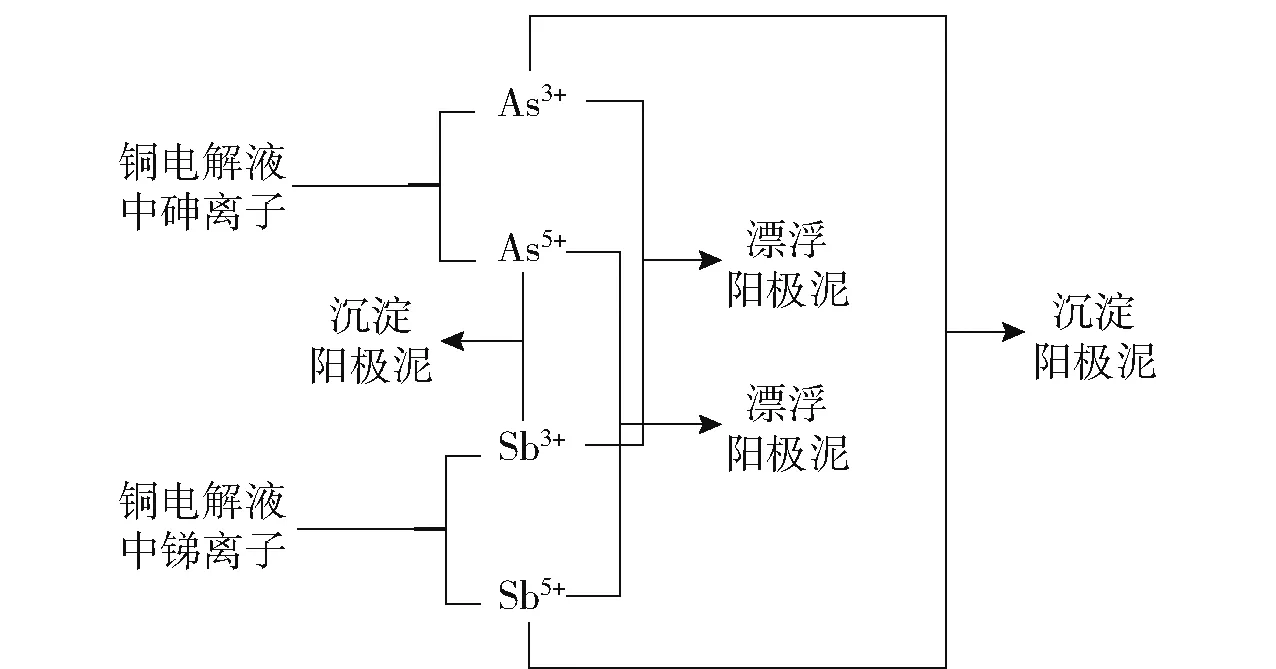
图2 铜电解过程阳极泥类型
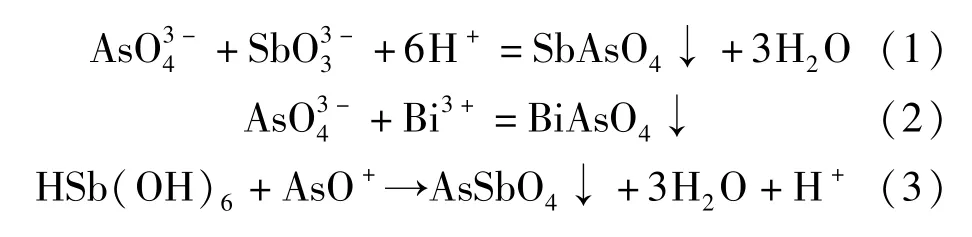
3 实验结果与分析
3.1 SO2 还原铜电解液实验
3.1.1 SO2进气浓度的确定
向铜电解液中通入SO2可将电解液中As5+还原为As3-,与电解液中的H+反应,导致AsH3的逸出。AsH3毒性极强,我国工作场所有害因素职业接触限值(MAC)为0.03 mg/m3[8],这是本次实验SO2进气浓度的限制条件。
量取500 mL 的铜电解液置于SO2反应罐中,同时开启SO2反应装置的加热装置、搅拌装置和砷化氢检测仪,在电解液温度55 ℃、搅拌速度250 r/min、反应时间10 min 的条件下,分别考察SO2进气浓度为0.125 g/L、0.25 g/L、0.375 g/L、0.5 g/L和0.625 g/L 时砷化氢的逸出量,实验结果见图3。
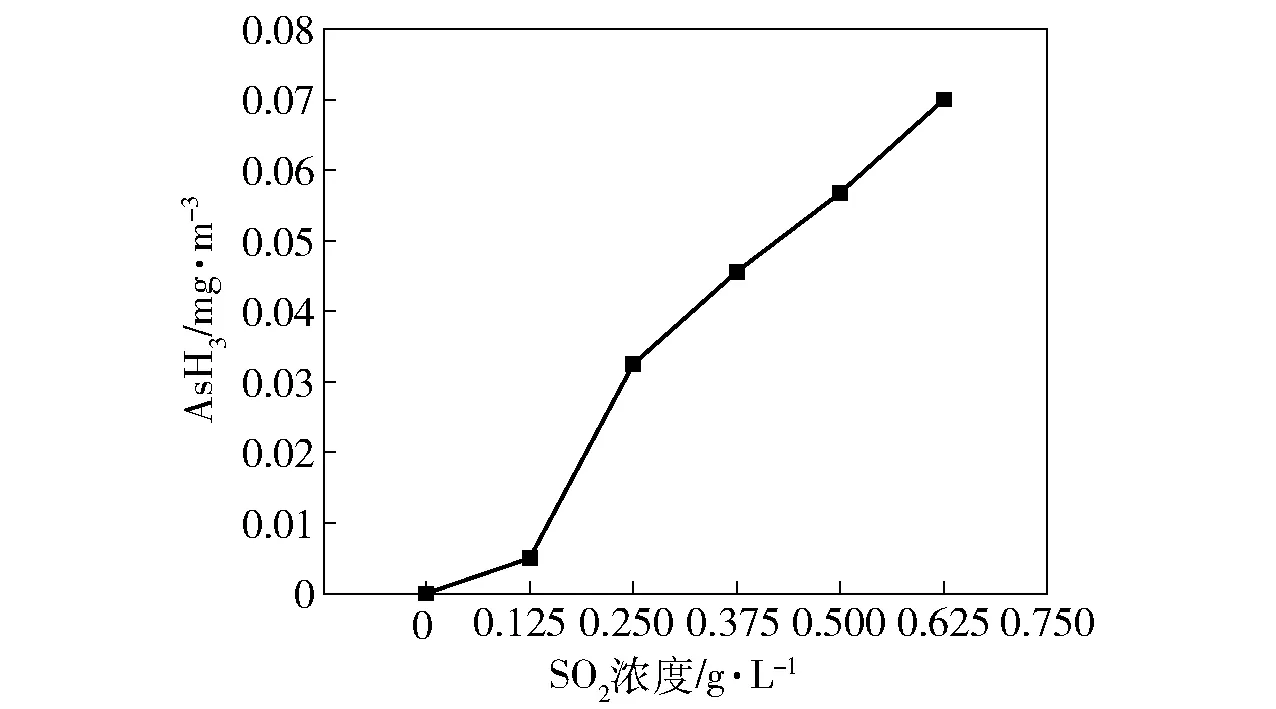
图3 SO2 浓度与逸出AsH3量的关系
由图3 可知,在一定条件下,SO2进气浓度对AsH3的生成影响较大,当SO2的进气浓度在0.25 g/L以上时,AsH3的逸出量大于0.03 mg/m3,超过安全限度。但SO2浓度太小时,对电解液产生的影响有限,因此,将SO2进气浓度设定为0.125 g/L。
3.1.2 温度对反应的影响
在SO2进气浓度0.125 g/L、搅拌速度250 r/min、反应时间60 min 的条件下,考察反应温度分别为45 ℃、50 ℃、55 ℃、60 ℃、65 ℃时铜、砷、锑、铋离子的浓度,实验结果见图4。
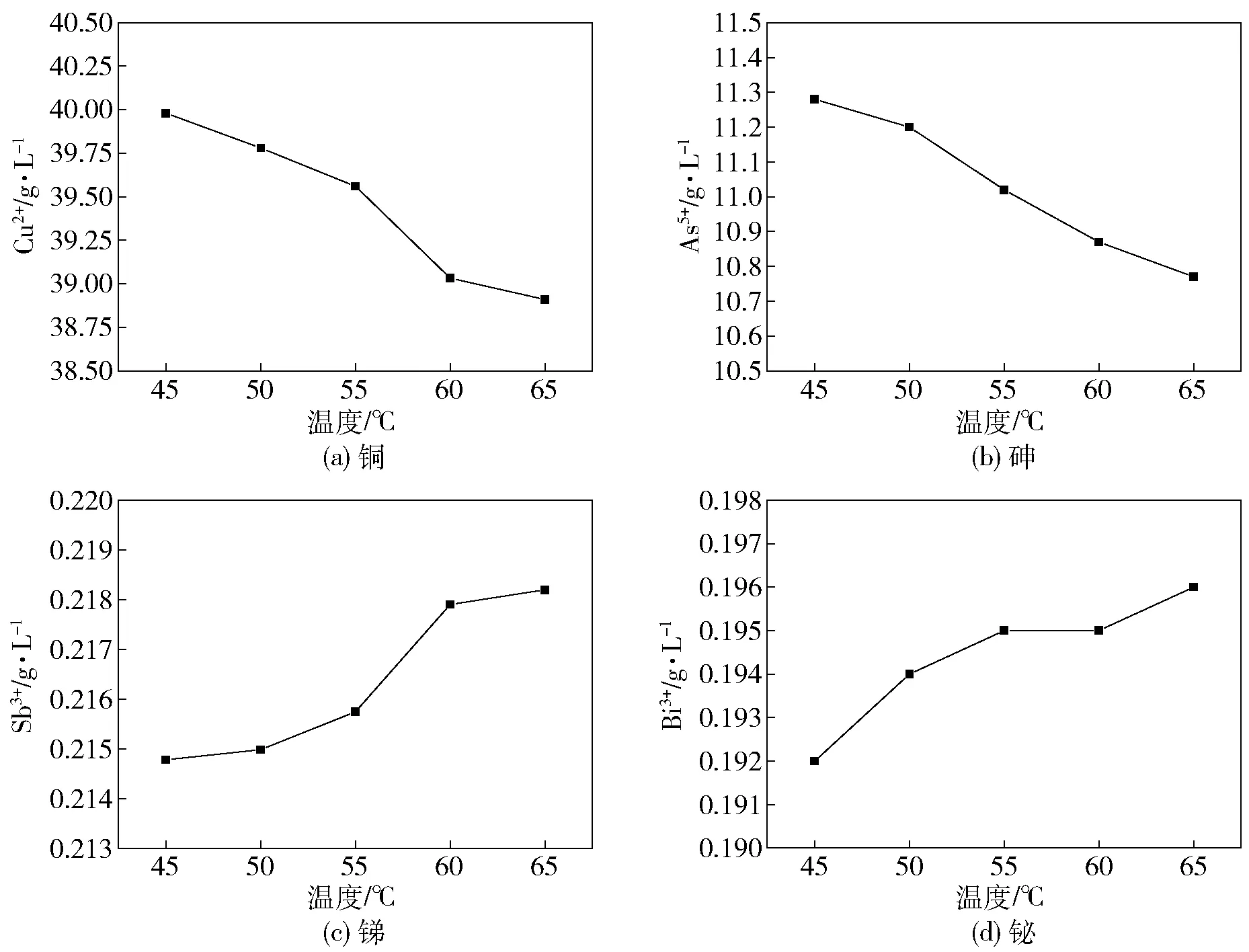
图4 SO2 还原温度对离子浓度的影响
由图4 可以看出,在一定条件下向电解液中通入SO2时,温度对离子浓度的影响较大。
图4(a)和图4(b)显示,实验条件下,随着温度的升高,铜、砷离子浓度逐步降低。当反应温度为65 ℃时,铜、砷离子浓度达到极小值,分别为38.91 g/L和10.77 g/L。
图4(c)和图4(d)显示,锑、铋离子浓度的变化趋势与砷、铜离子相反,随温度的升高而升高。当反应温度为65 ℃时,锑、铋离子浓度达到极大值,分别为0.218 g/L 和0.196 g/L。
常温下,向电解液中通入SO2有利于降低砷、锑离子浓度;但升高还原温度时,砷离子浓度降低,锑离子浓度升高,铋离子浓度也会升高。可见SO2还原温度对离子浓度的影响复杂。反应温度为45 ℃时,虽然有利于保持正常的铜酸比例,锑离子浓度最低(锑是形成漂浮阳极泥的核心元素),但在此温度下砷离子浓度降低程度不大,铋离子浓度较初始浓度也有增加趋势,导致电解液的清晰度改善程度有限。
3.2 H2O2 氧化铜电解液实验
3.2.1 H2O2加入量的确定
由于锑离子是形成漂浮阳极泥的核心元素[9-10],选取锑离子为参考对象确定H2O2的加入量。在搅拌速度250 r/min、反应时间60 min、电解液温度55 ℃的条件下,分别设置双氧水的滴加量为1 mL、2 mL、3 mL、4 mL、5 mL,考察双氧水的滴加量对锑离子浓度的影响。实验结果见图5。
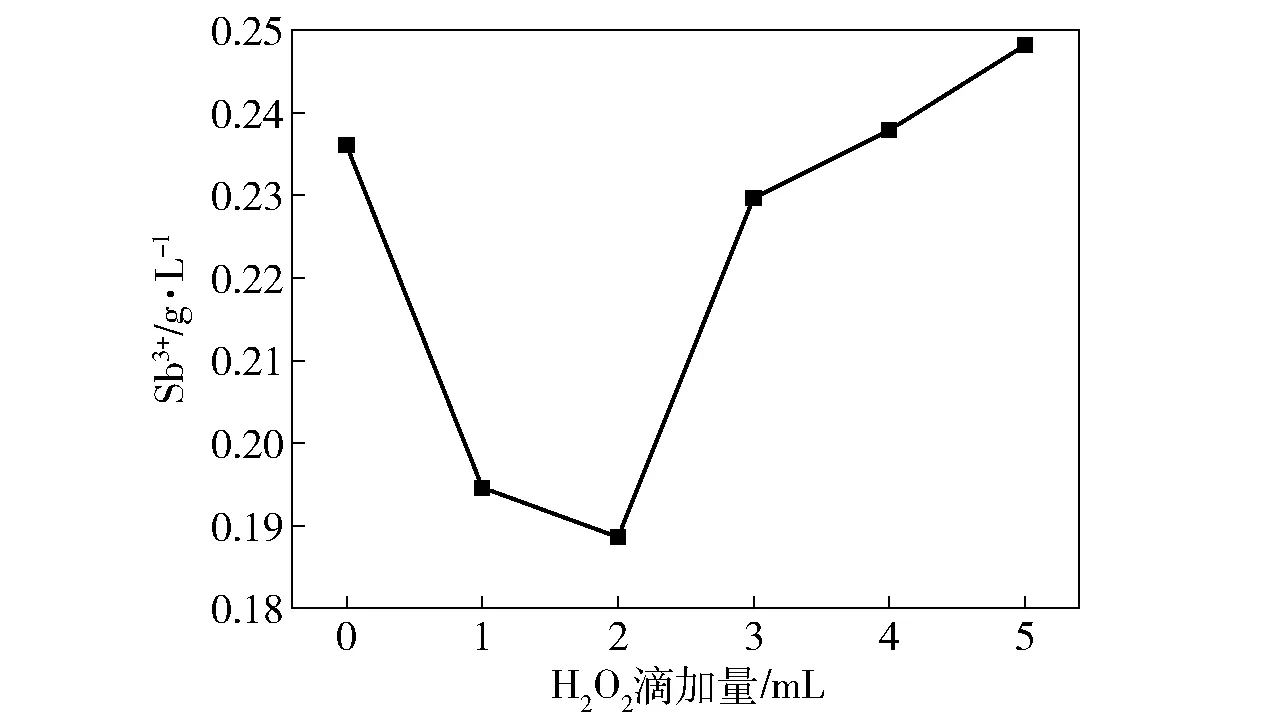
图5 H2O2 滴加量对Sb 离子浓度的影响
图5 显示,滴加H2O2可对Sb 离子浓度产生影响。Sb 离子浓度随着双氧水滴加量的增加出现先降低后增加的趋势,在双氧水滴加量为2 mL 时,Sb离子浓度达到较小值,为0.185 g/L。所以选择H2O2加入量为2 mL,以达到电解液中Sb 离子浓度最低、减少漂浮阳极泥形成量的目的。
3.2.2 温度对反应的影响
量取500 mL 的铜电解液于H2O2反应罐中,同时开启H2O2反应装置的加热装置、搅拌装置,在H2O2加入量2 mL、搅拌速度250 r/min、反应时间60 min 的条件下,分别设置电解液温度为45 ℃、50 ℃、55 ℃、60 ℃、65 ℃,考察温度对H2O2氧化铜电解液的影响。实验结果见图6。
由图6 可以看出,在一定条件下向电解液中滴加双氧水时,温度对离子浓度的影响较大。如图6(a)所示,实验条件下,Cu2+浓度随着温度的升高而升高,当反应温度为65 ℃时,其浓度达到极大值,为41.3 g/L;图6(b)和图6(c)显示,砷、锑离子浓度随温度的升高逐步降低,当反应温度为65 ℃时,其浓度达到极小值,分别为10.7 g/L 和0.186 g/L;图6(d)显示,铋离子浓度的变化趋势与铜离子大致相同,其浓度值随着温度的升高而升高,当反应温度为65 ℃时,其浓度达到极大值,为0.191 g/L。
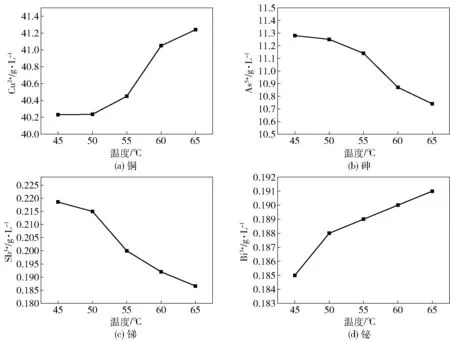
图6 温度对H2O2 氧化铜电解液的影响
3.3 温度对并流法沉淀铜电解液中杂质的影响
量取500 mL 的铜电解液分别置于SO2反应罐和H2O2反应罐中,同时开启两反应罐的加热装置(SO2反应罐维持温度45 ℃,H2O2反应罐维持温度65 ℃)、搅拌装置(搅拌速度250 r/min),H2O2加入量2 mL、SO2进气浓度0.125 g/L、反应时间60 min,分别设置混合反应装置温度为45 ℃、50 ℃、55 ℃、60 ℃、65 ℃,考察温度对并流法沉淀铜电解液中砷锑铋杂质的影响。试验结果见图7。
图7 显示,在一定条件下向电解液同时加入H2O2和SO2时,铜、砷、锑、铋离子的浓度随温度的变化趋势均不相同。图7(a)显示,同等条件下,Cu2+浓度随着温度的升高出现先降低后升高的趋势:当反应温度为50 ℃时,其浓度值与初始值基本相同;当反应温度为55 ℃时,其浓度达到极小值,为39.2 g/L;当反应温度为65 ℃时,其浓度达到极大值,为41.6 g/L。图7(b)、图7(c)、图7(d)显示,砷、锑、铋离子浓度随温度的升高出现无规律的变化,当反应温度为50 ℃时,砷锑铋离子浓度达到极小值,分别为9.86 g/L、0.204 g/L 和0.189 g/L。综合考虑,最佳反应温度选择50℃,此条件下向电解液中同时加入SO2和H2O2,可以在保证Cu2+浓度不变的前提下降低砷、锑、铋杂质离子浓度,提高电解液的清晰度。
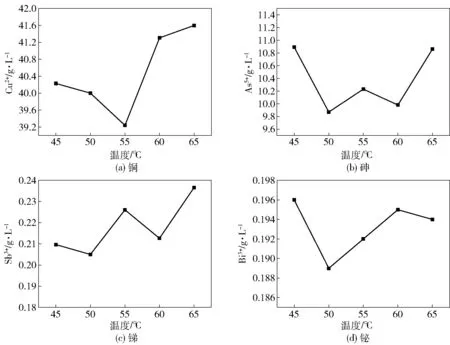
图7 温度对并流沉淀法沉淀铜电解液中杂质的影响
3.4 并流沉淀法最佳处理条件
一般情况下,铜电解过程中电解液温度在50~55 ℃范围波动。根据实验数据,在此温度区间内向电解液加入SO2,Cu2+浓度为39.50~39.75 g/L,砷离子浓度为11.20~11.25 g/L,锑离子浓度呈增高趋势,为0.194~0.195 g/L(图4)。单独滴加H2O2,Cu2+浓度为40.2~40.5 g/L,砷离子浓度为11.05~11.20 g/L,锑离子浓度为0.20~0.215 g/L,铋离子浓度呈增高趋势,为0.188~0.189 g/L(图6)。在反应温度为50 ℃时采用并流沉淀技术,Cu2+浓度为40.10 g/L,砷离子浓度为9.80 g/L,锑离子浓度为0.205 g/L,铋离子浓度为0.188 g/L。由此可以看出,并流沉淀技术可在维持Cu2+浓度稳定的前提下,最大限度地降低电解液中的砷锑铋离子浓度。
根据上述实验数据得出并流沉淀法的最佳条件:H2O2采用滴加方式,加入量为4 mL/L,SO2进气浓度为0.125 g/L,搅拌速度为250 r/min,反应温度为50 ℃,反应时间可依照电解时间以及电解液中的砷锑铋离子浓度而设置。
4 并流沉淀法处理后的铜电解液生产效果
4.1 阴极铜质量对比
在上述实验最佳处理条件下得到并流法沉淀后的铜电解液,将其进行电解,电解温度55 ℃、电压0.35 V、电流密度265 A/m2,开启直流电源进行电解,同时按照明胶100 g/t、硫脲100 g/t、盐酸100 g/t的量滴入电解槽中,电解24 h 后,观察阴极铜的表观质量,并与未经并流沉淀法处理的电解液阴极铜产品进行对比,见图8。图8 表明,并流沉淀法对阴极铜的质量有极大的改善作用。

图8 并流沉淀法对阴极铜质量的影响
4.2 工艺指标及经济效益对比
与传统电积脱铜除杂工艺相比,并流沉淀法通过强化铜电解液自净化的途径降低电解液中的砷锑铋杂质离子,工艺简便快捷,可避免传统电积法除杂形成黑铜泥而造成铜元素的浪费和成本高的缺陷;同时,并流沉淀法可以直接在电解槽中进行,可处理含杂质量高的电解液或阳极铜,避免因电解液中砷锑铋含量过大而来不及及时处理造成阴极铜结粒问题。根据现场统计,铜业公司阴极铜因阳极泥粒子,价格每吨降低200 元,阴极铜的平均结粒率25%,所以每年损失达到1 000 万元;采用并流沉淀技术,阴极铜结粒率降低20%,降低损失800 万元;由于SO2自产不计价,双氧水成本为400 万元,净液车间每年耗电800 万元,而且采用并流沉淀技术可以缓解净液压力,降低耗电量400 万元。综上,采用并流沉淀技术每年成本降低800 万元。
5 结论
1)向电解液中通入SO2,条件为:进气浓度为0.125 g/L,搅拌速度为250 r/min,反应时间为1 h,反应温度为45 ℃。此时,SO2会将Sb5+还原为Sb3+,As5+还原为As3+,促进SbAsO4、BiAsO4以及AsSbO4等沉淀的形成,最终降低Sb 离子浓度,但砷铋离子浓度的变化幅度不大。进一步提高温度会降低铜砷离子浓度,同时也会导致锑铋离子浓度回升。
2)向电解液中加入H2O2,条件为:搅拌速度250 r/min,反应时间60 min,电解液温度65 ℃,滴加量4 mL/L。此时,H2O2会将Sb3+氧化为Sb5+,As3+氧化为As5+,形成SbAsO4与AsSbO4等沉淀,降低砷锑离子浓度。但同时其也会降低铜铋离子浓度,严重时导致阳极钝化,较低温度对砷锑离子浓度影响不大。
3)采用并流沉淀技术可将SO2时还原成的As3+与双氧水氧化成的Sb5+形成沉淀化合物,便与Sb3+形成SbAsO4沉淀,最终实现降低铜电解液中砷锑铋杂质离子、提高电解液的清晰度,降低杂质离子对阴极铜质量的影响,减小阴极铜结粒数量的目的,并可弥补加入单一试剂时的缺陷,其最佳条件:SO2反应罐SO2进气浓度为0.125 g/L,搅拌速度为250 r/min,反应时间为60 min,温度为45 ℃;H2O2反应罐H2O2滴加量为4mL/L,搅拌速度为250 r/min,反应时间为60 min,温度为65 ℃;并流后混合反应罐的搅拌速度为250 r/min,反应罐中的温度维持50 ℃,反应时间为60 min。

