SGLT-2抑制剂治疗2型糖尿病合并非酒精性脂肪肝*
范梦迪 李俊 付威 李青菊
(郑州大学第二附属医院,河南 郑州 450014)
随着我国经济和生活方式的改变,2型糖尿病(Type 2 diabetes mellitus,T2DM)和非酒精性脂肪肝(Non-alcoholic fatty liver disease,NAFLD)的患病率显著增加,且NAFLD和T2DM共患可增加其向肝硬化、肝癌进展的风险[1],因此T2DM合并NAFLD逐渐引起重视。近年来,关于T2DM合并NAFLD的药物治疗的相关研究[2-3]相继被报道,目前GLP-1受体激动剂改善NAFLD的疗效被大多数人所认可,且不增加严重的不良反应。SGLT-2抑制剂是一种新型的降糖药,其对NAFLD肝功能的益处在国外研究中[4-5]已被报道,但国内相关研究较少,本研究旨在应用超声定量分析的方法观察SGLT-2抑制剂对T2DM合并NAFLD的疗效。现报告如下。
1 资料与方法
1.1 一般资料 选择2018年2月~2020年2月我院收治的T2DM合并NAFLD患者100例作为研究对象,随机分为对照组和观察组,每组各50例。纳入标准:①T2DM的诊断符合中国2型糖尿病的防治指南中的诊断标准[6]。②NAFLD的诊断参照中华医学会肝脏病学分会脂肪肝和酒精性肝病学组非酒精性脂肪性肝病诊疗指南2010年修订版[7]。③患者及家属知情并签署知情同意书。排除标准:①酒精性肝病(乙醇摄入量:男≥40 g/d,女≥20 g/d)。②慢性病毒性肝炎、自身免疫性肝炎、药物性肝损伤、胆道疾病、肝硬化、肝癌等。③共存有心肺或肾小球功能不全(估计肾小球滤过率<45 mL/min)。④存在活动性持续性尿路感染。⑤糖尿病的急性并发症。⑥1型糖尿病、妊娠期糖尿病以及其它类型糖尿病。本研究获医院伦理委员会审核同意。
1.2 方法 两组均接受生活方式干预。由于考虑对照组应用单一降糖药物血糖控制不佳,因此应用盐酸二甲双胍肠片(中美上海施贵宝制药有限公司,0.5 g/次,1次/d)联合格列美脲片(赛诺菲安万特制药有限公司,2 mg/次,1次/d)服用降糖治疗;观察组在对照组常规降糖药的基础上加用SGLT-2抑制剂降糖药达格列净片(阿斯利康制药有限公司,10 mg/次,1次/d)口服治疗。药物剂量依据血糖情况由起始剂量逐步调整。治疗持续24周。
1.3 观察指标 在研究的开始和结束时分别测量身高、体重、腰围、臀围;收集年龄、性别、糖尿病病程等资料;空腹8~12 h抽静脉血检测肝功能[谷草转氨酶(AST)、谷丙转氨酶(ALT)]、血脂[总胆固醇(TC)、甘油三酯(TG)]、空腹血糖(FPG)、糖化血红蛋白(HbA1C)、空腹胰岛素(FINS)。计算体重指数(BMI=体重/身高2)、腰臀比(WHR=腰围/臀围)、胰岛素抵抗指数(HOMA-IR=FPG×FINS/22.5)。
1.4 超声定量分析 由同一位经验丰富的主治医师及以上的超声科医生应用同一台E超诊断仪进行检查,收集标准图像,测量超声肝肾回声比值、超声肝脏衰减系数,通过标准公式[8]评估肝脏脂肪含量(LFC=62.592×标化超声肝肾回声比值+168.076×标化超声肝脏衰减系数)。
1.5 疗效评定 参考相关标准[9]对疗效进行评定:①显效:主要标准为超声显示脂肪肝治愈,次要指标为肝功能、血脂恢复正常。②有效:肝回声严重程度改善1个等级,次要指标为肝功能、血脂明显降低。③无效:超声显示肝回声无明显变化或增强,肝功能、血脂无明显降低甚至升高。总有效率=(显效+有效)/总例数×100%。
1.6 统计学处理 应用SPSS 23.0进行数据统计学分析,计数资料以率(%)表示,采用2检验。符合正态分布的计量资料以均数±标准差表示,采用t检验;不符合正态分布的计量资料以中位数表示,采用非参数检验分析。P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 共纳入100例受试者,观察组患者平均年龄(60.22±12.06)岁,男性病例占62%,糖尿病病程为(10.12±7.55)年;对照组患者平均年龄(59.25±12.7)岁,男性病例占66%,糖尿病病程为(12.03±6.57)年。两组患者一般资料比较差异无统计学意义(P>0.05)。两组治疗前各生化指标无显著性差异(P>0.05),具有可比性。
2.2 两组脂肪肝LFC及疗效对比 与基线相比,观察组LFC下降显著[治疗前LFC中位数为16.26(10.56,24.35),治疗后LFC中位数为11.32(6.60,17.79);P=0.001];对照组下降不显著[治疗前LFC中位数为16.49(10.05,25.21),治疗后LFC中位数为15.51(9.13,24.48);P=0.054]。观察组总有效率明显高于对照组(P<0.05),见表1。
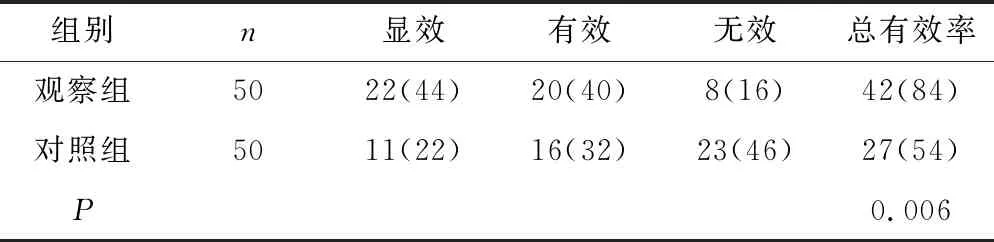
表1 两组脂肪肝临床有效率比较[n(×10-2)]Table 1 Comparison of clinical effective rate of fatty liver
2.3 两组治疗前后肝功能及血脂比较 治疗后,两组ALT、AST、TG、TC均显著改善(P<0.05),观察组改善程度更显著(P<0.05),见表2。
表2 两组肝功能及血脂改善情况对比Table 2 Comparison of the improvement of blood lipid and liver function
2.4 两组治疗前后胰岛素抵抗改善情况比较 观察组治疗后HOMA-IR、BMI、WHR较治疗前明显改善(P<0.05),对照组治疗后无明显改善(P>0.05),见表3。
表3 两组胰岛素抵抗改善情况对比Table 3 Comparison of the improvement of Insulin resistance between two groups
2.5 两组治疗前后血糖改善情况比较 两组治疗后FPG、HbA1C较治疗前均明显降低(P<0.05),但组间差异无统计学意义(P>0.05),见表4。
表4 两组血糖改善情况对比Table 4 Comparison of the improvement of blood sugar
3 讨论
NAFLD在全球广泛分布,普通成人患病率为20%~33%[10],T2DM患者中患病率高达55%[11]。T2DM和NAFLD共同发病机制为胰岛素抵抗(Insulin resistence,IR)[12]。因此,改善IR成为治疗NAFLD的一个重要突破口。SGLT-2抑制剂通过抑制肾近曲小管对葡萄糖和钠的重吸收,降低肾糖阈,增加尿糖排泄,实现降糖的目的。同时还可降低体重、血压和尿酸水平[13],通过减少内脏脂肪明显改善IR[14-15],因此可应用于T2DM合并NAFLD患者改善IR状态。
本研究中观察组选取50例T2DM合并NAFLD患者,在常规降糖药物(二甲双胍+格列美脲)的基础上给予达格列净10 mg/d服用,持续24周,采用肝脏超声定量技术评估脂肪含量。结果显示肝脏脂肪含量显著降低(从16.26%降至11.32%,P<0.05),同时ALT、AST、TC、TG显著下降,与国外相关研究结果基本一致[16]。除此之外,BMI、WHR、HOMA-IR显著下降,说明达格列净缓解脂肪肝的作用可能与其改善IR,降低血脂有关。FPG、HbA1C与对照组相比无明显差异(P>0.05),但磺脲类降糖药的剂量应用较对照组减少,且低血糖反应的发生率明显降低。磺脲类降糖药用量少,一方面可减少对肝功能的损害,另一方面可保护胰岛β细胞的功能,改善IR。本研究中采用超声肝/肾比值及肝脏衰减系数来量化肝脏脂肪含量,较国内以往研究中仅采用临床治疗有效率来观察药物疗效相比,准确性明显提高,且超声检查安全性高、价格低廉、可重复性高,可作为脂肪肝随访的首选检查方法。
关于SGLT-2抑制剂改善NAFLD的机制,我们提出了以下两种可能:①SGLT-2抑制剂可以通过增加尿糖排泄而丢失能量,这种能量损失会促进肝脏脂肪的β氧化,并诱导肝脏脂肪代谢,从而减少内脏脂肪[17]。伴随着内脏脂肪的减少,NAFLD可以得到缓解。②胰高血糖素的作用:SGLT-2抑制剂通过在胰岛α细胞中表达编码SGLT2的SLC5A2直接促进胰高血糖素的分泌[18],胰高血糖素通过PPARα和CPT-1α刺激肝脏中的糖异生和肝脏脂肪的β氧化[19],最终使肝脏脂肪沉积减少。
4 结论与启示
SGLT-2抑制剂可明显降低NAFLD患者肝脏的脂肪含量,改善肝功能及血脂,对NAFLD的疗效显著。同时可降低NAFLD合并T2DM患者的血糖水平,改善IR,帮助患者减轻体重负担,是一种具有治疗前途的抑制剂。本研究存在以下几点不足之处:①超声检查人为干扰性较大,没有肝脏CT值、肝脏MRI、肝脏活检的准确性高。②仅观察了肝功能、血脂、脂肪含量等指标,未进行纤维化等相关指标的研究。③NAFLD的诊断未依据肝脏活检。④样本数量偏少。后期研究将扩大样本量,进一步完善实验,以期获得更可靠的科研数据。

